名校
解题方法
1 . 我国科学家使用双功能催化剂催化水煤气变换反应:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH<0,在低温下获得高转化率与高反应速率,反应过程示意图如下,下列说法正确的是


| A.过程Ⅰ、过程Ⅱ均为放热过程 |
| B.图中显示:起始时的2个H2O都参与了反应过程 |
| C.过程Ⅲ只生成了极性共价键 |
| D.使用催化剂降低了水煤气变换反应的ΔH |
您最近一年使用:0次
2022-05-16更新
|
371次组卷
|
15卷引用:宁夏银川市第二中学2021-2022学年高二下学期期中考试化学试题
宁夏银川市第二中学2021-2022学年高二下学期期中考试化学试题山西省潞城第一中学2020-2021学年高二下学期3月月考化学试卷题福建省莆田第一中学2020-2021学年高二下学期期中考试化学试题天津市第二南开学校2022-2023学年度高二上学期期中质量调查化学试题上海财经大学附属中学2022-2023学年高二上学期期中考试化学试题【市级联考】四川省攀枝花市2019届高三下学期第三次统考理科综合化学试题(已下线)专题07 化学反应中的能量变化——2019年高考真题和模拟题化学分项汇编2019年湖南省郴州市高三第一次教学质量监测化学试题2020届高三《新题速递·化学》1月第02期(考点01-06)北京市通州区2020届高三上学期期末摸底考试化学试题北京市2020届高三下学期周末测试化学试题广东省佛山市第一中学2019-2020学年高一下学期第一次段考化学试题河南省顶级名校2021届高三年级上学期期中考试化学试题第34届(2021年)高中化学奥林匹克竞赛浙江省预赛试题甘肃省嘉峪关市第一中学2021届高三下学期六模考试理综化学试题
名校
解题方法
2 . 回答下列问题:
(1)我校化学社团做了如下探究实验:利用H2C2O4溶液和酸性KMnO4溶液之间的反应来探究外界条件改变对化学反应速率的影响。实验数据如表所示:
①写出该反应的离子方程式:_______ 。
②通过实验A、B可探究_______ (填外部因素)的改变对反应速率的影响,其中V1=_______ ;通过实验_______ (填实验序号)可探究温度变化对化学反应速率的影响。
③利用实验B中数据计算,用KMnO4溶液的浓度变化表示的反应速率v(KMnO4)=_______ 。
④实验中发现:反应一段时间后该反应速率会突然加快,造成此种变化的原因是反应体系中的某种粒子对KMnO4与H2C2O4之间的反应有某种特殊的作用,则该作用是_______ ,相应的粒子最有可能是_______ 。
(2)一种新型催化剂能使NO和CO发生反应:2NO+2CO 2CO2+N2。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如表所示。
2CO2+N2。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如表所示。
①表中a=_______ ,b=_______ 。
②能验证温度对化学反应速率影响规律的是实验_______ (填实验编号)。
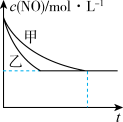
③实验I和实验Ⅱ中,NO的物质的量浓度c(NO)随时间t的变化曲线如图所示,其中表示实验II的是曲线_______ (填“甲”或“乙”)。
(1)我校化学社团做了如下探究实验:利用H2C2O4溶液和酸性KMnO4溶液之间的反应来探究外界条件改变对化学反应速率的影响。实验数据如表所示:
| 实验 序号 | 实验温度/K | KMnO4溶液(含硫酸) | H2C2O4溶液 | H2O | 溶液颜色褪至无色时所需时间/s | ||
 |  |  |  |  | |||
| A | 293 | 2 | 0.02 | 5 | 0.1 | 3 |  |
| B | 293 | 2 | 0.02 | 3 | 0.1 |  | 8 |
| C | 313 | 2 | 0.02 |  | 0.1 | 5 |  |
②通过实验A、B可探究
③利用实验B中数据计算,用KMnO4溶液的浓度变化表示的反应速率v(KMnO4)=
④实验中发现:反应一段时间后该反应速率会突然加快,造成此种变化的原因是反应体系中的某种粒子对KMnO4与H2C2O4之间的反应有某种特殊的作用,则该作用是
(2)一种新型催化剂能使NO和CO发生反应:2NO+2CO
 2CO2+N2。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如表所示。
2CO2+N2。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如表所示。实验 编号 | t/℃ | NO初始浓度/mol·L-1 | CO初始浓度/mol·L-1 | 催化剂的比表面积/m2/g |
| I | 280 |  |  | 82 |
| II | 280 |  | b | 124 |
| Ⅲ | 350 | a |  | 82 |
②能验证温度对化学反应速率影响规律的是实验
③实验I和实验Ⅱ中,NO的物质的量浓度c(NO)随时间t的变化曲线如图所示,其中表示实验II的是曲线

您最近一年使用:0次
名校
解题方法
3 . 我国科技工作者运用DFT计算研究HCOOH在不同催化剂(Pd和Rh)表面分解产生 的部分反应过程如图所示,其中吸附在催化剂表面的物种用*表示。下列说法正确的是
的部分反应过程如图所示,其中吸附在催化剂表面的物种用*表示。下列说法正确的是
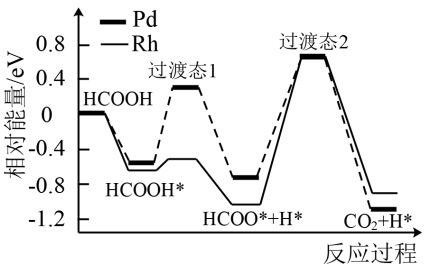
 的部分反应过程如图所示,其中吸附在催化剂表面的物种用*表示。下列说法正确的是
的部分反应过程如图所示,其中吸附在催化剂表面的物种用*表示。下列说法正确的是
A.Pd、Rh作催化剂时HCOOH分解产生 的 的 相同 相同 |
B.反应 在Pd和Rh表面进行时均为放热过程 在Pd和Rh表面进行时均为放热过程 |
C.HCOOH吸附在催化剂表面的过程 |
D.反应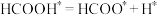 对总反应的速率影响相对较大 对总反应的速率影响相对较大 |
您最近一年使用:0次
2022-03-10更新
|
203次组卷
|
3卷引用:宁夏石嘴山市平罗中学2021-2022学年高二下学期第一次月考化学试题
名校
解题方法
4 . 某化学反应2A(g) B(g)+D(g)在四种不同条件下的恒容密闭容器中进行,B、D的起始浓度均为0,反应物A的浓度随反应时间的变化情况如下表所示:
B(g)+D(g)在四种不同条件下的恒容密闭容器中进行,B、D的起始浓度均为0,反应物A的浓度随反应时间的变化情况如下表所示:
下列说法错误的是
 B(g)+D(g)在四种不同条件下的恒容密闭容器中进行,B、D的起始浓度均为0,反应物A的浓度随反应时间的变化情况如下表所示:
B(g)+D(g)在四种不同条件下的恒容密闭容器中进行,B、D的起始浓度均为0,反应物A的浓度随反应时间的变化情况如下表所示:实验 序号 | 浓度/mol·L-1 温度/°C | 时间/min | ||||||
| 0 | 10 | 20 | 30 | 40 | 50 | 60 | ||
| I | 800 | 1.00 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| II | 800 | 1.00 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| III | 800 | c | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| IV | 820 | 1.00 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
| A.实验I中10~20min内的平均反应速率v(B)=0.013mol·L-1·min-1 |
| B.实验II与实验I条件不同,可能是使用了催化剂 |
| C.实验III中c=1.20 |
| D.比较实验I和实验IV可知,该反应为吸热反应 |
您最近一年使用:0次
2022-03-10更新
|
155次组卷
|
3卷引用:宁夏石嘴山市平罗中学2021-2022学年高二下学期第一次月考化学试题
5 . 在R存在下,某反应 分两步进行:①
分两步进行:①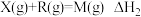 ,②
,②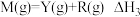 ,其能量变化与反应历程的关系如图所示。
,其能量变化与反应历程的关系如图所示。
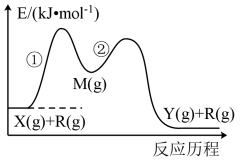
下列说法正确的是
 分两步进行:①
分两步进行:①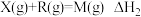 ,②
,②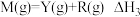 ,其能量变化与反应历程的关系如图所示。
,其能量变化与反应历程的关系如图所示。
下列说法正确的是
A. 、 、 、 、 都小于0 都小于0 | B.反应①的活化能小于反应② |
| C.反应②决定总反应的反应速率 | D.R是总反应的催化剂 |
您最近一年使用:0次
2022-02-25更新
|
206次组卷
|
4卷引用:宁夏石嘴山市平罗中学2021-2022学年高二下学期第一次月考化学试题
名校
解题方法
6 . 小李同学采用如图所示的实验装置测定锌与稀硫酸反应的速率,取1g锌粒与20mL0.5mol·L-1的硫酸进行反应,测得不同时刻反应生成的H2的体积(已折算为标准状况)如表。下列说法正确的是


| t/s | 0 | 5 | 10 | 15 | 20 | 25 |
| V(H2)/mL | 0.0 | 14.6 | 34.5 | 44.8 | 52.2 | 56.9 |
| A.反应结束时锌粒无剩余 |
| B.锌与稀硫酸反应初期速率逐渐加快,后又变慢 |
| C.应用锌粉代替锌粒进行实验,以节约实验时间 |
| D.假设溶液的体积不变,10~25s内的平均反应速率v(H2SO4)=0.02mol·L-1·min-1 |
您最近一年使用:0次
2022-02-15更新
|
395次组卷
|
6卷引用:宁夏石嘴山市平罗中学2021-2022学年高二下学期第一次月考化学试题
宁夏石嘴山市平罗中学2021-2022学年高二下学期第一次月考化学试题河南省部分名校大联考2021-2022学年高二上学期期末考试化学试题河南省豫北名校2021-2022学年高二下学期4月份教学质量检测化学试题(已下线)实验02 定性与定量研究影响化学反应速率的因素-【同步实验课】2023-2024学年高二化学教材实验大盘点(人教版2019选择性必修1)【精品卷】2.1.1 化学反应速率课堂例题-人教版2023-2024学年选择性必修1(已下线)寒假作业02 化学反应速率-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)
名校
7 . 分析图象是学习化学的基本能力。在密闭容器中进行反应: ,下列能正确表示该反应有关物理量变化规律的是
,下列能正确表示该反应有关物理量变化规律的是
 ,下列能正确表示该反应有关物理量变化规律的是
,下列能正确表示该反应有关物理量变化规律的是A. | B.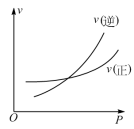 |
C.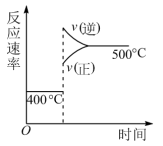 | D. |
您最近一年使用:0次
2022-01-08更新
|
231次组卷
|
3卷引用:宁夏青铜峡市高级中学2021-2022学年高二下学期开学考试化学试题
名校
解题方法
8 . 下列实验操作、现象和所得到的结论都正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 用坩埚钳夹住一小块用砂纸打磨过的铝箔,在酒精灯上加热,铝箔熔化并滴落 | 金属铝的熔点较低 |
| B | 相同条件下,在两支试管中各取4mL0.1mol∙L−1KMnO4,分别加入2mL0.1mol∙L−1H2C2O4和2mL0.01mol∙L−1H2C2O4,加入2mL0.1mol∙L−1H2C2O4溶液褪色较快 | 浓度越大,化学反应速率越快 |
| C | 向某溶液中滴加K3[Fe(CN)6]溶液,产生蓝色沉淀 | 原溶液中有Fe2+,无Fe3+ |
| D | 将浓硫酸滴入蔗糖中并搅拌,得到黑色蓬松的“黑面包”并产生有刺激性气味的气体 | 该过程体现了浓硫酸的脱水性和强氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-01-01更新
|
275次组卷
|
2卷引用:宁夏平罗中学2022-2023学年高二下学期期末考试(重点班)化学试题
名校
解题方法
9 . 化学反应的速率和限度对人类生产生活有重要的意义。
(1)已知Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O。甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响,设计实验如表(所取溶液体积均为2mL):
①上述实验中溶液最先变浑浊的是___________ (填实验编号,下同)。
②控制变量是科学研究的重要方法,为探究浓度对化学反应速率的影响,应选择___________
(2)在10 L的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
请回答:
①该反应的化学平衡常数表达式为K =___________ 。
②该反应为___________ (填“吸热”或“放热”)反应。
③能说明该反应达到化学平衡状态的是___________ (填字母)。
a.容器中压强不变 b.混合气体中 c(CO)不变
c.υ正(H2)=υ逆(H2O) d.c(CO2)=c(CO)
④某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为___________ ℃。
(1)已知Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O。甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响,设计实验如表(所取溶液体积均为2mL):
| 实验编号 | 温度/℃ | c(Na2S2O3)/mol·L-1 | c(H2SO4)/mol·L-1 |
| Ⅰ | 25 | 0.1 | 0.1 |
| Ⅱ | 25 | 0.2 | 0.1 |
| Ⅲ | 50 | 0.2 | 0.1 |
①上述实验中溶液最先变浑浊的是
②控制变量是科学研究的重要方法,为探究浓度对化学反应速率的影响,应选择
(2)在10 L的密闭容器中,进行如下化学反应:CO2(g)+H2(g)
 CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
请回答:
①该反应的化学平衡常数表达式为K =
②该反应为
③能说明该反应达到化学平衡状态的是
a.容器中压强不变 b.混合气体中 c(CO)不变
c.υ正(H2)=υ逆(H2O) d.c(CO2)=c(CO)
④某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为
您最近一年使用:0次
名校
解题方法
10 . 今年9月24日,中科院的科研人员在线发表成果宣布创制了一条利用二氧化碳和电能人工合成淀粉的路线(ASAP路线):通过光伏发电电解水产生氢气,然后通过催化剂利用氢气和二氧化碳生成甲醇,使用多种优选的酶逐步将甲醇最后转化为淀粉。1立方米生物反应器年产淀粉量相当于5亩土地玉米种植的淀粉产量。下列说法错误的是
| A.ASAP路线体现了光能—电能—化学能的转变 |
| B.催化剂可以提高氢气和二氧化碳的平衡转化率 |
| C.酶在合成路线中使各步化学反应更容易发生 |
| D.ASAP路线生产在未来的发展具有广阔前景 |
您最近一年使用:0次
2021-12-06更新
|
195次组卷
|
7卷引用:宁夏永宁县永宁中学2021-2022学年高二上学期期末考试化学试题



