解题方法
1 . 氨是一种重要的化工原料,合成氨工艺在不断的探索和优化,已知:
(1)工业合成氨的热化学方程式是___________ 。
(2)在合成氨过程中,需要不断分离出氨的原因为___________ 。
a.有利于平衡正向移动 b.防止催化剂中毒 c.改变反应的活化能
德国化学家埃特尔对工业合成氨的机理进行了实证研究获得2007年诺贝尔化学奖。在某一温度时,各步反应能量变化如下图所示(*代表吸附中心):

(3)反应历程中决速步骤反应的化学方程式是___________ 。
(4)合成氨工艺全球年均消耗能源3.5亿吨,占能源供应总量的1%以上;排放 超过4亿吨,占排放总量的约1.6%。请从分子结构角度解释工业合成氨的条件苛刻、耗能巨大的原因
超过4亿吨,占排放总量的约1.6%。请从分子结构角度解释工业合成氨的条件苛刻、耗能巨大的原因___________ 。
(5)针对合成氨工业中高耗能问题,中国科学家研制了一种新型催化剂,将合成氨温度、压强降低到350℃、1MPa,从反应机理角度分析新型催化剂降低能耗的原因是___________ 。
(6)针对合成氨中 大量排放问题,某研究团队提出利用金属锂元素合成氨,流程如下图所示。
大量排放问题,某研究团队提出利用金属锂元素合成氨,流程如下图所示。

①冶炼金属锂的化学方程式是___________ 。
② 合成氨过程中发生非氧化还原反应,此步反应的化学方程式是
合成氨过程中发生非氧化还原反应,此步反应的化学方程式是___________ 。此方案中可循环利用的物质是___________ 。
| 化学键 | N≡N | H-H | N-H |
键能/ | 946 | 436 | 391 |
(1)工业合成氨的热化学方程式是
(2)在合成氨过程中,需要不断分离出氨的原因为
a.有利于平衡正向移动 b.防止催化剂中毒 c.改变反应的活化能
德国化学家埃特尔对工业合成氨的机理进行了实证研究获得2007年诺贝尔化学奖。在某一温度时,各步反应能量变化如下图所示(*代表吸附中心):

(3)反应历程中决速步骤反应的化学方程式是
(4)合成氨工艺全球年均消耗能源3.5亿吨,占能源供应总量的1%以上;排放
 超过4亿吨,占排放总量的约1.6%。请从分子结构角度解释工业合成氨的条件苛刻、耗能巨大的原因
超过4亿吨,占排放总量的约1.6%。请从分子结构角度解释工业合成氨的条件苛刻、耗能巨大的原因(5)针对合成氨工业中高耗能问题,中国科学家研制了一种新型催化剂,将合成氨温度、压强降低到350℃、1MPa,从反应机理角度分析新型催化剂降低能耗的原因是
(6)针对合成氨中
 大量排放问题,某研究团队提出利用金属锂元素合成氨,流程如下图所示。
大量排放问题,某研究团队提出利用金属锂元素合成氨,流程如下图所示。
①冶炼金属锂的化学方程式是
②
 合成氨过程中发生非氧化还原反应,此步反应的化学方程式是
合成氨过程中发生非氧化还原反应,此步反应的化学方程式是
您最近一年使用:0次
2 . 定温度下,丙烷与 、
、 发生氯化和溴化反应方程式及产物含量如下:
发生氯化和溴化反应方程式及产物含量如下:不正确 的是
 、
、 发生氯化和溴化反应方程式及产物含量如下:
发生氯化和溴化反应方程式及产物含量如下:氯化:2CH3CH2CH3+2Cl2
 +2HCl
+2HCl
溴化:2CH3CH2CH3+2Br2
 +2HBr
+2HBr

A.HCl和HBr的键能差为 |
B.丙烷中仲氢(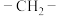 )比伯氢( )比伯氢( )活性强 )活性强 |
| C.升高温度可以提高体系中2-氯丙烷的含量 |
D.反应产物含量主要与 、 、 与 与 反应的活化能相对大小有关 反应的活化能相对大小有关 |
您最近一年使用:0次
解题方法
3 . 在反应原理部分,我们经常以H₂和I₂的反应为例来研究化学反应速率和平衡。
(1)对于反应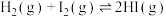 ,提出如下反应历程。
,提出如下反应历程。
第一步 (快速平衡)
(快速平衡)
第二步 (慢反应)
(慢反应)
其中可近似认为第二步反应不影响第一步的平衡。下列说法正确的是___________ (填字母序号)。
a.反应的中间产物只有I
b.第二步反应活化能较低
c.第二步中 与I的碰撞仅部分有效
与I的碰撞仅部分有效
d.v(第一步的逆反应)<v(第二步的逆反应)
(2)在某一容积为2L的密闭容器内,加入0.8mol的 和0.6mol的
和0.6mol的 ,在一定的条件下发生反应
,在一定的条件下发生反应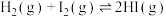
 。反应中各物质的浓度随时间变化情况如图。
。反应中各物质的浓度随时间变化情况如图。

①反应开始至达到平衡时,平均速率
___________ mol/(L·min)(保留3位有效数字,下同)。
② 的转化率
的转化率
___________ 。要提高 转化率,可采取的措施有
转化率,可采取的措施有___________ (答出两条即可)。
③该反应的化学平衡常数表达式
___________ ,若升高温度,K___________ (填“增大”“减小”或“不变”)。
(1)对于反应
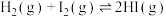 ,提出如下反应历程。
,提出如下反应历程。第一步
 (快速平衡)
(快速平衡)第二步
 (慢反应)
(慢反应)其中可近似认为第二步反应不影响第一步的平衡。下列说法正确的是
a.反应的中间产物只有I
b.第二步反应活化能较低
c.第二步中
 与I的碰撞仅部分有效
与I的碰撞仅部分有效d.v(第一步的逆反应)<v(第二步的逆反应)
(2)在某一容积为2L的密闭容器内,加入0.8mol的
 和0.6mol的
和0.6mol的 ,在一定的条件下发生反应
,在一定的条件下发生反应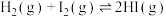
 。反应中各物质的浓度随时间变化情况如图。
。反应中各物质的浓度随时间变化情况如图。
①反应开始至达到平衡时,平均速率

②
 的转化率
的转化率
 转化率,可采取的措施有
转化率,可采取的措施有③该反应的化学平衡常数表达式

您最近一年使用:0次
解题方法
4 . 以某金属氧化物(用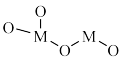 表示)为催化剂,同时消除
表示)为催化剂,同时消除 、NO污染的反应历程如图所示。下列说法错误的是
、NO污染的反应历程如图所示。下列说法错误的是
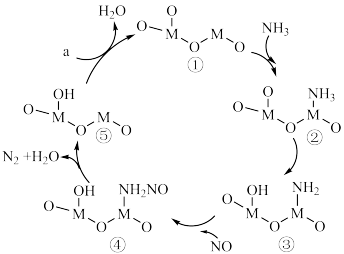
 表示)为催化剂,同时消除
表示)为催化剂,同时消除 、NO污染的反应历程如图所示。下列说法错误的是
、NO污染的反应历程如图所示。下列说法错误的是
A.在相同条件下, 比NO更易与M成键 比NO更易与M成键 |
| B.上述反应历程涉及极性键的断裂和形成 |
| C.通过定量测定发现,反应历程中物质④含量最少,其可能原因是③→④为快反应 |
D.若a为常见非金属单质,则⑤→①的反应可能为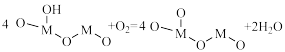 |
您最近一年使用:0次
2023-11-22更新
|
94次组卷
|
2卷引用:江西省2024届高三上学期11 月一轮总复习调研测试化学试题
解题方法
5 .  在一定条件下发生反应的能量变化如图所示,请根据所学知识回答下列问题:
在一定条件下发生反应的能量变化如图所示,请根据所学知识回答下列问题:
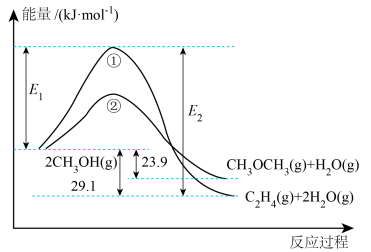
(1)写出图中所示反应①、反应②的热化学方程式:___________ 、___________ 。
(2) 为反应
为反应___________ (填“①”或“②”)___________ (填“正”或“逆”)反应的活化能。由图可知,若在一定条件下,某容器中同时发生反应①、反应②,则开始时,___________ [填“ ”或“
”或“ ”]的生成速率快。
”]的生成速率快。
(3) 与
与 为
为___________ (填“同素异形体”、“同分异构体”或“同系物”)。
(4)若 同时发生反应①、反应②,当
同时发生反应①、反应②,当 完全转化为
完全转化为 和
和 后,测得反应放出的总热量为
后,测得反应放出的总热量为 。则反应产物中
。则反应产物中 和
和 的物质的量分别为
的物质的量分别为___________ mol、___________ mol。
 在一定条件下发生反应的能量变化如图所示,请根据所学知识回答下列问题:
在一定条件下发生反应的能量变化如图所示,请根据所学知识回答下列问题:
(1)写出图中所示反应①、反应②的热化学方程式:
(2)
 为反应
为反应 ”或“
”或“ ”]的生成速率快。
”]的生成速率快。(3)
 与
与 为
为(4)若
 同时发生反应①、反应②,当
同时发生反应①、反应②,当 完全转化为
完全转化为 和
和 后,测得反应放出的总热量为
后,测得反应放出的总热量为 。则反应产物中
。则反应产物中 和
和 的物质的量分别为
的物质的量分别为
您最近一年使用:0次
2023-11-19更新
|
130次组卷
|
2卷引用:广东省湛江市2023-2024学年高二上学期11月期中考试化学试题
名校
6 . 无催化剂作用下,以乙二醛和 为原料制取乙醛酸的可能反应历程如图所承,TS表承过渡态,IM表示中间体。下列说法错误的是
为原料制取乙醛酸的可能反应历程如图所承,TS表承过渡态,IM表示中间体。下列说法错误的是
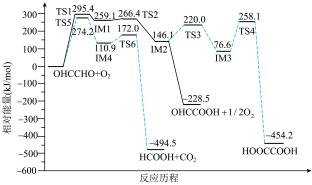
 为原料制取乙醛酸的可能反应历程如图所承,TS表承过渡态,IM表示中间体。下列说法错误的是
为原料制取乙醛酸的可能反应历程如图所承,TS表承过渡态,IM表示中间体。下列说法错误的是
A.乙二醛被 氧化可得3种有机产物 氧化可得3种有机产物 |
| B.反应很短一段时间内,IM4多于IM1 |
| C.乙二醛制乙二酸的最大能垒为181.5kJ/mol |
| D.选择合适的催化剂可提高乙醛酸的选择性 |
您最近一年使用:0次
2023-11-19更新
|
350次组卷
|
3卷引用:湖北省高中名校联盟2024届高三上学期第二次联合测评化学试题
湖北省高中名校联盟2024届高三上学期第二次联合测评化学试题(已下线)题型06 反应热的判断及计算-2024年高考化学答题技巧与模板构建新疆石河子第一中学2023-2024学年高三上学期11月月考化学试题
7 .  时,固体酸分子筛催化乙醇脱水,乙醇的分子间脱水和分子内脱水过程与相对能量变化如图所示:
时,固体酸分子筛催化乙醇脱水,乙醇的分子间脱水和分子内脱水过程与相对能量变化如图所示:不正确 的是
 时,固体酸分子筛催化乙醇脱水,乙醇的分子间脱水和分子内脱水过程与相对能量变化如图所示:
时,固体酸分子筛催化乙醇脱水,乙醇的分子间脱水和分子内脱水过程与相对能量变化如图所示: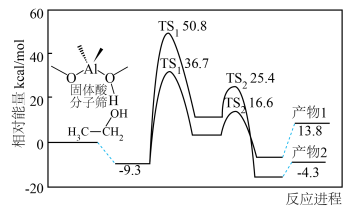
| A.乙醇通过氢键吸附于固体酸分子筛表面并放出热量 |
B.生成产物2的决速步活化能为 |
C.生成产物1的热化学方程式为: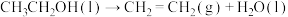 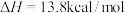 |
| D.升高温度、延长反应时间及选择合适催化剂均可提高产物1的产率 |
您最近一年使用:0次
2023-11-15更新
|
865次组卷
|
5卷引用:浙江省宁波市2023-2024学年高三上学期选考模拟考试化学试题
浙江省宁波市2023-2024学年高三上学期选考模拟考试化学试题2024新东方高二上期末考化学03(已下线)专题05 化学反应与能量(2大题型)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)新疆乌鲁木齐市2024届高三第一次质量监测化学试题(已下线)化学(辽宁卷02)-2024年高考押题预测卷
名校
解题方法
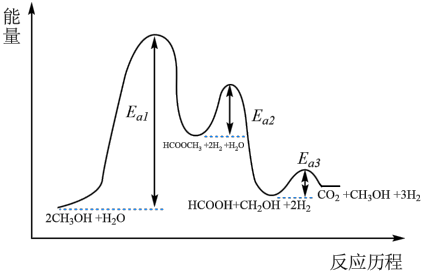
8 . 甲醇水蒸气催化重整是当前制取清洁能源氢气的主要方法,其原理为:CH3OH(g) + H2O(g) CO2(g) + 3H2(g) ΔH,该反应历程如下,写出决速步的化学方程式
CO2(g) + 3H2(g) ΔH,该反应历程如下,写出决速步的化学方程式___________ 。
 CO2(g) + 3H2(g) ΔH,该反应历程如下,写出决速步的化学方程式
CO2(g) + 3H2(g) ΔH,该反应历程如下,写出决速步的化学方程式
您最近一年使用:0次
名校
解题方法
9 . 氨的用途十分泛,如氨是制造硝酸和氮肥的重要原料。工业合成氨是人类科学技术的一项重大突破。回答下列问题:
(1)合成氨反应的历程和能量的变化如图所示,符号“·”可视为催化剂。

在合成氨的基元反应中,决速步骤的活化能为___________ kJ/mol。
(2)在不同条件下进行合成氨反应,下列反应速率由大到小的顺序是___________ (填选项序号)。
①v(N2)=0.5mol/(L·min) ②v(H2)=0.02mol/(L·s)
③v(NH3)=0.4mol/(L·min) ④v(NH3)=0.02mol/(L·s)
(3)对于合成氨反应而言,只控制一个变量,下列图像合理的是___________(填选项字母)。
(4)一定温度下,向2L恒容密闭容器中充入0.4molN2、1.2molH2发生反应,NH3的浓度随时间变化情况如表所示:
0~10min内,用H2表示的平均反应速率为___________ ;实验测得体系平衡时的压强为10MPa,则该反应的平衡常数Kp=___________ MPa-2(用分数表示,Kp为分压表示的平衡常数,分压=总压×体积分数);若维持温度不变,向另一2L恒容密闭容器中充入H2、N2和NH3各4mol时,该反应的v正___________ (填“>”“<”或“=”)v逆。
(1)合成氨反应的历程和能量的变化如图所示,符号“·”可视为催化剂。

在合成氨的基元反应中,决速步骤的活化能为
(2)在不同条件下进行合成氨反应,下列反应速率由大到小的顺序是
①v(N2)=0.5mol/(L·min) ②v(H2)=0.02mol/(L·s)
③v(NH3)=0.4mol/(L·min) ④v(NH3)=0.02mol/(L·s)
(3)对于合成氨反应而言,只控制一个变量,下列图像合理的是___________(填选项字母)。
A.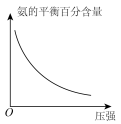 | B.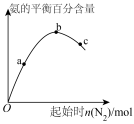 |
C.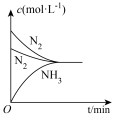 | D.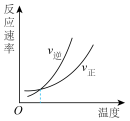 |
| 时间/min | 5 | 10 | 15 | 20 | 25 |
| 浓度/mol/L | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 |
您最近一年使用:0次
名校
解题方法
10 . 甲醛气体具有降解难度大,挥发周期长的特点,对室内环境的危害十分严重。纳米 是目前应用广泛的甲醛降解光催化剂,能够利用其良好的光催化活性对室内甲醛进行净化,其反应机理示意图如图所示。下列有关说法正确的是
是目前应用广泛的甲醛降解光催化剂,能够利用其良好的光催化活性对室内甲醛进行净化,其反应机理示意图如图所示。下列有关说法正确的是

 是目前应用广泛的甲醛降解光催化剂,能够利用其良好的光催化活性对室内甲醛进行净化,其反应机理示意图如图所示。下列有关说法正确的是
是目前应用广泛的甲醛降解光催化剂,能够利用其良好的光催化活性对室内甲醛进行净化,其反应机理示意图如图所示。下列有关说法正确的是
A.甲醛降解过程中存在反应: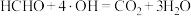 |
B.反应过程中甲醛断裂的共价键一定有 、 、 键 键 |
C. 活性羟基 活性羟基 中含有 中含有 个电子 个电子 |
D.纳米 增大了甲醛氧化分解的活化能,使得反应速率加快 增大了甲醛氧化分解的活化能,使得反应速率加快 |
您最近一年使用:0次
2023-11-13更新
|
54次组卷
|
2卷引用:广东省广州市培英中学2023-2024学年高二上学期期中考试化学试题



