名校
1 . 氮及其化合物在工农业生产中有广泛的应用。请回答下列问题:
(1)氨气是一种重要的工业原料,工业上利用氮气和氢气在一定条件下合成氨气:N2(g)+3H2(g) 2NH3(g) ΔH,该反应过程中的能量变化如图1所示(E1>0,E2>0),图中E1代表的意义是
2NH3(g) ΔH,该反应过程中的能量变化如图1所示(E1>0,E2>0),图中E1代表的意义是___________ ,反应热ΔH的表达式为___________ (用E1,E2表示)

(2)NH3催化还原氮氧化物(SCR)技术是目前应用最广的烟气氮氧化物脱除技术。反应原理如图A所示:

①图B是催化剂Mn和Cr在不同温度下对应的脱氧率,由图综合考虑可知最佳的催化剂和相应的温度分别为___________ 、___________
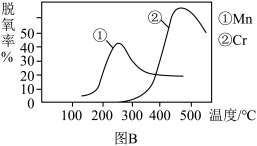
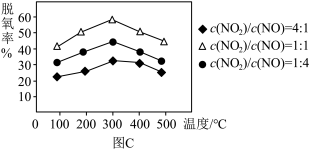
②用Fe做催化剂时,在氨气足量的情况下,不同 对应的脱氧率如图C所示,脱氧效果最佳的
对应的脱氧率如图C所示,脱氧效果最佳的
___________
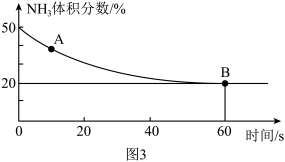
(3)工业上合成尿素的反应:2NH3(g)+CO2(g) H2O(g)+CO(NH2)2(l) ΔH,在一个真空恒容密闭容器中充入CO2和NH3发生上述反应,恒定温度下混合气体中NH3的体积分数如图3所示,则A点的正反应速率v正(CO2)
H2O(g)+CO(NH2)2(l) ΔH,在一个真空恒容密闭容器中充入CO2和NH3发生上述反应,恒定温度下混合气体中NH3的体积分数如图3所示,则A点的正反应速率v正(CO2)___________ B点的逆反应速率v逆(CO2)(填“>”、“<”或“=”),CO2的平衡转化率为___________
(4)尿液也能发电。化学家正在研究尿素动力燃料电池,用这种电池直接除去城市废水中的尿素,既能产生净化的水又能发电,其工作原理为2CO(NH2)+3O2=2N2+2CO2+4H2O。电解质溶液为硫酸,则负极的电极反应式为___________ 。
(1)氨气是一种重要的工业原料,工业上利用氮气和氢气在一定条件下合成氨气:N2(g)+3H2(g)
 2NH3(g) ΔH,该反应过程中的能量变化如图1所示(E1>0,E2>0),图中E1代表的意义是
2NH3(g) ΔH,该反应过程中的能量变化如图1所示(E1>0,E2>0),图中E1代表的意义是
(2)NH3催化还原氮氧化物(SCR)技术是目前应用最广的烟气氮氧化物脱除技术。反应原理如图A所示:

①图B是催化剂Mn和Cr在不同温度下对应的脱氧率,由图综合考虑可知最佳的催化剂和相应的温度分别为

②用Fe做催化剂时,在氨气足量的情况下,不同
 对应的脱氧率如图C所示,脱氧效果最佳的
对应的脱氧率如图C所示,脱氧效果最佳的

(3)工业上合成尿素的反应:2NH3(g)+CO2(g)
 H2O(g)+CO(NH2)2(l) ΔH,在一个真空恒容密闭容器中充入CO2和NH3发生上述反应,恒定温度下混合气体中NH3的体积分数如图3所示,则A点的正反应速率v正(CO2)
H2O(g)+CO(NH2)2(l) ΔH,在一个真空恒容密闭容器中充入CO2和NH3发生上述反应,恒定温度下混合气体中NH3的体积分数如图3所示,则A点的正反应速率v正(CO2)
(4)尿液也能发电。化学家正在研究尿素动力燃料电池,用这种电池直接除去城市废水中的尿素,既能产生净化的水又能发电,其工作原理为2CO(NH2)+3O2=2N2+2CO2+4H2O。电解质溶液为硫酸,则负极的电极反应式为
您最近一年使用:0次
名校
2 . 化学与科学、技术、社会和环境密切相关。下列说法错误的是
| A.工业生产中使用催化剂不能改变化学反应的焓变 |
B.已知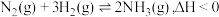 ,工业上采用高温提高 ,工业上采用高温提高 的转化率 的转化率 |
C.工业上用 合成 合成 ,增加氧气的量可提高 ,增加氧气的量可提高 的利用率 的利用率 |
D.工业上 ,高温下能自发进行 ,高温下能自发进行 |
您最近一年使用:0次
2023-12-14更新
|
92次组卷
|
2卷引用:广东省江门市新会第一中学2023-2024学年高二上学期期中考试化学试题
名校
3 . 某同学为了探究哪些因素会影响反应速率,设计了以下表格实验,
请回答下列问题:
(1)写出实验①发生的化学方程式___________ 。
(2)a =___________ ,理由是___________ 。
(3)实验①③的实验目的是___________ 。
(4)b =___________ ,c = ___________ ;通过实验①④,可以得到的结论是___________ 。
(5)某同学在50 mL一定浓度的H2O2溶液中加入一定量的二氧化锰,放出气体的体积(标准状况下)与反应时间的关系如下图所示,分析判断OE、EF、FG三段中,___________ 段化学反应速率最快。

| 实验序号 | 10% H2O2溶液/mL | 蒸馏水/mL | 温度/℃ | 催化剂 |
| ① | 10 | 0 | 25 | 1滴FeCl3 |
| ② | 5 | a | 25 | 1滴FeCl3 |
| ③ | 10 | 0 | 40 | 1滴FeCl3 |
| ④ | b | c | 25 | 无 |
(1)写出实验①发生的化学方程式
(2)a =
(3)实验①③的实验目的是
(4)b =
(5)某同学在50 mL一定浓度的H2O2溶液中加入一定量的二氧化锰,放出气体的体积(标准状况下)与反应时间的关系如下图所示,分析判断OE、EF、FG三段中,

您最近一年使用:0次
名校
4 . 在化工生产中,调控反应条件很重要。下列能提高合成氨反应速率的是
| A.使用空气做反应物 | B.减小c(H2) |
| C.使用合适的催化剂 | D.降低温度 |
您最近一年使用:0次
2023-03-08更新
|
653次组卷
|
3卷引用:广东省开平市忠源纪念中学2022-2023学年高一下学期4月期中考试(合格考)化学试题
解题方法
5 . 下列对有关事实或解释不正确的
| 选项 | 事实 | 解释 |
| A | 用铝粉代替铝片与稀盐酸反应,反应速率加快 | 改用铝粉,固体表面积增大,故反应速率加快 |
| B | 5%的双氧水中加入二氧化锰粉末,分解速率迅速加快 | 降低了反应的焓变,活化分子数增多,有效碰撞增多,速率加快 |
| C | 锌与稀硫酸反应,滴入少量硫酸铜溶液,生成氢气的速率加快 | 锌置换出铜,形成原电池,反应速率加快 |
| D | 密闭容器中反应: ,当温度、压强不变,充入惰性气体,反应速率减慢 ,当温度、压强不变,充入惰性气体,反应速率减慢 | 容器体积增大,反应物浓度减小,反应速率减慢 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-02-07更新
|
293次组卷
|
2卷引用:广东省江门市2022-2023学年高二化学上学期期末调研考试化学试题
名校
解题方法
6 . 二氧化硫的催化氧化是工业制硫酸的基础: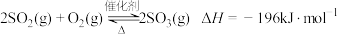 。下列叙述正确的是
。下列叙述正确的是
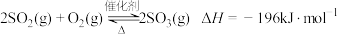 。下列叙述正确的是
。下列叙述正确的是A. 和 和 充分反应能放出 充分反应能放出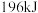 的热量 的热量 |
| B.工业上使用催化剂是通过加快反应速率提高生产效率的 |
C.实际工业选用的温度为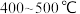 ,其目的是为了提高 ,其目的是为了提高 的平衡转化率 的平衡转化率 |
| D.增大压强,正反应速率增大,逆反应速率减小 |
您最近一年使用:0次
2023-01-10更新
|
302次组卷
|
6卷引用:广东省江门市第一中学2022-2023学年高二上学期期末考试(线上考试)化学试题
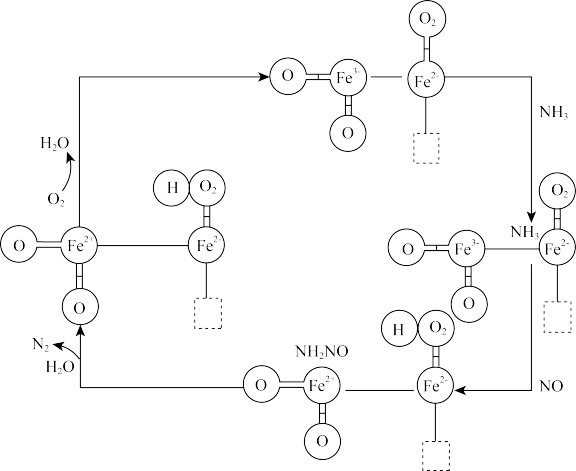
7 . 某科研团队利用缺陷工程(贫氧环境焙烧)制备了含有大量氧缺陷和表面羟基的 ,该
,该 参与如图所示的
参与如图所示的 还原。下列说法正确的是
还原。下列说法正确的是
 ,该
,该 参与如图所示的
参与如图所示的 还原。下列说法正确的是
还原。下列说法正确的是
A. 为该过程的氧化剂 为该过程的氧化剂 |
B.图中总反应可能为 |
| C.整个流程中含铁元素的物质中铁的化合价均相同 |
| D.该催化合成时,溶液的pH越小越好 |
您最近一年使用:0次
2022-12-11更新
|
235次组卷
|
5卷引用:广东省江门市2022-2023学年高三上学期联考化学试题
广东省江门市2022-2023学年高三上学期联考化学试题重庆市好教育联盟2023届高三12月调研考试化学试题河北省唐山市部分学校2022-2023学年高三上学期12月月考化学试题吉林省部分学校2022-2023学年高三上学期12月联考化学试题(已下线)广东省广州市天河区2023届高三二模化学试题变式题(选择题6-10)
8 . 已知试剂1为镍-膦配合物,其在某一偶联反应中的催化机理如下图所示。

下列说法错误的是

下列说法错误的是
A. 的电子排布式为 的电子排布式为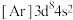 |
| B.1与2发生的是取代反应 |
| C.4和6都是反应的中间体 |
D.图中的总过程可表示为:RMgX+R′-X R′-R+XMgX R′-R+XMgX |
您最近一年使用:0次
2022-03-17更新
|
354次组卷
|
4卷引用:广东省江门市第一中学2022-2023学年高二下学期3月月考化学试题
名校
9 . 我国科学家在国际上首次实现二氧化碳到淀粉的全合成,对实现“碳中和”与“碳达峰”有重要意义,下列说法正确的是
| A.全合成过程一定包含能量的变化 |
| B.使用催化剂能提升全合成过程的平衡转化率 |
| C.以相同反应物合成淀粉,人工合成与自然合成两种途径反应热不相同 |
| D.全合成的第一步为吸热反应,则反应物的键能总和低于生成物的键能总和 |
您最近一年使用:0次
2022-01-19更新
|
326次组卷
|
8卷引用:广东省 江门市棠下中学2023-2024学年高二上学期期中考试化学试题
解题方法
10 . 氮及其化合物在科研及生产中均有重要的应用。根据已学知识回答下列问题:
(1)氮气与氧气在一定压强和 条件下发生催化氧化反应时,可发生不同反应,
条件下发生催化氧化反应时,可发生不同反应,
反应i: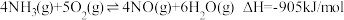
反应ii: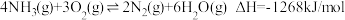
①该条件下氮气被氧气氧化为 的热化学方程式为
的热化学方程式为___________ 。
②反应i与反应ii有关物质产率与温度的关系如图甲。下列说法正确的是__ (填序号)。
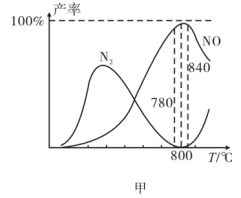
A.氨催化氧化生成 时,温度应控制在
时,温度应控制在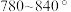
B.提高物料比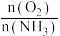 的值,主要目的是提高反应速率
的值,主要目的是提高反应速率
C.对反应加压可提高反应物平衡转化率
D.高于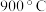 时
时 的产率降低的原因可能与高温下催化剂的活性降低有关
的产率降低的原因可能与高温下催化剂的活性降低有关
(2)有毒气体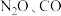 在上
在上 催化下发生反应:
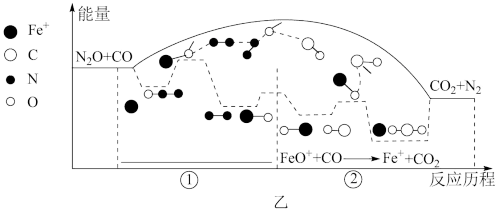
催化下发生反应: 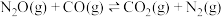 ,其反应分两步进行(如图乙所示),写出其中反应①的化学方程式:
,其反应分两步进行(如图乙所示),写出其中反应①的化学方程式:___________ 。总反应速率的快慢主要由其中一步反应决定,该反应是___________ (填“①”或“②”)。
(3)某科研小组向一密闭容器中通入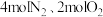 ,控制适当条件使其发生如下反应:
,控制适当条件使其发生如下反应: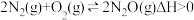 ,测出
,测出 的某种平衡物理量X(体积百分数或转化率)随着温度、压强变化而变化的情况如图丙所示。
的某种平衡物理量X(体积百分数或转化率)随着温度、压强变化而变化的情况如图丙所示。
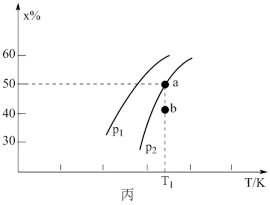
①X___________ (填“能”或“不能”)表示平衡体系中 的体积頁分数;
的体积頁分数; 的相对大小关系为
的相对大小关系为
___________  (填“>”=”或“<”)。
(填“>”=”或“<”)。
②若 ,计算
,计算 时的平衡常数
时的平衡常数 (
( 为用分压表示的平衡常数),写出计算过程
为用分压表示的平衡常数),写出计算过程______ 。
(1)氮气与氧气在一定压强和
 条件下发生催化氧化反应时,可发生不同反应,
条件下发生催化氧化反应时,可发生不同反应,反应i:
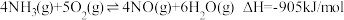
反应ii:
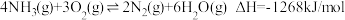
①该条件下氮气被氧气氧化为
 的热化学方程式为
的热化学方程式为②反应i与反应ii有关物质产率与温度的关系如图甲。下列说法正确的是

A.氨催化氧化生成
 时,温度应控制在
时,温度应控制在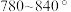
B.提高物料比
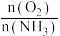 的值,主要目的是提高反应速率
的值,主要目的是提高反应速率C.对反应加压可提高反应物平衡转化率
D.高于
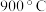 时
时 的产率降低的原因可能与高温下催化剂的活性降低有关
的产率降低的原因可能与高温下催化剂的活性降低有关(2)有毒气体
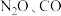 在上
在上 催化下发生反应:
催化下发生反应: 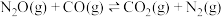 ,其反应分两步进行(如图乙所示),写出其中反应①的化学方程式:
,其反应分两步进行(如图乙所示),写出其中反应①的化学方程式:
(3)某科研小组向一密闭容器中通入
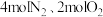 ,控制适当条件使其发生如下反应:
,控制适当条件使其发生如下反应: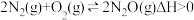 ,测出
,测出 的某种平衡物理量X(体积百分数或转化率)随着温度、压强变化而变化的情况如图丙所示。
的某种平衡物理量X(体积百分数或转化率)随着温度、压强变化而变化的情况如图丙所示。
①X
 的体积頁分数;
的体积頁分数; 的相对大小关系为
的相对大小关系为
 (填“>”=”或“<”)。
(填“>”=”或“<”)。②若
 ,计算
,计算 时的平衡常数
时的平衡常数 (
( 为用分压表示的平衡常数),写出计算过程
为用分压表示的平衡常数),写出计算过程
您最近一年使用:0次



