名校
解题方法
1 . 羟醛缩合反应常用于增长碳链。脯氨酸(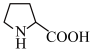 )催化某羟醛缩合反应的机理如图所示。下列说法错误的是
)催化某羟醛缩合反应的机理如图所示。下列说法错误的是
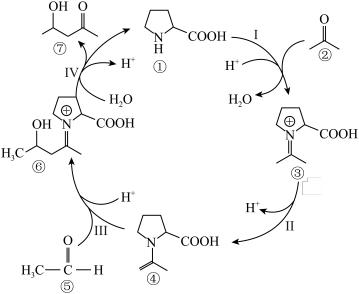
A.步骤Ⅰ中涉及 键和 键和 键的断裂和形成 键的断裂和形成 |
| B.物质①、③、④、⑥中N原子的杂化方式相同 |
C.该过程的总方程式为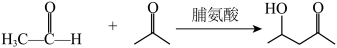 |
D.若用含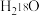 的溶剂和 的溶剂和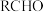 、 、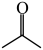 进行该反应,可能得到 进行该反应,可能得到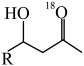 |
您最近一年使用:0次
2 . 室温下,探究0.1 mol·L-1 FeCl3溶液的性质,下列实验方案能达到探究目的的是
| 选项 | 探究方案 | 探究目的 |
| A | 向两支试管中分别加入5 mL 5%的H2O2溶液,再向两支试管中滴入3滴浓度均为0.1 mol·L-1 的FeCl3和CuSO4,观察产生气体的速率 | 比较Fe3+和Cu2+的催化效率 |
| B | 向2 mL 0.1 mol·L-1 FeCl3溶液中加入1 mL 0.1 mol·L-1 KI溶液,充分振荡后滴加KSCN溶液,观察颜色变化 | 2Fe3++2I-=2Fe2++I2是否为可逆反应 |
| C | 向苯酚溶液中滴加几滴0.1 mol·L-1 FeCl3溶液,溶液呈紫色 | FeCl3与苯酚发生了氧化还原反应 |
| D | 将5 mL 0.1 mol·L-1 FeCl3溶液和15 mL 0.1 mol·L-1 NaHCO3溶液混合,生成红褐色沉淀和气体 | Fe3+与 发生了双水解反应 发生了双水解反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7日内更新
|
166次组卷
|
2卷引用:江苏省连云港高级中学2023-2024学年高三下学期4月期中考试化学试题
名校
3 . 常温常压下利用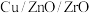 催化剂实现二氧化碳加氢制甲醇的反应历程和能量变化图如下(其中吸附在催化剂表面上的粒子用*标注):
催化剂实现二氧化碳加氢制甲醇的反应历程和能量变化图如下(其中吸附在催化剂表面上的粒子用*标注):
 催化剂实现二氧化碳加氢制甲醇的反应历程和能量变化图如下(其中吸附在催化剂表面上的粒子用*标注):
催化剂实现二氧化碳加氢制甲醇的反应历程和能量变化图如下(其中吸附在催化剂表面上的粒子用*标注):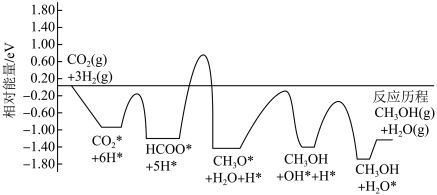
| A.反应过程中只存在极性键的断裂和形成 |
B.使用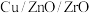 催化剂,降低了反应的 催化剂,降低了反应的 |
C.转化历程有四个基元反应,决速步为: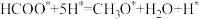 |
D.寻找高效催化剂;有利于 的回收利用,使该反应原子利用率达到100% 的回收利用,使该反应原子利用率达到100% |
您最近一年使用:0次
4 . 已知催化剂 对吸热反应
对吸热反应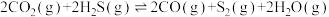 具有高选择性,通过理论计算得到反应的主要路径如下图所示,下列说法错误的是
具有高选择性,通过理论计算得到反应的主要路径如下图所示,下列说法错误的是
 对吸热反应
对吸热反应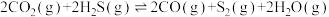 具有高选择性,通过理论计算得到反应的主要路径如下图所示,下列说法错误的是
具有高选择性,通过理论计算得到反应的主要路径如下图所示,下列说法错误的是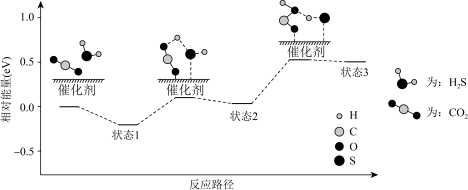
A.加入催化剂 ,会加快该反应的化学反应速率 ,会加快该反应的化学反应速率 |
B.反应过程中当 和 和 的浓度比不变的时候,该反应达到了化学平衡状态 的浓度比不变的时候,该反应达到了化学平衡状态 |
C.状态2可表示为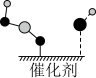 |
| D.若将该反应生成物中水的状态改成液态,那么反应前后的能量变化数值偏大 |
您最近一年使用:0次
名校
5 . 金表面发生分解反应: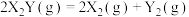 ,其速率方程为
,其速率方程为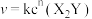 ,已知部分信息如下:
,已知部分信息如下: 为速率常数,只与催化剂、温度、固体接触面积有关;在某温度下,实验测得生成物浓度与时间变化的关系如下表所示:
为速率常数,只与催化剂、温度、固体接触面积有关;在某温度下,实验测得生成物浓度与时间变化的关系如下表所示:
下列叙述不正确的是
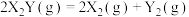 ,其速率方程为
,其速率方程为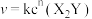 ,已知部分信息如下:
,已知部分信息如下: 为速率常数,只与催化剂、温度、固体接触面积有关;在某温度下,实验测得生成物浓度与时间变化的关系如下表所示:
为速率常数,只与催化剂、温度、固体接触面积有关;在某温度下,实验测得生成物浓度与时间变化的关系如下表所示:t/min c/(mol·L-1) | 0 | 20 | 40 | 60 | 80 | 100 |
| X2Y | 0.100 | 0.040 | 0.020 | 0 | ||
| X2 | 0 | 0.020 | ||||
| Y2 | 0 | 0.020 |
| A.提高反应物浓度,反应速率不变 |
B. |
C.其他条件不变,若 起始浓度为 起始浓度为 ,则反应物浓度减半所需时间为 ,则反应物浓度减半所需时间为 |
D.当升高温度,反应 时 时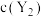 可能小于 可能小于 |
您最近一年使用:0次
名校
解题方法
6 . 氮是自然界各种生物体生命活动不可缺少的重要元素。
(1)下列说法中,不正确的是___________ (填字母序号)。
a.氮原子的最外层有5个电子,氮气分子中存在氮氮三键,常温下化学性质稳定
b.氮元素位于元素周期表的第二周期,第VA族
c.氮元素的最低化合价为-3价,最高化合价为+5价
d.根据元素周期律推测,氮化硅的化学式为SiN
(2)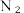 分子不能被大多数动植物直接吸收。植物吸收和利用效果最好的是
分子不能被大多数动植物直接吸收。植物吸收和利用效果最好的是 (铵根离子),将
(铵根离子),将 转化为
转化为  需与
需与___________ (填“酸”或“碱”)反应。写出该反应离子方程式:___________ 和 的电子式
的电子式___________ 。
(3)大自然通过闪电可将空气中的氮气转化为含氮化合物,从而实现自然固氮。该过程中生成的含氮化合物是___________ 。
(4)我国科研团队借助一种固体催化剂(LDH),在常温常压和可见光作用下实现了人工固氮。其过程如图所示。写出该过程中反应的化学方程式:___________ 。___________ 。
(6)上述流程中,需要使用催化剂的反应是___________ (填“Ⅰ”、“Ⅱ”或“Ⅲ”),使用催化剂的目的是___________ 。
(7)工业合成氨反应为: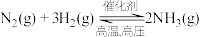 对其描述正确的是___________(填序号)。
对其描述正确的是___________(填序号)。
(8)采用上述工业制硝酸的流程,若 (已折算成标准状况的气体体积)完全反应生成硝酸,理论上生成硝酸的质量为
(已折算成标准状况的气体体积)完全反应生成硝酸,理论上生成硝酸的质量为___________ g。
(1)下列说法中,不正确的是
a.氮原子的最外层有5个电子,氮气分子中存在氮氮三键,常温下化学性质稳定
b.氮元素位于元素周期表的第二周期,第VA族
c.氮元素的最低化合价为-3价,最高化合价为+5价
d.根据元素周期律推测,氮化硅的化学式为SiN
(2)
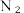 分子不能被大多数动植物直接吸收。植物吸收和利用效果最好的是
分子不能被大多数动植物直接吸收。植物吸收和利用效果最好的是 (铵根离子),将
(铵根离子),将 转化为
转化为  需与
需与 的电子式
的电子式(3)大自然通过闪电可将空气中的氮气转化为含氮化合物,从而实现自然固氮。该过程中生成的含氮化合物是
(4)我国科研团队借助一种固体催化剂(LDH),在常温常压和可见光作用下实现了人工固氮。其过程如图所示。写出该过程中反应的化学方程式:
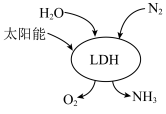
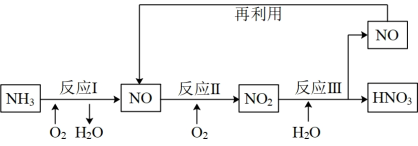
(6)上述流程中,需要使用催化剂的反应是
(7)工业合成氨反应为:
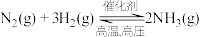 对其描述正确的是___________(填序号)。
对其描述正确的是___________(填序号)。A.在上述条件下,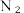 能全部转化为 能全部转化为 |
| B.若其他条件一定时,增大氮气的浓度,可增大反应速率 |
| C.达到平衡时,体系中各物质的浓度一定相等 |
| D.当正反应速率等于逆反应速率且不为零时,该反应达到平衡状态 |
(8)采用上述工业制硝酸的流程,若
 (已折算成标准状况的气体体积)完全反应生成硝酸,理论上生成硝酸的质量为
(已折算成标准状况的气体体积)完全反应生成硝酸,理论上生成硝酸的质量为
您最近一年使用:0次
7 . 根据实验操作和现象,对应结论正确的是
选项 | 实验操作 | 现象 | 结论 |
A | 将 固体粉末加入过量NaOH溶液,搅拌 固体粉末加入过量NaOH溶液,搅拌 | 固体完全溶解,形成无色溶液 |  既体现酸性又体现碱性 既体现酸性又体现碱性 |
B | 用洁净的铂丝蘸取某溶液在酒精灯火焰灼烧 | 火焰呈黄色 | 该溶液是钠的盐溶液 |
C | 将银和硝酸银溶液与铜和硫酸铜稀溶液组成原电池,连通后一段时间 | 银表面有金属沉积,铜附近溶液蓝色变深 | 铜的金属性比银强 |
D | 向两支均盛有5mL 10%  溶液的试管中,分别加入0.1 溶液的试管中,分别加入0.1 的 的 溶液和0.1 溶液和0.1  溶液 溶液 | 产生气泡,加入 溶液的试管中产生气泡快 溶液的试管中产生气泡快 |  比 比 的催化效果更好 的催化效果更好 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 下列实验目的或结论及操作、现象均正确的是
选项 | 实验操作及现象 | 目的或结论 |
A | 称取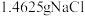 ,置于 ,置于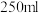 容量瓶中,加水至刻度线 容量瓶中,加水至刻度线 | 配制 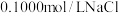 溶液 溶液 |
B | 向某溶液中加入浓 溶液并加热,能产生使湿润的红色石蕊试纸变蓝的气体 溶液并加热,能产生使湿润的红色石蕊试纸变蓝的气体 | 溶液中含有 |
C | 向 溶液中同时通入 溶液中同时通入 和 和 ,产生白色沉淀 ,产生白色沉淀 |  将 将 氧化成了 氧化成了 |
D | 向体积和浓度均相同的 中分别加入等体积的 中分别加入等体积的 的 的 和 和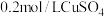 溶液 溶液 | 验证 、 、 对 对 催化分解速率的影响 |
| A. | B.B | C.C | D.D |
您最近一年使用:0次
9 . 压强一定,向四个体积相同的密闭容器中分别充入一定量的N2和H2进行合成氨的反应,开始反应时,按反应速率由大到小的顺序排列正确的是
甲:500℃,2molN2和3molH2反应
乙:500℃,催化剂,2molN2和3molH2反应
丙:450℃,1molN2和3molH2反应
丁:500℃,1molN2和3molH2反应
甲:500℃,2molN2和3molH2反应
乙:500℃,催化剂,2molN2和3molH2反应
丙:450℃,1molN2和3molH2反应
丁:500℃,1molN2和3molH2反应
| A.乙、甲、丁、丙 | B.乙、甲、丙、丁 |
| C.甲、乙、丙、丁 | D.丁、丙、乙、甲 |
您最近一年使用:0次
名校
10 . 近年来,利用半导体光催化还原氮气制备氨气的实现引起了全世界的极大关注。在半导体光催化的作用下, 被光催化材料捕获进而被还原实现“
被光催化材料捕获进而被还原实现“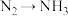 ”的转化(示意图如图所示)。已知:
”的转化(示意图如图所示)。已知: 的燃烧为放热反应,下列说法错误的是
的燃烧为放热反应,下列说法错误的是
 被光催化材料捕获进而被还原实现“
被光催化材料捕获进而被还原实现“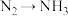 ”的转化(示意图如图所示)。已知:
”的转化(示意图如图所示)。已知: 的燃烧为放热反应,下列说法错误的是
的燃烧为放热反应,下列说法错误的是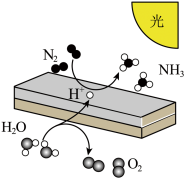
| A.该过程涉及光能到化学能的转化 |
| B.此方法与工业合成氨均属于人工固氮技术 |
| C.该反应中反应物的总能量小于生成物的总能量 |
| D.该反应证明了氮气的氧化性大于氧气的氧化性 |
您最近一年使用:0次



