解题方法
1 . 在酸性条件下,黄铁矿( ,其中S为~1价)催化氧化的反应转化如图所示。
,其中S为~1价)催化氧化的反应转化如图所示。
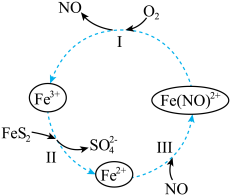
总反应:
(1)分别写出反应Ⅰ、Ⅱ的离子方程式:
①反应Ⅰ:_______ 。
②反应Ⅱ:_______ 。
(2)NO在总反应中的作用是_______ 。
 ,其中S为~1价)催化氧化的反应转化如图所示。
,其中S为~1价)催化氧化的反应转化如图所示。
总反应:

(1)分别写出反应Ⅰ、Ⅱ的离子方程式:
①反应Ⅰ:
②反应Ⅱ:
(2)NO在总反应中的作用是
您最近一年使用:0次
2023高三·全国·专题练习
2 . 化学反应都伴随着能量的变化。回答下列问题:
(1)可用焓变和熵变来判断化学反应进行的方向,下列都是能自发进行的化学反应,其中是吸热反应且反应后熵增的是___________(填字母)。
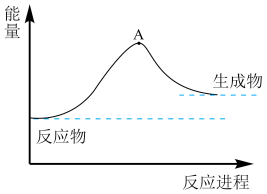
(2)一种分解海水制氢气的方法为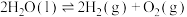 。如图为该反应的能量变化示意图,使用催化剂
。如图为该反应的能量变化示意图,使用催化剂 后,图中A点将
后,图中A点将_______ (填“升高”、“降低”或“不变”)。
(3)已知: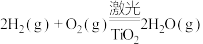
 ,部分化学键的键能数据如表:
,部分化学键的键能数据如表:
由此计算x=___________ 。(用含a、c、d的代数式表示)
(1)可用焓变和熵变来判断化学反应进行的方向,下列都是能自发进行的化学反应,其中是吸热反应且反应后熵增的是___________(填字母)。
A. | B. |
C. | D.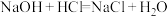 |
(2)一种分解海水制氢气的方法为
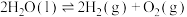 。如图为该反应的能量变化示意图,使用催化剂
。如图为该反应的能量变化示意图,使用催化剂 后,图中A点将
后,图中A点将
(3)已知:
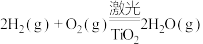
 ,部分化学键的键能数据如表:
,部分化学键的键能数据如表:| 化学键 |  |  |  |
 | x | c | d |
您最近一年使用:0次
名校
解题方法
3 . 二氧化硫的污染治理是化学研究的重要课题。
(1)石灰石-石膏法是一种常见的“钙基固硫”方法。其中,石灰石的溶解率与脱硫效果有着密切的关系。
可将催化条件下CaCO3吸收SO2宏观反应分为三步:
i.CaCO3由固相溶解进入液相,溶解速率为RA;
ii.SO2由气相扩散进入液相,扩散速率为RB;
iii.在催化剂作用下,溶解的SO2和Ca2+发生化学反应,且反应在液相中进行,反应速率为RC。温度变化对总反应速率的影响如图所示。___________ (填“RA”、“RB”或“Rc”)控制。
②45~55℃(催化剂活性不变)曲线呈下降趋势的原因:一是二氧化硫溶解度随温度升高而降低;二是___________ 。
(2)利用MnO2与SO2反应既可消除污染又可以制备MnSO4,将含有SO2尾气和一定比例的空气通入MnO2悬浊液中,保持温度不变的情况下,测得溶液中c(Mn2+)和c( )随反应时间的变化如图所示。导致溶液中c(Mn2+)和c(
)随反应时间的变化如图所示。导致溶液中c(Mn2+)和c( )的变化产生明显差异的原因是:
)的变化产生明显差异的原因是:_______ 。 与NO2反应的离子方程式为
与NO2反应的离子方程式为___________ 。
②请描述水催化促进硫酸盐形成的化学机制:通过“水分子桥”,处于纳米液滴中的 或
或 可以将电子快速转移给周围的气相NO2分子,
可以将电子快速转移给周围的气相NO2分子,___________ 。
(1)石灰石-石膏法是一种常见的“钙基固硫”方法。其中,石灰石的溶解率与脱硫效果有着密切的关系。
可将催化条件下CaCO3吸收SO2宏观反应分为三步:
i.CaCO3由固相溶解进入液相,溶解速率为RA;
ii.SO2由气相扩散进入液相,扩散速率为RB;
iii.在催化剂作用下,溶解的SO2和Ca2+发生化学反应,且反应在液相中进行,反应速率为RC。温度变化对总反应速率的影响如图所示。
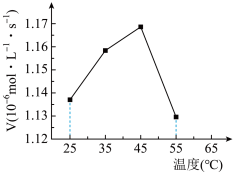
②45~55℃(催化剂活性不变)曲线呈下降趋势的原因:一是二氧化硫溶解度随温度升高而降低;二是
(2)利用MnO2与SO2反应既可消除污染又可以制备MnSO4,将含有SO2尾气和一定比例的空气通入MnO2悬浊液中,保持温度不变的情况下,测得溶液中c(Mn2+)和c(
 )随反应时间的变化如图所示。导致溶液中c(Mn2+)和c(
)随反应时间的变化如图所示。导致溶液中c(Mn2+)和c( )的变化产生明显差异的原因是:
)的变化产生明显差异的原因是: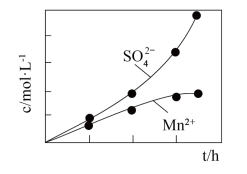
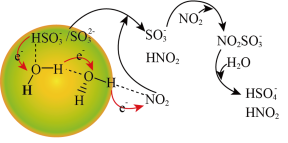
 与NO2反应的离子方程式为
与NO2反应的离子方程式为②请描述水催化促进硫酸盐形成的化学机制:通过“水分子桥”,处于纳米液滴中的
 或
或 可以将电子快速转移给周围的气相NO2分子,
可以将电子快速转移给周围的气相NO2分子,
您最近一年使用:0次
2023-12-25更新
|
307次组卷
|
5卷引用:江苏省建湖高级中学2023-2024学年高三上学期暑期学情检测(一)化学试题
江苏省建湖高级中学2023-2024学年高三上学期暑期学情检测(一)化学试题江苏省如皋中学2023-2024学年高三上学期阶段考试(二) 化学试题江苏省南师附中、天一中学、海安中学、海门中学四校2021-2022学年高三12月联考化学试题江苏省丹阳高级中学2023届高三上学期第一次阶段考试化学试题(已下线)通关练02 重要无机化合物的性质及应用-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)
名校
4 . 回答下列问题:
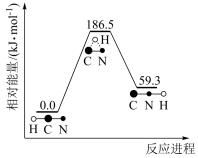
(1)理论研究表明,在101kPa和298K下,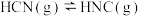 异构化反应过程的能量变化如图所示。下列说法不正确的是 。
异构化反应过程的能量变化如图所示。下列说法不正确的是 。
(2)已知共价键的健能与热化学方程式信息如下表:
则 的
的 为
为
(1)理论研究表明,在101kPa和298K下,
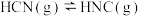 异构化反应过程的能量变化如图所示。下列说法不正确的是 。
异构化反应过程的能量变化如图所示。下列说法不正确的是 。
| A.HCN比HNC稳定 | B.该异构化反应的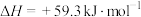 |
| C.正反应与逆反应的活化能相等 | D.使用催化剂,可以改变反应的反应热 |
(2)已知共价键的健能与热化学方程式信息如下表:
| 共价键 | H-H | H-O |
键能/( ) ) | 436 | 463 |
| 热化学方程式 |   | |
 的
的 为
为 A.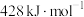 | B.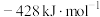 | C.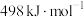 | D.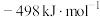 |
您最近一年使用:0次
2023高三·全国·专题练习
5 . 下列关于化学反应的调控措施说法不正确 的是________ 。
A.硫酸工业中,为使黄铁矿充分燃烧,可将矿石粉碎
B.硝酸工业中,氨的氧化使用催化剂是为了增大反应速率,提高生产效率
C.合成氨工业中,为提高氮气和氢气的利用率,采用循环操作
D.对于合成氨的反应,调控反应条件至最好,也不能使一种反应物的转化率达到100%
E.工业上增加炼铁高炉的高度可以有效降低尾气中CO的含量
F.合成氨工业中,从生产实际条件考虑,可盲目增大反应压强
G.合成氨工业中,为提高氮气和氢气的利用率,采用循环操作
A.硫酸工业中,为使黄铁矿充分燃烧,可将矿石粉碎
B.硝酸工业中,氨的氧化使用催化剂是为了增大反应速率,提高生产效率
C.合成氨工业中,为提高氮气和氢气的利用率,采用循环操作
D.对于合成氨的反应,调控反应条件至最好,也不能使一种反应物的转化率达到100%
E.工业上增加炼铁高炉的高度可以有效降低尾气中CO的含量
F.合成氨工业中,从生产实际条件考虑,可盲目增大反应压强
G.合成氨工业中,为提高氮气和氢气的利用率,采用循环操作
您最近一年使用:0次
名校
解题方法
6 . 自科学家们开始研究物质的结构与性质以来,氢元素时常担任主角,例如氢原子光谱启发了人们对原子结构的探索。此外,氢气与氢能源也是时下热门的一种绿色能源。氢能是最具发展潜力的清洁能源,但当下的生产条件非常苛刻且纯度不高。因此,科学家们正在寻找更经济、环境友好的方法,电解水便是其中一种。
(1)已知在298K和100kPa的条件下,液态水分解生成氢气:
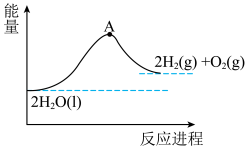
 。下图为该反应的能量变化示意图,而在实际生产生活中常会使用催化剂,例如
。下图为该反应的能量变化示意图,而在实际生产生活中常会使用催化剂,例如 ,那么图中A点将
,那么图中A点将___________ (填“升高”、“降低”或“不变”)。
(2)部分化学键的键能和反应焓变的数据如下:
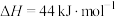 ,
, ,
,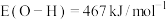 ,
,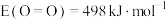 ,由此可计算得上述反应的
,由此可计算得上述反应的 为
为___________ 。又知该反应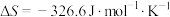 ,那么该反应在298K条件下能否自发进行?
,那么该反应在298K条件下能否自发进行?___________ 。
(3)试从绿色化学的角度比较并评价直接电解海水与太阳能( 作催化剂)分解淡水两种制备氢气的方案
作催化剂)分解淡水两种制备氢气的方案___________ 。
(1)已知在298K和100kPa的条件下,液态水分解生成氢气:

 。下图为该反应的能量变化示意图,而在实际生产生活中常会使用催化剂,例如
。下图为该反应的能量变化示意图,而在实际生产生活中常会使用催化剂,例如 ,那么图中A点将
,那么图中A点将
(2)部分化学键的键能和反应焓变的数据如下:

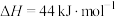 ,
, ,
,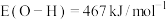 ,
,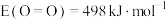 ,由此可计算得上述反应的
,由此可计算得上述反应的 为
为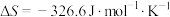 ,那么该反应在298K条件下能否自发进行?
,那么该反应在298K条件下能否自发进行?(3)试从绿色化学的角度比较并评价直接电解海水与太阳能(
 作催化剂)分解淡水两种制备氢气的方案
作催化剂)分解淡水两种制备氢气的方案
您最近一年使用:0次
7 . 我国力争2060年前实现碳中和, 的资源化利用具有重要意义。
的资源化利用具有重要意义。
(1)钙循环捕集 与CaO/
与CaO/ 储热体系耦合工艺
储热体系耦合工艺
以石灰石为原料的钙循环耦合工艺流程如图所示。

①循环I中, 含量较高的是
含量较高的是___________ (填“A”或“B”)处。
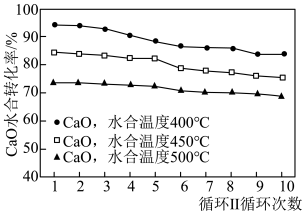
②若仅进行循环II,控制不同水合温度反应相同时间,水合反应器中水合温度对CaO水合转化率的影响如题图所示,在最佳水合温度下发生反应的化学方程式为___________ 。
③经历多次循环I后,高温煅烧造成CaO孔隙大量减少,捕集 效率降低。分析经历多次循环I再经历多次循环II后的CaO能有效提高
效率降低。分析经历多次循环I再经历多次循环II后的CaO能有效提高 捕集效率的可能原因是
捕集效率的可能原因是___________ 。
④从能量转化与物质资源综合利用角度分析,该工艺的优点是___________ 。
(2)利用光催化还原 制HCOOH等液态燃料
制HCOOH等液态燃料
光催化过程包括催化剂的光激发、光生电子( )与缺电子空穴(
)与缺电子空穴( )的分离或复合、光生电子的迁移及后续的氧化与还原反应。
)的分离或复合、光生电子的迁移及后续的氧化与还原反应。
①光催化还原 制备HCOOH的原理如图所示,该过程机理可描述为
制备HCOOH的原理如图所示,该过程机理可描述为___________ 。
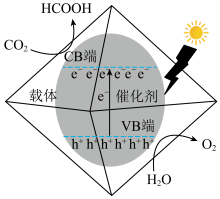
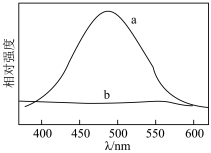
②催化剂对光的吸收强度是影响其光催化性能的重要因素之一。荧光强度越强,光生电子和空穴复合几率越大。催化剂a和b的荧光光谱如图所示,请判断哪一种催化剂催化效果更好,并说明理由___________ 。
 的资源化利用具有重要意义。
的资源化利用具有重要意义。(1)钙循环捕集
 与CaO/
与CaO/ 储热体系耦合工艺
储热体系耦合工艺以石灰石为原料的钙循环耦合工艺流程如图所示。

①循环I中,
 含量较高的是
含量较高的是②若仅进行循环II,控制不同水合温度反应相同时间,水合反应器中水合温度对CaO水合转化率的影响如题图所示,在最佳水合温度下发生反应的化学方程式为

③经历多次循环I后,高温煅烧造成CaO孔隙大量减少,捕集
 效率降低。分析经历多次循环I再经历多次循环II后的CaO能有效提高
效率降低。分析经历多次循环I再经历多次循环II后的CaO能有效提高 捕集效率的可能原因是
捕集效率的可能原因是④从能量转化与物质资源综合利用角度分析,该工艺的优点是
(2)利用光催化还原
 制HCOOH等液态燃料
制HCOOH等液态燃料光催化过程包括催化剂的光激发、光生电子(
 )与缺电子空穴(
)与缺电子空穴( )的分离或复合、光生电子的迁移及后续的氧化与还原反应。
)的分离或复合、光生电子的迁移及后续的氧化与还原反应。①光催化还原
 制备HCOOH的原理如图所示,该过程机理可描述为
制备HCOOH的原理如图所示,该过程机理可描述为
②催化剂对光的吸收强度是影响其光催化性能的重要因素之一。荧光强度越强,光生电子和空穴复合几率越大。催化剂a和b的荧光光谱如图所示,请判断哪一种催化剂催化效果更好,并说明理由

您最近一年使用:0次
2023-11-10更新
|
334次组卷
|
2卷引用:江苏省无锡市2023-2024学年高三上学期期中教学质量调研测试化学试卷题
2023高三·全国·专题练习
8 . 氨是人类科学技术发展史上的一项重大突破,目前工业上用氢气和氨气直接合成氨。
(1)固氮一直是科学家致力研究的重要课题,有关热力学数据如下:
常温下,大气固氮的倾向___________ 工业固氮(填“大于”或“小于”)。
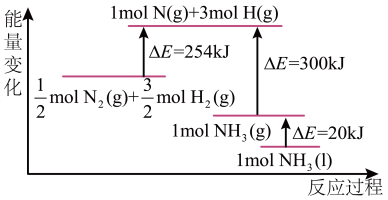
(2)N2(g)与H2(g) 反应的能量变化如图所示,则N2(g)与H2(g)反应制备NH3(l)的热化学方程式为:___________ 。
(3)T ℃时,在2 L恒容密闭容器中加入1.2 mol N2和2 mol H2模拟一定条件下工业固氮[N2(g)+3H2(g) 2NH3(g)],体系中n(NH3)随时间的变化如图所示:
2NH3(g)],体系中n(NH3)随时间的变化如图所示:
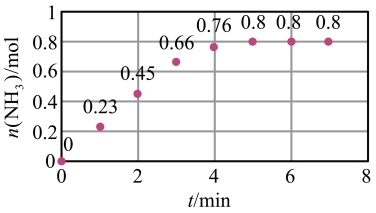
①前2分钟内的平均反应速率v(NH3)=___________ mol·L-1·min-1;
②有关工业固氮的说法正确的是___________ (选填序号)。
A.使用催化剂可提高反应物的转化率
B.循环使用N2、H2可提高NH3的产率
C.温度控制在500 ℃左右有利于反应向正方向进行
D.增大压强有利于加快反应速率,所以压强越大越好
③T ℃时,该反应的平衡常数为___________ ;
(4)研究表明某些过渡金属催化剂可以加速氨气的分解,某温度下,用等质量的不同金属分别催化等浓度的氨气,测得氨气分解的初始速率(单位:mmol/min)与催化剂的对应关系如表所示。
在不同催化剂的催化作用下,氨气分解反应中的活化能最大的催化剂是 ___________ (填化学式)。
(1)固氮一直是科学家致力研究的重要课题,有关热力学数据如下:
| 反应 | 大气固氮 N2(g)+O2(g)  2NO(g) 2NO(g) | 工业固氮 N2(g)+3H2(g)  2NH3(g) 2NH3(g) | ||||
| 温度/℃ | 25 | 2 000 | 25 | 350 | 400 | 450 |
| 平衡常数K | 3.84×10-31 | 0.1 | 5×108 | 1.847 | 0.504 | 0.152 |
(2)N2(g)与H2(g) 反应的能量变化如图所示,则N2(g)与H2(g)反应制备NH3(l)的热化学方程式为:

(3)T ℃时,在2 L恒容密闭容器中加入1.2 mol N2和2 mol H2模拟一定条件下工业固氮[N2(g)+3H2(g)
 2NH3(g)],体系中n(NH3)随时间的变化如图所示:
2NH3(g)],体系中n(NH3)随时间的变化如图所示:
①前2分钟内的平均反应速率v(NH3)=
②有关工业固氮的说法正确的是
A.使用催化剂可提高反应物的转化率
B.循环使用N2、H2可提高NH3的产率
C.温度控制在500 ℃左右有利于反应向正方向进行
D.增大压强有利于加快反应速率,所以压强越大越好
③T ℃时,该反应的平衡常数为
(4)研究表明某些过渡金属催化剂可以加速氨气的分解,某温度下,用等质量的不同金属分别催化等浓度的氨气,测得氨气分解的初始速率(单位:mmol/min)与催化剂的对应关系如表所示。
| 催化剂 | Fe | Pd | Ru | Rh | Pt | Ni |
| 初始速率 | 0.5 | 1.8 | 7.9 | 4.0 | 2.2 | 3.0 |
您最近一年使用:0次
2023高三上·全国·专题练习
9 . 如图中:E1=134kJ·mol-1,E2=368kJ·mol-1,根据要求回答问题:

(1)如图是1molNO2(g)和1molCO(g)反应生成CO2(g)和NO(g)过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是_____ (填“增大”“减小”或“不变”,下同),ΔH的变化是_____ 。请写出NO2(g)和CO(g)反应生成CO2(g)和NO(g)的热化学方程式:_____ 。
(2)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应的热化学方程式如下:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=+49.0kJ·mol-1
②CH3OH(g)+ O2(g)=CO2(g)+2H2(g) ΔH=-192.9kJ·mol-1
O2(g)=CO2(g)+2H2(g) ΔH=-192.9kJ·mol-1
又知③H2O(g)=H2O(l) ΔH=-44kJ·mol-1,则甲醇蒸气燃烧为液态水的热化学方程式为_____ 。
(3)已知在常温常压下:
④2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH=-1275.6kJ·mol-1
⑤2CO(g)+O2(g)=2CO2(g) ΔH=-566.0kJ·mol-1
⑥H2O(g)=H2O(l) ΔH=-44.0kJ·mol-1
请写出1mol甲醇不完全燃烧生成1mol一氧化碳和液态水的热化学方程式:_____ 。

(1)如图是1molNO2(g)和1molCO(g)反应生成CO2(g)和NO(g)过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是
(2)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应的热化学方程式如下:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=+49.0kJ·mol-1
②CH3OH(g)+
 O2(g)=CO2(g)+2H2(g) ΔH=-192.9kJ·mol-1
O2(g)=CO2(g)+2H2(g) ΔH=-192.9kJ·mol-1又知③H2O(g)=H2O(l) ΔH=-44kJ·mol-1,则甲醇蒸气燃烧为液态水的热化学方程式为
(3)已知在常温常压下:
④2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH=-1275.6kJ·mol-1
⑤2CO(g)+O2(g)=2CO2(g) ΔH=-566.0kJ·mol-1
⑥H2O(g)=H2O(l) ΔH=-44.0kJ·mol-1
请写出1mol甲醇不完全燃烧生成1mol一氧化碳和液态水的热化学方程式:
您最近一年使用:0次
22-23高一下·上海徐汇·期末
名校
10 . 近年来,将氯化氢转化为氟气的技术成为科学研究的热点。工业上用O2将HCl转化为Cl2,可减少污染。在传统催化剂并加热条件下可实现该转化(反应混合物均为气态),方程式如下: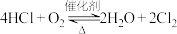
(1)某温度下,将一定量的O2和HCl通入4L的密闭容器中,反应过程中氧气的变化量如图所示,则0~20min平均反应速率v(HCI)为___________ 。

(2)下列选项中,能证明上述反应达到达到平衡状态的是___________。
(3)对该反应达到平衡后,以下分析正确的是___________。
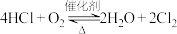
(1)某温度下,将一定量的O2和HCl通入4L的密闭容器中,反应过程中氧气的变化量如图所示,则0~20min平均反应速率v(HCI)为

(2)下列选项中,能证明上述反应达到达到平衡状态的是___________。
| A.单位时间内生成1molO2的同时生成2molCl2 |
| B.v(H2O)=v(Cl2) |
| C.容器中气体的平均相对分子质量不随时间变化而变化 |
| D.容器中气体密度不随时间变化而变化 |
| A.增加n(HCl),对正反应的反应速率影响更大 |
| B.体积不变加入稀有气体,对正反应的反应速率影响更大 |
| C.压强不变加入稀有气体,对逆反应的反应速率影响更大 |
| D.其他条件不变,使用不同催化剂,Cl2(g)的产率不同 |
您最近一年使用:0次



