1 . 苯酚是一种重要的化工原料,一种制取苯酚的反应机理如图。下列说法正确的是
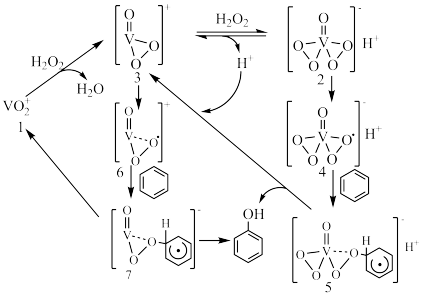
| A.苯和过氧化氢为非极性分子,水和苯酚为极性分子 |
| B.中间产物5转化为3的过程中,还生成了H2O |
| C.反应涉及O-H、V-O、C-H键的断裂和生成 |
| D.中间产物2和3之间的转化是氧化还原反应 |
您最近半年使用:0次
2 . 氢能是清洁、绿色能源,我国在开发氢能领域取得突破性进展。
I.氨分解制备氢。
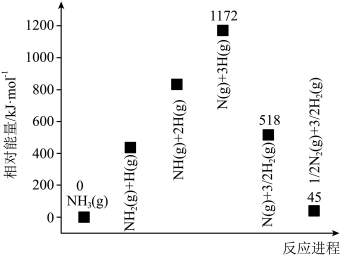
在铁或钨催化剂作用下,氨分解过程中能量变化如图所示。
(1)根据图推知,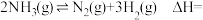
___________  。
。 键能为
键能为___________  。
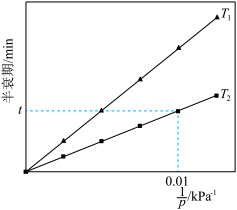
。 ,实验测得氨气分解反应半衰期与温度(T)、初始压强(
,实验测得氨气分解反应半衰期与温度(T)、初始压强(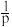 )的关系如图所示。
)的关系如图所示。
___________ (填“>”“<”或“=”) ,
, 温度下,反应进行到
温度下,反应进行到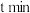 时容器内反应体系总压强为
时容器内反应体系总压强为___________  。
。
(3)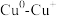 界面协同催化
界面协同催化 键断裂促进甲醇重整高效产氢的反应历程如图所示(
键断裂促进甲醇重整高效产氢的反应历程如图所示( 代表过渡态,*表示吸附在催化剂
代表过渡态,*表示吸附在催化剂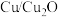 表面):控速步骤的化学方程式为
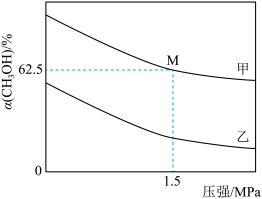
表面):控速步骤的化学方程式为___________ 。 的转化率与压强关系如图所示。进料组成
的转化率与压强关系如图所示。进料组成 ;进料组成
;进料组成 ,
,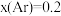 。[物质i的物质的量分数:
。[物质i的物质的量分数: ]
]___________ (填“甲”或“乙”)。
②M点 的体积分数为
的体积分数为___________ ,对应温度下,该反应的平衡常数 为
为___________ (用分数表示结果)。
I.氨分解制备氢。
在铁或钨催化剂作用下,氨分解过程中能量变化如图所示。
(1)根据图推知,
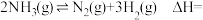
 。
。 键能为
键能为 。
。
 ,实验测得氨气分解反应半衰期与温度(T)、初始压强(
,实验测得氨气分解反应半衰期与温度(T)、初始压强(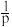 )的关系如图所示。
)的关系如图所示。
 ,
, 温度下,反应进行到
温度下,反应进行到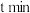 时容器内反应体系总压强为
时容器内反应体系总压强为 。
。
(3)
 界面协同催化
界面协同催化 键断裂促进甲醇重整高效产氢的反应历程如图所示(
键断裂促进甲醇重整高效产氢的反应历程如图所示( 代表过渡态,*表示吸附在催化剂
代表过渡态,*表示吸附在催化剂 表面):控速步骤的化学方程式为
表面):控速步骤的化学方程式为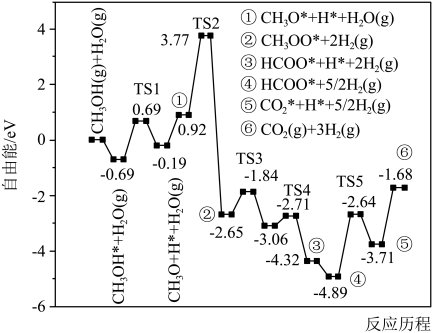
 的转化率与压强关系如图所示。进料组成
的转化率与压强关系如图所示。进料组成 ;进料组成
;进料组成 ,
,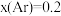 。[物质i的物质的量分数:
。[物质i的物质的量分数: ]
]
②M点
 的体积分数为
的体积分数为 为
为
您最近半年使用:0次
3 . 精脱硫技术主要用于煤气中羰基硫(COS)和二硫化碳(CS2)的转化。回答下列问题:
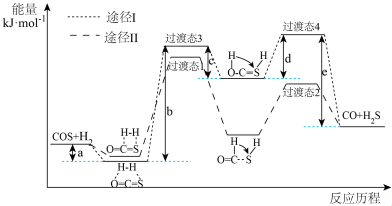
(1)利用焦炉煤气中的H2可脱除煤气中羰基硫(COS)。羰基硫氢化反应历程有途径I和途径Ⅱ两种可能,如图所示:___________ (填“I”或“Ⅱ”)。
②反应 的△H=
的△H=___________ kJ·mol-1。
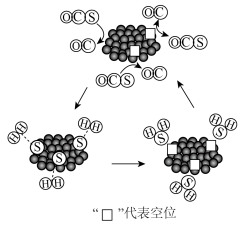
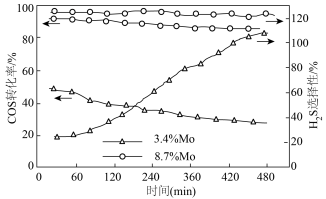
(2)MoS2可作羰基硫氢化反应的催化剂,催化机理如图所示:___________ (填“3.4%Mo”或“8.7%Mo”)作催化剂效果最好;当H2S选择性低于100%时表明部分COS气体与催化剂发生了反应,催化剂有吸硫现象,若H2S选择性高于100%,可能的原因是___________ 。
(3)金属Mo的晶胞如图所示,若原子a、b的坐标分别为(0,0,0)、(1,0,0),则原子c的坐标为___________ ,设晶体密度为ρg·cm3,则晶胞参数为___________ pm(阿伏加德罗常数的值为NA)。 ,容器内气体压强随时间变化如下表所示。
,容器内气体压强随时间变化如下表所示。
①0-250min内,H2分压的平均变化值为___________ kPa·min-l。
②该温度下,平衡常数Kp=___________ (kPa)-2(列出计算式)。
(1)利用焦炉煤气中的H2可脱除煤气中羰基硫(COS)。羰基硫氢化反应历程有途径I和途径Ⅱ两种可能,如图所示:
②反应
 的△H=
的△H=(2)MoS2可作羰基硫氢化反应的催化剂,催化机理如图所示:
(3)金属Mo的晶胞如图所示,若原子a、b的坐标分别为(0,0,0)、(1,0,0),则原子c的坐标为

 ,容器内气体压强随时间变化如下表所示。
,容器内气体压强随时间变化如下表所示。| 时间/min | 0 | 50 | 100 | 150 | 200 | 250 | 300 |
| 压强/kPa | 100 | 88.0 | 79.8 | 72.4 | 68.2 | 65.0 | 65.0 |
②该温度下,平衡常数Kp=
您最近半年使用:0次
4 . 乙醇是一种清洁的替代能源,催化加氢制备乙醇技术是当前的研究热点。
(1) 催化加氢制备乙醇的反应为
催化加氢制备乙醇的反应为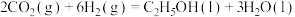 。
。
①若要计算上述反应的 ,须查阅的两个数据是
,须查阅的两个数据是 的燃烧热和
的燃烧热和___________ 。
②某金属有机骨架负载的铜基催化剂上, 加氢生成
加氢生成 的部分反应机理如图所示。
的部分反应机理如图所示。 过程中两个
过程中两个 均参与反应,画出
均参与反应,画出 的结构式(注明电荷)
的结构式(注明电荷)___________ 。
(2)乙酸甲酯催化加氢制备乙醇主要涉及如下反应:
反应Ⅰ:

反应Ⅱ:
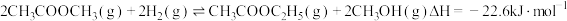
在其他条件不变时,将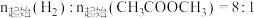 的混合气体以一定流速通入装有铜基催化剂的反应管,测得
的混合气体以一定流速通入装有铜基催化剂的反应管,测得 转化率、
转化率、 选择性
选择性 选择性
选择性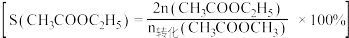 ]随温度的变化如图所示。
]随温度的变化如图所示。 与
与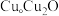 的晶胞如图所示(立方体),
的晶胞如图所示(立方体), 晶体的密度可表示为
晶体的密度可表示为___________  (用含
(用含 的代数式表示,
的代数式表示, 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。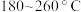 下均有
下均有 ,其原因是
,其原因是___________ 。
③ 范围内,
范围内, 转化率随温度升高而迅速增大的主要原因是
转化率随温度升高而迅速增大的主要原因是___________ 。
④温度高于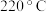 时,催化剂的催化活性下降,其原因可能是
时,催化剂的催化活性下降,其原因可能是___________ 。
(1)
 催化加氢制备乙醇的反应为
催化加氢制备乙醇的反应为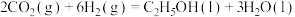 。
。①若要计算上述反应的
 ,须查阅的两个数据是
,须查阅的两个数据是 的燃烧热和
的燃烧热和②某金属有机骨架负载的铜基催化剂上,
 加氢生成
加氢生成 的部分反应机理如图所示。
的部分反应机理如图所示。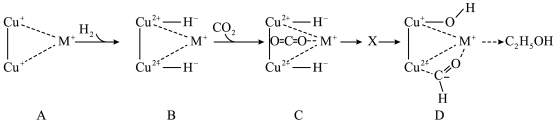
 过程中两个
过程中两个 均参与反应,画出
均参与反应,画出 的结构式(注明电荷)
的结构式(注明电荷)(2)乙酸甲酯催化加氢制备乙醇主要涉及如下反应:
反应Ⅰ:

反应Ⅱ:
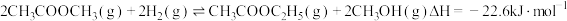
在其他条件不变时,将
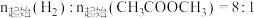 的混合气体以一定流速通入装有铜基催化剂的反应管,测得
的混合气体以一定流速通入装有铜基催化剂的反应管,测得 转化率、
转化率、 选择性
选择性 选择性
选择性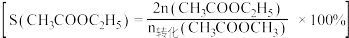 ]随温度的变化如图所示。
]随温度的变化如图所示。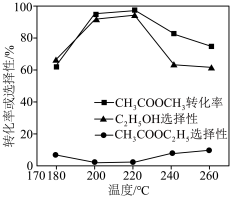
 与
与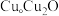 的晶胞如图所示(立方体),
的晶胞如图所示(立方体), 晶体的密度可表示为
晶体的密度可表示为 (用含
(用含 的代数式表示,
的代数式表示, 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。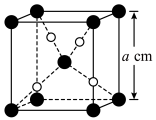
 下均有
下均有 ,其原因是
,其原因是③
 范围内,
范围内, 转化率随温度升高而迅速增大的主要原因是
转化率随温度升高而迅速增大的主要原因是④温度高于
 时,催化剂的催化活性下降,其原因可能是
时,催化剂的催化活性下降,其原因可能是
您最近半年使用:0次
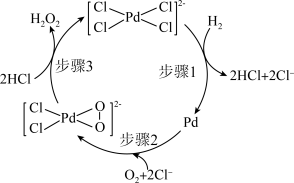
5 . 一种利用 和
和 直接合成
直接合成 的反应历程如下图所示。下列说法中错误的是
的反应历程如下图所示。下列说法中错误的是
| A.总反应的原子利用率理论上可达100% |
B.步骤2中,若 完全反应,则理论上转移电子数目为2NA 完全反应,则理论上转移电子数目为2NA |
C.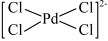 降低了反应的活化能,加快了反应速率 降低了反应的活化能,加快了反应速率 |
D. 和 和 中Pd的化合价不相同 中Pd的化合价不相同 |
您最近半年使用:0次
6 . 化学在治理空气污染方面发挥着重要的作用,将污染气体吸收或转化为对环境友好的气体是环境科学研究的热点。
Ⅰ、工业制硫酸中尾气SO2的处理。
1.SO2分子的空间结构为_____ ;SO2的键角_____ H2O(选填“>”或“<”)
2.下图是工业制硫酸中的转化器,有关说法正确的是_____。(不定项)
利用活性炭催化可去除尾气中SO2,并使其“热再生”,机理如下图1(*代表吸附态)。_____ 。
Ⅱ、N2O的转化
在Fe+催化作用下与CO发生反应:N2O(g)+CO(g) N2(g)+CO2(g)
N2(g)+CO2(g)
4.该反应分两步进行,第一步:Fe++N2O FeO++N2,则第二步反应为
FeO++N2,则第二步反应为_____ 。已知第二步反应几乎不影响总反应达到平衡所用的时间,由此推知,第一步反应的活化能_____ (选填“>”“<”或“=”)第二步反应的活化能。
Ⅰ、工业制硫酸中尾气SO2的处理。
1.SO2分子的空间结构为
2.下图是工业制硫酸中的转化器,有关说法正确的是_____。(不定项)
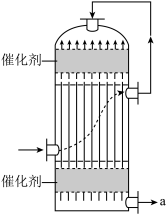
| A.该装置能充分利用热能 |
| B.进入转化器气体要净化操作 |
| C.温度475℃,此时SO2转化率最大 |
| D.该装置a端出来的气体只有SO3 |
利用活性炭催化可去除尾气中SO2,并使其“热再生”,机理如下图1(*代表吸附态)。
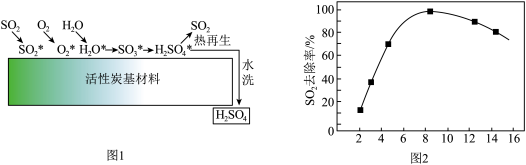
Ⅱ、N2O的转化
在Fe+催化作用下与CO发生反应:N2O(g)+CO(g)
 N2(g)+CO2(g)
N2(g)+CO2(g)4.该反应分两步进行,第一步:Fe++N2O
 FeO++N2,则第二步反应为
FeO++N2,则第二步反应为
您最近半年使用:0次
解题方法
7 . 水气变换反应(CO+H2O H2+CO2)是工业上大规模制氢的重要方法,HCOOH是中间产物。在密封石英管内完全充满1 mol·L-1 HCOOH水溶液,某温度下HCOOH分解,反应如下。
H2+CO2)是工业上大规模制氢的重要方法,HCOOH是中间产物。在密封石英管内完全充满1 mol·L-1 HCOOH水溶液,某温度下HCOOH分解,反应如下。
i.HCOOH(aq) CO(aq) + H2O(l)
CO(aq) + H2O(l)
ii.HCOOH(aq) CO2(aq) + H2(aq)
CO2(aq) + H2(aq)
含碳粒子浓度与反应时间的变化关系如图所示(忽略碳元素的其他存在形式)。
下列说法不正确 的是
 H2+CO2)是工业上大规模制氢的重要方法,HCOOH是中间产物。在密封石英管内完全充满1 mol·L-1 HCOOH水溶液,某温度下HCOOH分解,反应如下。
H2+CO2)是工业上大规模制氢的重要方法,HCOOH是中间产物。在密封石英管内完全充满1 mol·L-1 HCOOH水溶液,某温度下HCOOH分解,反应如下。i.HCOOH(aq)
 CO(aq) + H2O(l)
CO(aq) + H2O(l)ii.HCOOH(aq)
 CO2(aq) + H2(aq)
CO2(aq) + H2(aq)含碳粒子浓度与反应时间的变化关系如图所示(忽略碳元素的其他存在形式)。
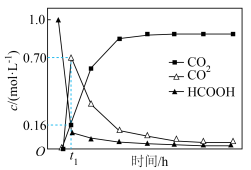
下列说法
| A.反应开始至t1,反应速率:i > ii |
| B.t1时,HCOOH的分解率为86% |
| C.相同条件下,若起始时溶液中同时还含有0.1 mol·L-1 盐酸,c(CO)的最大值将变大 |
| D.相同条件下,若起始时溶液中同时还含有0.1 mol·L-1 盐酸,c(CO2)的最大值将变小 |
您最近半年使用:0次
8 . 对于放热的可逆反应,某一给定转化率下,最大反应速率对应的温度称为最适宜温度。反应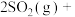
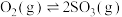
 在催化剂作用下原料的总转化率与最适宜温度(曲线Ⅰ)、原料的总平衡转化率与温度(曲线Ⅱ)的关系曲线示意图最合理的是
在催化剂作用下原料的总转化率与最适宜温度(曲线Ⅰ)、原料的总平衡转化率与温度(曲线Ⅱ)的关系曲线示意图最合理的是
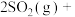
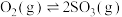
 在催化剂作用下原料的总转化率与最适宜温度(曲线Ⅰ)、原料的总平衡转化率与温度(曲线Ⅱ)的关系曲线示意图最合理的是
在催化剂作用下原料的总转化率与最适宜温度(曲线Ⅰ)、原料的总平衡转化率与温度(曲线Ⅱ)的关系曲线示意图最合理的是A.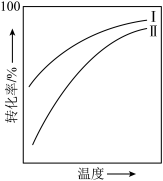 | B.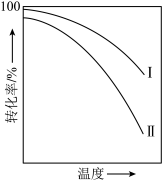 |
C.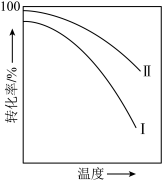 | D.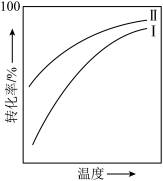 |
您最近半年使用:0次
名校
9 . 有机反应中经常采用实验和量子学手段进行反应的微观探究。一种铜催化某有机反应历程如下,下列说法错误的是

| A.碘元素位于周期表p区 |
| B.催化剂可降低该反应的活化能,加快反应速率 |
| C.Tpy-[CuⅡ]CN-是中间产物 |
D.总反应方程式是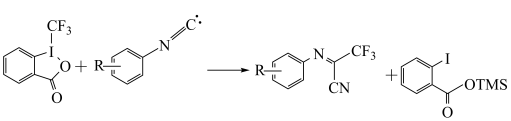 |
您最近半年使用:0次
名校
解题方法
10 . 研究表明, 催化
催化 分解的微观机制是复杂的,可以形成以下基本观点:
分解的微观机制是复杂的,可以形成以下基本观点: 与
与 循环反应;且
循环反应;且 与
与 反应产生的强氧化性羟基自由基(·OH)起到了关键作用,该过程被称为类-Fenton反应,如图所示,下列说法正确的是
反应产生的强氧化性羟基自由基(·OH)起到了关键作用,该过程被称为类-Fenton反应,如图所示,下列说法正确的是
 催化
催化 分解的微观机制是复杂的,可以形成以下基本观点:
分解的微观机制是复杂的,可以形成以下基本观点: 与
与 循环反应;且
循环反应;且 与
与 反应产生的强氧化性羟基自由基(·OH)起到了关键作用,该过程被称为类-Fenton反应,如图所示,下列说法正确的是
反应产生的强氧化性羟基自由基(·OH)起到了关键作用,该过程被称为类-Fenton反应,如图所示,下列说法正确的是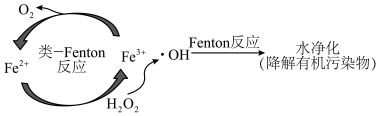
A.0.1mol羟基自由基(·OH)所含电子的数目为 |
B. 可以改变反应历程,降低 可以改变反应历程,降低 分解反应的反应热 分解反应的反应热 |
C. 与 与 反应产生羟基自由基的反应为 反应产生羟基自由基的反应为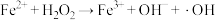 |
| D.去除废水中难降解的有机污染物,主要利用了羟基自由基的还原性 |
您最近半年使用:0次
2024-04-13更新
|
137次组卷
|
2卷引用:2024届河北省雄安新区雄安部分高中高三下学期一模化学试题



