解题方法
1 . 四氧化锇与烯烃的反应历程如图所示,下列说法错误的是
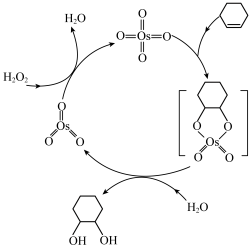

| A.H2O2作氧化剂 |
| B.利用此法乙烯可能转化为乙二醇 |
C.OsO4与 中Os的化合价均为+8价 中Os的化合价均为+8价 |
D.该历程中总反应式为: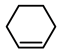 +H2O2 +H2O2 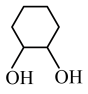 |
您最近半年使用:0次
解题方法
2 . 科研工作者持续进行“碳达峰”“碳中和”的相关研究。根据要求回答下列问题。
Ⅰ.石灰生产工业利用开采的碳酸钙进行分解,并产生大量 ,主要反应如下:
,主要反应如下: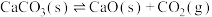
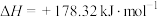
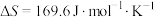 ①
①
(1)已知ΔG=0时的临界温度称为热力学分解温度,反应①的分解温度为___________ ℃。(保留整数位)
(2)恒温恒压体系内进行反应①,达到平衡后,分别进行如下操作,请填空:
操作1:加入 ,平衡
,平衡___________ (填“正向”“逆向”或“不”,下同)移动;
操作2:缓慢加入 ,平衡
,平衡___________ 移动。
Ⅱ. 和
和 占温室气体排放的98%以上。甲烷二氧化碳重整反应可在低温条件下将
占温室气体排放的98%以上。甲烷二氧化碳重整反应可在低温条件下将 和
和 这两种温室气体转化为合成气(CO和
这两种温室气体转化为合成气(CO和 )。
)。
主反应为 ②
②
副反应主要有 ③
③
 ④
④
Co基活性中心在甲烷二氧化碳重整过程有较好的反应活性,其中吸附在催化剂表面的物质用*标注。催化反应机理如下图:

(3)写出催化过程中步骤B的反应方程式:___________ ,该过程为___________ (填“放热”或“吸热”)反应。
(4)路径1和路径2同时进行,容易发生碳耦合过程最终导致积碳,使催化剂失活。根据反应机理推测可能发生的积碳反应除反应③外,还有可能的积碳反应为有___________ (填反应方程式)。
(5)相同条件下按甲烷、二氧化碳、氮气体积比为45%、45%、10%的量进行催化重整反应,若发生②③④三个反应,已知甲烷的转化率为70%, 的转化率为80%,附着在催化剂表面的积碳占总碳元素的24%,则CO的选择性S=
的转化率为80%,附着在催化剂表面的积碳占总碳元素的24%,则CO的选择性S=___________ [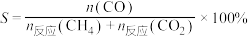 ,生成的C理论上都附着在催化剂表面]。
,生成的C理论上都附着在催化剂表面]。
Ⅰ.石灰生产工业利用开采的碳酸钙进行分解,并产生大量
 ,主要反应如下:
,主要反应如下: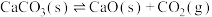
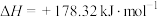
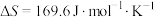 ①
①(1)已知ΔG=0时的临界温度称为热力学分解温度,反应①的分解温度为
(2)恒温恒压体系内进行反应①,达到平衡后,分别进行如下操作,请填空:
操作1:加入
 ,平衡
,平衡操作2:缓慢加入
 ,平衡
,平衡Ⅱ.
 和
和 占温室气体排放的98%以上。甲烷二氧化碳重整反应可在低温条件下将
占温室气体排放的98%以上。甲烷二氧化碳重整反应可在低温条件下将 和
和 这两种温室气体转化为合成气(CO和
这两种温室气体转化为合成气(CO和 )。
)。主反应为
 ②
②副反应主要有
 ③
③ ④
④Co基活性中心在甲烷二氧化碳重整过程有较好的反应活性,其中吸附在催化剂表面的物质用*标注。催化反应机理如下图:

(3)写出催化过程中步骤B的反应方程式:
(4)路径1和路径2同时进行,容易发生碳耦合过程最终导致积碳,使催化剂失活。根据反应机理推测可能发生的积碳反应除反应③外,还有可能的积碳反应为有
(5)相同条件下按甲烷、二氧化碳、氮气体积比为45%、45%、10%的量进行催化重整反应,若发生②③④三个反应,已知甲烷的转化率为70%,
 的转化率为80%,附着在催化剂表面的积碳占总碳元素的24%,则CO的选择性S=
的转化率为80%,附着在催化剂表面的积碳占总碳元素的24%,则CO的选择性S=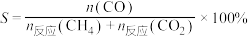 ,生成的C理论上都附着在催化剂表面]。
,生成的C理论上都附着在催化剂表面]。
您最近半年使用:0次
名校
解题方法
3 . 我国科学家成功利用光伏发电,将电解水获得的 与
与 反应合成甲醇,再由甲醇经若干酶促反应合成淀粉。该研究成果已在国际学术期刊《科学》上发表。回答下列问题:
反应合成甲醇,再由甲醇经若干酶促反应合成淀粉。该研究成果已在国际学术期刊《科学》上发表。回答下列问题:
(1) 人工合成转化为淀粉只需要11步,其中前两步涉及的反应如图所示。
人工合成转化为淀粉只需要11步,其中前两步涉及的反应如图所示。 的
的
__________ (用含 、
、 、
、 、
、 的代数式表示)。
的代数式表示)。
(2)有学者结合实验和计算机模拟结果,得出 的一种反应历程如图所示,其中吸附在催化剂表面的物种用“·”标注,TS1、TS2、TS3、TS4均为过渡态。决速步骤对应的化学方程式为
的一种反应历程如图所示,其中吸附在催化剂表面的物种用“·”标注,TS1、TS2、TS3、TS4均为过渡态。决速步骤对应的化学方程式为__________ ;TS3对应的步骤适合在__________ (填“高温”或“低温”)条件下进行。 和
和 ,发生反应
,发生反应
 ,在催化剂作用下单位时间内
,在催化剂作用下单位时间内 的转化率与温度、催化剂的关系如图所示。
的转化率与温度、催化剂的关系如图所示。 的生成速率
的生成速率__________ (填“>”“<”或“=”,下同) 的消耗速率;催化效率:Cat2
的消耗速率;催化效率:Cat2__________ Cat1。
②b点之后 的转化率降低,可能的原因是
的转化率降低,可能的原因是__________ 。
(4)已知 催化加氢的主要反应如下:
催化加氢的主要反应如下:
反应Ⅰ.
反应Ⅱ.
①230℃时,将 和
和 按物质的量之比为1:3混合通入恒温刚性密闭容器中,在催化剂作用下同时发生反应Ⅰ和反应Ⅱ,容器内压强随时间的变化如下表所示。
按物质的量之比为1:3混合通入恒温刚性密闭容器中,在催化剂作用下同时发生反应Ⅰ和反应Ⅱ,容器内压强随时间的变化如下表所示。
平衡时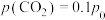 ,则该温度下反应Ⅰ的化学平衡常数
,则该温度下反应Ⅰ的化学平衡常数
__________  (用含
(用含 的代数式表示)。
的代数式表示)。
②二氧化碳催化加氢合成甲醇反应往往伴随副反应Ⅱ。一定温度和压强条件下,为了提高反应速率和甲醇选择性,应当__________ 。
 与
与 反应合成甲醇,再由甲醇经若干酶促反应合成淀粉。该研究成果已在国际学术期刊《科学》上发表。回答下列问题:
反应合成甲醇,再由甲醇经若干酶促反应合成淀粉。该研究成果已在国际学术期刊《科学》上发表。回答下列问题:(1)
 人工合成转化为淀粉只需要11步,其中前两步涉及的反应如图所示。
人工合成转化为淀粉只需要11步,其中前两步涉及的反应如图所示。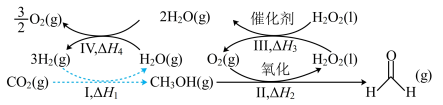
 的
的
 、
、 、
、 、
、 的代数式表示)。
的代数式表示)。(2)有学者结合实验和计算机模拟结果,得出
 的一种反应历程如图所示,其中吸附在催化剂表面的物种用“·”标注,TS1、TS2、TS3、TS4均为过渡态。决速步骤对应的化学方程式为
的一种反应历程如图所示,其中吸附在催化剂表面的物种用“·”标注,TS1、TS2、TS3、TS4均为过渡态。决速步骤对应的化学方程式为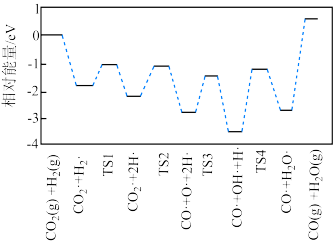
 和
和 ,发生反应
,发生反应
 ,在催化剂作用下单位时间内
,在催化剂作用下单位时间内 的转化率与温度、催化剂的关系如图所示。
的转化率与温度、催化剂的关系如图所示。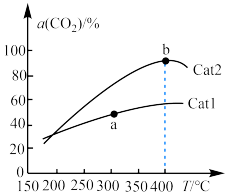
 的生成速率
的生成速率 的消耗速率;催化效率:Cat2
的消耗速率;催化效率:Cat2②b点之后
 的转化率降低,可能的原因是
的转化率降低,可能的原因是(4)已知
 催化加氢的主要反应如下:
催化加氢的主要反应如下:反应Ⅰ.

反应Ⅱ.

①230℃时,将
 和
和 按物质的量之比为1:3混合通入恒温刚性密闭容器中,在催化剂作用下同时发生反应Ⅰ和反应Ⅱ,容器内压强随时间的变化如下表所示。
按物质的量之比为1:3混合通入恒温刚性密闭容器中,在催化剂作用下同时发生反应Ⅰ和反应Ⅱ,容器内压强随时间的变化如下表所示。时间/min | 0 | 20 | 40 | 60 | 80 |
压强/MPa |
|
|
|
|
|
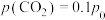 ,则该温度下反应Ⅰ的化学平衡常数
,则该温度下反应Ⅰ的化学平衡常数
 (用含
(用含 的代数式表示)。
的代数式表示)。②二氧化碳催化加氢合成甲醇反应往往伴随副反应Ⅱ。一定温度和压强条件下,为了提高反应速率和甲醇选择性,应当
您最近半年使用:0次
2024-04-07更新
|
337次组卷
|
4卷引用:广西壮族自治区部分学校2023-2024学年高三下学期教学质量监测联考(二模)化学试题
解题方法
4 . PtNiFe-LDHGO催化甲醛氧化的反应机理如图:
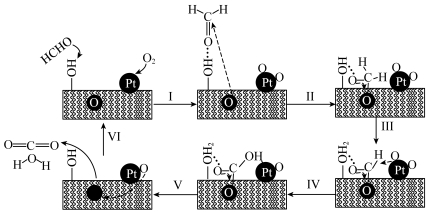
下列说法错误的是

下列说法错误的是
A.步骤Ⅰ中甲醛通过氢键吸附在催化剂表面的 上 上 |
| B.上述反应机理涉及极性键和非极性键的形成 |
C.该反应每生成  ,转移 ,转移 电子 电子 |
| D.PtNiFe-LDHGO降低了该反应的活化能 |
您最近半年使用:0次
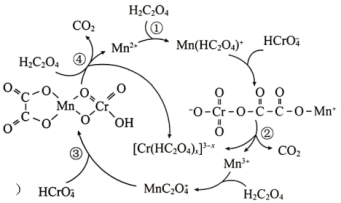
5 .  是
是 还原工业废水中六价Cr的催化剂,反应机理如图所示。
还原工业废水中六价Cr的催化剂,反应机理如图所示。
下列叙述错误 的是
 是
是 还原工业废水中六价Cr的催化剂,反应机理如图所示。
还原工业废水中六价Cr的催化剂,反应机理如图所示。
下列叙述
| A.反应①、③均不属于氧化还原反应 |
B.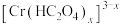 中Cr元素的化合价为+3价 中Cr元素的化合价为+3价 |
| C.加入Mn能够降低活化能,提高六价铬的转化率 |
D.总反应 |
您最近半年使用:0次
6 . 下列“实验结论”与“实验操作及事实”相符的一组是
选项 | 实验操作及事实 | 实验结论 |
A | 在两支试管中各加入2mL5% 溶液,再分别滴入3滴 溶液,再分别滴入3滴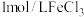 、和 、和 溶液,摇匀,两支试管中都有气泡产生,滴入 溶液,摇匀,两支试管中都有气泡产生,滴入 溶液产生的气泡更快些 溶液产生的气泡更快些 |  对 对 分解的催化效果强于 分解的催化效果强于 |
B | 向溴水中加入苯,振荡后静置,水层颜色变浅 | 溴与苯发生了加成反应 |
C | 向蔗糖溶液中滴加稀硫酸,水浴加热、加入新制的 悬浊液,无砖红色沉淀 悬浊液,无砖红色沉淀 | 蔗糖未发生水解 |
D | 往 溶液中滴加KSCN溶液,再加入少量 溶液中滴加KSCN溶液,再加入少量 固体,溶液先变成红色后无明显变化 固体,溶液先变成红色后无明显变化 |  与 与 的反应不可逆 的反应不可逆 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
7 . 2023 年杭州亚运会主火炬创新使用了绿色“零碳甲醇”作为燃料,这不仅在亚运史上是第一次,在全球大型体育赛事上也是首次实现了废碳的再生利用。“零碳甲醇”是符合“碳中和”属性的绿色能源。
请回答下列问题:
(1)工业上主要利用以下反应合成甲醇: CO2(g)+3H2(g) CH3OH(g)+H2O(g)。已知在一定条件下该反应的
CH3OH(g)+H2O(g)。已知在一定条件下该反应的 = -akJ⋅mol-1,ΔS=-bJ⋅mol-1⋅K-1(a>0,b >0),假设该反应的焓变和熵变不随温度的改变而改变,请计算该反应能够发生的适宜温度T的取值范围
= -akJ⋅mol-1,ΔS=-bJ⋅mol-1⋅K-1(a>0,b >0),假设该反应的焓变和熵变不随温度的改变而改变,请计算该反应能够发生的适宜温度T的取值范围 ___________ K(用含a、b的代数式表示)。
(2)目前有多种用于工业捕集CO2的方法,主要分为吸收(物理吸收、化学吸收、生物吸收)、吸附、深冷分离和膜分离等,也有将不同捕集方法相结合的方法。一种模拟脱除工业尾气中CO2的示意图如图所示: 后,
后, 则该溶液的pOH=
则该溶液的pOH=___________ (该温度下H2CO3的Ka1=4.6×10-7,Ka2=5.0×10-11 Kw=1×10-a,用含a的代数式表示)。
(3)CO2合成甲醇的工艺主要分为两类,一类称为直接法:CO2直接加H2合成甲醇;一类称为间接法:CO2和H2通过逆水煤气反应,先合成CO后,CO和H2再合成甲醇。
I.CO2 (g)+3H2 (g) CH3OH(g)+H2O(g) ΔH1=-48.9kJ⋅mol-1
CH3OH(g)+H2O(g) ΔH1=-48.9kJ⋅mol-1
Ⅱ.CO2(g)+H2(g) CO(g)+H2O(g) ΔH2= +41.1 kJ·mol-1
CO(g)+H2O(g) ΔH2= +41.1 kJ·mol-1
Ⅲ.CO(g)+2H2(g) 3CH3OH(g) ΔH3=-90kJ⋅mol-1
3CH3OH(g) ΔH3=-90kJ⋅mol-1
①若利用间接工艺法合成甲醇,反应的决速步为逆水煤气反应,下列示意图中能体现上述反应体系能量变化的是___________ (填字母)。___________ 。
③工业生产中测定体系的压强具有实际意义。一定温度下,仅利用反应Ⅰ直接合成甲醇,将体积分数为a% CO2、3a% H2 的进料气(含杂质气体),以 Cu/Zn/Al/Zr纳米纤维为催化剂,控制压强为50 bar(1 bar=100 kPa)发生反应I,进料气中杂质气体不反应,达到平衡时二氧化碳的转化率为90%,达到平衡时, p(H2) =___________ bar,反应I的平衡常数Kp= ___________ bar-2(Kp为用分压表示的平衡常数,分压=总压×物质的量分数,用含a的代数式表示)。
(4)甲醇便于运输,是一种具有前景的液体燃料,利用手持技术,通过测定甲醇、乙醇、正丙醇等三种物质在温度传感器尖头处蒸发时的温度变化曲线,根据曲线下降的幅度和速率的快慢,可以比较它们之间的分子间作用力的大小。请判断表示甲醇的曲线是___________ ,理由是___________ 。
请回答下列问题:
(1)工业上主要利用以下反应合成甲醇: CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。已知在一定条件下该反应的
CH3OH(g)+H2O(g)。已知在一定条件下该反应的 = -akJ⋅mol-1,ΔS=-bJ⋅mol-1⋅K-1(a>0,b >0),假设该反应的焓变和熵变不随温度的改变而改变,请计算该反应能够发生的适宜温度T的取值范围
= -akJ⋅mol-1,ΔS=-bJ⋅mol-1⋅K-1(a>0,b >0),假设该反应的焓变和熵变不随温度的改变而改变,请计算该反应能够发生的适宜温度T的取值范围 (2)目前有多种用于工业捕集CO2的方法,主要分为吸收(物理吸收、化学吸收、生物吸收)、吸附、深冷分离和膜分离等,也有将不同捕集方法相结合的方法。一种模拟脱除工业尾气中CO2的示意图如图所示:
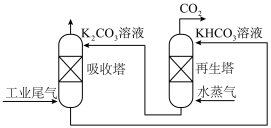
 后,
后, 则该溶液的pOH=
则该溶液的pOH=(3)CO2合成甲醇的工艺主要分为两类,一类称为直接法:CO2直接加H2合成甲醇;一类称为间接法:CO2和H2通过逆水煤气反应,先合成CO后,CO和H2再合成甲醇。
I.CO2 (g)+3H2 (g)
 CH3OH(g)+H2O(g) ΔH1=-48.9kJ⋅mol-1
CH3OH(g)+H2O(g) ΔH1=-48.9kJ⋅mol-1Ⅱ.CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2= +41.1 kJ·mol-1
CO(g)+H2O(g) ΔH2= +41.1 kJ·mol-1Ⅲ.CO(g)+2H2(g)
 3CH3OH(g) ΔH3=-90kJ⋅mol-1
3CH3OH(g) ΔH3=-90kJ⋅mol-1①若利用间接工艺法合成甲醇,反应的决速步为逆水煤气反应,下列示意图中能体现上述反应体系能量变化的是
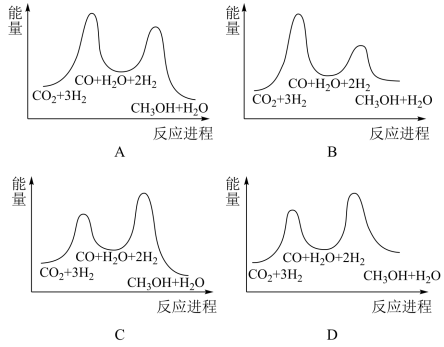
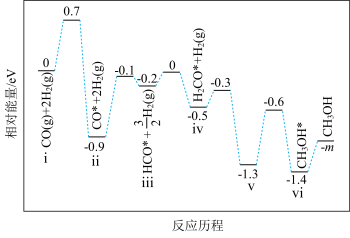
③工业生产中测定体系的压强具有实际意义。一定温度下,仅利用反应Ⅰ直接合成甲醇,将体积分数为a% CO2、3a% H2 的进料气(含杂质气体),以 Cu/Zn/Al/Zr纳米纤维为催化剂,控制压强为50 bar(1 bar=100 kPa)发生反应I,进料气中杂质气体不反应,达到平衡时二氧化碳的转化率为90%,达到平衡时, p(H2) =
(4)甲醇便于运输,是一种具有前景的液体燃料,利用手持技术,通过测定甲醇、乙醇、正丙醇等三种物质在温度传感器尖头处蒸发时的温度变化曲线,根据曲线下降的幅度和速率的快慢,可以比较它们之间的分子间作用力的大小。请判断表示甲醇的曲线是
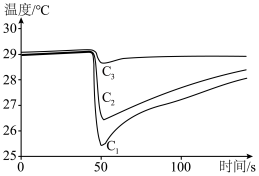
您最近半年使用:0次
2024-04-02更新
|
146次组卷
|
2卷引用:安徽省示范高中皖北协作区2024届高三联考化学试题
名校
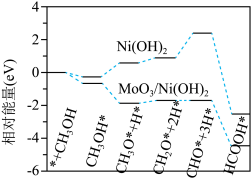
8 . 镍基材料作为甲醇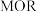 反应催化剂已被广泛研究。近日,广东省科学院测试分析研究所提出
反应催化剂已被广泛研究。近日,广东省科学院测试分析研究所提出 和
和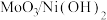 均能催化甲醇
均能催化甲醇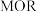 反应,其反应历程的片段如图所示,其中吸附在催化剂表面上的物种用*标注。下列说法正确的是
反应,其反应历程的片段如图所示,其中吸附在催化剂表面上的物种用*标注。下列说法正确的是
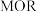 反应催化剂已被广泛研究。近日,广东省科学院测试分析研究所提出
反应催化剂已被广泛研究。近日,广东省科学院测试分析研究所提出 和
和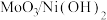 均能催化甲醇
均能催化甲醇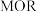 反应,其反应历程的片段如图所示,其中吸附在催化剂表面上的物种用*标注。下列说法正确的是
反应,其反应历程的片段如图所示,其中吸附在催化剂表面上的物种用*标注。下列说法正确的是
A.文献中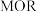 反应指的是还原反应 反应指的是还原反应 |
B.吸附甲醇的效果: 劣于 劣于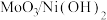 |
C. 催化下,消耗 催化下,消耗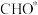 的步骤为决速步 的步骤为决速步 |
D.上述历程中碳原子的杂化类型由 转化为 转化为 |
您最近半年使用:0次
9 . 甲醇直接脱氢制无水甲醛是具有工业化前景的新工艺。回答下列问题:
(1)在标准压强(100kPa)、298K下,一些物质的热力学数据如下表,标准摩尔生成焓是指由稳定的单质合成1mol该物质的反应焓变;
甲醇脱氢制甲醛的反应方程式为:

___________ ,该反应高温能自发进行的原因是___________ 。
(2)已知Arrhenius经验公式为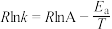 (
( 为活化能,k为速率常数,R、A为常数)。一定条件下,催化剂1作用下甲醇脱氢制甲醛反应的Arrhenius经验公式的实验数据如图中曲线a所示。
为活化能,k为速率常数,R、A为常数)。一定条件下,催化剂1作用下甲醇脱氢制甲醛反应的Arrhenius经验公式的实验数据如图中曲线a所示。
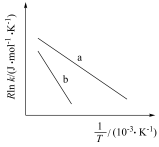
①升高温度,速率常数k___________ (填“增大”“减小”或“不变”);
②催化剂Ⅱ作用下,实验数据如图中b线所示,则催化效果:催化剂Ⅰ___________ 催化剂Ⅱ(填“>”成“<”)。
(3)催化剂1作用下,恒容密闭容器中充入一定量的 发生反应
发生反应 ,达到平衡时,容器总压、
,达到平衡时,容器总压、 的体积分数随温度的变化曲线如图所示。
的体积分数随温度的变化曲线如图所示。
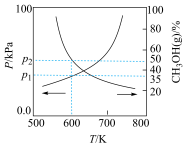
①随着温度的升高,压强不断增大的原因是___________ 。
②600K达到平衡时,
___________ kPa(用含“p”的式子表示,下同), 的转化率为
的转化率为___________ ,
___________ 。
(1)在标准压强(100kPa)、298K下,一些物质的热力学数据如下表,标准摩尔生成焓是指由稳定的单质合成1mol该物质的反应焓变;
| 物质 |  | HCHO |  |
标准摩尔生成焓(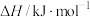 ) ) | 0 | -115.8 | -201 |
熵(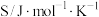 ) ) | 130.7 | 218.7 | 239.9 |


(2)已知Arrhenius经验公式为
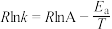 (
( 为活化能,k为速率常数,R、A为常数)。一定条件下,催化剂1作用下甲醇脱氢制甲醛反应的Arrhenius经验公式的实验数据如图中曲线a所示。
为活化能,k为速率常数,R、A为常数)。一定条件下,催化剂1作用下甲醇脱氢制甲醛反应的Arrhenius经验公式的实验数据如图中曲线a所示。
①升高温度,速率常数k
②催化剂Ⅱ作用下,实验数据如图中b线所示,则催化效果:催化剂Ⅰ
(3)催化剂1作用下,恒容密闭容器中充入一定量的
 发生反应
发生反应 ,达到平衡时,容器总压、
,达到平衡时,容器总压、 的体积分数随温度的变化曲线如图所示。
的体积分数随温度的变化曲线如图所示。
①随着温度的升高,压强不断增大的原因是
②600K达到平衡时,

 的转化率为
的转化率为
您最近半年使用:0次
解题方法
10 . 中科大某课题组通过自由基杂环反应直接合成各种 稠合的内酰胺,应用于钙钛矿电池器件中。底物与Cu(Ⅰ)物种通过电子转移经历两种途径得到目标产物D。下列说法错误的是
稠合的内酰胺,应用于钙钛矿电池器件中。底物与Cu(Ⅰ)物种通过电子转移经历两种途径得到目标产物D。下列说法错误的是
 稠合的内酰胺,应用于钙钛矿电池器件中。底物与Cu(Ⅰ)物种通过电子转移经历两种途径得到目标产物D。下列说法错误的是
稠合的内酰胺,应用于钙钛矿电池器件中。底物与Cu(Ⅰ)物种通过电子转移经历两种途径得到目标产物D。下列说法错误的是
| A.Cu(Ⅰ)物种是催化剂 | B.底物具有氧化性 |
| C.两种途径不同,总反应的反应热也不同 | D.合成过程中 中碳碳双键断裂 中碳碳双键断裂 |
您最近半年使用:0次