名校
1 . 有机反应中经常采用实验和量子学手段进行反应的微观探究。一种铜催化某有机反应历程如下,下列说法错误的是

| A.碘元素位于周期表p区 |
| B.催化剂可降低该反应的活化能,加快反应速率 |
| C.Tpy-[CuⅡ]CN-是中间产物 |
D.总反应方程式是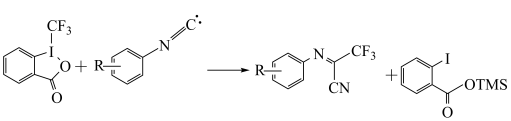 |
您最近半年使用:0次
名校
解题方法
2 . 研究表明, 催化
催化 分解的微观机制是复杂的,可以形成以下基本观点:
分解的微观机制是复杂的,可以形成以下基本观点: 与
与 循环反应;且
循环反应;且 与
与 反应产生的强氧化性羟基自由基(·OH)起到了关键作用,该过程被称为类-Fenton反应,如图所示,下列说法正确的是
反应产生的强氧化性羟基自由基(·OH)起到了关键作用,该过程被称为类-Fenton反应,如图所示,下列说法正确的是
 催化
催化 分解的微观机制是复杂的,可以形成以下基本观点:
分解的微观机制是复杂的,可以形成以下基本观点: 与
与 循环反应;且
循环反应;且 与
与 反应产生的强氧化性羟基自由基(·OH)起到了关键作用,该过程被称为类-Fenton反应,如图所示,下列说法正确的是
反应产生的强氧化性羟基自由基(·OH)起到了关键作用,该过程被称为类-Fenton反应,如图所示,下列说法正确的是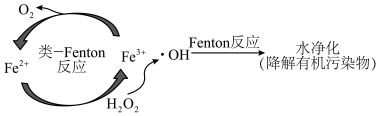
A.0.1mol羟基自由基(·OH)所含电子的数目为 |
B. 可以改变反应历程,降低 可以改变反应历程,降低 分解反应的反应热 分解反应的反应热 |
C. 与 与 反应产生羟基自由基的反应为 反应产生羟基自由基的反应为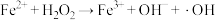 |
| D.去除废水中难降解的有机污染物,主要利用了羟基自由基的还原性 |
您最近半年使用:0次
2024-04-13更新
|
137次组卷
|
2卷引用:2024届河北省雄安新区雄安部分高中高三下学期一模化学试题
名校
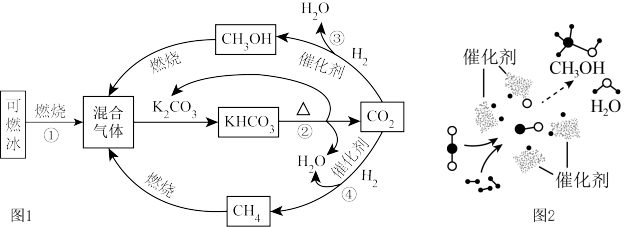
3 . 为解决能源与环境问题,有学者提出如图1所示的含碳物质转化的技术路线。 )完全燃烧的化学方程式为
)完全燃烧的化学方程式为______ 。
(2)反应②属于______ 反应(填基本反应类型)。
(3)我国学者开发促进反应③的一种新型催化剂,催化过程如图2所示。该过程的中间产物______ (填化学式)、氧和氢进一步作用生成甲醇( )和水。
)和水。
(4)反应④的化学方程式为______ 。
(5)该技术路线有利用于实现______ (填字母)。
A.碳循环利用 B.减少碳排放 C.减少白色污染
 )完全燃烧的化学方程式为
)完全燃烧的化学方程式为(2)反应②属于
(3)我国学者开发促进反应③的一种新型催化剂,催化过程如图2所示。该过程的中间产物
 )和水。
)和水。(4)反应④的化学方程式为
(5)该技术路线有利用于实现
A.碳循环利用 B.减少碳排放 C.减少白色污染
您最近半年使用:0次
解题方法
4 . 采用可再生的生物质原料生产乙醇,再脱水制乙烯的技术是调整能源结构、减少环境污染、促进国民经济的重要途径之一、一定温度下,在某密闭容器中进行乙醇脱水制乙烯的反应: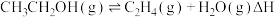 ,有、无催化剂时,该反应的能量变化与反应进程如图所示,下列说法错误的是
,有、无催化剂时,该反应的能量变化与反应进程如图所示,下列说法错误的是
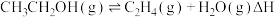 ,有、无催化剂时,该反应的能量变化与反应进程如图所示,下列说法错误的是
,有、无催化剂时,该反应的能量变化与反应进程如图所示,下列说法错误的是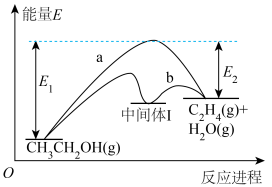
A.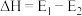 |
B.在 路径中,乙醇 路径中,乙醇 中间体Ⅰ为反应的决速步骤 中间体Ⅰ为反应的决速步骤 |
C.b路径的反应速率大于 路径的 路径的 |
D.反应达到平衡后, 路径中 路径中 的产率比 的产率比 路径的高 路径的高 |
您最近半年使用:0次
名校
解题方法
5 . 聚苯乙烯是一类重要的高分子材料,可通过苯乙烯聚合制得。
I.工业常采用乙苯脱氢的方法制备苯乙烯,其原理为:C6H5-CH2CH3(g) C6H5-CH=CH2(g)+H2(g)
C6H5-CH=CH2(g)+H2(g)  。通过计算机模拟一个乙苯分子在催化剂表面脱氢制苯乙烯的反应,其历程如图1所示(吸附在催化剂表面的物质用*标注):
。通过计算机模拟一个乙苯分子在催化剂表面脱氢制苯乙烯的反应,其历程如图1所示(吸附在催化剂表面的物质用*标注):
(2)写出该反应历程(过渡态1和2中)的决速步骤反应方程式:___________ 。
(3)实验测得乙苯脱氢反应的速率方程为v正=k正p乙苯,v逆=k逆p苯乙烯p氢气(k正、k逆为速率常数,只与温度有关),图2中③代表lgk逆随 的变化关系,则能代表lgk正随
的变化关系,则能代表lgk正随 的变化关系的是___________。
的变化关系的是___________。
(4)某温度下,向1.0L恒容密闭容器中充入0.10mol C6H5-CH2CH3(g),测得乙苯脱氢反应时间(t)与容器的气体总压强(p)的数据见表:
该温度下的浓度平衡常数K=___________ mol/L(结果保留至小数点后两位)。
(5)实际生产中常在恒压条件下掺入高温水蒸气作为反应体系的稀释剂(水蒸气不参加反应),乙苯的转化率随稀释比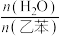 的变化如图所示,说明乙苯转化率变化的原因。
的变化如图所示,说明乙苯转化率变化的原因。___________
又已知水的汽化热为40.8kJ·mol-1。根据以上数据,计算CO2氧化乙苯脱氢反应的 =
=___________ 。
(7)该反应在催化剂表面发生的历程如图所示:___________ ;pH过高时,___________ 。
(8)相对于乙苯脱氢法,CO2氧化法制备苯乙烯工艺的优点为合成速率快、单位时间内的产量高;其缺点为:①反应需要控制酸度,工艺较为复杂;②___________ ;③___________ 。
I.工业常采用乙苯脱氢的方法制备苯乙烯,其原理为:C6H5-CH2CH3(g)
 C6H5-CH=CH2(g)+H2(g)
C6H5-CH=CH2(g)+H2(g)  。通过计算机模拟一个乙苯分子在催化剂表面脱氢制苯乙烯的反应,其历程如图1所示(吸附在催化剂表面的物质用*标注):
。通过计算机模拟一个乙苯分子在催化剂表面脱氢制苯乙烯的反应,其历程如图1所示(吸附在催化剂表面的物质用*标注):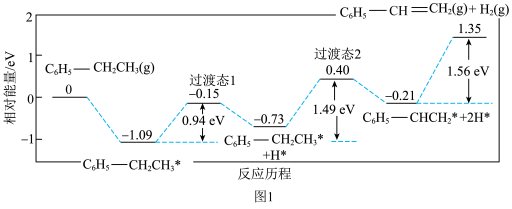
| A.大于0 | B.等于0 | C.小于0 | D.无法确定 |
(2)写出该反应历程(过渡态1和2中)的决速步骤反应方程式:
(3)实验测得乙苯脱氢反应的速率方程为v正=k正p乙苯,v逆=k逆p苯乙烯p氢气(k正、k逆为速率常数,只与温度有关),图2中③代表lgk逆随
 的变化关系,则能代表lgk正随
的变化关系,则能代表lgk正随 的变化关系的是___________。
的变化关系的是___________。
| A.① | B.② | C.④ | D.⑤ |
(4)某温度下,向1.0L恒容密闭容器中充入0.10mol C6H5-CH2CH3(g),测得乙苯脱氢反应时间(t)与容器的气体总压强(p)的数据见表:
| 时间t/h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 | 30 |
| 总压强p/100kPa | 4.91 | 5.58 | 6.32 | 7.31 | 8.54 | 9.26 | 9.32 | 9.33 | 9.33 |
(5)实际生产中常在恒压条件下掺入高温水蒸气作为反应体系的稀释剂(水蒸气不参加反应),乙苯的转化率随稀释比
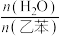 的变化如图所示,说明乙苯转化率变化的原因。
的变化如图所示,说明乙苯转化率变化的原因。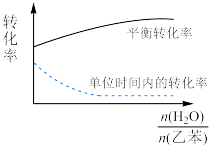
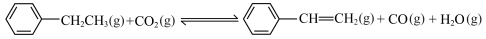
| 物质 |
|
| CO(g) |
| 燃烧热/kJ·mol-1 | -4610.2 | -4376.9 | -283.5 |
 =
=(7)该反应在催化剂表面发生的历程如图所示:
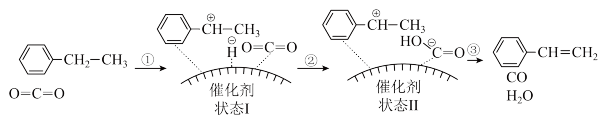
(8)相对于乙苯脱氢法,CO2氧化法制备苯乙烯工艺的优点为合成速率快、单位时间内的产量高;其缺点为:①反应需要控制酸度,工艺较为复杂;②
您最近半年使用:0次
解题方法
6 . 在铜、银催化下,乙烯与氧气反应生成环氧乙烷( )和乙醛,下图是该反应的部分历程。
)和乙醛,下图是该反应的部分历程。

(2)鉴别以上产物乙醛和环氧乙烷可以用___________。
| A.原子发射光谱 | B.原子吸收光谱 | C.核磁共振氢谱 | D.红外光谱 |
(3)以下电子排布式和价电子轨道表示式中,正确且对应微粒为基态原子的是___________。
A.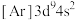 | B.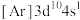 |
C. | D.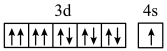 |
(4)已知
 的熔点为1235℃,
的熔点为1235℃, 的熔点为1130℃,二者晶体结构类似,且熔点都较高,但
的熔点为1130℃,二者晶体结构类似,且熔点都较高,但 熔点比
熔点比 高,其原因是
高,其原因是(5)
 晶胞结构如图所示,其中
晶胞结构如图所示,其中 代表的原子是
代表的原子是 ,晶胞参数为a pm,则阿伏加德罗常数值
,晶胞参数为a pm,则阿伏加德罗常数值
 和a的代数式表示)
和a的代数式表示)
 可以形成一种配位化合物,其结构如下图所示。以下说法正确的是___________。
可以形成一种配位化合物,其结构如下图所示。以下说法正确的是___________。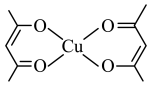
A. 的配位数是2 的配位数是2 |
| B.此配合物中存在配位键、极性键、非极性键 |
| C.配体中O原子提供空轨道 |
D. 提供孤电子对 提供孤电子对 |
(7)已知:常温下,①
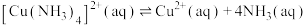
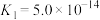 ;
;②


则常温下
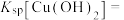
您最近半年使用:0次
名校
解题方法
7 . 卤代烃是重要的工业原料,同时对环境造成严重影响,如破坏臭氧层等,请回答下列问题:
 破坏臭氧层的机理为(以下物质均为气态)
破坏臭氧层的机理为(以下物质均为气态)
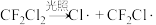 反应①
反应①
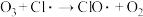 反应②
反应②
 反应③
反应③
(1)活性氯( )的作用是
)的作用是_____ 。
反应②和反应③的能量变化图如下所示
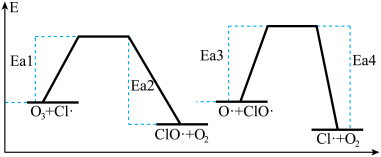
(2)利用上图数据计算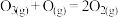 的
的
_____ 。
 破坏臭氧层的机理为(以下物质均为气态)
破坏臭氧层的机理为(以下物质均为气态)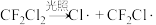 反应①
反应①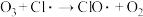 反应②
反应② 反应③
反应③(1)活性氯(
 )的作用是
)的作用是反应②和反应③的能量变化图如下所示

(2)利用上图数据计算
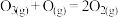 的
的
您最近半年使用:0次
解题方法
8 . 水合肼 在储氢领域有广阔的应用前景,其水溶液呈弱碱性。
在储氢领域有广阔的应用前景,其水溶液呈弱碱性。
(1)肼分解制氢的主要反应为 ,肼的理论储氢密度
,肼的理论储氢密度 。测得肼实际分解时产生的气体中含
。测得肼实际分解时产生的气体中含 ,肼实际储氢密度小于理论值的原因是
,肼实际储氢密度小于理论值的原因是__________ (用化学方程式表示)。
(2)水合肼制氢过程中涉及肼在 催化剂表面分解,如题图1所示。已知催化剂中起作用的部分并不是整个催化剂表面,而是一些特定的位点。
催化剂表面分解,如题图1所示。已知催化剂中起作用的部分并不是整个催化剂表面,而是一些特定的位点。
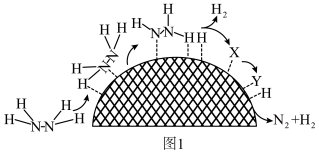
①X的结构简式为__________ 。
②催化剂表面存在 和
和 两种活性位点,两种活性位点分别带不同电性的电荷。肼中的氢原子吸附于
两种活性位点,两种活性位点分别带不同电性的电荷。肼中的氢原子吸附于__________ (填 或
或 )活性位点。已知:断开
)活性位点。已知:断开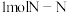 键需要吸收
键需要吸收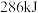 能量,断开
能量,断开 键需要吸收
键需要吸收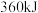 能量。肼在该催化剂表面反应断裂的化学键不是
能量。肼在该催化剂表面反应断裂的化学键不是 键,而是
键,而是 键,原因是
键,原因是__________ 。
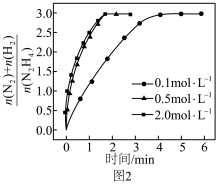
③催化剂存在下,不同浓度的 分解时,测得
分解时,测得 随时间的变化如题图2所示。当
随时间的变化如题图2所示。当 浓度从
浓度从 增加到
增加到 时,反应速率加快;从
时,反应速率加快;从 增加到
增加到 时,反应速率几乎不变,其原因是
时,反应速率几乎不变,其原因是__________ 。
 在储氢领域有广阔的应用前景,其水溶液呈弱碱性。
在储氢领域有广阔的应用前景,其水溶液呈弱碱性。(1)肼分解制氢的主要反应为
 ,肼的理论储氢密度
,肼的理论储氢密度 。测得肼实际分解时产生的气体中含
。测得肼实际分解时产生的气体中含 ,肼实际储氢密度小于理论值的原因是
,肼实际储氢密度小于理论值的原因是(2)水合肼制氢过程中涉及肼在
 催化剂表面分解,如题图1所示。已知催化剂中起作用的部分并不是整个催化剂表面,而是一些特定的位点。
催化剂表面分解,如题图1所示。已知催化剂中起作用的部分并不是整个催化剂表面,而是一些特定的位点。
①X的结构简式为
②催化剂表面存在
 和
和 两种活性位点,两种活性位点分别带不同电性的电荷。肼中的氢原子吸附于
两种活性位点,两种活性位点分别带不同电性的电荷。肼中的氢原子吸附于 或
或 )活性位点。已知:断开
)活性位点。已知:断开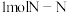 键需要吸收
键需要吸收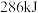 能量,断开
能量,断开 键需要吸收
键需要吸收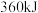 能量。肼在该催化剂表面反应断裂的化学键不是
能量。肼在该催化剂表面反应断裂的化学键不是 键,而是
键,而是 键,原因是
键,原因是③催化剂存在下,不同浓度的
 分解时,测得
分解时,测得 随时间的变化如题图2所示。当
随时间的变化如题图2所示。当 浓度从
浓度从 增加到
增加到 时,反应速率加快;从
时,反应速率加快;从 增加到
增加到 时,反应速率几乎不变,其原因是
时,反应速率几乎不变,其原因是
您最近半年使用:0次
名校
解题方法
9 . 工业上以硫黄或黄铁矿为原料制备硫酸的原理示意图如下。下列叙述错误的是


| A.通过量的空气可将硫黄直接转化为SO3 |
| B.控制温度400-500℃可增大催化剂活性 |
| C.吸收剂b可选用98.3%的浓硫酸 |
| D.工业上可用氨水处理尾气中的SO2 |
您最近半年使用:0次
名校
10 . 含氨污染物治理及其回收利用是重要课题。
(1)用碱液脱硝是目前研究的课题之一。将 通入石灰乳中可制备重要的工业原料
通入石灰乳中可制备重要的工业原料 。该工艺需控制
。该工艺需控制 和
和 物质的量之比接近
物质的量之比接近 。若
。若 ,则会导致
,则会导致___________ 。若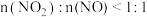 ,则会导致
,则会导致___________ 。
(2)用尿素 (N元素为
(N元素为 价)吸收氮氧化物是一种可行的方法。尿素在高温条存下与
价)吸收氮氧化物是一种可行的方法。尿素在高温条存下与 反应转化成无毒气体,该反应的化学方程式:
反应转化成无毒气体,该反应的化学方程式:___________ 。
(3)工业上在催化剂作用下用 还原工业废气中所含少量
还原工业废气中所含少量 生成
生成 和
和 达到脱除目的,但当温度高于
达到脱除目的,但当温度高于 时,
时, 脱除率下降,原因可能是
脱除率下降,原因可能是___________ 。
(4)用纳米铁粉处理废水中的 :
:
①酸性条件下,纳米铁粉与废水中 反应生成
反应生成 与
与 ,其反应的离子方程式是
,其反应的离子方程式是___________ 。
②研究发现,废水中溶解氧会对 的去除产生一定影响。在初始
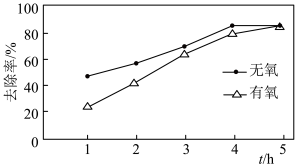
的去除产生一定影响。在初始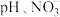 初始浓度、纳米铁粉与硝酸盐质量比均一定的条件下,有氧与无氧条作下
初始浓度、纳米铁粉与硝酸盐质量比均一定的条件下,有氧与无氧条作下 的去除率随反应时间的变化如图所示。
的去除率随反应时间的变化如图所示。 时,有氧条件下
时,有氧条件下 去除率低于无氧条件下,其可能的原因是
去除率低于无氧条件下,其可能的原因是___________ 。
(5)将 铜与
铜与 一定浓度的硝酸反应,铜完全溶解,产生的气体为
一定浓度的硝酸反应,铜完全溶解,产生的气体为 和
和 混合气体,其在标准状况下的体积为
混合气体,其在标准状况下的体积为 ,则混合气体中
,则混合气体中 的体积为
的体积为___________ 。(写出计算过程)
(1)用碱液脱硝是目前研究的课题之一。将
 通入石灰乳中可制备重要的工业原料
通入石灰乳中可制备重要的工业原料 。该工艺需控制
。该工艺需控制 和
和 物质的量之比接近
物质的量之比接近 。若
。若 ,则会导致
,则会导致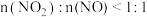 ,则会导致
,则会导致(2)用尿素
 (N元素为
(N元素为 价)吸收氮氧化物是一种可行的方法。尿素在高温条存下与
价)吸收氮氧化物是一种可行的方法。尿素在高温条存下与 反应转化成无毒气体,该反应的化学方程式:
反应转化成无毒气体,该反应的化学方程式:(3)工业上在催化剂作用下用
 还原工业废气中所含少量
还原工业废气中所含少量 生成
生成 和
和 达到脱除目的,但当温度高于
达到脱除目的,但当温度高于 时,
时, 脱除率下降,原因可能是
脱除率下降,原因可能是(4)用纳米铁粉处理废水中的
 :
:①酸性条件下,纳米铁粉与废水中
 反应生成
反应生成 与
与 ,其反应的离子方程式是
,其反应的离子方程式是②研究发现,废水中溶解氧会对
 的去除产生一定影响。在初始
的去除产生一定影响。在初始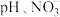 初始浓度、纳米铁粉与硝酸盐质量比均一定的条件下,有氧与无氧条作下
初始浓度、纳米铁粉与硝酸盐质量比均一定的条件下,有氧与无氧条作下 的去除率随反应时间的变化如图所示。
的去除率随反应时间的变化如图所示。 时,有氧条件下
时,有氧条件下 去除率低于无氧条件下,其可能的原因是
去除率低于无氧条件下,其可能的原因是
(5)将
 铜与
铜与 一定浓度的硝酸反应,铜完全溶解,产生的气体为
一定浓度的硝酸反应,铜完全溶解,产生的气体为 和
和 混合气体,其在标准状况下的体积为
混合气体,其在标准状况下的体积为 ,则混合气体中
,则混合气体中 的体积为
的体积为
您最近半年使用:0次