1 . 氮氧化物会导致光化学烟雾和酸雨,在 的催化作用下,
的催化作用下, 可将NO还原为无污染的气体,反应历程如图,下列说法正确的是
可将NO还原为无污染的气体,反应历程如图,下列说法正确的是
 的催化作用下,
的催化作用下, 可将NO还原为无污染的气体,反应历程如图,下列说法正确的是
可将NO还原为无污染的气体,反应历程如图,下列说法正确的是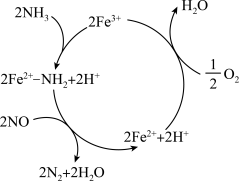
A.基态 的价层电子排布式为 的价层电子排布式为 |
| B.电负性:N>O>H>Fe |
| C.该过程中存在极性键和非极性键的断裂和形成 |
D.图中的总反应可表示为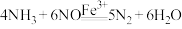 |
您最近一年使用:0次
2024-02-25更新
|
268次组卷
|
6卷引用:福建省福州第三中学2023-2024学年高三上学期第五次质量检测化学试题
名校
解题方法
2 . 金属Ni可活化C2H6放出CH4,其反应历程如图所示:

下列说法正确的是

下列说法正确的是
| A.中间体1→中间体2的过程决定整个历程的反应速率 |
| B.加入催化剂可降低反应的活化能,加快反应速率 |
| C.整个历程中有碳碳键的断裂与形成 |
| D.中间体2→中间体3的过程是放热过程 |
您最近一年使用:0次
名校
3 . 下列实验操作不能达到相应实验目的的是
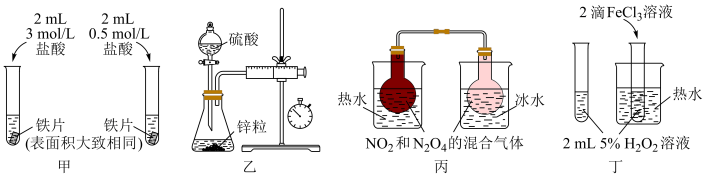

| A.利用甲装置探究浓度对化学反应速率的影响 |
| B.利用乙装置来测定化学反应速率 |
| C.利用丙装置来探究温度对化学平衡的影响 |
| D.利用丁装置来探究催化剂对化学反应速率的影响 |
您最近一年使用:0次
4 . 2021年中国政府工作报告中提出碳中和目标:在2030年前达到最高值,2060年前达到碳中和。因此对二氧化碳的综合利用显得尤为重要。
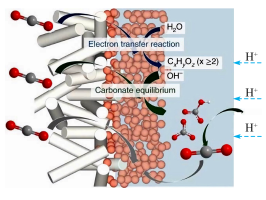

(1)通过电解的方式可实现对二氧化碳的综合利用。2022年7月香港中文大学王莹教授研发新型电解槽实现二氧化碳回收转化效率达到60%以上。转化示意图如图所示,请写出其电极反应方程式:_____ 。
(2)在席夫碱(含“—RC=N—”有机物)修饰的纳米金催化剂上,CO2直接催化加氢成甲酸。其反应历程如图所示,其中吸附在催化剂表面上的物质用*标注。该历程中起决速步骤的化学方程式是_____ 。
(3)通过使用不同新型催化剂,实现二氧化碳加氢合成转化为二甲醚(CH3OCH3)也有广泛的应用。
反应1:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=-49.01KJ/mol
CH3OH(g)+H2O(g) △H=-49.01KJ/mol
反应2:2CH3OH(g) CH3OCH3(g)+H2O(g) △H=-24.52KJ/mol
CH3OCH3(g)+H2O(g) △H=-24.52KJ/mol
反应3:CO2(g)+H2(g) CO(g)+H2O(g) △H=+41.17KJ/mol
CO(g)+H2O(g) △H=+41.17KJ/mol
2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g) △H=
CH3OCH3(g)+3H2O(g) △H=_____ KJ/mol
起始压强为4.0MPa、恒压条件下,通入氢气和二氧化碳的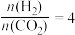 的情况下,不同温度下CO2的平衡转化率和产物的选择性(选择性是指生成某物质消耗的CO2占CO2消耗总量的百分比)如图所示:
的情况下,不同温度下CO2的平衡转化率和产物的选择性(选择性是指生成某物质消耗的CO2占CO2消耗总量的百分比)如图所示:
当温度超过290℃,CO2的平衡转化率随温度升高而增大的原因是_____ 。在图中,在200℃时,若经过0.2s该平衡体系即达到平衡。计算CO2分压的平均变化速率为_____ MPa/s;此时对于反应1的Kp=_____ (MPa)-2(计算的表达式)。



(1)通过电解的方式可实现对二氧化碳的综合利用。2022年7月香港中文大学王莹教授研发新型电解槽实现二氧化碳回收转化效率达到60%以上。转化示意图如图所示,请写出其电极反应方程式:
(2)在席夫碱(含“—RC=N—”有机物)修饰的纳米金催化剂上,CO2直接催化加氢成甲酸。其反应历程如图所示,其中吸附在催化剂表面上的物质用*标注。该历程中起决速步骤的化学方程式是
(3)通过使用不同新型催化剂,实现二氧化碳加氢合成转化为二甲醚(CH3OCH3)也有广泛的应用。
反应1:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H=-49.01KJ/mol
CH3OH(g)+H2O(g) △H=-49.01KJ/mol反应2:2CH3OH(g)
 CH3OCH3(g)+H2O(g) △H=-24.52KJ/mol
CH3OCH3(g)+H2O(g) △H=-24.52KJ/mol反应3:CO2(g)+H2(g)
 CO(g)+H2O(g) △H=+41.17KJ/mol
CO(g)+H2O(g) △H=+41.17KJ/mol2CO2(g)+6H2(g)
 CH3OCH3(g)+3H2O(g) △H=
CH3OCH3(g)+3H2O(g) △H=起始压强为4.0MPa、恒压条件下,通入氢气和二氧化碳的
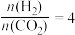 的情况下,不同温度下CO2的平衡转化率和产物的选择性(选择性是指生成某物质消耗的CO2占CO2消耗总量的百分比)如图所示:
的情况下,不同温度下CO2的平衡转化率和产物的选择性(选择性是指生成某物质消耗的CO2占CO2消耗总量的百分比)如图所示:当温度超过290℃,CO2的平衡转化率随温度升高而增大的原因是

您最近一年使用:0次
名校
5 . 铜-铈氧化物(xCuO·yCeO2)可除去H2中少量CO,反应机理如图。Ce是一种活泼金属,价电子为4f15d16s2,步骤(ⅰ)中Cu、Ce的化合价均发生变化。


| A.反应ⅰ中,Cu元素的化合价从+2变成+1 |
| B.反应ⅰ中,Ce元素的化合价从+4变成+2 |
| C.当温度超过150℃时,CO转化率明显下降,可能是因为催化剂的催化活性下降 |
| D.温度过高,催化剂中Cu2+(或Cu+)可能被H2(或CO)还原为Cu造成催化活性下降 |
您最近一年使用:0次
2024-02-24更新
|
275次组卷
|
2卷引用:江苏省无锡市第一中学2023-2024学年高三上学期综合练习(三)化学试题
名校
解题方法
6 . 2021年9月,中国科学院天津工业生物技术研究所成果“无细胞化学酶系统催化 合成淀粉”在国际学术期刊《自然》上发表,引发化学界的极大关注。其中部分核心反应转化如图所示。下列叙述正确的是
合成淀粉”在国际学术期刊《自然》上发表,引发化学界的极大关注。其中部分核心反应转化如图所示。下列叙述正确的是
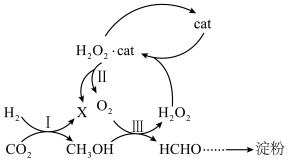
 合成淀粉”在国际学术期刊《自然》上发表,引发化学界的极大关注。其中部分核心反应转化如图所示。下列叙述正确的是
合成淀粉”在国际学术期刊《自然》上发表,引发化学界的极大关注。其中部分核心反应转化如图所示。下列叙述正确的是
A.反应Ⅰ中消耗2mol ,生成 ,生成 为1mol 为1mol |
B.反应Ⅲ需要额外从环境中补充 |
| C.合成过程可采用高温条件,以加快反应速率 |
D.HCHO转化为淀粉[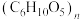 ]的原子利用率可达100% ]的原子利用率可达100% |
您最近一年使用:0次
名校
解题方法
7 . 研究催化剂对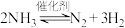 反应速率的影响。恒温恒容时,c(NH3)随时间的变化如下。
反应速率的影响。恒温恒容时,c(NH3)随时间的变化如下。
下列说法不正确 的是
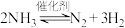 反应速率的影响。恒温恒容时,c(NH3)随时间的变化如下。
反应速率的影响。恒温恒容时,c(NH3)随时间的变化如下。| 时间/min 催化剂 c(NH3)/(×10−3 mol·L−1) | 0 | 20 | 40 | 60 | 80 |
| 催化剂Ⅰ | 2.40 | 2.00 | 1.60 | 1.20 | 0.80 |
| 催化剂Ⅱ | 2.40 | 1.60 | 0.80 | 0.40 | 0.40 |
| A.使用催化剂Ⅰ,0~20 min的平均反应速率v(N2)=1.00×10−5 mol·L−1·min−1 |
B.使用催化剂Ⅰ,达平衡后容器内的压强是初始时的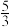 倍 倍 |
| C.相同条件下,使用催化剂Ⅱ可使该反应的活化能降低更多,反应更快 |
| D.相同条件下,使用催化剂Ⅱ不会使该反应的化学平衡常数更大 |
您最近一年使用:0次
名校
解题方法
8 . 在催化剂作用下,HCOOH分解生成CO2和H2可能的反应机理如图所示。下列说法不正确的是
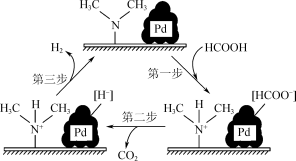

| A.该反应的ΔS>0 |
| B.第一步转化N与H间形成配位键 |
| C.若用HCOOD催化释氢,反应除生成CO2外,还生成D2 |
| D.若用HCOOK溶液代替HCOOH最终所得气体中H2的纯度会提高 |
您最近一年使用:0次
名校
解题方法
9 . 我国对世界郑重承诺:2030年前实现碳达峰,2060年前实现碳中和,而研发CO2的碳捕捉和碳利用技术则是关键。
(1)烟气中CO2的捕集可通过如下所示的物质转化实现。
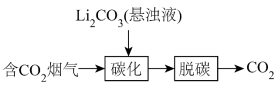
“脱碳”的化学反应方程式为_________ 。
(2)研究脱除烟气中的NO也是环境保护、促进社会可持续发展的重要课题。有氧条件下,在Fe基催化剂表面,NH3还原NO的反应机理如图所示,该过程可描述为_______ 。

(3)2021年9月,《科学》杂志发表论文,介绍人类首次以二氧化碳为原料,不依赖植物光合作用,直接经过11步路径人工合成淀粉。前两步,是先将二氧化碳还原为甲醛。
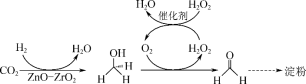
请写出前两步总反应的化学方程式:_________ 。
(4)一种有机多孔电极材料(铜粉沉积在一种有机物的骨架上)电催化还原CO2的装置示意图如左图所示。其他条件一定时,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率(FE%)随电解电压的变化如图所示:

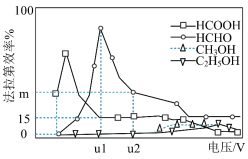
法拉第效率(FE)表示为:FE(B)%= ×100%
×100%
①b电极生成HCOOH的电极反应式为_______ 。
②科研小组利用13CO2代替原有的CO2进行研究,其目的是________ 。
③当电解电压为U2V时,电解生成的HCOOH和HCHO的物质的量之比为3:2,则生成HCHO的法拉第效率m为_______ 。
(1)烟气中CO2的捕集可通过如下所示的物质转化实现。

“脱碳”的化学反应方程式为
(2)研究脱除烟气中的NO也是环境保护、促进社会可持续发展的重要课题。有氧条件下,在Fe基催化剂表面,NH3还原NO的反应机理如图所示,该过程可描述为

(3)2021年9月,《科学》杂志发表论文,介绍人类首次以二氧化碳为原料,不依赖植物光合作用,直接经过11步路径人工合成淀粉。前两步,是先将二氧化碳还原为甲醛。

请写出前两步总反应的化学方程式:
(4)一种有机多孔电极材料(铜粉沉积在一种有机物的骨架上)电催化还原CO2的装置示意图如左图所示。其他条件一定时,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率(FE%)随电解电压的变化如图所示:


法拉第效率(FE)表示为:FE(B)%=
 ×100%
×100%①b电极生成HCOOH的电极反应式为
②科研小组利用13CO2代替原有的CO2进行研究,其目的是
③当电解电压为U2V时,电解生成的HCOOH和HCHO的物质的量之比为3:2,则生成HCHO的法拉第效率m为
您最近一年使用:0次
名校
10 . 恒温恒容的密闭容器中,在某催化剂表面上发生氨的分解反应: ,测得不同起始浓度和催化剂表面积下氨浓度随时间的变化,如下表所示,下列说法不正确的是
,测得不同起始浓度和催化剂表面积下氨浓度随时间的变化,如下表所示,下列说法不正确的是
 ,测得不同起始浓度和催化剂表面积下氨浓度随时间的变化,如下表所示,下列说法不正确的是
,测得不同起始浓度和催化剂表面积下氨浓度随时间的变化,如下表所示,下列说法不正确的是| 编号 | 时间/min c(NH3)/(10-3mol/L) 表面积/cm2 | 0 | 20 | 40 | 60 | 80 |
| ① | a | 2.40 | 2.00 | 1.60 | 1.20 | 0.80 |
| ② | a | 1.20 | 0.80 | 0.40 | x | |
| ③ | 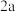 | 2.40 | 1.60 | 0.80 | 0.40 | 0.40 |
A.相同条件下,增加 的浓度,反应速率增大 的浓度,反应速率增大 |
B.实验①, , ,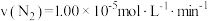 |
C.实验②, 时处于平衡状态, 时处于平衡状态, |
| D.相同条件下,增加催化剂的表面积,反应速率增大 |
您最近一年使用:0次



