解题方法
1 . 合成氨的化学反应为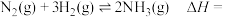
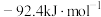 。最近,吉林大学与韩国、加拿大科研人员合作研究,提出基于机械化学(“暴力”干扰使铁活化)在温和条件下由氮气合成氨的新方案(过程如图所示),利用这种方案所得氨的体积分数最终可高达82.5%。下列有关分析错误的是
。最近,吉林大学与韩国、加拿大科研人员合作研究,提出基于机械化学(“暴力”干扰使铁活化)在温和条件下由氮气合成氨的新方案(过程如图所示),利用这种方案所得氨的体积分数最终可高达82.5%。下列有关分析错误的是
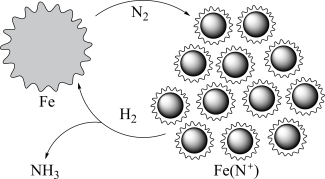
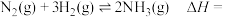
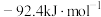 。最近,吉林大学与韩国、加拿大科研人员合作研究,提出基于机械化学(“暴力”干扰使铁活化)在温和条件下由氮气合成氨的新方案(过程如图所示),利用这种方案所得氨的体积分数最终可高达82.5%。下列有关分析错误的是
。最近,吉林大学与韩国、加拿大科研人员合作研究,提出基于机械化学(“暴力”干扰使铁活化)在温和条件下由氮气合成氨的新方案(过程如图所示),利用这种方案所得氨的体积分数最终可高达82.5%。下列有关分析错误的是
| A.铁是该合成氨反应的催化剂 |
| B.采用该方案生产氨气,正反应的活化能降低 |
C.采用该方案生产氨气, 不变 不变 |
| D.该方案氨的含量高,与反应温度较低无关 |
您最近半年使用:0次
解题方法
2 . 钴(Co)合金广泛应用于机械制造等领域。
(1)Co2+和Fe3+与KSCN溶液发生的反应相似。向CoCl2溶液中加入KSCN溶液,生成某种带有两个单位负电荷的蓝色离子,其化学式为_____ 。
(2)推测Co+催化剂表面促进NH3还原NOx的反应历程如图所示。
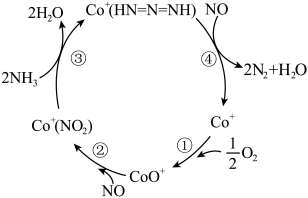
①在反应②中NO作_____ (填“氧化剂”或“还原剂”),与反应④中NO的作用_____ (填“是”或“不是”)一样的。
②写出步骤③对应的离子方程式:_____ 。
③整个历程中氧化剂与还原剂的物质的量之比为_____ 。
(3)现将35.7gCoCO3在空气中加热,可得24.1g钴的氧化物和另一种氧化物。试写出CoCO3在空气中受热时发生反应的化学方程式:_____ 。
(1)Co2+和Fe3+与KSCN溶液发生的反应相似。向CoCl2溶液中加入KSCN溶液,生成某种带有两个单位负电荷的蓝色离子,其化学式为
(2)推测Co+催化剂表面促进NH3还原NOx的反应历程如图所示。

①在反应②中NO作
②写出步骤③对应的离子方程式:
③整个历程中氧化剂与还原剂的物质的量之比为
(3)现将35.7gCoCO3在空气中加热,可得24.1g钴的氧化物和另一种氧化物。试写出CoCO3在空气中受热时发生反应的化学方程式:
您最近半年使用:0次
3 . 下列关于有效碰撞理论与影响速率因素之间关系正确的是
| A.增大反应物浓度,可以提高活化分子百分数,从而提高反应速率 |
| B.对于气体反应来说,通过压缩体积增大压强,可以提高单位体积内活化分子数,从而提高反应速率 |
| C.温度升高,反应所需活化能减少,反应速率增大 |
| D.选用适当的催化剂,分子运动加快,增加了碰撞频率,故反应速率增大 |
您最近半年使用:0次
4 . 下图是我国科研工作者研究MgO(s)与CH4(g)作用最终生成Mg(s)与CH3OH (g)的物质相对能量-反应进程曲线。下列叙述错误的是
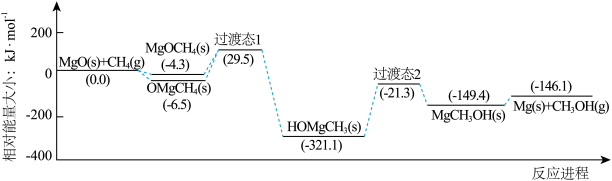

| A.中间体OMgCH4(s)比MgOCH4(s)更稳定 |
| B.MgCH3OH(s)→Mg(s)+CH3OH(g)的速率决定总反应的速率 |
| C.生成HOMgCH3(s)的过程中有极性键的断裂和形成 |
| D.总反应的热化学方程式为MgO(s)+CH4(g)=Mg(s)+CH3OH (g) ΔH= -146.1kJ·mol-1 |
您最近半年使用:0次
5 . 18O标记的乙酸甲酯在足量NaOH溶液中发生水解,部分反应历程可表示为如下所示:
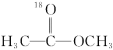 +OH-
+OH-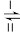
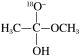
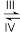
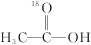 +CH3O-
+CH3O-
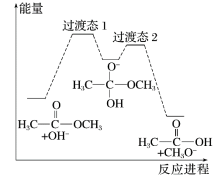
已知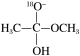

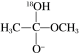 为快速平衡,下列说法正确的是
为快速平衡,下列说法正确的是
| A.反应Ⅱ、Ⅲ为决速步 |
| B.反应结束后,溶液中存在18OH- |
| C.反应结束后,溶液中存在CH318OH |
| D.反应Ⅰ与反应Ⅳ活化能的差值等于图示总反应的焓变 |
您最近半年使用:0次
解题方法
6 . 恒温条件下,将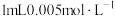 酸性
酸性 溶液和
溶液和 溶液混合,发生反应:
溶液混合,发生反应: 。用
。用 浓度的变化表示的反应速率
浓度的变化表示的反应速率 随时间的变化关系如图所示。下列说法不正确的是
随时间的变化关系如图所示。下列说法不正确的是
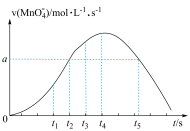
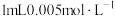 酸性
酸性 溶液和
溶液和 溶液混合,发生反应:
溶液混合,发生反应: 。用
。用 浓度的变化表示的反应速率
浓度的变化表示的反应速率 随时间的变化关系如图所示。下列说法不正确的是
随时间的变化关系如图所示。下列说法不正确的是
A.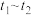 时间段消耗的 时间段消耗的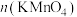 比 比 时间段消耗的少 时间段消耗的少 |
B. 与 与 时刻的 时刻的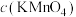 相等 相等 |
C.反应速率逐渐增大的原因可能是生成的 起催化作用 起催化作用 |
D.随着反应进行,溶液中 减小 减小 |
您最近半年使用:0次
7 . 某化学兴趣小组,利用NaHSO3溶液和酸性KMnO4溶液(使用稀H2SO4酸化)反应探究外界因素对化学反应速率的影响。
Ⅰ.原理分析:
(1)反应过程中 被氧化为
被氧化为 ,
, 被还原为Mn2+,请写出实验过程中的离子方程式
被还原为Mn2+,请写出实验过程中的离子方程式_______________ 。
(2)实验过程中,NaHSO3的用量要保证足量,通过比较________ (填“实验现象”)所需时间的长短来判断反应的快慢。
Ⅱ.实验过程
该化学兴趣小组设计如下实验方案:
(3)对比实验①②,使用探究________ 对化学反应速率的影响;若实验②③是用来探究温度对化学反应速率的影响,则V1=________ mL。
(4)若t1=25s,则用HSO 表示实验①的化学反应速率v(
表示实验①的化学反应速率v( )=
)= ________ 。
Ⅲ.实验分析和探究
该化学兴趣小组通过反复实验发现,该反应的化学反应速率总是先增大后减小,该化学兴趣小组猜想可能有两个原因,并作出了猜想:
猜想1:该反应放热,使溶液温度升高,化学反应速率加快
猜想2:新生成的微粒Mn2+对该反应有催化的作用
该化学兴趣小组,通过监测实验①反应过程的温度变化情况,数据显示反应过程中混合溶液的温度基本保持不变,排除猜想1的可能性。并设计第④组实验验证猜想2。设计如下:
(5)为了实验结论的可靠性,试剂X应该选择________。
(6)实验后,若t4_____ t1(填“大于”、“小于”或 “等于”),说明猜想2成立。
Ⅰ.原理分析:
(1)反应过程中
 被氧化为
被氧化为 ,
, 被还原为Mn2+,请写出实验过程中的离子方程式
被还原为Mn2+,请写出实验过程中的离子方程式(2)实验过程中,NaHSO3的用量要保证足量,通过比较
Ⅱ.实验过程
该化学兴趣小组设计如下实验方案:
| 编号 | 实验温度/℃ | 所用试剂的体积/mL | 达到(2)中现象所需时间/min | ||
| 0.6mol/L NaHSO3溶液 | 0.2mol/L酸性KMnO4溶液 | 水 | |||
| ① | 25 | 20 | 20 | 10 | t1 |
| ② | 25 | 25 | 20 | 5 | t2 |
| ③ | 50 | V1 | 20 | 5 | t3 |
(3)对比实验①②,使用探究
(4)若t1=25s,则用HSO
 表示实验①的化学反应速率v(
表示实验①的化学反应速率v( )=
)= Ⅲ.实验分析和探究
该化学兴趣小组通过反复实验发现,该反应的化学反应速率总是先增大后减小,该化学兴趣小组猜想可能有两个原因,并作出了猜想:
猜想1:该反应放热,使溶液温度升高,化学反应速率加快
猜想2:新生成的微粒Mn2+对该反应有催化的作用
该化学兴趣小组,通过监测实验①反应过程的温度变化情况,数据显示反应过程中混合溶液的温度基本保持不变,排除猜想1的可能性。并设计第④组实验验证猜想2。设计如下:
| 编号 | 实验温度/℃ | 所用试剂的体积/mL | 达到(2)中现象所需时间/min | ||
| 0.5mol/L NaHSO3溶液 | 0.2mol/L 酸性KMnO4溶液 | 试剂X | |||
| ④ | 25 | 20 | 20 | 10 | t4 |
(5)为了实验结论的可靠性,试剂X应该选择________。
| A.MnCl2溶液 | B.MnSO4溶液 |
| C.Mn(NO3)2溶液 | D.Mn(HSO3)2溶液 |
(6)实验后,若t4
您最近半年使用:0次
8 . 制造水煤气时发生可逆反应C(s)+H2O(g) CO(g)+H2(g) ΔH >0,下列措施既能提高化学反应速率,又能提高平衡转化率的是
CO(g)+H2(g) ΔH >0,下列措施既能提高化学反应速率,又能提高平衡转化率的是
 CO(g)+H2(g) ΔH >0,下列措施既能提高化学反应速率,又能提高平衡转化率的是
CO(g)+H2(g) ΔH >0,下列措施既能提高化学反应速率,又能提高平衡转化率的是| A.增大压强 | B.升高温度 | C.增大C的用量 | D.加入催化剂 |
您最近半年使用:0次
解题方法
9 . 中国学者在水煤气变换[CO(g)+H2O(g)=CO2(g)+H2(g)]中突破了低温下高转化率与高反应速率不能兼得的难题,该过程是基于双功能催化剂(能吸附不同粒子)催化实现的,反应过程示意图如下:
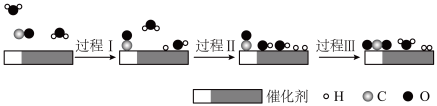
下列说法正确 的是

下列说法
| A.过程Ⅰ和过程Ⅲ均为放热过程 |
| B.图示过程中的3个过程都涉及到了H2O |
| C.过程Ⅲ生成了具有极性共价键的H2、CO2 |
| D.使用催化剂缩小反应物和生成物的能量差 |
您最近半年使用:0次
名校
10 . 工业上常采用氨氧化法制硝酸,其流程是将氨和空气混合后通入灼热的铂铑合金网,反应生成NO(g),生成的一氧化氮与残余的氧气继续反应生成二氧化氮:2NO(g)+O2(g) = 2NO2(g);ΔH = -116.4 kJ·mol-1。随后将二氧化氮通入水中制取硝酸。对于反应2NO(g)+O2(g)  2NO2(g),下列说法正确的是
2NO2(g),下列说法正确的是
 2NO2(g),下列说法正确的是
2NO2(g),下列说法正确的是| A.该反应能够自发的原因是ΔS > 0 |
| B.工业上使用合适的催化剂可提高NO2的生产效率 |
| C.升高温度,该反应V(逆)减小,V(正)增大,平衡向逆反应方向移动 |
| D.2 mol NO(g)和1 mol O2(g)中所含化学键能总和比2 mol NO2(g)中大116.4 kJ·mol-1 |
您最近半年使用:0次



