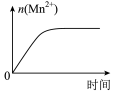
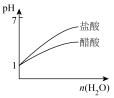
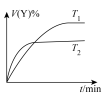
1 . 化学中常用图像直观地描述化学反应的进程或结果。下列对图像描述错误的是
|
|
|
|
 |  |  |  |
A.图 可表示 可表示 酸性溶液与过量的 酸性溶液与过量的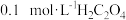 溶液混合时, 溶液混合时, 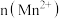 随时间的变化 随时间的变化 |
B.图 可表示体积相等、 可表示体积相等、 的醋酸溶液与盐酸加入等量水稀释时的 的醋酸溶液与盐酸加入等量水稀释时的 变化 变化 |
C.图 可表示温度对可逆反应 可表示温度对可逆反应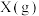  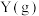 , , 的影响 的影响 |
D.图 可表示压强对可逆反应 可表示压强对可逆反应  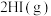 的影响 的影响 |
您最近半年使用:0次
2 . 已知反应3A(g)+2B(g)≒C(g)+4D(g) ΔH<0。如图:a、b表示在一定条件下,D的体积分数D%随时间t的变化情况。若使曲线b变为曲线a ,可采取的措施是
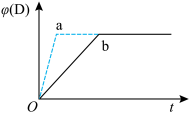
| A.只有⑤ | B.①③ | C.③⑤ | D.②③⑤ |
您最近半年使用:0次
3 . 回答下列问题。
(1)已知在K2Cr2O7的溶液中存在如下平衡:Cr2O (橙色)+H2O
(橙色)+H2O 2CrO
2CrO (黄色)+2H+,向5mL0.1mol/L K7Cr2O7溶液中滴加5-10滴6mol/LNaOH溶液,
(黄色)+2H+,向5mL0.1mol/L K7Cr2O7溶液中滴加5-10滴6mol/LNaOH溶液,___________ 色加深,在此基础上再滴加3~10滴浓H2SO4溶液,___________ 色加深。
(2)草酸与高猛酸钾在酸性条件下能够发生如下反应:2MnO +5H2C2O4+6H+=2Mn2++10CO2↑+8H2O用4mL0.001mol/LKMnO4溶液与2mL0.01mol/LH2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:
+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O用4mL0.001mol/LKMnO4溶液与2mL0.01mol/LH2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:
①如果研究催化剂对化学反应速率的影响,使用实验___________ 和___________ (用 ~
~ 表示,下同);如果研究温度对化学反应速率的影响,使用实验
表示,下同);如果研究温度对化学反应速率的影响,使用实验___________ 和___________ 。
②对比实验 和
和 ,可以研究
,可以研究___________ 对化学反应速率的影响。
(1)已知在K2Cr2O7的溶液中存在如下平衡:Cr2O
 (橙色)+H2O
(橙色)+H2O 2CrO
2CrO (黄色)+2H+,向5mL0.1mol/L K7Cr2O7溶液中滴加5-10滴6mol/LNaOH溶液,
(黄色)+2H+,向5mL0.1mol/L K7Cr2O7溶液中滴加5-10滴6mol/LNaOH溶液,(2)草酸与高猛酸钾在酸性条件下能够发生如下反应:2MnO
 +5H2C2O4+6H+=2Mn2++10CO2↑+8H2O用4mL0.001mol/LKMnO4溶液与2mL0.01mol/LH2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:
+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O用4mL0.001mol/LKMnO4溶液与2mL0.01mol/LH2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:| 组别 | 10%硫酸体积/mL | 温度/℃ | 其他物质 |
 | 2mL | 20 | |
 | 2mL | 20 | 少量MnSO4粉末 |
 | 2mL | 30 | |
 | 1mL | 20 | 1mL蒸馏水 |
 ~
~ 表示,下同);如果研究温度对化学反应速率的影响,使用实验
表示,下同);如果研究温度对化学反应速率的影响,使用实验②对比实验
 和
和 ,可以研究
,可以研究
您最近半年使用:0次
4 . 3H2(g) + 3CO(g) CH3OCH3(g) + CO2(g) ΔH>0一定条件下的密闭容器中,该反应达到平衡后,若要提高CO的转化率,可以采取的措施是
CH3OCH3(g) + CO2(g) ΔH>0一定条件下的密闭容器中,该反应达到平衡后,若要提高CO的转化率,可以采取的措施是___________ (填字母代号)。
a.高温高压 b.加入催化剂 c.减少CO2的浓度 d.增加CO的浓度 e.分离出二甲醚
 CH3OCH3(g) + CO2(g) ΔH>0一定条件下的密闭容器中,该反应达到平衡后,若要提高CO的转化率,可以采取的措施是
CH3OCH3(g) + CO2(g) ΔH>0一定条件下的密闭容器中,该反应达到平衡后,若要提高CO的转化率,可以采取的措施是a.高温高压 b.加入催化剂 c.减少CO2的浓度 d.增加CO的浓度 e.分离出二甲醚
您最近半年使用:0次
5 . 合成氨反应N2 (g)+3H2(g) 2NH3(g)
2NH3(g)  H。若在恒温、恒压条件下向平衡体系中通入氩气,则平衡向
H。若在恒温、恒压条件下向平衡体系中通入氩气,则平衡向___________ 移动(填“正向”、“逆向”或“不”);若使用催化剂,上述反应的 H
H___________ (填“增大”、“减小” 或“不变”)。
 2NH3(g)
2NH3(g)  H。若在恒温、恒压条件下向平衡体系中通入氩气,则平衡向
H。若在恒温、恒压条件下向平衡体系中通入氩气,则平衡向 H
H
您最近半年使用:0次
6 . 图像更能直接地体现化学反应的伴随现象,如能量、速率、浓度等物理量的变化。下列说法错误的是

A.由图甲可知  , ,  ,则 ,则 |
B.图乙是在一定条件下,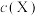 随时间t的变化,正反应 随时间t的变化,正反应 ,M点正反应速率<N点逆反应速率 ,M点正反应速率<N点逆反应速率 |
C.图丙所示反应的热化学方程式为 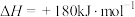 |
D.图丁中t时刻改变的条件可能是增大 的浓度,同时减小 的浓度,同时减小 的浓度 的浓度 |
您最近半年使用:0次
7 . 下列说法正确的是
A.在恒容恒温条件下,当 达到平衡后,再充入一定量的 达到平衡后,再充入一定量的 后达平衡, 后达平衡, 转化率将增大 转化率将增大 |
B.对于反应 达平衡后,缩小容器体积, 达平衡后,缩小容器体积, 的浓度增大 的浓度增大 |
| C.可逆反应达到平衡后,增大任何一种反应物的量,都可使平衡正向移动 |
D.在恒温条件下,当 反应平衡后,缩小体积,活化分子百分数增加 反应平衡后,缩小体积,活化分子百分数增加 |
您最近半年使用:0次
名校
8 . 工业上常用羰基法提纯镍,其原理是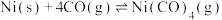
 ,速率方程式为
,速率方程式为 (
( 为速率常数)。在恒容密闭容器中充入足量的含难熔杂质的镍粉和4molCO发生上述反应,测得CO浓度与温度关系如图所示。下列叙述正确的是
为速率常数)。在恒容密闭容器中充入足量的含难熔杂质的镍粉和4molCO发生上述反应,测得CO浓度与温度关系如图所示。下列叙述正确的是
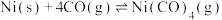
 ,速率方程式为
,速率方程式为 (
( 为速率常数)。在恒容密闭容器中充入足量的含难熔杂质的镍粉和4molCO发生上述反应,测得CO浓度与温度关系如图所示。下列叙述正确的是
为速率常数)。在恒容密闭容器中充入足量的含难熔杂质的镍粉和4molCO发生上述反应,测得CO浓度与温度关系如图所示。下列叙述正确的是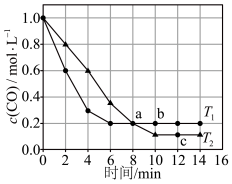
A.上述反应中, |
B.净反应速率: |
C.a点正反应速率: |
D. 温度下,2~6min内用 温度下,2~6min内用 表示的平均反应速率为0.025mol∙L-1∙min-1 表示的平均反应速率为0.025mol∙L-1∙min-1 |
您最近半年使用:0次
7日内更新
|
80次组卷
|
2卷引用:江西省部分学校2023-2024学年高三下学期二轮复习联考验收化学试卷
9 . 合成氨对于合成化肥工业具有重要意义。回答下列问题:
(1)一定温度下,向容积恒定的密闭容器中,通入一定量的 和
和 ,反应达到平衡后,仅改变某一外界条件,反应速率与时间的变化关系如图所示,其中
,反应达到平衡后,仅改变某一外界条件,反应速率与时间的变化关系如图所示,其中 、
、 、
、 时刻所改变的条件可能是:
时刻所改变的条件可能是:
__________ (填标号,下同),
__________ ,
__________ 。
(2)温度为T℃时,将 和
和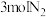 通入2L恒容密闭容器中,15min末,容器内的压强不再改变,测得
通入2L恒容密闭容器中,15min末,容器内的压强不再改变,测得 的转化率为20%。
的转化率为20%。
①下列情况能表明该反应已达到平衡状态的有__________ (填标号)。
A.混合气体的密度不再改变
B. 的物质的量分数不再改变
的物质的量分数不再改变
C.消耗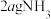 的同时消耗了
的同时消耗了
D.断裂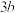 个
个 键的同时断裂
键的同时断裂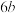 个
个 键
键
②0~15min内, 的平均反应速率
的平均反应速率
__________  ;达到平衡时,容器内
;达到平衡时,容器内 的质量为
的质量为__________ g。
(3)法国化学家勒夏特列根据大量的事实总结出一条经验规律:如果改变影响平衡的一个因素(如温度、压强或参加反应的物质的浓度),平衡就向着能够减弱这种改变的方向移动仅从产率角度考虑,合成氨应在__________ (填“高”或“低”)温条件下进行。工业上通常选择在400~500℃下进行,原因可能是__________ 。
(1)一定温度下,向容积恒定的密闭容器中,通入一定量的
 和
和 ,反应达到平衡后,仅改变某一外界条件,反应速率与时间的变化关系如图所示,其中
,反应达到平衡后,仅改变某一外界条件,反应速率与时间的变化关系如图所示,其中 、
、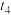 、
、 时刻所改变的条件可能是:
时刻所改变的条件可能是:
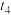

(2)温度为T℃时,将
 和
和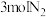 通入2L恒容密闭容器中,15min末,容器内的压强不再改变,测得
通入2L恒容密闭容器中,15min末,容器内的压强不再改变,测得 的转化率为20%。
的转化率为20%。①下列情况能表明该反应已达到平衡状态的有
A.混合气体的密度不再改变
B.
 的物质的量分数不再改变
的物质的量分数不再改变C.消耗
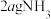 的同时消耗了
的同时消耗了
D.断裂
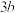 个
个 键的同时断裂
键的同时断裂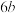 个
个 键
键②0~15min内,
 的平均反应速率
的平均反应速率
 ;达到平衡时,容器内
;达到平衡时,容器内 的质量为
的质量为(3)法国化学家勒夏特列根据大量的事实总结出一条经验规律:如果改变影响平衡的一个因素(如温度、压强或参加反应的物质的浓度),平衡就向着能够减弱这种改变的方向移动仅从产率角度考虑,合成氨应在
您最近半年使用:0次
10 . 在密闭容器中发生反应:xA(g)+yB(g)  zC(g)平衡时测得A的浓度为0.50mol•L-1保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.30 mol•L-1。下列判断正确的是
zC(g)平衡时测得A的浓度为0.50mol•L-1保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.30 mol•L-1。下列判断正确的是
 zC(g)平衡时测得A的浓度为0.50mol•L-1保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.30 mol•L-1。下列判断正确的是
zC(g)平衡时测得A的浓度为0.50mol•L-1保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.30 mol•L-1。下列判断正确的是| A.x+y<z | B.平衡向正反应方向移动 | C.C的体积分数增大 | D.B的转化率降低 |
您最近半年使用:0次