23-24高三上·上海浦东新·阶段练习
名校
解题方法
1 . 化石燃料的合理开发利用。2023年3月,科研成果“温和压力条件下实现乙二醇合成”入选2022年度中国科学十大进展,该成果有望促进煤化工的绿色发展,降低我国乙二醇产业对石油的依赖。
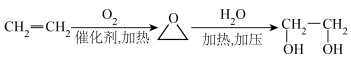
(1)在实际工业生产中,乙二醇可通过环氧乙烷与水直接化合的方法合成,其合成路线如图所示,下列说法正确的是___________ 。
(2)乙二醛是一种重要的精细化工产品,主要用于纺织工业,做纤维处理剂能增加棉花、尼龙等纤维的纺缩和防皱性,可利用乙二醇气相氧化法进行工业制备。
已知: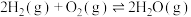
 kJ/mol,
kJ/mol,

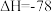 kJ/mol,
kJ/mol,
则乙二醇气相氧化反应 的
的
___________ ;相同温度下,该反应的化学平衡常数
___________ (用含 、
、 的代数式表示)。
的代数式表示)。
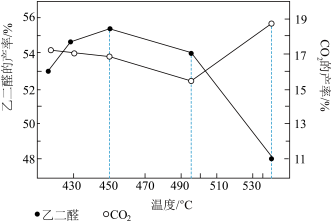
(3)对于上述乙二醇气相氧化反应,当原料气中氧醇比为1.35时,乙二醛和副产物 的产率与反应温度的关系如下图所示,反应温度在450~495℃之间和超过495℃时,乙二醛产率降低的主要原因分别是
的产率与反应温度的关系如下图所示,反应温度在450~495℃之间和超过495℃时,乙二醛产率降低的主要原因分别是___________ 、___________ 。
(4)在恒温恒容下,如果从反应物出发建立平衡,一定能说明乙二醇气相氧化反应达到平衡状态的是___________(填选项字母)。
(5)合成环已酮缩乙二醇的原理为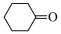 +HOCH2CH2OH
+HOCH2CH2OH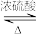
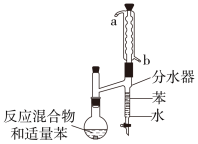
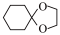 +H2O,在反应体系中加入适量苯,利用如图装置(加热及夹持装置省略)制备环已酮缩乙二醇,下列说法正确的是
+H2O,在反应体系中加入适量苯,利用如图装置(加热及夹持装置省略)制备环已酮缩乙二醇,下列说法正确的是___________ 。
(1)在实际工业生产中,乙二醇可通过环氧乙烷与水直接化合的方法合成,其合成路线如图所示,下列说法正确的是

| A.乙二醇可用于生产汽车防冻液 | B. 的结构简式为 的结构简式为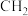 |
| C.乙二醇和甘油互为同系物 | D.上述合成路线的设计不符合“绿色化学”理念 |
已知:
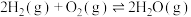
 kJ/mol,
kJ/mol,

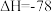 kJ/mol,
kJ/mol,
则乙二醇气相氧化反应
 的
的

 、
、 的代数式表示)。
的代数式表示)。(3)对于上述乙二醇气相氧化反应,当原料气中氧醇比为1.35时,乙二醛和副产物
 的产率与反应温度的关系如下图所示,反应温度在450~495℃之间和超过495℃时,乙二醛产率降低的主要原因分别是
的产率与反应温度的关系如下图所示,反应温度在450~495℃之间和超过495℃时,乙二醛产率降低的主要原因分别是
(4)在恒温恒容下,如果从反应物出发建立平衡,一定能说明乙二醇气相氧化反应达到平衡状态的是___________(填选项字母)。
| A.体系压强不再变化 | B.氧醇比保持不变 |
| C.混合气体的密度保持不变 | D.气体平均相对分子质量保持不变 |
 +HOCH2CH2OH
+HOCH2CH2OH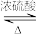
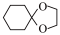 +H2O,在反应体系中加入适量苯,利用如图装置(加热及夹持装置省略)制备环已酮缩乙二醇,下列说法正确的是
+H2O,在反应体系中加入适量苯,利用如图装置(加热及夹持装置省略)制备环已酮缩乙二醇,下列说法正确的是
| A.a是冷却水的进水口 |
B.苯可将反应产生的水及时带出,也可用 替代苯 替代苯 |
| C.当苯即将回流至烧瓶中时,应将分水器中的水和苯放出 |
| D.利用分水器分离出水,可提高环已酮缩乙二醇的产率 |
您最近一年使用:0次
名校
2 . 随着时代的进步,人类对能源的需求量与日俱增,我国全球首套焦炉气化学合成法生产无水乙醇的工业示范项目打通全流程实现,项目投产成功。
(1)3CO(g)+6H2(g) CH3CH2OH(g)+CH3OH(g)+H2O(g) ΔH=
CH3CH2OH(g)+CH3OH(g)+H2O(g) ΔH=_______ (用含ΔH1、ΔH2、ΔH3的代数式表示)。
已知:i.2CO(g)+4H2(g) CH3OCH3(g)+H2O(g) ΔH1
CH3OCH3(g)+H2O(g) ΔH1
ii.CH3OCH3(g)+CO(g) CH3COOCH3(g) ΔH2
CH3COOCH3(g) ΔH2
iii.CH3COOCH3(g)+2H2(g) CH3CH2OH(g)+CH3OH(g) ΔH3
CH3CH2OH(g)+CH3OH(g) ΔH3
在恒温恒容密闭容器中充入3molCO(g)和7molH2(g)仅发生反应3CO(g)+6H2(g) CH3CH2OH(g)+CH3OH(g)+H2O(g),下列叙述正确的是
CH3CH2OH(g)+CH3OH(g)+H2O(g),下列叙述正确的是_______ (填标号)。
A.混合气体总压强不随时间变化时,反应达到平衡状态
B.反应达到平衡时,CH3CH2OH体积分数可能为25%
C.反应达到平衡后,再充入少量CO,CO的平衡转化率增大
D.反应达到平衡后,再加入高效催化剂,乙醇产率保持不变
(2)醋酸酯加氢制乙醇是一个乙酰基产物制备乙醇的路线。
①醋酸酯加氢的催化效能如表所示:
上述实验中,催化效能最好的为实验_______ (填序号),与之对比,实验3中,醋酸酯平衡转化率较低的主要原因可能是________ (从表中所给条件的角度分析)。
②醋酸甲酯加氢历程一般认为可分为如下步骤(*代表催化剂位点,已知:CH3CO*+H·→CH3CHO):
a.CH3COOCH3→CH3CO·+CH3O·
b.CH3CO·+*→CH3CO*(慢)
c.CH3O·+*→CH3O*(快)
d.CH3CO*+3H·→CH3CH2OH
e.CH3O*+H·→CH3OH
……
其中,在b和c的步骤中,活化能较小的是_______ (填标号,下同),控制总反应速率的步骤是_______ ,分析上述步骤,副产物除CH3OH外,还可能有_______ (写一种即可)。
(3)甲醇也是新能源的重要组成部分。
以CO2、H2为原料合成CH3OH涉及的反应如下:
iv.CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH4<0
CH3OH(g)+H2O(g) ΔH4<0
v.CO2(g)+H2(g) CO(g)+H2O(g) ΔH5>0
CO(g)+H2O(g) ΔH5>0
vi.CO(g)+2H2(g) CH3OH(g) ΔH6<0
CH3OH(g) ΔH6<0
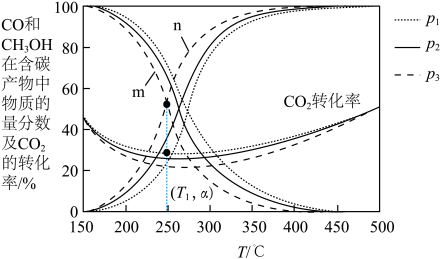
在不同压强下、按照n(CO2)∶n(H2)=1∶3进行投料,在容器中发生上述3个反应,平衡时,CO和CH3OH在含碳产物(即CH3OH和CO)中物质的量分数及CO2的转化率随温度的变化如图,压强p1、p2、p3由大到小的顺序为_______ ,曲线_______ (填“m”或“n”)代表CH3OH在含碳产物中物质的量分数,在T1℃下,压强为p3时,反应v的浓度平衡常数Kc=_______ (填含α的表达式)。
(1)3CO(g)+6H2(g)
 CH3CH2OH(g)+CH3OH(g)+H2O(g) ΔH=
CH3CH2OH(g)+CH3OH(g)+H2O(g) ΔH=已知:i.2CO(g)+4H2(g)
 CH3OCH3(g)+H2O(g) ΔH1
CH3OCH3(g)+H2O(g) ΔH1ii.CH3OCH3(g)+CO(g)
 CH3COOCH3(g) ΔH2
CH3COOCH3(g) ΔH2iii.CH3COOCH3(g)+2H2(g)
 CH3CH2OH(g)+CH3OH(g) ΔH3
CH3CH2OH(g)+CH3OH(g) ΔH3在恒温恒容密闭容器中充入3molCO(g)和7molH2(g)仅发生反应3CO(g)+6H2(g)
 CH3CH2OH(g)+CH3OH(g)+H2O(g),下列叙述正确的是
CH3CH2OH(g)+CH3OH(g)+H2O(g),下列叙述正确的是A.混合气体总压强不随时间变化时,反应达到平衡状态
B.反应达到平衡时,CH3CH2OH体积分数可能为25%
C.反应达到平衡后,再充入少量CO,CO的平衡转化率增大
D.反应达到平衡后,再加入高效催化剂,乙醇产率保持不变
(2)醋酸酯加氢制乙醇是一个乙酰基产物制备乙醇的路线。
①醋酸酯加氢的催化效能如表所示:
| 实验组 | 催化剂 | 原料 | 反应条件 | 反应性能 | ||
| 温度/°C | 压力/MPa | 转化率/% | 选择性/% | |||
| 1 | Cu/SiO2 | 醋酸甲酯 | 190 | 28 | 96.1 | 99.0 |
| 2 | Cu-Cr | 醋酸乙酯 | 250 | 2.8 | 接近完全 | 93.8 |
| 3 | Cu/ZnO | 醋酸乙酯 | 185 | 1 | 56 | 99.0 |
| 4 | Cu/SiO2 | 醋酸乙酯 | 280 | 4.0 | 94.6 | 96.6 |
②醋酸甲酯加氢历程一般认为可分为如下步骤(*代表催化剂位点,已知:CH3CO*+H·→CH3CHO):
a.CH3COOCH3→CH3CO·+CH3O·
b.CH3CO·+*→CH3CO*(慢)
c.CH3O·+*→CH3O*(快)
d.CH3CO*+3H·→CH3CH2OH
e.CH3O*+H·→CH3OH
……
其中,在b和c的步骤中,活化能较小的是
(3)甲醇也是新能源的重要组成部分。
以CO2、H2为原料合成CH3OH涉及的反应如下:
iv.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH4<0
CH3OH(g)+H2O(g) ΔH4<0v.CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH5>0
CO(g)+H2O(g) ΔH5>0vi.CO(g)+2H2(g)
 CH3OH(g) ΔH6<0
CH3OH(g) ΔH6<0在不同压强下、按照n(CO2)∶n(H2)=1∶3进行投料,在容器中发生上述3个反应,平衡时,CO和CH3OH在含碳产物(即CH3OH和CO)中物质的量分数及CO2的转化率随温度的变化如图,压强p1、p2、p3由大到小的顺序为

您最近一年使用:0次
2023-03-13更新
|
613次组卷
|
4卷引用:辽宁省锦州市部分学校2022-2023学年高三3月联考化学试题
3 . 我国科研人员成功研制出一条从二氧化碳合成淀粉的途径,其中第一步为 ,为推进“碳达峰”和“碳中和”目标实现的技术路线提供了一种新思路。
,为推进“碳达峰”和“碳中和”目标实现的技术路线提供了一种新思路。
(1)计算机模拟该反应的反应历程如下图所示,其中吸附在催化剂上面的物质用“*”标注,“TS”表示过渡状态。

① =
=_______ kJ∙mol-1。
②该反应历程中反应速率最快步骤的化学方程式为_______ 。
(2)实验研究表明,其他条件相同时,使用分子筛(分子筛能选择性分离出水蒸气)能有效提高甲醇的平衡产率,其原因是_______ 。
(3)540K下,分别按初始投料比 进行该反应,得到不同压强下H2的平衡转化率关系如图:
进行该反应,得到不同压强下H2的平衡转化率关系如图:

①投料比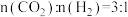 的曲线为
的曲线为_______ (填“a”、“b”或“c”),说明理由_______ 。
②该反应压强平衡常数的表达式
_______ 0(用平衡分压代替平衡浓度)。
③已知540K下该反应 ,某时刻测得某容器内
,某时刻测得某容器内 ,
, ,
,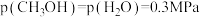 ,此时v(正)
,此时v(正)_______ v(逆)(填“>”、“=”或“>”)。
(4)目前,科研人员在研究光电催化CO2还原为甲醇的领域也取得了一定的进展,其原理如图所示,则生成甲醇的电极反应式为_______ 。

 ,为推进“碳达峰”和“碳中和”目标实现的技术路线提供了一种新思路。
,为推进“碳达峰”和“碳中和”目标实现的技术路线提供了一种新思路。(1)计算机模拟该反应的反应历程如下图所示,其中吸附在催化剂上面的物质用“*”标注,“TS”表示过渡状态。

①
 =
=②该反应历程中反应速率最快步骤的化学方程式为
(2)实验研究表明,其他条件相同时,使用分子筛(分子筛能选择性分离出水蒸气)能有效提高甲醇的平衡产率,其原因是
(3)540K下,分别按初始投料比
 进行该反应,得到不同压强下H2的平衡转化率关系如图:
进行该反应,得到不同压强下H2的平衡转化率关系如图:
①投料比
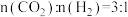 的曲线为
的曲线为②该反应压强平衡常数的表达式

③已知540K下该反应
 ,某时刻测得某容器内
,某时刻测得某容器内 ,
, ,
,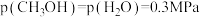 ,此时v(正)
,此时v(正)(4)目前,科研人员在研究光电催化CO2还原为甲醇的领域也取得了一定的进展,其原理如图所示,则生成甲醇的电极反应式为

您最近一年使用:0次
解题方法
4 . “Cl化学”是指以碳单质或分子中含1个碳原子的物质(如CO、CO2、CH4、CH3OH等)为原料合成工业产品的化学工艺,对开发新能源和控制环境污染有重要意义。中科院天津工生所利用化学催化剂将高浓度二氧化碳在高密度氢能作用下还原成碳一(C1)化合物,然后通过设计构建碳一聚合新酶,依据化学聚糖反应原理将碳一化合物聚合成碳三(C3)化合物,最后通过生物途径优化,将碳三化合物聚合成碳六(C6)化合物,再进一步合成直链和支链淀粉(Cn化合物)。在实验室中首次实现从二氧化碳到淀粉分子的全合成。
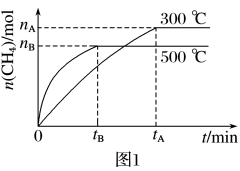
(1)科学家成功研制出一种新型催化剂,能将CO2转变为甲烷。在常压、300℃条件下,CO2与H2按体积之比1∶4反应,CO2转化率可达90%。一定条件下,某兴趣小组在容积为V L的密闭容器中发生此反应达到化学平衡状态。
①该反应的平衡常数表达式为___________ 。
②由如图可知该反应的△H___________ 0(填“>”、“<”或“=”);300℃时,从反应开始到达平衡,以H2的浓度变化表示的化学反应速率是___________ (用 、
、 、V表示)。
、V表示)。
(2)已知 ,
, ,控制一定条件,该反应能自发进行,则
,控制一定条件,该反应能自发进行,则
___________ 0(填“>”,“<”或“=”)。在一定温度下,向一容积可变的容器中充入 、
、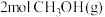 ,
, 的转化率与反应时间的关系如图所示。在t时加压,若t1时容器容积为1000 mL,则t2时容器容积为
的转化率与反应时间的关系如图所示。在t时加压,若t1时容器容积为1000 mL,则t2时容器容积为___________ mL。

(3)利用回收的 制取甲醛的反应为
制取甲醛的反应为

①为提高上述反应中H2的平衡转化率,可以采取的措施有___________ 、___________ (任写两条)。
②实验室在2 L恒容密闭容器中模拟上述合成HCHO的实验。 时将
时将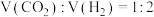 的
的 和
和 混合气体充入容器中,每隔一定时间测得容器内混合气体压强如表所示:
混合气体充入容器中,每隔一定时间测得容器内混合气体压强如表所示:
已知: ,即用B物质的分压变化表示
,即用B物质的分压变化表示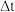 时间内反应的平均反应速率。0~10min内该反应的平均反应速率
时间内反应的平均反应速率。0~10min内该反应的平均反应速率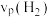 为
为___________  。10min时,CO2的转化率为
。10min时,CO2的转化率为___________ (保留小数点后一位)。
(1)科学家成功研制出一种新型催化剂,能将CO2转变为甲烷。在常压、300℃条件下,CO2与H2按体积之比1∶4反应,CO2转化率可达90%。一定条件下,某兴趣小组在容积为V L的密闭容器中发生此反应达到化学平衡状态。
①该反应的平衡常数表达式为
②由如图可知该反应的△H
 、
、 、V表示)。
、V表示)。
(2)已知
 ,
, ,控制一定条件,该反应能自发进行,则
,控制一定条件,该反应能自发进行,则
 、
、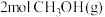 ,
, 的转化率与反应时间的关系如图所示。在t时加压,若t1时容器容积为1000 mL,则t2时容器容积为
的转化率与反应时间的关系如图所示。在t时加压,若t1时容器容积为1000 mL,则t2时容器容积为
(3)利用回收的
 制取甲醛的反应为
制取甲醛的反应为

①为提高上述反应中H2的平衡转化率,可以采取的措施有
②实验室在2 L恒容密闭容器中模拟上述合成HCHO的实验。
 时将
时将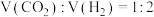 的
的 和
和 混合气体充入容器中,每隔一定时间测得容器内混合气体压强如表所示:
混合气体充入容器中,每隔一定时间测得容器内混合气体压强如表所示:| 时间/min | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 压强/kPa | 1.08 | 0.96 | 0.88 | 0.82 | 0.80 | 0.80 | 0.80 |
 ,即用B物质的分压变化表示
,即用B物质的分压变化表示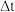 时间内反应的平均反应速率。0~10min内该反应的平均反应速率
时间内反应的平均反应速率。0~10min内该反应的平均反应速率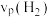 为
为 。10min时,CO2的转化率为
。10min时,CO2的转化率为
您最近一年使用:0次
名校
解题方法
5 . 氢能是一种很有前景的新能源,位于成都市郫都区的油氢合建站为成都大运会氢燃料电池汽车零排放、零污染、绿色低碳的办赛理念提供了能源保障。CH4-CO2催化重整是目前制取氢气的同时减缓温室效应的重要方法。
已知:CH4-CO2催化重整的反应阶段如下:
Ⅰ:CH4(g) C(s)+2H2(g) △H1 K1
C(s)+2H2(g) △H1 K1
Ⅱ:CO2(g)+C(s) 2CO(g) △H2 K2
2CO(g) △H2 K2
回答下列问题:
(1)CH4、CO2催化重整生成CO、H2的热化学方程式为________ (反应热用△H1、△H2表示),该反应的平衡常数K=________ (用K1、K2表示)。
(2)在恒温恒压下,向甲、乙两个密闭容器中均通入10molCH4和10molCO2进行催化重整,并分别加入两种不同催化剂ⅰ和ⅱ,测得相同时间内CO的平衡百分含量随温度的变化关系如图所示。
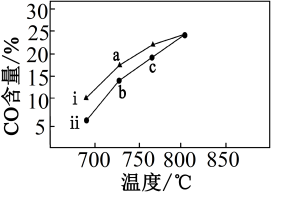
①由图可知,△H_______ 0(填“>”或“<”)。催化剂_______ (填“ⅰ”或“ⅱ”)效果更好。
②能够说明CH4-CO2催化重整生成CO、H2达到化学平衡状态的是_______ (填标号)。
A.容器内气体密度保持不变
B.化学平衡常数保持不变
C.CO2的体积分数保持不变
D.相同时间内,断裂4molC-H的同时生成2molH-H键
(3)利用工业废气中的CO2合成甲醇,选用氢气或水作为氢源,可能设计出以下两个反应:
Ⅰ.CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
Ⅱ.CO2(g)+2H2O(g) CH3OH(g)+
CH3OH(g)+ O2(g)
O2(g)
上述两个化学反应的焓变和熵变如表所示(假设反应的焓变和熵变不随温度的改变而改变):
你认为反应_______ (填“Ⅰ”或“Ⅱ”)更适宜甲替的工业生产,理由是_______ 。
(4)实验室在模拟CO2(g)+3H2(g) CH3OH(g)+H2O(g)制取甲醇的过程中,将气体体积比为1:1的CO2和H2混合气体按相同流速通过反应器,CO2的转化率[α(CO2)]随温度和压强的变化关系如图所示(已知:该反应的催化剂活性受温度影响变化不大。):
CH3OH(g)+H2O(g)制取甲醇的过程中,将气体体积比为1:1的CO2和H2混合气体按相同流速通过反应器,CO2的转化率[α(CO2)]随温度和压强的变化关系如图所示(已知:该反应的催化剂活性受温度影响变化不大。):
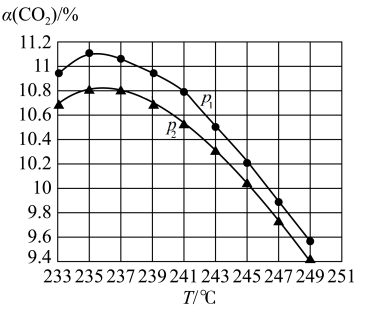
①p1_______ p2(填“>”“<”或“=”)。
②分析236℃后曲线变化的原因:________ 。
已知:CH4-CO2催化重整的反应阶段如下:
Ⅰ:CH4(g)
 C(s)+2H2(g) △H1 K1
C(s)+2H2(g) △H1 K1Ⅱ:CO2(g)+C(s)
 2CO(g) △H2 K2
2CO(g) △H2 K2回答下列问题:
(1)CH4、CO2催化重整生成CO、H2的热化学方程式为
(2)在恒温恒压下,向甲、乙两个密闭容器中均通入10molCH4和10molCO2进行催化重整,并分别加入两种不同催化剂ⅰ和ⅱ,测得相同时间内CO的平衡百分含量随温度的变化关系如图所示。

①由图可知,△H
②能够说明CH4-CO2催化重整生成CO、H2达到化学平衡状态的是
A.容器内气体密度保持不变
B.化学平衡常数保持不变
C.CO2的体积分数保持不变
D.相同时间内,断裂4molC-H的同时生成2molH-H键
(3)利用工业废气中的CO2合成甲醇,选用氢气或水作为氢源,可能设计出以下两个反应:
Ⅰ.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)Ⅱ.CO2(g)+2H2O(g)
 CH3OH(g)+
CH3OH(g)+ O2(g)
O2(g)上述两个化学反应的焓变和熵变如表所示(假设反应的焓变和熵变不随温度的改变而改变):
| 反应 | △H/(kJ•mol-1) | △S/(J•mol-1•K-1) |
| Ⅰ | -48.97 | -177.16 |
| Ⅱ | +676.48 | -43.87 |
(4)实验室在模拟CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)制取甲醇的过程中,将气体体积比为1:1的CO2和H2混合气体按相同流速通过反应器,CO2的转化率[α(CO2)]随温度和压强的变化关系如图所示(已知:该反应的催化剂活性受温度影响变化不大。):
CH3OH(g)+H2O(g)制取甲醇的过程中,将气体体积比为1:1的CO2和H2混合气体按相同流速通过反应器,CO2的转化率[α(CO2)]随温度和压强的变化关系如图所示(已知:该反应的催化剂活性受温度影响变化不大。):
①p1
②分析236℃后曲线变化的原因:
您最近一年使用:0次
2023-11-03更新
|
274次组卷
|
3卷引用:四川省遂宁市射洪中学校2023-2024学年高二上学期(强基班)11月月考化学试题
6 . 二氧化铈 是一种用途广泛的稀土化合物。以氟碳铈矿(主要含
是一种用途广泛的稀土化合物。以氟碳铈矿(主要含 )为原料制备
)为原料制备 的一种工艺流程如图所示:
的一种工艺流程如图所示: 能与
能与 结合成
结合成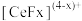 ,也能与
,也能与 结合成
结合成 ;
;
②在硫酸体系中 能被萃取剂
能被萃取剂 萃取,而
萃取,而 不能。
不能。
回答下列问题:
(1)氧化焙烧中氧化的目的是_______ 。
(2)“萃取”时存在反应: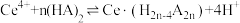 ,如图中D是分配比,表示
,如图中D是分配比,表示 分别在有机层中与水层中存在形式的物质的量浓度之比
分别在有机层中与水层中存在形式的物质的量浓度之比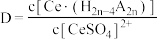 保持其它条件不变,若在起始料液中加入不同量的
保持其它条件不变,若在起始料液中加入不同量的 以改变水层中的
以改变水层中的 ,请解释D随起始料液中
,请解释D随起始料液中 变化的原因:
变化的原因:_______ 。 的作用下
的作用下 转化为
转化为 ,反应的离子方程式为:
,反应的离子方程式为:_______ 。
(4)向水层中加入 溶液来调节溶液的
溶液来调节溶液的 ,
, 应大于
应大于_______ 时, 完全生成
完全生成 沉淀。(已知
沉淀。(已知 )
)
(5)“氧化”步骤中氧化剂与还原剂物质的量之比为_______ 。
(6) 是汽车尾气净化催化剂的关键成分,它能在还原气氛中供氧,在氧化气氛中耗氧,在尾气消除过程中发生着
是汽车尾气净化催化剂的关键成分,它能在还原气氛中供氧,在氧化气氛中耗氧,在尾气消除过程中发生着 的循环,请写出
的循环,请写出 消除
消除 尾气(气体产物是空气的某一成分)的化学方程式
尾气(气体产物是空气的某一成分)的化学方程式_______ 。
(7)氧化铈 ,常用作玻璃工业添加剂,在其立方晶胞中掺杂
,常用作玻璃工业添加剂,在其立方晶胞中掺杂 ,
, 占据原来
占据原来 的位置,可以得到更稳定的结构,如图所示,
的位置,可以得到更稳定的结构,如图所示, 晶胞中
晶胞中 与最近
与最近 的核间距为
的核间距为 。(已知:
。(已知: 的空缺率
的空缺率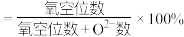 )
) 点原子的分数坐标为
点原子的分数坐标为 ,则
,则 点原子的分数坐标为
点原子的分数坐标为_______ 。
② 晶胞中与
晶胞中与 最近的
最近的 的个数为
的个数为_______ 。
③ 晶体的密度为
晶体的密度为_______ (只需列出表达式)。
④若掺杂 后得到
后得到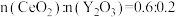 的晶体,则此晶体中
的晶体,则此晶体中 的空缺率为
的空缺率为_______ 。
 是一种用途广泛的稀土化合物。以氟碳铈矿(主要含
是一种用途广泛的稀土化合物。以氟碳铈矿(主要含 )为原料制备
)为原料制备 的一种工艺流程如图所示:
的一种工艺流程如图所示: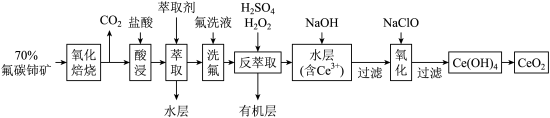
 能与
能与 结合成
结合成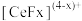 ,也能与
,也能与 结合成
结合成 ;
;②在硫酸体系中
 能被萃取剂
能被萃取剂 萃取,而
萃取,而 不能。
不能。回答下列问题:
(1)氧化焙烧中氧化的目的是
(2)“萃取”时存在反应:
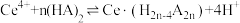 ,如图中D是分配比,表示
,如图中D是分配比,表示 分别在有机层中与水层中存在形式的物质的量浓度之比
分别在有机层中与水层中存在形式的物质的量浓度之比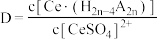 保持其它条件不变,若在起始料液中加入不同量的
保持其它条件不变,若在起始料液中加入不同量的 以改变水层中的
以改变水层中的 ,请解释D随起始料液中
,请解释D随起始料液中 变化的原因:
变化的原因: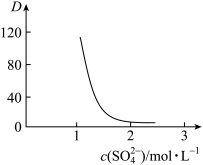
 的作用下
的作用下 转化为
转化为 ,反应的离子方程式为:
,反应的离子方程式为:(4)向水层中加入
 溶液来调节溶液的
溶液来调节溶液的 ,
, 应大于
应大于 完全生成
完全生成 沉淀。(已知
沉淀。(已知 )
)(5)“氧化”步骤中氧化剂与还原剂物质的量之比为
(6)
 是汽车尾气净化催化剂的关键成分,它能在还原气氛中供氧,在氧化气氛中耗氧,在尾气消除过程中发生着
是汽车尾气净化催化剂的关键成分,它能在还原气氛中供氧,在氧化气氛中耗氧,在尾气消除过程中发生着 的循环,请写出
的循环,请写出 消除
消除 尾气(气体产物是空气的某一成分)的化学方程式
尾气(气体产物是空气的某一成分)的化学方程式(7)氧化铈
 ,常用作玻璃工业添加剂,在其立方晶胞中掺杂
,常用作玻璃工业添加剂,在其立方晶胞中掺杂 ,
, 占据原来
占据原来 的位置,可以得到更稳定的结构,如图所示,
的位置,可以得到更稳定的结构,如图所示, 晶胞中
晶胞中 与最近
与最近 的核间距为
的核间距为 。(已知:
。(已知: 的空缺率
的空缺率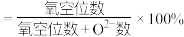 )
)
 点原子的分数坐标为
点原子的分数坐标为 ,则
,则 点原子的分数坐标为
点原子的分数坐标为②
 晶胞中与
晶胞中与 最近的
最近的 的个数为
的个数为③
 晶体的密度为
晶体的密度为④若掺杂
 后得到
后得到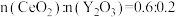 的晶体,则此晶体中
的晶体,则此晶体中 的空缺率为
的空缺率为
您最近一年使用:0次
7 . 我国提出争取在2030年前实现碳达峰、2060年前实现碳中和,这对于改善环境、实现绿色发展至关重要,其中二氧化碳转化甲醇技术是当前研究热点之一。
Ⅰ. 加氢合成
加氢合成 的反应体系中主要包含以下反应:
的反应体系中主要包含以下反应:
反应①

反应②

(1)已知:
 ,反应①的
,反应①的
___________ ,反应①在___________ (填“高温”“低温”或“任何温度”)下有利于正反应自发进行。
(2)在恒容、绝热密闭容器中只发生反应 ,下列能说明该反应已达到平衡状态的是___________(填标号)。
,下列能说明该反应已达到平衡状态的是___________(填标号)。
(3)当原料组成为 时,上述反应体系在一定条件下建立平衡后,含碳产物中
时,上述反应体系在一定条件下建立平衡后,含碳产物中 的物质的量分数(Y)及
的物质的量分数(Y)及 的转化率与反应温度的关系曲线如下图所示。
的转化率与反应温度的关系曲线如下图所示。
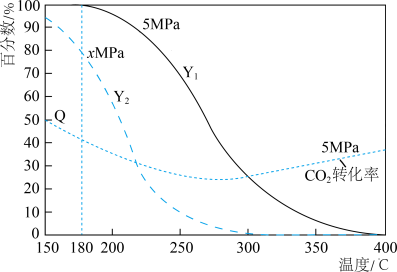
①分析压强对 加氢合成
加氢合成 的影响,可知图中x
的影响,可知图中x___________ 5(填“大于”或“小于”),理由是___________ 。
②Q点时,只发生反应①,此时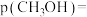
___________ MPa,反应①的平衡常数
___________  (
( 以分压表示,分压
以分压表示,分压 总压
总压 物质的量分数)。
物质的量分数)。
Ⅱ.电化学还原二氧化碳制甲醇:其中将双极膜应用于二氧化碳制备甲醇过程中的电解原理如图所示。已知:双板膜由阳高子交换膜和阴离子交换膜构成,在直流电场的作用下,双极膜间 解离成
解离成 和
和 ,并向两极迁移。
,并向两极迁移。
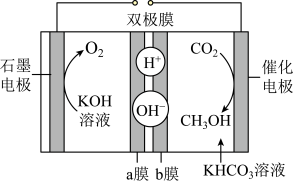
(4)催化电极上的电极反应式为___________ ,双极膜内每消耗54 g水,理论上石墨电极上产生___________  (标准状况)。
(标准状况)。
Ⅰ.
 加氢合成
加氢合成 的反应体系中主要包含以下反应:
的反应体系中主要包含以下反应:反应①


反应②


(1)已知:

 ,反应①的
,反应①的
(2)在恒容、绝热密闭容器中只发生反应
 ,下列能说明该反应已达到平衡状态的是___________(填标号)。
,下列能说明该反应已达到平衡状态的是___________(填标号)。| A.气体的平均摩尔质量不再随时间而变化 |
| B.气体的密度不再随时间而变化 |
| C.反应体系的温度保持不变 |
D.单位时间内断裂 键数目与断裂 键数目与断裂 键数目相等 键数目相等 |
 时,上述反应体系在一定条件下建立平衡后,含碳产物中
时,上述反应体系在一定条件下建立平衡后,含碳产物中 的物质的量分数(Y)及
的物质的量分数(Y)及 的转化率与反应温度的关系曲线如下图所示。
的转化率与反应温度的关系曲线如下图所示。
①分析压强对
 加氢合成
加氢合成 的影响,可知图中x
的影响,可知图中x②Q点时,只发生反应①,此时
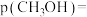

 (
( 以分压表示,分压
以分压表示,分压 总压
总压 物质的量分数)。
物质的量分数)。Ⅱ.电化学还原二氧化碳制甲醇:其中将双极膜应用于二氧化碳制备甲醇过程中的电解原理如图所示。已知:双板膜由阳高子交换膜和阴离子交换膜构成,在直流电场的作用下,双极膜间
 解离成
解离成 和
和 ,并向两极迁移。
,并向两极迁移。
(4)催化电极上的电极反应式为
 (标准状况)。
(标准状况)。
您最近一年使用:0次
8 . 柳酸甲酯( )常用于医药制剂的赋香剂,实验小组利用邻羟基苯甲酸(
)常用于医药制剂的赋香剂,实验小组利用邻羟基苯甲酸( )和甲醇在浓硫酸催化下合成少量柳酸甲酯。
)和甲醇在浓硫酸催化下合成少量柳酸甲酯。
I.实验原理:
II.相关数据如下表:
III.实验步骤:
合成:向A中加入6.9g邻羟基苯甲酸、适量固态酸性催化剂、24g甲醇,10mL甲苯(甲苯与水能形成的共沸物,沸点为85℃,易将水蒸出)加热回流1.5小时;
提纯:反应完毕,待装置冷却后,分离出固态催化剂,依次用水洗、5%的NaHCO3溶液洗、水洗,将产物移至干燥的烧杯中加入0.5g无水氯化钙,一段时间后,过滤,蒸馏有机层获得4.5g纯品。

回答下列问题:
(1)甲苯蒸气、甲醇蒸气、水蒸气冷凝为液体,然后通过分水器,甲苯、甲醇重新流回到A中,打开活塞将水从下口放出。下列有关说法中错误的是___________(填字母)。
(2)在提纯步骤中,一定没有用到下列仪器中的___________ (填仪器名称)。
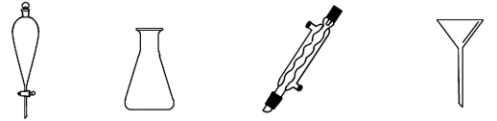
(3)提纯步骤中第二次水洗的目的是___________ ;无水氯化钙的作用是___________ 。
(4)本实验的产率为___________ %(保留三位有效数字)。
(5)实验小组为了探究影响产率的因素,采集了如下数据(邻羟基苯甲酸易溶于甲醇):
①实验IV中x=___________ ;设计实验IV是为了探究___________ 对产率的影响。
②增加甲醇的体积会提高产率,但甲醇超过一定量时,反应时间相同的情况下,产率反而下降,试从速率角度分析产率下降的主要原因:___________ 。
 )常用于医药制剂的赋香剂,实验小组利用邻羟基苯甲酸(
)常用于医药制剂的赋香剂,实验小组利用邻羟基苯甲酸( )和甲醇在浓硫酸催化下合成少量柳酸甲酯。
)和甲醇在浓硫酸催化下合成少量柳酸甲酯。I.实验原理:

II.相关数据如下表:
| 名称 | 分子量 | 颜色状态 | 相对密度 | 熔点(℃) | 沸点(℃) | 溶解性(中) |
| 柳酸甲酯 | 152 | 无色液体 | 1.18 | -8.6 | 224 | 微溶 |
| 邻羟基苯甲酸 | 138 | 白色晶体 | 1.44 | 158 | 210 | 不溶 |
| 甲醇 | 32 | 无色液体 | 0.792 | -97 | 64.7 | 互溶 |
合成:向A中加入6.9g邻羟基苯甲酸、适量固态酸性催化剂、24g甲醇,10mL甲苯(甲苯与水能形成的共沸物,沸点为85℃,易将水蒸出)加热回流1.5小时;
提纯:反应完毕,待装置冷却后,分离出固态催化剂,依次用水洗、5%的NaHCO3溶液洗、水洗,将产物移至干燥的烧杯中加入0.5g无水氯化钙,一段时间后,过滤,蒸馏有机层获得4.5g纯品。

回答下列问题:
(1)甲苯蒸气、甲醇蒸气、水蒸气冷凝为液体,然后通过分水器,甲苯、甲醇重新流回到A中,打开活塞将水从下口放出。下列有关说法中错误的是___________(填字母)。
| A.使用分水器能提高反应物的利用率 |
| B.使用分水器能够促使反应正向进行 |
| C.分水器中的水面不再变化时,反应达到最大限度 |
| D.10mL甲苯也可用四氯化碳代替 |

(3)提纯步骤中第二次水洗的目的是
(4)本实验的产率为
(5)实验小组为了探究影响产率的因素,采集了如下数据(邻羟基苯甲酸易溶于甲醇):
| 编号 | 邻羟基苯甲酸/g | 甲醇/mL | 反应时间/min | 催化剂用量/g | 产率/% |
| I | 4.8 | 4.0 | 8 | 1.4 | 61.67 |
| II | 4.8 | 4.0 | 8 | 1.0 | 55.42 |
| III | 4.8 | 5.0 | 8 | 1.4 | 65.42 |
| IV | 4.8 | x | 4 | 1.4 | — |
②增加甲醇的体积会提高产率,但甲醇超过一定量时,反应时间相同的情况下,产率反而下降,试从速率角度分析产率下降的主要原因:
您最近一年使用:0次
名校
9 . 合成氨是人类科学技术上的一项重大突破:
(1)根据下表中键能写出合成氨的热化学方程式_________ 。
(2)科研小组模拟不同条件下的合成氨反应,向容器中充入 和
和 ,不同温度下平衡混合物中氨气的体积分数与总压强(p)的关系如图:
,不同温度下平衡混合物中氨气的体积分数与总压强(p)的关系如图:

① 、
、 、
、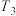 由大到小的排序为
由大到小的排序为_______ 。
②在 、60MPa条件下,A点
、60MPa条件下,A点
_____  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
③如下图表示500℃、60MPa条件下,合成氨反应原料气投料比与平衡时 体积分数的关系。根据图中a点数据计算
体积分数的关系。根据图中a点数据计算 的平衡转化率为
的平衡转化率为_____ %(结果保留一位小数)。

(3)固体燃料是目前我国合成氦生产的主要原料,随着煤气化技术的进步,多煤种均可作为合成氨的原料,以煤为原料的合成氨生产流程由三个基本部分组成:
原料气的制备→原料气的净化→气体的压缩与氨的合成
原料气的制备过程中主要发生反应:
Ⅰ.

Ⅱ.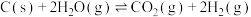

图1为碳与水蒸气反应的平衡常数与温度的关系图,图2表示了氧煤比对气化过程的影响,氧煤比的大小是影响气化炉温度、碳转化率、煤中有效气体(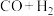 )含量高低的重要因素。
)含量高低的重要因素。

①由图1可知,高温有利于提高______ 和______ 的含量。
②试分析原料气制备过程中通入 的原因:
的原因:_______ ;合适的氧煤比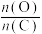 应保证在
应保证在_____ 左右。
(4)原料气的净化过程中,脱碳工序须将 去除,N-甲基二乙醇胺(简称MDEA,分子式可简写为
去除,N-甲基二乙醇胺(简称MDEA,分子式可简写为 )水溶液因其选择性高、溶剂消耗少、对设备腐蚀小、可再生等优点被广泛使用。MDEA吸收
)水溶液因其选择性高、溶剂消耗少、对设备腐蚀小、可再生等优点被广泛使用。MDEA吸收 的反应可表示为:
的反应可表示为: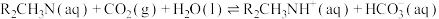 。标准平衡常数
。标准平衡常数 可以表示平衡时各物质的浓度关系:如反应
可以表示平衡时各物质的浓度关系:如反应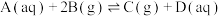 的
的 ,其中
,其中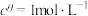 ,
, 为标准大气压,
为标准大气压, 、
、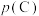 分别为气体的分压,分压=气体物质的量分数×总压。在T℃时的刚性密闭容器中,用20L2.3mol/L的MDEA溶液吸收总压为
分别为气体的分压,分压=气体物质的量分数×总压。在T℃时的刚性密闭容器中,用20L2.3mol/L的MDEA溶液吸收总压为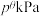 的合成氨原料气(含体积分数分别为30%的
的合成氨原料气(含体积分数分别为30%的 、55%的
、55%的 、15%的
、15%的 ),充分吸收后,MDEA浓度降低为2.0mol/L,二氧化碳的吸收率为60%,忽略反应过程中溶液的体积变化,则反应的标准平衡常数
),充分吸收后,MDEA浓度降低为2.0mol/L,二氧化碳的吸收率为60%,忽略反应过程中溶液的体积变化,则反应的标准平衡常数
______ (保留2位有效数字)。
(1)根据下表中键能写出合成氨的热化学方程式
化学键 |
|
|
|
|
E/kJ⋅mol−1 | 436 | 465 | 946 | 391 |
(2)科研小组模拟不同条件下的合成氨反应,向容器中充入
 和
和 ,不同温度下平衡混合物中氨气的体积分数与总压强(p)的关系如图:
,不同温度下平衡混合物中氨气的体积分数与总压强(p)的关系如图:
①
 、
、 、
、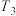 由大到小的排序为
由大到小的排序为②在
 、60MPa条件下,A点
、60MPa条件下,A点
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。③如下图表示500℃、60MPa条件下,合成氨反应原料气投料比与平衡时
 体积分数的关系。根据图中a点数据计算
体积分数的关系。根据图中a点数据计算 的平衡转化率为
的平衡转化率为
(3)固体燃料是目前我国合成氦生产的主要原料,随着煤气化技术的进步,多煤种均可作为合成氨的原料,以煤为原料的合成氨生产流程由三个基本部分组成:
原料气的制备→原料气的净化→气体的压缩与氨的合成
原料气的制备过程中主要发生反应:
Ⅰ.


Ⅱ.
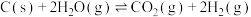

图1为碳与水蒸气反应的平衡常数与温度的关系图,图2表示了氧煤比对气化过程的影响,氧煤比的大小是影响气化炉温度、碳转化率、煤中有效气体(
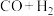 )含量高低的重要因素。
)含量高低的重要因素。
①由图1可知,高温有利于提高
②试分析原料气制备过程中通入
 的原因:
的原因: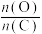 应保证在
应保证在(4)原料气的净化过程中,脱碳工序须将
 去除,N-甲基二乙醇胺(简称MDEA,分子式可简写为
去除,N-甲基二乙醇胺(简称MDEA,分子式可简写为 )水溶液因其选择性高、溶剂消耗少、对设备腐蚀小、可再生等优点被广泛使用。MDEA吸收
)水溶液因其选择性高、溶剂消耗少、对设备腐蚀小、可再生等优点被广泛使用。MDEA吸收 的反应可表示为:
的反应可表示为: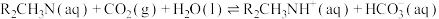 。标准平衡常数
。标准平衡常数 可以表示平衡时各物质的浓度关系:如反应
可以表示平衡时各物质的浓度关系:如反应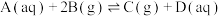 的
的 ,其中
,其中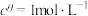 ,
, 为标准大气压,
为标准大气压, 、
、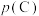 分别为气体的分压,分压=气体物质的量分数×总压。在T℃时的刚性密闭容器中,用20L2.3mol/L的MDEA溶液吸收总压为
分别为气体的分压,分压=气体物质的量分数×总压。在T℃时的刚性密闭容器中,用20L2.3mol/L的MDEA溶液吸收总压为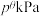 的合成氨原料气(含体积分数分别为30%的
的合成氨原料气(含体积分数分别为30%的 、55%的
、55%的 、15%的
、15%的 ),充分吸收后,MDEA浓度降低为2.0mol/L,二氧化碳的吸收率为60%,忽略反应过程中溶液的体积变化,则反应的标准平衡常数
),充分吸收后,MDEA浓度降低为2.0mol/L,二氧化碳的吸收率为60%,忽略反应过程中溶液的体积变化,则反应的标准平衡常数
您最近一年使用:0次
名校
10 . “碳中和”有利于全球气候改善,转化和吸收 的研究成为迫切的任务。
的研究成为迫切的任务。
(1)某研究所研究了 催化加
催化加 合成低碳烯烃的反应。
合成低碳烯烃的反应。
已知Ⅰ.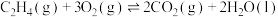
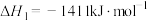
Ⅱ.

Ⅲ.
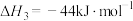
在催化剂的作用下 和
和 发生反应Ⅳ:
发生反应Ⅳ:

_______  。
。
(2)利用反应Ⅳ转化 有利于全球气候改善。一定条件下进行该反应不考虑副反应,在不同温度、压强和相同催化剂条件下,按照
有利于全球气候改善。一定条件下进行该反应不考虑副反应,在不同温度、压强和相同催化剂条件下,按照 投料只发生反应Ⅳ,测
投料只发生反应Ⅳ,测 的平衡转化率与温度、压强变化关系如图所示。
的平衡转化率与温度、压强变化关系如图所示。

 、
、 和
和 由大到小的顺序是
由大到小的顺序是________ ,其原因是___________ 。若要提高 的平衡转化率,除改变温度、压强外,还可采取的措施为
的平衡转化率,除改变温度、压强外,还可采取的措施为________ 。
(3)理论计算表明,反应Ⅳ在原料初始组成 ,体系压强为0.1MPa,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示。
,体系压强为0.1MPa,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示。
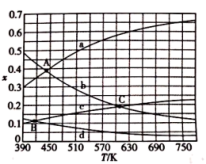
①图中,表示a曲线变化的物质是________ 。
②经反应一段时间后,图中交点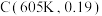 时,该反应的平衡常数
时,该反应的平衡常数
_______  (列出计算式)。
(列出计算式)。
③图中交点A、B、C对应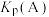 、
、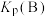 、
、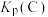 由大到小关系为
由大到小关系为_______ 。
(4)催化电解吸收 的KOH溶液可将
的KOH溶液可将 转化为有机物。在相同条件下,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率(
转化为有机物。在相同条件下,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率(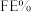 )随电解电压的变化如图所示。
)随电解电压的变化如图所示。
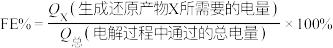
其中, ,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。
,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。
①当电解电压为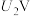 时,阴极由
时,阴极由 生成
生成 的电极反应式为
的电极反应式为________ 。
②当电解电压为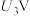 时,电解生成的
时,电解生成的 和
和 的物质的量之比为
的物质的量之比为_______ 。
 的研究成为迫切的任务。
的研究成为迫切的任务。(1)某研究所研究了
 催化加
催化加 合成低碳烯烃的反应。
合成低碳烯烃的反应。已知Ⅰ.
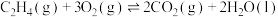
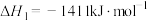
Ⅱ.


Ⅲ.

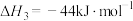
在催化剂的作用下
 和
和 发生反应Ⅳ:
发生反应Ⅳ:

 。
。(2)利用反应Ⅳ转化
 有利于全球气候改善。一定条件下进行该反应不考虑副反应,在不同温度、压强和相同催化剂条件下,按照
有利于全球气候改善。一定条件下进行该反应不考虑副反应,在不同温度、压强和相同催化剂条件下,按照 投料只发生反应Ⅳ,测
投料只发生反应Ⅳ,测 的平衡转化率与温度、压强变化关系如图所示。
的平衡转化率与温度、压强变化关系如图所示。
 、
、 和
和 由大到小的顺序是
由大到小的顺序是 的平衡转化率,除改变温度、压强外,还可采取的措施为
的平衡转化率,除改变温度、压强外,还可采取的措施为(3)理论计算表明,反应Ⅳ在原料初始组成
 ,体系压强为0.1MPa,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示。
,体系压强为0.1MPa,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示。
①图中,表示a曲线变化的物质是
②经反应一段时间后,图中交点
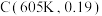 时,该反应的平衡常数
时,该反应的平衡常数
 (列出计算式)。
(列出计算式)。③图中交点A、B、C对应
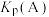 、
、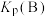 、
、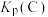 由大到小关系为
由大到小关系为(4)催化电解吸收
 的KOH溶液可将
的KOH溶液可将 转化为有机物。在相同条件下,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率(
转化为有机物。在相同条件下,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率(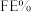 )随电解电压的变化如图所示。
)随电解电压的变化如图所示。
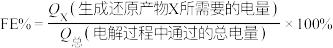
其中,
 ,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。
,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。①当电解电压为
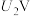 时,阴极由
时,阴极由 生成
生成 的电极反应式为
的电极反应式为②当电解电压为
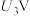 时,电解生成的
时,电解生成的 和
和 的物质的量之比为
的物质的量之比为
您最近一年使用:0次






