名校
1 . 1841年美国学者Fremy首次合成了 ,它是一种“环境友好型氧化剂”。某小组拟制备
,它是一种“环境友好型氧化剂”。某小组拟制备 ,并探究其性质。已知20℃时KCl的溶解度为37.4g,
,并探究其性质。已知20℃时KCl的溶解度为37.4g, 的溶解度为11.1g。
的溶解度为11.1g。
实验(一)制备 ,装置如图所示:
,装置如图所示:

(1)乙装置的作用是___________ 。
(2)甲装置中副产物为氯化钾,写出生成 的离子方程式:
的离子方程式:___________ 。
(3)实验完毕后,对甲装置中混合液蒸发浓缩、___________ 、过滤、洗涤、低温干燥。
实验(二)探究 性质及应用。
性质及应用。
取10g草酸溶于40mL水中,加入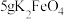 粉末,充分混合,观察到有大量气泡产生,并产生黑色固体,将所得气体通入足量澄清石灰水中,溶液变浑浊。
粉末,充分混合,观察到有大量气泡产生,并产生黑色固体,将所得气体通入足量澄清石灰水中,溶液变浑浊。
(4)根据上述实验现象,可以判断产生的气体中含有___________ ,产生该气体的原因是___________ ,经测定所得气体中还含有 。
。
(5)实验完毕后,将混合物经过滤、洗涤、干燥得到黑色固体,利用如图实验装置探究黑色固体的成分。
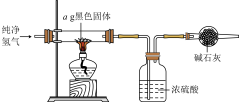
当黑色固体完全反应后,测得浓硫酸质量净增bg,当 等于
等于___________ (用分数表示)时,黑色固体为 。
。
(6)在其他条件相同时,测得一定浓度的 稳定性(用
稳定性(用 浓度表示)与pH关系如左图,其消毒效率与温度关系如右图所示:
浓度表示)与pH关系如左图,其消毒效率与温度关系如右图所示:
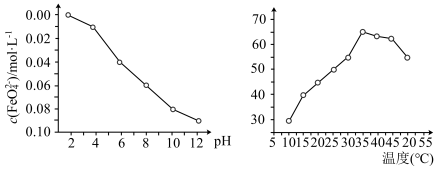
①根据左图得出结论是___________ 。
②在相同条件下, 作消毒剂最佳温度是
作消毒剂最佳温度是___________ 。
(7)查阅资料可知, 溶液呈紫红色,为探究
溶液呈紫红色,为探究 和
和 的电位相对大小,设计如下方案。(已知:电位一般指“电势”,用“
的电位相对大小,设计如下方案。(已知:电位一般指“电势”,用“ ”表示。氧化剂的电位是衡量其氧化性强度主要参数,电位越高,对应条件下氧化剂的氧化性越强。)
”表示。氧化剂的电位是衡量其氧化性强度主要参数,电位越高,对应条件下氧化剂的氧化性越强。)
方案1:在 溶液中加过量的
溶液中加过量的 粉末,溶液呈紫红色。
粉末,溶液呈紫红色。
方案2:如图所示,关闭K时,观察到电流计指针偏转,铂极产生红褐色物质,石墨极附近无色溶液变紫红色。

实验___________ (填“1”或“2”)能证明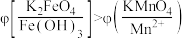 。
。
 ,它是一种“环境友好型氧化剂”。某小组拟制备
,它是一种“环境友好型氧化剂”。某小组拟制备 ,并探究其性质。已知20℃时KCl的溶解度为37.4g,
,并探究其性质。已知20℃时KCl的溶解度为37.4g, 的溶解度为11.1g。
的溶解度为11.1g。实验(一)制备
 ,装置如图所示:
,装置如图所示:
(1)乙装置的作用是
(2)甲装置中副产物为氯化钾,写出生成
 的离子方程式:
的离子方程式:(3)实验完毕后,对甲装置中混合液蒸发浓缩、
实验(二)探究
 性质及应用。
性质及应用。取10g草酸溶于40mL水中,加入
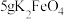 粉末,充分混合,观察到有大量气泡产生,并产生黑色固体,将所得气体通入足量澄清石灰水中,溶液变浑浊。
粉末,充分混合,观察到有大量气泡产生,并产生黑色固体,将所得气体通入足量澄清石灰水中,溶液变浑浊。(4)根据上述实验现象,可以判断产生的气体中含有
 。
。(5)实验完毕后,将混合物经过滤、洗涤、干燥得到黑色固体,利用如图实验装置探究黑色固体的成分。

当黑色固体完全反应后,测得浓硫酸质量净增bg,当
 等于
等于 。
。(6)在其他条件相同时,测得一定浓度的
 稳定性(用
稳定性(用 浓度表示)与pH关系如左图,其消毒效率与温度关系如右图所示:
浓度表示)与pH关系如左图,其消毒效率与温度关系如右图所示:
①根据左图得出结论是
②在相同条件下,
 作消毒剂最佳温度是
作消毒剂最佳温度是(7)查阅资料可知,
 溶液呈紫红色,为探究
溶液呈紫红色,为探究 和
和 的电位相对大小,设计如下方案。(已知:电位一般指“电势”,用“
的电位相对大小,设计如下方案。(已知:电位一般指“电势”,用“ ”表示。氧化剂的电位是衡量其氧化性强度主要参数,电位越高,对应条件下氧化剂的氧化性越强。)
”表示。氧化剂的电位是衡量其氧化性强度主要参数,电位越高,对应条件下氧化剂的氧化性越强。)方案1:在
 溶液中加过量的
溶液中加过量的 粉末,溶液呈紫红色。
粉末,溶液呈紫红色。方案2:如图所示,关闭K时,观察到电流计指针偏转,铂极产生红褐色物质,石墨极附近无色溶液变紫红色。

实验
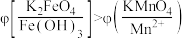 。
。
您最近一年使用:0次
名校
2 . 二氧化氯(ClO2)具有强氧化性,是优良的饮用水消毒剂。ClO2常温下为黄绿色气体,熔点-59℃,沸点11℃,极易溶于水且不与水反应,浓的ClO2受热时易爆炸。我国广泛使用的方法是用干燥的Cl2与NaClO2固体反应制取ClO2,实验室模拟制备ClO2装置如图所示:
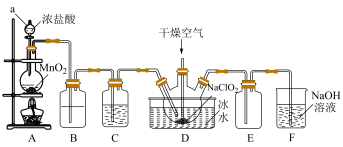
(1)仪器a的名称是:___________ ,装置A中反应的离子方程式为:___________ 。
(2)装置B中盛装的试剂是___________ ,装置C中试剂的作用是:___________ 。
(3)为防止ClO2制备装置发生爆炸,实验中采取的措施:①将装置置于冰水浴中降温,②___________ 。
(4)装置E为ClO2的收集装置,应将其置于___________ 水浴中(填“热”或“冰”)。
(5)装置F为氯气的尾气吸收装置,小组同学用胶头滴管将新制的饱和氯水慢慢滴入含有酚酞的NaOH溶液中,当滴到一定量时,红色突然褪去,小组同学对褪色原因提出假设:
假设1:___________ 。
假设2:可能是氯水中存在HClO具有强氧化性,漂白褪色。
该小组同学设计实验证明假设1是否成立。实验方案为:取少许褪色后的溶液于试管中,滴加足量的NaOH溶液,若___________ (填“实验现象”),则假设1成立。

(1)仪器a的名称是:
(2)装置B中盛装的试剂是
(3)为防止ClO2制备装置发生爆炸,实验中采取的措施:①将装置置于冰水浴中降温,②
(4)装置E为ClO2的收集装置,应将其置于
(5)装置F为氯气的尾气吸收装置,小组同学用胶头滴管将新制的饱和氯水慢慢滴入含有酚酞的NaOH溶液中,当滴到一定量时,红色突然褪去,小组同学对褪色原因提出假设:
假设1:
假设2:可能是氯水中存在HClO具有强氧化性,漂白褪色。
该小组同学设计实验证明假设1是否成立。实验方案为:取少许褪色后的溶液于试管中,滴加足量的NaOH溶液,若
您最近一年使用:0次
2023-11-06更新
|
632次组卷
|
2卷引用:江西省广信中学2023-2024学年高一上学期11月月考化学试题
名校
解题方法
3 . 碘化钠在光学器件石油探测、安检、环境监测等领域有重要应用。某研究小组开发设计的制备高纯NaI的简化流程如图:
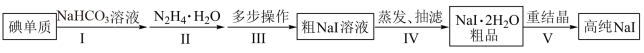
已知:
①I2(s)+I-(aq) I
I (aq)。
(aq)。
②水合肼(N2H4•H2O)具有强还原性,可分别将碘的各种酸根和I2还原为I-,本身被氧化为无毒物质。
③NaI易溶于水,也易溶于酒精,在酒精中的溶解度随温度的升高增加不大。
请回答:
(1)步骤Ⅰ,I2与NaHCO3溶液发生歧化反应,生成物中含IO-和IO 离子。
离子。
①I2与NaHCO3溶液反应适宜温度为40~70℃,则采用的加热方式为__ 。
②实验过程中,加少量NaI固体能使反应速率加快,其原因是__ 。
(2)步骤Ⅱ,水合肼与IO-反应的离子方程式为__ 。
(3)步骤Ⅲ,多步操作为:
①将步骤Ⅱ得到的pH为6.5~7的溶液调整pH值至9~10,在100℃下保温8h,得到溶液A;
②将溶液A的pH值调整至3~4,在70~80℃下保温4h,得溶液B;
③将溶液B的pH调整至6.5~7,得溶液C;
④在溶液C中加入活性炭,混合均匀后煮沸,静置10~24h后,过滤除杂得粗NaI溶液。
上述①②③操作中,调整pH值时依次加入的试剂为__ 。
A.NaOH B.HI C.NH3•H2O D.高纯水
(4)步骤Ⅳ,采用改进的方案为用“减压蒸发”代替“常压蒸发”。
①“减压蒸发”需选用的仪器除了圆底烧瓶、蒸馏头、温度计、接收管、接收瓶之外,还有__ 。
A.直形冷凝管 B.球形冷凝管 C.烧杯 D.抽气泵
②采用“减压蒸发”的优点为__ 。
(5)将制备的NaI•2H2O粗品以95%乙醇为溶剂进行重结晶。请给出合理的操作排序__ 。
加热95%乙醇→____→___→___→____→纯品(选填序号)。
①减压蒸发结晶 ②NaI•2H2O粗品溶解 ③趁热过滤 ④真空干燥
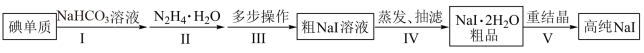
已知:
①I2(s)+I-(aq)
 I
I (aq)。
(aq)。②水合肼(N2H4•H2O)具有强还原性,可分别将碘的各种酸根和I2还原为I-,本身被氧化为无毒物质。
③NaI易溶于水,也易溶于酒精,在酒精中的溶解度随温度的升高增加不大。
请回答:
(1)步骤Ⅰ,I2与NaHCO3溶液发生歧化反应,生成物中含IO-和IO
 离子。
离子。①I2与NaHCO3溶液反应适宜温度为40~70℃,则采用的加热方式为
②实验过程中,加少量NaI固体能使反应速率加快,其原因是
(2)步骤Ⅱ,水合肼与IO-反应的离子方程式为
(3)步骤Ⅲ,多步操作为:
①将步骤Ⅱ得到的pH为6.5~7的溶液调整pH值至9~10,在100℃下保温8h,得到溶液A;
②将溶液A的pH值调整至3~4,在70~80℃下保温4h,得溶液B;
③将溶液B的pH调整至6.5~7,得溶液C;
④在溶液C中加入活性炭,混合均匀后煮沸,静置10~24h后,过滤除杂得粗NaI溶液。
上述①②③操作中,调整pH值时依次加入的试剂为
A.NaOH B.HI C.NH3•H2O D.高纯水
(4)步骤Ⅳ,采用改进的方案为用“减压蒸发”代替“常压蒸发”。
①“减压蒸发”需选用的仪器除了圆底烧瓶、蒸馏头、温度计、接收管、接收瓶之外,还有
A.直形冷凝管 B.球形冷凝管 C.烧杯 D.抽气泵
②采用“减压蒸发”的优点为
(5)将制备的NaI•2H2O粗品以95%乙醇为溶剂进行重结晶。请给出合理的操作排序
加热95%乙醇→____→___→___→____→纯品(选填序号)。
①减压蒸发结晶 ②NaI•2H2O粗品溶解 ③趁热过滤 ④真空干燥
您最近一年使用:0次
2020-07-10更新
|
308次组卷
|
4卷引用:江西省南昌市第二中学2020届高三下学期校测(一)理科综合化学试题
名校
4 . 这次中美贸易战的矛盾激化,也让我们看到了中国半导体产业存在的诸多不足,俗话说“亡羊补牢,为时未晚”,找出存在的不足,然后针对地去解决问题,才能让半导体产业链发展壮大起来。三氯化氧磷(POCl3)是一种重要的化工原料,常用作半导体掺杂剂及光导纤维原料。一研究小组在实验室模PCl3+SO2+Cl2→POCl3+SOCl2制备POCl3并测定产品含量。

资料卡片:
请回答下列问题:
(1)若选用Na2SO3固体与70%浓H2SO4制取SO2,反应的化学方程式是:______ 。
(2)溶液A为饱和食盐水,乙装置中应该盛装的试剂为______ (填“P2O5”或“碱石灰”或“浓H2SO4”或“无水硫酸铜”);反应装置图的虚框中未画出的仪器最好选择______ (填“己”或“庚”)。
(3)甲、丁装置的作用除了用于气体的净化除杂外,还有______ 。
(4)水浴加热三颈烧瓶,控制反应温度在60~65℃,其原因是______ 。
(5)通过佛尔哈德法可测定经过提纯后的产品中POCl3的含量:准确称取1.600g样品在水解瓶中摇动至完全水解,将水解液配成100mL溶液,取10.00mL于锥形瓶中,加入0.2000mol·L-1的AgNO3溶液20.00mL(Ag++C1-=AgC1↓),再加少许硝基苯,用力振荡,使沉淀被有机物覆盖。加入NH4Fe(SO4)2作指示剂,用0.1000mol·L-1KSCN标准溶液滴定过量的AgNO3至终点(Ag++SCN-=AgSCN↓),做平行实验,平均消耗KSCN标准溶液10.00mL。
①达到滴定终点的现象是______ 。
②POCl3的质量分数为______ (保留三位有效数字)。
③已知:Ksp(AgC1)=3.2×10-10mol2·L-2,Ksp(AgSCN)=2×10-12mol2·L-2,若无硝基苯覆盖沉淀表面,测定POCl3的质量分数将______ (填“偏大”、“偏小”、“无影响”)。

资料卡片:
| 物质 | 熔点/℃ | 沸点/℃ | 相对分子质量 | 其他 |
| PCl3 | -93.6 | 76.1 | 137.5 | 遇水剧烈水解,易与O2反应 |
| POCl3 | 1.25 | 105.8 | 153.5 | 遇水剧烈水解,能溶于PCl3 |
| SOCl2 | -105 | 78.8 | 119 | 遇水剧烈水解,受热易分解 |
请回答下列问题:
(1)若选用Na2SO3固体与70%浓H2SO4制取SO2,反应的化学方程式是:
(2)溶液A为饱和食盐水,乙装置中应该盛装的试剂为
(3)甲、丁装置的作用除了用于气体的净化除杂外,还有
(4)水浴加热三颈烧瓶,控制反应温度在60~65℃,其原因是
(5)通过佛尔哈德法可测定经过提纯后的产品中POCl3的含量:准确称取1.600g样品在水解瓶中摇动至完全水解,将水解液配成100mL溶液,取10.00mL于锥形瓶中,加入0.2000mol·L-1的AgNO3溶液20.00mL(Ag++C1-=AgC1↓),再加少许硝基苯,用力振荡,使沉淀被有机物覆盖。加入NH4Fe(SO4)2作指示剂,用0.1000mol·L-1KSCN标准溶液滴定过量的AgNO3至终点(Ag++SCN-=AgSCN↓),做平行实验,平均消耗KSCN标准溶液10.00mL。
①达到滴定终点的现象是
②POCl3的质量分数为
③已知:Ksp(AgC1)=3.2×10-10mol2·L-2,Ksp(AgSCN)=2×10-12mol2·L-2,若无硝基苯覆盖沉淀表面,测定POCl3的质量分数将
您最近一年使用:0次
2020-08-22更新
|
167次组卷
|
4卷引用:江西省信丰中学2021-2022学年高二下学期第一次月考(A层)化学试题
名校
解题方法
5 . 肼(N2H4)的熔点2.0℃、沸点113.5℃,极易溶于水,在碱性介质中具有还原性。在强碱性介质中,用次氯酸钠氧化尿素[CO(NH2)2]可得粗肼,再经蒸馏得到肼溶液。回答下列问题:
I.制备NaClO强碱性溶液
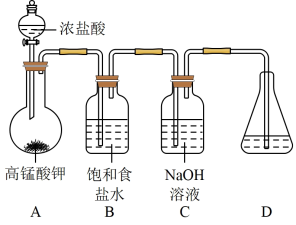
(1)在加入实验药品之前必须进行的操作是_______ 。
(2)A为氯气发生装置,A中反应的化学方程式是_______ 。
(3)次氯酸钠高于35℃容易分解。制备NaClO 强碱性溶液时需要注意的两个关键问题是_______ 。
II.制备N2H4

(4)仪器F的名称是_______ 。
(5)通入N2目的是_______ 。
(6)次氯酸钠氧化尿素的温度一般控制在105~108℃。E中制得肼的离子方程式为_______ .。
(7)向三颈烧瓶中加入NaClO强碱性溶液应当_______ . (填“一次大量”或“分批少量”)加入,充分反应后制得粗肼。蒸馏提纯时应调节控温槽的温度略高于_______ ℃,得到肼溶液。
I.制备NaClO强碱性溶液

(1)在加入实验药品之前必须进行的操作是
(2)A为氯气发生装置,A中反应的化学方程式是
(3)次氯酸钠高于35℃容易分解。制备NaClO 强碱性溶液时需要注意的两个关键问题是
II.制备N2H4

(4)仪器F的名称是
(5)通入N2目的是
(6)次氯酸钠氧化尿素的温度一般控制在105~108℃。E中制得肼的离子方程式为
(7)向三颈烧瓶中加入NaClO强碱性溶液应当
您最近一年使用:0次
2021-03-05更新
|
585次组卷
|
3卷引用:江西省南昌市八一中学2021届高三第三次模拟考试理科综合化学试题
19-20高三·江西南昌·期中
解题方法
6 . 氮的氧化物是造成大气污染的主要物质,研究氮氧化物的反应机理对于减少环境污染有重要意义。
(1)NH3催化还原NO是重要的烟气脱硝技术。一定条件下,用NH3消除NO污染,其反应原理为4NH3+6NO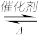 5N2+6H2O。
5N2+6H2O。
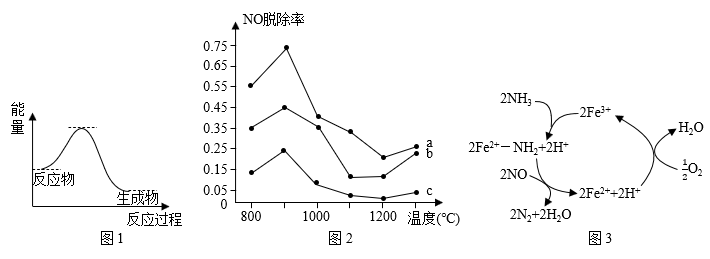
①NH3催化还原NO的反应过程与能量的关系如图1所示,该反应的逆反应为____ (填“放热反应”或“吸热反应”)。
②n(NH3):n(NO)的物质的量之比分别为4:1、3:1、1:3时,得到NO脱除率曲线如图2所示。n(NH3):n(NO)的物质的量之比为1:3时,对应的是曲线____ (填“a”“b”或“c”)。
(2)研究发现在以Fe(Ⅲ)为主催化剂时发生的反应过程如图3,总反应的化学方程式为____ 。
(3)NO的氧化反应2NO(g)+O2(g) 2NO2(g)分两步进行:Ⅰ.2NO(g)→N2O2(g);Ⅱ.N2O2(g)+O2(g)→2NO2(g)。其反应过程能量变化如图4所示。决定NO氧化反应速率的是反应
2NO2(g)分两步进行:Ⅰ.2NO(g)→N2O2(g);Ⅱ.N2O2(g)+O2(g)→2NO2(g)。其反应过程能量变化如图4所示。决定NO氧化反应速率的是反应___ (填“I”或“Ⅱ”)。
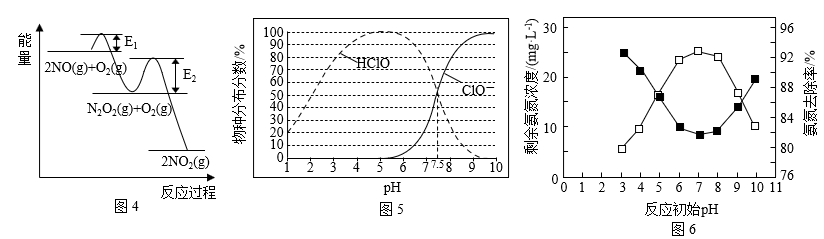
(4)NaClO溶液中ClO-与H2O反应产生氧化性更强的HClO,可将水体中氨氮氧化为N2(NH3比NH 更易被氧化)
更易被氧化)
①向NaClO溶液中通入过量CO2,发生反应的离子方程式为___ 。
②室温时,取氨氮废水200mL,在转速、NaClO投加量相同且均反应30min时,反应初始pH对剩余氨氮浓度及氨氮去除率的影响如图6所示。pH在3~7时,随着pH增大,氨氮去除率逐渐升高的原因是___ 。pH在7~9时,随着pH增大,氨氮去除率逐渐降低的原因是__ 。
(1)NH3催化还原NO是重要的烟气脱硝技术。一定条件下,用NH3消除NO污染,其反应原理为4NH3+6NO
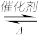 5N2+6H2O。
5N2+6H2O。
①NH3催化还原NO的反应过程与能量的关系如图1所示,该反应的逆反应为
②n(NH3):n(NO)的物质的量之比分别为4:1、3:1、1:3时,得到NO脱除率曲线如图2所示。n(NH3):n(NO)的物质的量之比为1:3时,对应的是曲线
(2)研究发现在以Fe(Ⅲ)为主催化剂时发生的反应过程如图3,总反应的化学方程式为
(3)NO的氧化反应2NO(g)+O2(g)
 2NO2(g)分两步进行:Ⅰ.2NO(g)→N2O2(g);Ⅱ.N2O2(g)+O2(g)→2NO2(g)。其反应过程能量变化如图4所示。决定NO氧化反应速率的是反应
2NO2(g)分两步进行:Ⅰ.2NO(g)→N2O2(g);Ⅱ.N2O2(g)+O2(g)→2NO2(g)。其反应过程能量变化如图4所示。决定NO氧化反应速率的是反应
(4)NaClO溶液中ClO-与H2O反应产生氧化性更强的HClO,可将水体中氨氮氧化为N2(NH3比NH
 更易被氧化)
更易被氧化)①向NaClO溶液中通入过量CO2,发生反应的离子方程式为
②室温时,取氨氮废水200mL,在转速、NaClO投加量相同且均反应30min时,反应初始pH对剩余氨氮浓度及氨氮去除率的影响如图6所示。pH在3~7时,随着pH增大,氨氮去除率逐渐升高的原因是
您最近一年使用:0次
名校
7 . 戴口罩是防控新型冠状病毒的重要手段,口罩生产的主要原料聚丙烯由丙烯聚合而来。丙烷脱氢是丙烯工业生产的重要途径。反应的热化学方程式为C3H8(g) C3H6(g)+H2(g) △H>0。回答下列问题:
C3H6(g)+H2(g) △H>0。回答下列问题:
(1)从工业生产的角度来看。制备丙烯所用的丙烷可以从下面工业气体中获得的是___ 。
A.液化石油气 B.炼铁高炉尾气 C.水煤气 D.焦炉气
(2)104Pa、105Pa时由一定量丙烷脱氢制丙烯,反应在不同温度下达到平衡,测得丙烷、丙烯的物质的量分数变化关系如图所示。

①104Pa时丙烷及丙烯的物质的量分数随温度变化关系的曲线分别是___ 、___ 。
②丙烷脱氢制丙烯反应在___ (选“高温”或“低温”)时更加容易自发进行。
③起始时充入一定量的丙烷发生反应,计算Q点对应温度下该反应的平衡常数KP=___ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)一种丙烷脱氢制丙烯工艺生产中增加了氧化脱氢部分,O2被引入到脱氢反应体系中,这样做的好处是___ 。
(4)利用CO2的弱氧化性,开发了丙烷氧化脱氢制丙烯的新工艺。其反应机理如图所示。

已知:CO和C3H4、C3H6的燃烧热△H分别为-283•0kJ•mol-1、-2217.8kJ•mol-1、-2049.0kJ•mol-1。
②298K时,该工艺总反应的热化学方程式为___ 。
②该工艺可以有效消除催化剂表面的积炭,维持催化剂活性,原因是___ 。
 C3H6(g)+H2(g) △H>0。回答下列问题:
C3H6(g)+H2(g) △H>0。回答下列问题:(1)从工业生产的角度来看。制备丙烯所用的丙烷可以从下面工业气体中获得的是
A.液化石油气 B.炼铁高炉尾气 C.水煤气 D.焦炉气
(2)104Pa、105Pa时由一定量丙烷脱氢制丙烯,反应在不同温度下达到平衡,测得丙烷、丙烯的物质的量分数变化关系如图所示。

①104Pa时丙烷及丙烯的物质的量分数随温度变化关系的曲线分别是
②丙烷脱氢制丙烯反应在
③起始时充入一定量的丙烷发生反应,计算Q点对应温度下该反应的平衡常数KP=
(3)一种丙烷脱氢制丙烯工艺生产中增加了氧化脱氢部分,O2被引入到脱氢反应体系中,这样做的好处是
(4)利用CO2的弱氧化性,开发了丙烷氧化脱氢制丙烯的新工艺。其反应机理如图所示。

已知:CO和C3H4、C3H6的燃烧热△H分别为-283•0kJ•mol-1、-2217.8kJ•mol-1、-2049.0kJ•mol-1。
②298K时,该工艺总反应的热化学方程式为
②该工艺可以有效消除催化剂表面的积炭,维持催化剂活性,原因是
您最近一年使用:0次
2020-08-28更新
|
544次组卷
|
5卷引用:江西省吉安一中2021-2022学年高二上学期第一次段考化学试题
江西省吉安一中2021-2022学年高二上学期第一次段考化学试题河南省洛阳市2020届高三第三次统一考试理综化学试题(已下线)专题14 化学反应原理综合-2020年高考真题和模拟题化学分项汇编河南省洛阳市2020届高三三模化学试卷山西省大同市第一中学2021届高三上学期期中质量检测化学试题
解题方法
8 . 大气中CO2含量的增加会加剧温室效应,为减少其排放,需将工业生产中产生的CO2分离出来进行储存和利用。
(1)CO2溶于水生成碳酸,碳酸和亚硝酸(HNO2)的电离常数如下表所示,下列事实中,能说明亚硝酸酸性比碳酸强的是(填字母代号)____________ 。
A 常温下,亚硝酸电离常数比碳酸一级电离常数大
B 亚硝酸的氧化性比碳酸的氧化性强
C 亚硝酸与碳酸钠反应生成CO2
D 相同浓度的碳酸钠溶液的pH比亚硝酸钠的大
(2).CO2与NH3反应可合成尿素[化学式为CO(NH2)2],反应2NH3(g)+CO2(g)⇌CO(NH2)2(1)+H2O(g)在合成塔中进行,图中Ⅰ,Ⅱ,Ⅲ三条曲线分别表示温度为T℃时,按不同氨碳比 和水碳比
和水碳比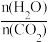 投料时,二氧化碳平衡转化率的情况。
投料时,二氧化碳平衡转化率的情况。

①曲线Ⅰ,Ⅱ,Ⅲ中水碳比的数值分别为0.6~0.7,1~1.1,1.5~1.6,则生产中应选用的水碳比数值范围是____________ 。
②推测生产中氨碳比应控制在____________ (选填“4.0”或“4.5”)左右比较适宜。
③若曲线Ⅱ中水碳比为1,初始时CO2的浓度为1mol/L,则T℃时该反应的平衡常数K=____________ (保留有数数字至小数点后两位)。
(3)以TiO2/Cu2Al2O4为催化剂,可以将CO2和CH4直接转化为乙酸,请写出该反应的化学方程式:____________ 。在不同温度下催化剂的催化效率与乙酸的生成速率的关系如图所示。在温度为____________ 时,催化剂的活性最好,效率最高。请解释图中250~400℃时乙酸生成速率变化的原因:250~300℃时____________ ;300~400℃时____________ 。

(1)CO2溶于水生成碳酸,碳酸和亚硝酸(HNO2)的电离常数如下表所示,下列事实中,能说明亚硝酸酸性比碳酸强的是(填字母代号)
| 弱酸 | HNO2 | H2CO3 |
| 电离常数 | Ka=5.1×10-4 | Ka1=4.6×10-7 |
| Ka2=5.6×10-11 |
B 亚硝酸的氧化性比碳酸的氧化性强
C 亚硝酸与碳酸钠反应生成CO2
D 相同浓度的碳酸钠溶液的pH比亚硝酸钠的大
(2).CO2与NH3反应可合成尿素[化学式为CO(NH2)2],反应2NH3(g)+CO2(g)⇌CO(NH2)2(1)+H2O(g)在合成塔中进行,图中Ⅰ,Ⅱ,Ⅲ三条曲线分别表示温度为T℃时,按不同氨碳比
 和水碳比
和水碳比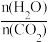 投料时,二氧化碳平衡转化率的情况。
投料时,二氧化碳平衡转化率的情况。
①曲线Ⅰ,Ⅱ,Ⅲ中水碳比的数值分别为0.6~0.7,1~1.1,1.5~1.6,则生产中应选用的水碳比数值范围是
②推测生产中氨碳比应控制在
③若曲线Ⅱ中水碳比为1,初始时CO2的浓度为1mol/L,则T℃时该反应的平衡常数K=
(3)以TiO2/Cu2Al2O4为催化剂,可以将CO2和CH4直接转化为乙酸,请写出该反应的化学方程式:

您最近一年使用:0次
名校
解题方法
9 . 金属钪可用作宇航材料、火箭和飞机的制造材料;氧化钪可提高计算机记忆元件性能。铝土矿(主要成分 )经碱初步溶解后得到的赤泥含有丰富的钪元素,另含少量CaO、
)经碱初步溶解后得到的赤泥含有丰富的钪元素,另含少量CaO、 、
、 、
、 等氧化物。一种从赤泥中提取氧化钪的工艺流程如下图所示,已知:P2O4(磷酸酯浸取剂)是一种酸性萃取剂。
等氧化物。一种从赤泥中提取氧化钪的工艺流程如下图所示,已知:P2O4(磷酸酯浸取剂)是一种酸性萃取剂。
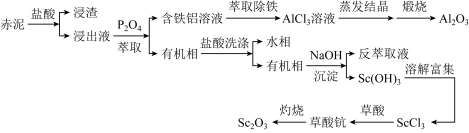
回答下列问题:
(1)写出铝土矿经碱初步溶解时所发生的主要离子方程式:_____ 。
(2)写出赤泥经盐酸处理后所得“浸渣”的一种用途:_____ 。
(3)反萃取时, 完全沉淀(浓度为
完全沉淀(浓度为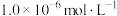 )时,反萃取液的pH为
)时,反萃取液的pH为_____ 。(已知: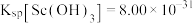 ,
, ,结果保留小数点后2位)。
,结果保留小数点后2位)。
(4)草酸钪灼烧分解在无氧环境下进行,其反应的化学方程式为_____ 。
(5)在流程中可循环使用的物质有_____ 。
 )经碱初步溶解后得到的赤泥含有丰富的钪元素,另含少量CaO、
)经碱初步溶解后得到的赤泥含有丰富的钪元素,另含少量CaO、 、
、 、
、 等氧化物。一种从赤泥中提取氧化钪的工艺流程如下图所示,已知:P2O4(磷酸酯浸取剂)是一种酸性萃取剂。
等氧化物。一种从赤泥中提取氧化钪的工艺流程如下图所示,已知:P2O4(磷酸酯浸取剂)是一种酸性萃取剂。
回答下列问题:
(1)写出铝土矿经碱初步溶解时所发生的主要离子方程式:
(2)写出赤泥经盐酸处理后所得“浸渣”的一种用途:
(3)反萃取时,
 完全沉淀(浓度为
完全沉淀(浓度为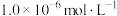 )时,反萃取液的pH为
)时,反萃取液的pH为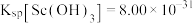 ,
, ,结果保留小数点后2位)。
,结果保留小数点后2位)。(4)草酸钪灼烧分解在无氧环境下进行,其反应的化学方程式为
(5)在流程中可循环使用的物质有
您最近一年使用:0次
10 . 雾霾严重危害人类健康和生态环境,开发稳定高效的脱硫脱硝工艺是当前国内外研究的热点。
(1)天然气中含有的微量H2S会腐蚀管道和设备,在1200℃下进行脱硫处理,H2S会被氧气氧化为SO2,并产生水蒸气。
请写出该反应的热化学方程式:__________________ 。
(2)利用 NaClO2/H2O2酸性复合吸收剂可同时有效脱硫、脱硝,将NO、SO2氧化为硝酸和硫酸而除去。在温度一定时, 、溶液pH对脱硫脱硝的影响如下图所示:
、溶液pH对脱硫脱硝的影响如下图所示:
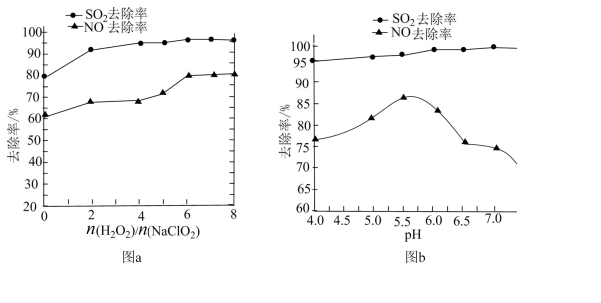
①从图a和图b中可知脱硫脱硝最佳 是
是_______ 、最佳pH是________ 。
②图b中SO2的去除率随pH的增大而增大,而NO的去除率在pH>5.5时反而减小,请解释NO去除率减小的可能原因___________________ 。
(3)臭氧也是理想的烟气脱硝剂,其脱硝的反应之一为 2NO2(g)+O3(g) N2O5(g)+O2(g),不同温度下,在体积为1 L的甲、乙两个恒容密闭容器中均充入l mol O3和2 mol NO2,相关信息如下图所示,请回答下列问题:
N2O5(g)+O2(g),不同温度下,在体积为1 L的甲、乙两个恒容密闭容器中均充入l mol O3和2 mol NO2,相关信息如下图所示,请回答下列问题:
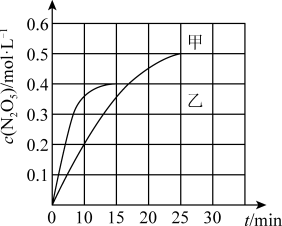
①0~15 min内乙容器中反应的平均速率:v(NO2)=__________ 。(保留2位有效数字)
②下列措施能提高容器乙中 NO2转化率的是________ (填字母标号)
A.向容器中充入氦气,增大容器的压强
B.升高容器的温度
C.向容器中再充人一定量的 NO2
D.向容器中再充入l mol O3和2 mol NO2
(1)天然气中含有的微量H2S会腐蚀管道和设备,在1200℃下进行脱硫处理,H2S会被氧气氧化为SO2,并产生水蒸气。
| 化学键 | H-S | O=O | H-O | SO2中共价键 |
| 键能/(kJ▪mol-1) | 339 | 498 | 464 | 1083 |
请写出该反应的热化学方程式:
(2)利用 NaClO2/H2O2酸性复合吸收剂可同时有效脱硫、脱硝,将NO、SO2氧化为硝酸和硫酸而除去。在温度一定时,
 、溶液pH对脱硫脱硝的影响如下图所示:
、溶液pH对脱硫脱硝的影响如下图所示:
①从图a和图b中可知脱硫脱硝最佳
 是
是②图b中SO2的去除率随pH的增大而增大,而NO的去除率在pH>5.5时反而减小,请解释NO去除率减小的可能原因
(3)臭氧也是理想的烟气脱硝剂,其脱硝的反应之一为 2NO2(g)+O3(g)
 N2O5(g)+O2(g),不同温度下,在体积为1 L的甲、乙两个恒容密闭容器中均充入l mol O3和2 mol NO2,相关信息如下图所示,请回答下列问题:
N2O5(g)+O2(g),不同温度下,在体积为1 L的甲、乙两个恒容密闭容器中均充入l mol O3和2 mol NO2,相关信息如下图所示,请回答下列问题:
①0~15 min内乙容器中反应的平均速率:v(NO2)=
②下列措施能提高容器乙中 NO2转化率的是
A.向容器中充入氦气,增大容器的压强
B.升高容器的温度
C.向容器中再充人一定量的 NO2
D.向容器中再充入l mol O3和2 mol NO2
您最近一年使用:0次
2020-10-10更新
|
397次组卷
|
4卷引用:江西省南昌市第二中学2020-2021学年高二上学期第一次月考化学试题



