解题方法
1 . 甘肃矿产资源丰富,镍、钴、铂等金属储量全国领先,有色金属冶炼在国民经济发展有着重要作用。利用紫硫镍铁矿石提取粗镍并回收铁、铜、钴等元素的工艺流程如下:
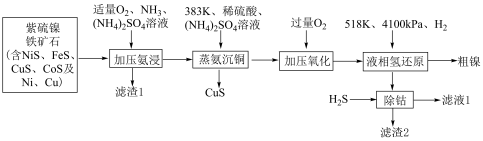
已知:①“加压氨浸”过程中镍硫化物发生反应的方程式为: ;在此过程中,钴硫化物的反应与镍硫化物相似。
;在此过程中,钴硫化物的反应与镍硫化物相似。
②以上流程中均无SO2产生。
请回答:
(1)滤渣1的主要成分为___________ 。
(2)结合下列图表选择“加压氨浸”的最佳条件___________ 。

(3)“加压氨浸”过程中“加压”的目的是___________ 、___________ ;Cu发生反应的化学方程式为___________ 。
(4)“加压氧化”的目的是氧化残留的___________ (填离子符号)。
(5)“除钴”过程中发生反应的离子方程式为___________ 。
(6)流程中可以循环利用的物质有___________ (填化学式)。

已知:①“加压氨浸”过程中镍硫化物发生反应的方程式为:
 ;在此过程中,钴硫化物的反应与镍硫化物相似。
;在此过程中,钴硫化物的反应与镍硫化物相似。②以上流程中均无SO2产生。
请回答:
(1)滤渣1的主要成分为
(2)结合下列图表选择“加压氨浸”的最佳条件

(3)“加压氨浸”过程中“加压”的目的是
(4)“加压氧化”的目的是氧化残留的
(5)“除钴”过程中发生反应的离子方程式为
(6)流程中可以循环利用的物质有
您最近一年使用:0次
23-24高三上·天津·阶段练习
名校
2 . 某温度下发生反应:3H2(g)+N2(g)⇌2NH3(g) ΔH=-92.4kJ/mol,N2的转化率(α)与体系总压强(p)的关系如图所示,下列说法中正确的是
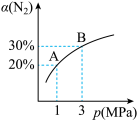

| A.将1molN2、3molH2置于1L密闭容器中发生反应,放出的热量为92.4kJ |
| B.平衡状态由A变到B时,平衡常数KA<KB |
| C.上述反应在达到平衡后,增大压强,H2的转化率增大 |
| D.合成氨工业中常采用400~500℃的高温以提高原料的转化率 |
您最近一年使用:0次
23-24高三上·贵州贵阳·阶段练习
名校
解题方法
3 . “中国芯”的发展离不开单晶硅,工业上制高纯硅,先制得粗硅,再制高纯硅。
Ⅰ.请回答:
(1)工业制粗硅反应的化学方程式为___________ 。
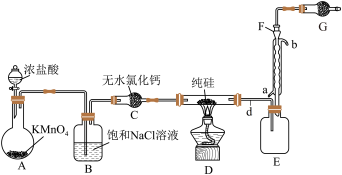
Ⅱ.某小组拟在实验室用如图所示装置模拟探究四氯化硅的制备和应用(夹持装置已省略)。
① ,
, ;
;
② 遇水剧烈水解,
遇水剧烈水解, 的熔点、沸点分别为
的熔点、沸点分别为 、
、 。
。
请回答下列问题:
(2)装无水氯化钙的仪器名称是___________ 。
(3)若拆去B装置,可能的后果是___________ (写出一个即可)。
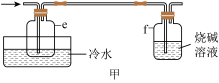
(4)有同学最初将E、F、G装置设计成图甲所示装置,图甲装置的主要缺点是___________ (写出一个即可)。 在高温条件下易分解生成
在高温条件下易分解生成 和
和 。利用
。利用 和
和 制备新型无机非金属材料(
制备新型无机非金属材料( )的装置如图乙,写出该反应的化学方程式:
)的装置如图乙,写出该反应的化学方程式:___________ 。利用尾气制备盐酸,宜选择下列装置中的___________ (填序号)。
(6) 也是制取高纯硅的重要原料,它在浓的
也是制取高纯硅的重要原料,它在浓的 溶液中的反应方程式为
溶液中的反应方程式为___________ 。
Ⅰ.请回答:
(1)工业制粗硅反应的化学方程式为
Ⅱ.某小组拟在实验室用如图所示装置模拟探究四氯化硅的制备和应用(夹持装置已省略)。
①
 ,
, ;
;②
 遇水剧烈水解,
遇水剧烈水解, 的熔点、沸点分别为
的熔点、沸点分别为 、
、 。
。请回答下列问题:
(2)装无水氯化钙的仪器名称是
(3)若拆去B装置,可能的后果是
(4)有同学最初将E、F、G装置设计成图甲所示装置,图甲装置的主要缺点是
 在高温条件下易分解生成
在高温条件下易分解生成 和
和 。利用
。利用 和
和 制备新型无机非金属材料(
制备新型无机非金属材料( )的装置如图乙,写出该反应的化学方程式:
)的装置如图乙,写出该反应的化学方程式: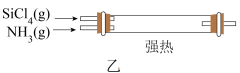

(6)
 也是制取高纯硅的重要原料,它在浓的
也是制取高纯硅的重要原料,它在浓的 溶液中的反应方程式为
溶液中的反应方程式为
您最近一年使用:0次
2024-01-06更新
|
1074次组卷
|
4卷引用:专题09 化学实验综合题-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)
(已下线)专题09 化学实验综合题-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)贵州省贵阳市第一中学2023-2024学年高三上学期11月高考适应性月考化学试卷(三)(已下线)题型17 化学实验综合-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)河北省廊坊市2023-2024学年高一下学期3月月考化学试题
4 . 氮氧化物的转化和综合利用既有利于节约资源,又有利于保护环境。
(1)SO2经过净化后与空气混合进行催化氧化可制取硫酸,其中SO2发生催化氧化的反应为: 2SO2(g)+O2(g) 2SO3(g)。若在T1℃、0.1MPa条件下,往一密闭容器通入SO2和O2[其中n(SO2)∶n(O2)=2∶1],测得容器内总压强与反应时间的关系如图所示。
2SO3(g)。若在T1℃、0.1MPa条件下,往一密闭容器通入SO2和O2[其中n(SO2)∶n(O2)=2∶1],测得容器内总压强与反应时间的关系如图所示。

①图中A点时,SO2的转化率为___________ 。
②在其他条件不变的情况下,测得T2℃时压强的变化曲线如图所示,则C点的正反应速率v(C)正与A点的逆反应速率v(A)逆的大小关系为v(C)正___________ v(A)逆(填“>”“<”或 “=”)。
③图中B点的压强平衡常数Kp=___________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(2)利用脱氮菌可净化低浓度NO废气。当废气在塔内停留时间均为90 s的情况下,测得不同条件下NO的脱氮率如图Ⅰ、Ⅱ所示。

①由图Ⅰ知,当废气中的NO含量增加时,宜选用___________ 法提高脱氮效率。
②图Ⅱ中,循环吸收液加入Fe2+、Mn2+提高了脱氮的效率,其可能原因为___________ 。
(3)研究表明:NaClO2/H2O2酸性复合吸收剂可同时有效脱硫、脱硝。图Ⅲ所示为复合吸收剂组成一定时,温度对脱硫脱硝的影响。

①写出废气中的SO2与NaClO2反应的离子方程式:___________ 。
②温度高于60 ℃后,NO去除率随温度升高而下降的原因为___________
(1)SO2经过净化后与空气混合进行催化氧化可制取硫酸,其中SO2发生催化氧化的反应为: 2SO2(g)+O2(g)
 2SO3(g)。若在T1℃、0.1MPa条件下,往一密闭容器通入SO2和O2[其中n(SO2)∶n(O2)=2∶1],测得容器内总压强与反应时间的关系如图所示。
2SO3(g)。若在T1℃、0.1MPa条件下,往一密闭容器通入SO2和O2[其中n(SO2)∶n(O2)=2∶1],测得容器内总压强与反应时间的关系如图所示。
①图中A点时,SO2的转化率为
②在其他条件不变的情况下,测得T2℃时压强的变化曲线如图所示,则C点的正反应速率v(C)正与A点的逆反应速率v(A)逆的大小关系为v(C)正
③图中B点的压强平衡常数Kp=
(2)利用脱氮菌可净化低浓度NO废气。当废气在塔内停留时间均为90 s的情况下,测得不同条件下NO的脱氮率如图Ⅰ、Ⅱ所示。

①由图Ⅰ知,当废气中的NO含量增加时,宜选用
②图Ⅱ中,循环吸收液加入Fe2+、Mn2+提高了脱氮的效率,其可能原因为
(3)研究表明:NaClO2/H2O2酸性复合吸收剂可同时有效脱硫、脱硝。图Ⅲ所示为复合吸收剂组成一定时,温度对脱硫脱硝的影响。

①写出废气中的SO2与NaClO2反应的离子方程式:
②温度高于60 ℃后,NO去除率随温度升高而下降的原因为
您最近一年使用:0次
5 . 现代工业的发展导致CO2大量排放,对环境造成的影响日益严重,通过各国科技工作者的努力,现已开发出多项将CO2回收利用的技术。某科研小组提出CO2催化加氢合成乙烯。回答下列问题:
(1)已知:H2(g)、C2H4(g)的燃烧热(∆H)分别为-285.8 kJ·mol-1、-1411 kJ·mol-1,
H2O(g)=H2O(l) ∆H=-44 kJ·mol-1。
则2CO2(g)+6H2(g) C2H4(g)+4H2O(g) ∆H=
C2H4(g)+4H2O(g) ∆H=__ kJ·mol-1。
(2)某科研小组利用含铁复合催化剂催化合成乙烯,其反应机理如图:
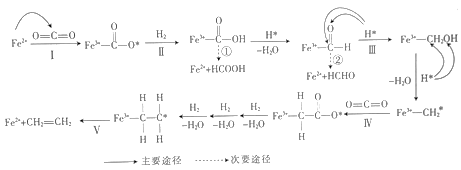
在上述反应途径中,生成的副产物主要有__ (填化学式),写出反应Ⅱ的化学方程式:__ 。
(3)在使用不同催化剂的作用下可发生CO2(g)+4H2(g) CH4(g)+2H2O(g)。我国化学工作者对该反应的催化剂及催化效率进行了深入的研究。在起始压强为2 MPa、气体流速为20 mL·min-1'时研究温度对催化剂催化性能的影响,得到CO2的转化率(%)如表:
CH4(g)+2H2O(g)。我国化学工作者对该反应的催化剂及催化效率进行了深入的研究。在起始压强为2 MPa、气体流速为20 mL·min-1'时研究温度对催化剂催化性能的影响,得到CO2的转化率(%)如表:
①分析表中数据可知:催化剂___ (填标号)的催化性能更好。
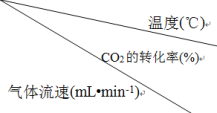
②调整气体流速,研究其对某催化剂催化效率的影响,得到CO2的转化率(%)如表:
分析表中数据可知:相同温度时,随着气体流速增大,CO2的转化率__ (填“增大”或“减小”),其可能的原因是__ 。
③在上述实验条件中,反应肯定达到化学平衡状态的温度是__ ℃。
(4)在温度为T ℃时,将2 mol CO2和6 mol H2通入压强为p的恒容密闭容器内,使用含铁复合催化剂发生反应2CO2(g)+6H2(g) C2H4(g)+4H2O(g)(副产物含量较少,可忽略)。实验测得反应达到平衡时,CO2的转化率为80%、则Kp=
C2H4(g)+4H2O(g)(副产物含量较少,可忽略)。实验测得反应达到平衡时,CO2的转化率为80%、则Kp=___ (列出计算式即可)。
(1)已知:H2(g)、C2H4(g)的燃烧热(∆H)分别为-285.8 kJ·mol-1、-1411 kJ·mol-1,
H2O(g)=H2O(l) ∆H=-44 kJ·mol-1。
则2CO2(g)+6H2(g)
 C2H4(g)+4H2O(g) ∆H=
C2H4(g)+4H2O(g) ∆H=(2)某科研小组利用含铁复合催化剂催化合成乙烯,其反应机理如图:

在上述反应途径中,生成的副产物主要有
(3)在使用不同催化剂的作用下可发生CO2(g)+4H2(g)
 CH4(g)+2H2O(g)。我国化学工作者对该反应的催化剂及催化效率进行了深入的研究。在起始压强为2 MPa、气体流速为20 mL·min-1'时研究温度对催化剂催化性能的影响,得到CO2的转化率(%)如表:
CH4(g)+2H2O(g)。我国化学工作者对该反应的催化剂及催化效率进行了深入的研究。在起始压强为2 MPa、气体流速为20 mL·min-1'时研究温度对催化剂催化性能的影响,得到CO2的转化率(%)如表: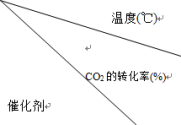 | 180 | 200 | 220 | 280 | 300 | 320 | 340 | 360 |
| a | 5.0 | 15.3 | 33.5 | 64.8 | 80.1 | 82.7 | 95.6 | 91.1 |
| b | 0.5 | 1.2 | 3.8 | 24.5 | 36.8 | 51.6 | 61.1 | 60.0 |
②调整气体流速,研究其对某催化剂催化效率的影响,得到CO2的转化率(%)如表:
 | 180 | 200 | 220 | 280 | 300 | 320 | 340 | 360 |
| 10 | 8.0 | 20.3 | 38.5 | 78.8 | 89.2 | 95.8 | 98.8 | 98.0 |
| 20 | 3.0 | 13.3 | 30.5 | 60.8 | 78.1 | 81.7 | 91.6 | 90.0 |
| 30 | 1.2 | 10.4 | 25.5 | 58.8 | 72.2 | 74.8 | 76.2 | 75.3 |
| 40 | 1.0 | 8.9 | 24.3 | 55.6 | 70.1 | 73.9 | 74.1 | 73.6 |
③在上述实验条件中,反应肯定达到化学平衡状态的温度是
(4)在温度为T ℃时,将2 mol CO2和6 mol H2通入压强为p的恒容密闭容器内,使用含铁复合催化剂发生反应2CO2(g)+6H2(g)
 C2H4(g)+4H2O(g)(副产物含量较少,可忽略)。实验测得反应达到平衡时,CO2的转化率为80%、则Kp=
C2H4(g)+4H2O(g)(副产物含量较少,可忽略)。实验测得反应达到平衡时,CO2的转化率为80%、则Kp=
您最近一年使用:0次
名校
6 . 下列说法中正确的是
A.已知 t1℃时,反应 C(g)+CO2(g)  2CO(g) ΔH >0 的速率为 υ,若升高温度,逆反应速率减小 2CO(g) ΔH >0 的速率为 υ,若升高温度,逆反应速率减小 |
B.恒压容器中发生反应 N2(g)+O2(g)  2NO(g),若在容器中充入 He,正逆反应速率均不变 2NO(g),若在容器中充入 He,正逆反应速率均不变 |
| C.当一定量的锌粉和过量的 6mol•L-1盐酸反应时,为了减慢反应速率,又不影响产生 H2的总量,可向反应器中加入少量的 CuSO4溶液 |
D.对于工业合成氨反应 N2(g)+3H2(g)  2NH3(g) ΔH﹤0,选用 450℃主要为了提高催化剂(铁触媒)的催化效率 2NH3(g) ΔH﹤0,选用 450℃主要为了提高催化剂(铁触媒)的催化效率 |
您最近一年使用:0次
7 . 氢气是一种清洁能源。在冶金、电力、材料等领域应用广泛。请回答下列问题:
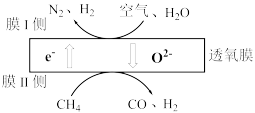
(1)某科研团队利用透氧膜获得N2、H2的工作原理如图所示(空气中N2和O2的物质的量之比为4:1)。上述过程中,膜I侧所得气体的物质的量之比为n(H2):n(N2)=3:1,则氧化作用的物质为_______________ ,膜Ⅱ侧发生的电极反应式为_________________
(2)用CO和H2合成甲醇的热化学方程式为CO(g)+2H2(g) ⇌CH3OH(g) △H1
已知CO2(g)+3H2(g) ⇌CH3OH(g)+H2O(g) △H2=-49.0kJ/mol
CO(g)+H2O(g) ⇌CO2(g)+H2(g) △H3=-41.1kJ/mol
则△H1=________________
(3)向体积可变的密闭容器中充入1molCO和2.2molH2,在恒温恒压条件下发生反应:CO(g)+2H2(g) ⇌CH3OH(g),平衡时,CO的转化率α(CO)随温度、压强的变化情况如图1所示。
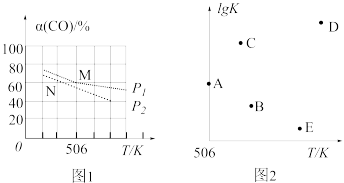
①压强p1_____ (填“>”、“<”或“=”)p2;M点时,该反应的平衡常数Kp=______ (用平衡分压表示,分压=总压×物质的量分数)
②不同温度下,该反应的平衡常数的对数值lgK如图2,其中A点为506K时平衡常数的对数值,则B、C、D、E四点中能正确表示该反应的lgK与温度(T)的关系的是_____________
(4)H2还原NO的反应为2NO(g)+2H2(g)⇌N2(g)+2H2O(l),实验测得反应速率的表达式为v=k·cm(NO)·cn(H2)(k是速率常数,只与温度有关)。
①某温度下,反应速率与反应物浓度的变化关系如下表所示。
由表中数据可知,m=_______ ,n=_______ 。
②上述反应分两步进行:ⅰ2NO(g)+2H2(g) ⇌N2(g)+H2O2(l)(慢反应)
ⅱH2O2(l)+H2(g) ⇌2H2O(l)(快反应)。下列说法正确的是_______
A. H2O2是该反应的催化剂 B. 总反应速率由反应ⅱ的速率决定
C. 反应ⅰ的活化能较高 D.反应ⅰ中NO和H2的碰撞仅部分有效
(1)某科研团队利用透氧膜获得N2、H2的工作原理如图所示(空气中N2和O2的物质的量之比为4:1)。上述过程中,膜I侧所得气体的物质的量之比为n(H2):n(N2)=3:1,则氧化作用的物质为

(2)用CO和H2合成甲醇的热化学方程式为CO(g)+2H2(g) ⇌CH3OH(g) △H1
已知CO2(g)+3H2(g) ⇌CH3OH(g)+H2O(g) △H2=-49.0kJ/mol
CO(g)+H2O(g) ⇌CO2(g)+H2(g) △H3=-41.1kJ/mol
则△H1=
(3)向体积可变的密闭容器中充入1molCO和2.2molH2,在恒温恒压条件下发生反应:CO(g)+2H2(g) ⇌CH3OH(g),平衡时,CO的转化率α(CO)随温度、压强的变化情况如图1所示。

①压强p1
②不同温度下,该反应的平衡常数的对数值lgK如图2,其中A点为506K时平衡常数的对数值,则B、C、D、E四点中能正确表示该反应的lgK与温度(T)的关系的是
(4)H2还原NO的反应为2NO(g)+2H2(g)⇌N2(g)+2H2O(l),实验测得反应速率的表达式为v=k·cm(NO)·cn(H2)(k是速率常数,只与温度有关)。
①某温度下,反应速率与反应物浓度的变化关系如下表所示。
| 编号 | c(H2)/(mol·L-1) | c(NO)/(mol·L-1) | v/(mol·L-1·min-1) |
| 1 | 0.10 | 0.10 | 0.414 |
| 2 | 0.10 | 0.20 | 1.656 |
| 3 | 0.50 | 0.10 | 2.070 |
由表中数据可知,m=
②上述反应分两步进行:ⅰ2NO(g)+2H2(g) ⇌N2(g)+H2O2(l)(慢反应)
ⅱH2O2(l)+H2(g) ⇌2H2O(l)(快反应)。下列说法正确的是
A. H2O2是该反应的催化剂 B. 总反应速率由反应ⅱ的速率决定
C. 反应ⅰ的活化能较高 D.反应ⅰ中NO和H2的碰撞仅部分有效
您最近一年使用:0次
8 . 碳酸锰是制取其他含锰化合物的原料,也可用作脱硫的催化剂等。一种焙烧氯化铵和菱锰矿粉制备高纯度碳酸锰的工艺流程如图所示
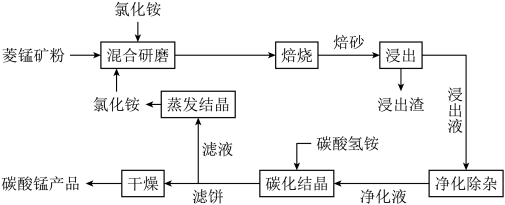
已知①菱锰矿粉的主要成分是MnCO3,还有少量的Fe、Al、Ca、Mg等元素
②常温下,相关金属离子在浓度为0.1mol/L时形成M(OH)n沉淀的pH范围如表
③常温下,Ksp(CaF2)=1.46×10−10,Ksp(MgF2)=7.42×10−11;Ka(HF)=1.00×10−4
回答下列问题:
(1)“混合研磨”的作用为_______________________
(2)“焙烧”时发生的主要反应的化学方程式为_________________________________
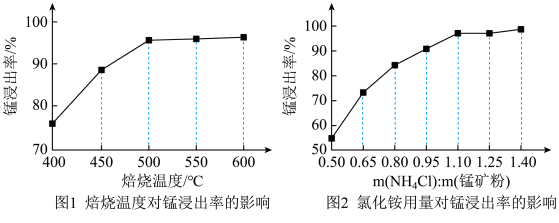
(3)分析图1、图2,焙烧氯化铵、菱锰矿粉的最佳条件是_____________________________
(4)净化除杂流程如下
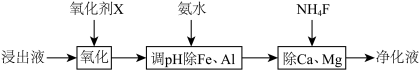
①已知几种物质氧化能力的强弱顺序为(NH4)2S2O8>KMnO4>MnO2>Fe3+,则氧化剂X宜选择__________
A. (NH4)2S2O8 B. MnO2 C. KMnO4
②调节pH时,pH可取的范围为_________________
③常温下加入NH4F将Ca2+、Mg2+沉淀除去,此时溶液中, =
=______ 若此时pH为6,c(Mg2+)= a mol/L,则c(HF)为______________ mol/L (用a表示)
(5)“碳化结晶”过程中不能用碳酸铵代替碳酸氢铵,可能的原因是__________________

已知①菱锰矿粉的主要成分是MnCO3,还有少量的Fe、Al、Ca、Mg等元素
②常温下,相关金属离子在浓度为0.1mol/L时形成M(OH)n沉淀的pH范围如表
| 金属离子 | Al3+ | Fe3+ | Fe2+ | Ca2+ | Mn2+ | Mg2+ |
| 开始沉淀的pH | 3.8 | 1.5 | 6.3 | 10.6 | 8.8 | 9.6 |
| 沉淀完全的pH | 5.2 | 2.8 | 8.3 | 12.6 | 10.8 | 11.6 |
回答下列问题:
(1)“混合研磨”的作用为
(2)“焙烧”时发生的主要反应的化学方程式为
(3)分析图1、图2,焙烧氯化铵、菱锰矿粉的最佳条件是

(4)净化除杂流程如下

①已知几种物质氧化能力的强弱顺序为(NH4)2S2O8>KMnO4>MnO2>Fe3+,则氧化剂X宜选择
A. (NH4)2S2O8 B. MnO2 C. KMnO4
②调节pH时,pH可取的范围为
③常温下加入NH4F将Ca2+、Mg2+沉淀除去,此时溶液中,
 =
=(5)“碳化结晶”过程中不能用碳酸铵代替碳酸氢铵,可能的原因是
您最近一年使用:0次
名校
解题方法
9 . 氧化铬绿(Cr2O3)的性质独特,在冶金、颜料等领域有着不可替代的地位。一种利用淀粉水热还原铬酸钠制备氧化铬绿的工艺流程如下:

已知:①向含少量Na2CO3的铬酸钠碱性溶液中通入CO2可制得不同碳化率的铬酸钠碳化母液;
②“还原”反应剧烈放热,可制得Cr(OH)3浆料。
(1)该工艺中“还原”反应最初使用的是蔗糖或甲醛,后来改用价格低廉的淀粉。请写出甲醛(HCHO)与铬酸钠(Na2CrO4)溶液反应的离子方程式_________ 。
(2)将混合均匀的料液加入反应釜,密闭搅拌,恒温发生“还原”反应,下列有关说法错误 的是_____ (填标号)。
A 该反应一定无需加热即可进行 B 必要时可使用冷却水进行温度控制
C 铬酸钠可适当过量,使淀粉充分反应 D 应建造废水回收池,回收含铬废水
(3)测得反应完成后在不同恒温温度、不同碳化率下Cr(Ⅵ)还原率如下图。实际生产过程中Cr(Ⅵ)还原率可高达99.5%以上,“还原”阶段采用的最佳反应条件为_________ 。
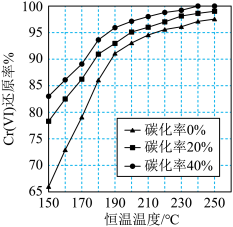
(4)滤液中所含溶质为_______ 。该水热法制备氧化铬绿工艺的优点有_________ 、________ (请写出两条)。
(5)由水热法制备的氢氧化铬为无定型氢氧化铬[Cr(OH)3·nH2O]。将洗涤并干燥后的氢氧化铬滤饼充分煅烧,质量损失与固体残留质量比为9:19,经计算得出n=_________ 。
(6)重铬酸钠(Na2Cr2O7·H2O)与硫酸铵热分解法也是一种生产氧化铬绿的方法,生产过程中产生的气体对环境无害,其化学反应方程式为_________ 。

已知:①向含少量Na2CO3的铬酸钠碱性溶液中通入CO2可制得不同碳化率的铬酸钠碳化母液;
②“还原”反应剧烈放热,可制得Cr(OH)3浆料。
(1)该工艺中“还原”反应最初使用的是蔗糖或甲醛,后来改用价格低廉的淀粉。请写出甲醛(HCHO)与铬酸钠(Na2CrO4)溶液反应的离子方程式
(2)将混合均匀的料液加入反应釜,密闭搅拌,恒温发生“还原”反应,下列有关说法
A 该反应一定无需加热即可进行 B 必要时可使用冷却水进行温度控制
C 铬酸钠可适当过量,使淀粉充分反应 D 应建造废水回收池,回收含铬废水
(3)测得反应完成后在不同恒温温度、不同碳化率下Cr(Ⅵ)还原率如下图。实际生产过程中Cr(Ⅵ)还原率可高达99.5%以上,“还原”阶段采用的最佳反应条件为

(4)滤液中所含溶质为
(5)由水热法制备的氢氧化铬为无定型氢氧化铬[Cr(OH)3·nH2O]。将洗涤并干燥后的氢氧化铬滤饼充分煅烧,质量损失与固体残留质量比为9:19,经计算得出n=
(6)重铬酸钠(Na2Cr2O7·H2O)与硫酸铵热分解法也是一种生产氧化铬绿的方法,生产过程中产生的气体对环境无害,其化学反应方程式为
您最近一年使用:0次
2020-03-13更新
|
697次组卷
|
4卷引用:甘肃省兰州市第一中学2020届高三冲刺模拟考试(三)理科综合化学试题
甘肃省兰州市第一中学2020届高三冲刺模拟考试(三)理科综合化学试题广东省深圳市2020年普通高中高三年级线上统一测试(全国I卷)理综化学试题湖北省黄冈中学2020届高三化学测试(已下线)学科网2020年5月高三大联考考后强化卷(新课标Ⅰ卷)化学试题
名校
10 . 锰是重要的合金材料和催化剂,在工农业生产和科技领域有广泛的用途。请回答下列问题:
(1)溶液中的Mn2+可被酸性 溶液氧化为MnO4-,该方法可用于检验Mn2+。
溶液氧化为MnO4-,该方法可用于检验Mn2+。
①检验时的实验现象为_________ 。
②该反应的离子方程式为___________ 。
③ 可看成两分子硫酸偶合所得,若硫酸的结构式为
可看成两分子硫酸偶合所得,若硫酸的结构式为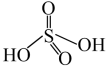 ,则
,则 的结构式为
的结构式为_________ 。
(2)实验室用含锰废料(主要成分 ,含有少量
,含有少量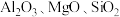 )制备Mn的流程如下:
)制备Mn的流程如下:
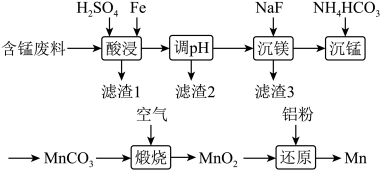
已知:Ⅰ.难溶物的溶度积常数如下表所示:
Ⅱ.溶液中离子浓度≤10-5 mol·L-1时,认为该离子沉淀完全。
①“酸浸”时, 将Fe氧化为Fe3+。该反应的离子方程式为
将Fe氧化为Fe3+。该反应的离子方程式为________ ;该过程中时间和液固比对锰浸出率的影响分别如图1、图2所示:
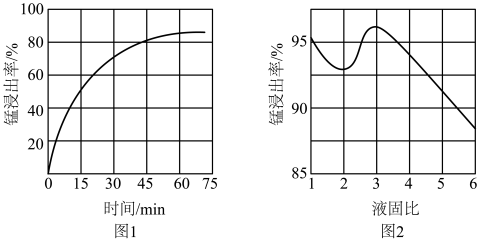
则适宜的浸出时间和液固比分别为___________ 、___________ 。
②若“酸浸”后所得滤液中c(Mn2+)=0.18 mol·L-1,则“调pH”的范围为___________ 。
③“煅烧”反应中氧化剂和还原剂的物质的量之比为_______ 。“还原”时所发生的反应在化学上又叫做_________ 。
(1)溶液中的Mn2+可被酸性
 溶液氧化为MnO4-,该方法可用于检验Mn2+。
溶液氧化为MnO4-,该方法可用于检验Mn2+。①检验时的实验现象为
②该反应的离子方程式为
③
 可看成两分子硫酸偶合所得,若硫酸的结构式为
可看成两分子硫酸偶合所得,若硫酸的结构式为 ,则
,则 的结构式为
的结构式为(2)实验室用含锰废料(主要成分
 ,含有少量
,含有少量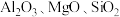 )制备Mn的流程如下:
)制备Mn的流程如下:
已知:Ⅰ.难溶物的溶度积常数如下表所示:
| 难溶物 |  |  |  |  |
溶度积常数( ) ) | 4.0×10-38 | 1.0×10-33 | 1.8×10-11 | 1.8×10-13 |
①“酸浸”时,
 将Fe氧化为Fe3+。该反应的离子方程式为
将Fe氧化为Fe3+。该反应的离子方程式为
则适宜的浸出时间和液固比分别为
②若“酸浸”后所得滤液中c(Mn2+)=0.18 mol·L-1,则“调pH”的范围为
③“煅烧”反应中氧化剂和还原剂的物质的量之比为
您最近一年使用:0次



