名校
解题方法
1 . 氟铈矿(含CeFCO3、BaO、SiO2等)是稀土元素最主要的来源,其中不仅含有丰富的稀土元素Ce(31.51%,以CeO2计),还含有大量的F资源(8.92%)和其他稀土资源(30.71%,用RE表示),其分离工艺流程如下:

已知:①氧化焙烧时,Ce元素转化成CeO2;
②酸浸后,Ce元素主要以Ce4+形式存在,其他稀土RE主要以RE3+形式存在;
③Ce4+能与F-结合成[CeF2]2+,Al3+能与F-结合成[AlFx]3-x,均易溶于水,难溶于有机溶剂,不能被P204萃取剂萃取。
回答下列问题:
(1)为了提高生产效率,焙烧时可以采取的操作___________ 。
(2)废渣的主要成分是___________ 。
(3)氧化焙烧时及萃取之前,均加入铝盐,其目的是___________ 。
(4)萃取Ce4+时,选用经典的酸性有机萃取剂P204(可用HA表示),萃取的过程可以表示成 ,通过将萃取后的有机相pH值调
,通过将萃取后的有机相pH值调___________ (填“高”或“低”)来将Ce4+从萃取剂中分离出来。
(5)将上述过程中获得Ce4+还原成Ce3+,再加入NH4HCO3溶液,即可获得稀土发光材料Ce2(CO3)3,但实际操作中,通常固体产品中含有少量Ce(OH)3,则当溶液Ce3+恰好完全沉淀时,即 ,
,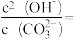
___________ ,为了使该条件下获得的固体产品中不含Ce(OH)3,应控制pH不超过___________ 。(已知常温下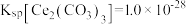 ,
,
(6)水相2中,n(Al):n(F)=1:4,请写出生成Na3AlF6沉淀的离子方程式___________ 。

已知:①氧化焙烧时,Ce元素转化成CeO2;
②酸浸后,Ce元素主要以Ce4+形式存在,其他稀土RE主要以RE3+形式存在;
③Ce4+能与F-结合成[CeF2]2+,Al3+能与F-结合成[AlFx]3-x,均易溶于水,难溶于有机溶剂,不能被P204萃取剂萃取。
回答下列问题:
(1)为了提高生产效率,焙烧时可以采取的操作
(2)废渣的主要成分是
(3)氧化焙烧时及萃取之前,均加入铝盐,其目的是
(4)萃取Ce4+时,选用经典的酸性有机萃取剂P204(可用HA表示),萃取的过程可以表示成
 ,通过将萃取后的有机相pH值调
,通过将萃取后的有机相pH值调(5)将上述过程中获得Ce4+还原成Ce3+,再加入NH4HCO3溶液,即可获得稀土发光材料Ce2(CO3)3,但实际操作中,通常固体产品中含有少量Ce(OH)3,则当溶液Ce3+恰好完全沉淀时,即
 ,
,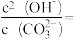
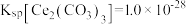 ,
,
(6)水相2中,n(Al):n(F)=1:4,请写出生成Na3AlF6沉淀的离子方程式
您最近一年使用:0次
名校
解题方法
2 . 回答下列问题:
(1)在一定温度下,有a.盐酸;b.硫酸;c.醋酸三种酸:
a.若三者 相同时,物质的量浓度由大到小的顺序是
相同时,物质的量浓度由大到小的顺序是_______ 。
b.将 相同且体积也相同的三种酸,分别与等浓度的NaOH稀溶液反应至pH=7,则消耗NaOH溶液液的体积大小关系为
相同且体积也相同的三种酸,分别与等浓度的NaOH稀溶液反应至pH=7,则消耗NaOH溶液液的体积大小关系为_______ 。
c.将体积均为10毫升pH均为3的a和c溶液加入水稀释至pH均为6,则加入水的体积a_______ c(填“>”“<”或“=”)。
d.将浓度均为0.1mol/L a和c溶液加入水稀释至相同pH则加入水的体积a_______ c(填“>”“<”或“=”)。
(2)当 浓度较低时常用纯碱溶液进行吸收。表为
浓度较低时常用纯碱溶液进行吸收。表为 、
、 的电离平衡常数。
的电离平衡常数。
纯碱溶液吸收少量 的离子方程式为
的离子方程式为_______ 。
(3)磷酸是三元弱酸,常温下三级电离常数分别是 ,
,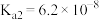 ,
, ,解答下列问题:
,解答下列问题:
a.常温下将相同物质的量浓度的氢氧化钠溶液与磷酸溶液按1:1的体积比混合,所得的溶液中 、
、 、
、 的浓度从大到小的顺序为
的浓度从大到小的顺序为_______ ;
b.常温下,将相同物质的量浓度的磷酸二氢钠溶液与磷酸钠溶液按1:1的体积比混合,所得的溶液中离子浓度位于前三位的依次是_______ (填微粒符号)。
(4)在新制氯水中加入少量的NaCl固体,水的电离平衡_______ 移动(填“向右”、“向左”、或“不”)。
(5)某温度下,纯水中的 。若温度不变,滴入稀硫酸使
。若温度不变,滴入稀硫酸使 ,则由水电离出的
,则由水电离出的 为
为_______ mol/L。
(1)在一定温度下,有a.盐酸;b.硫酸;c.醋酸三种酸:
a.若三者
 相同时,物质的量浓度由大到小的顺序是
相同时,物质的量浓度由大到小的顺序是b.将
 相同且体积也相同的三种酸,分别与等浓度的NaOH稀溶液反应至pH=7,则消耗NaOH溶液液的体积大小关系为
相同且体积也相同的三种酸,分别与等浓度的NaOH稀溶液反应至pH=7,则消耗NaOH溶液液的体积大小关系为c.将体积均为10毫升pH均为3的a和c溶液加入水稀释至pH均为6,则加入水的体积a
d.将浓度均为0.1mol/L a和c溶液加入水稀释至相同pH则加入水的体积a
(2)当
 浓度较低时常用纯碱溶液进行吸收。表为
浓度较低时常用纯碱溶液进行吸收。表为 、
、 的电离平衡常数。
的电离平衡常数。| 电离平衡常数 | 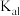 | 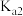 |
 |  | 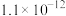 |
 | 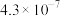 | 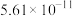 |
纯碱溶液吸收少量
 的离子方程式为
的离子方程式为(3)磷酸是三元弱酸,常温下三级电离常数分别是
 ,
,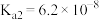 ,
, ,解答下列问题:
,解答下列问题:a.常温下将相同物质的量浓度的氢氧化钠溶液与磷酸溶液按1:1的体积比混合,所得的溶液中
 、
、 、
、 的浓度从大到小的顺序为
的浓度从大到小的顺序为b.常温下,将相同物质的量浓度的磷酸二氢钠溶液与磷酸钠溶液按1:1的体积比混合,所得的溶液中离子浓度位于前三位的依次是
(4)在新制氯水中加入少量的NaCl固体,水的电离平衡
(5)某温度下,纯水中的
 。若温度不变,滴入稀硫酸使
。若温度不变,滴入稀硫酸使 ,则由水电离出的
,则由水电离出的 为
为
您最近一年使用:0次
解题方法
3 . 黑色金属材料是工业上对铁、铬、锰的统称, 、
、 、
、 及其化合物在日常生活生产中的用途相当广泛。
及其化合物在日常生活生产中的用途相当广泛。
Ⅰ. 根据所学知识,回答下列问题:
(1) 具有净水作用,
具有净水作用, 净水的原理是
净水的原理是_______ 。
(2)向 溶液中加入
溶液中加入 溶液至过量,微热。再通入
溶液至过量,微热。再通入 ,可观察到溶液呈紫色(高铁酸钾:
,可观察到溶液呈紫色(高铁酸钾: )。写出此过程发生反应的离子方程式:
)。写出此过程发生反应的离子方程式:_______ 。
(3) 可用于治疗缺铁性贫血症,为验证药品的还原性,某实验小组取少量药用
可用于治疗缺铁性贫血症,为验证药品的还原性,某实验小组取少量药用 配制成溶液,并取
配制成溶液,并取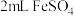 溶液于试管中,滴入几滴浓硝酸,振荡,试管中产生红棕色气体,溶液变为深棕色。为探究溶液没有变为黄色的原因补充了如下实验:向
溶液于试管中,滴入几滴浓硝酸,振荡,试管中产生红棕色气体,溶液变为深棕色。为探究溶液没有变为黄色的原因补充了如下实验:向 溶液和
溶液和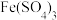 溶液中分别通入
溶液中分别通入 ,观察到
,观察到 溶液变为深棕色,
溶液变为深棕色,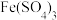 溶液无明显变化。
溶液无明显变化。
①“试管中产生红棕色气体,溶液变为深棕色”的原因是_______ 。
②实验小组改进实验,观察到溶液变为黄色的实验操作是_______ 。
Ⅱ.在 溶液中存在下列平衡:
溶液中存在下列平衡: 。
。
(4)下列有关 溶液的说法正确的是_______(填标号)。
溶液的说法正确的是_______(填标号)。
Ⅲ. 可用作电讯器材元件材料。还可用作瓷釉、颜料及制造锰盐的原料。它在空气中加热易转化为不同价态锰的氧化物,其固体残留率(
可用作电讯器材元件材料。还可用作瓷釉、颜料及制造锰盐的原料。它在空气中加热易转化为不同价态锰的氧化物,其固体残留率( )随温度的变化如图所示。
)随温度的变化如图所示。

(5) 时,剩余固体中
时,剩余固体中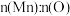 为
为_______ 。
(6)图中C点对应固体的成分为_______ (填化学式)。
 、
、 、
、 及其化合物在日常生活生产中的用途相当广泛。
及其化合物在日常生活生产中的用途相当广泛。Ⅰ. 根据所学知识,回答下列问题:
(1)
 具有净水作用,
具有净水作用, 净水的原理是
净水的原理是(2)向
 溶液中加入
溶液中加入 溶液至过量,微热。再通入
溶液至过量,微热。再通入 ,可观察到溶液呈紫色(高铁酸钾:
,可观察到溶液呈紫色(高铁酸钾: )。写出此过程发生反应的离子方程式:
)。写出此过程发生反应的离子方程式:(3)
 可用于治疗缺铁性贫血症,为验证药品的还原性,某实验小组取少量药用
可用于治疗缺铁性贫血症,为验证药品的还原性,某实验小组取少量药用 配制成溶液,并取
配制成溶液,并取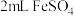 溶液于试管中,滴入几滴浓硝酸,振荡,试管中产生红棕色气体,溶液变为深棕色。为探究溶液没有变为黄色的原因补充了如下实验:向
溶液于试管中,滴入几滴浓硝酸,振荡,试管中产生红棕色气体,溶液变为深棕色。为探究溶液没有变为黄色的原因补充了如下实验:向 溶液和
溶液和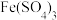 溶液中分别通入
溶液中分别通入 ,观察到
,观察到 溶液变为深棕色,
溶液变为深棕色,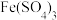 溶液无明显变化。
溶液无明显变化。①“试管中产生红棕色气体,溶液变为深棕色”的原因是
②实验小组改进实验,观察到溶液变为黄色的实验操作是
Ⅱ.在
 溶液中存在下列平衡:
溶液中存在下列平衡: 。
。(4)下列有关
 溶液的说法正确的是_______(填标号)。
溶液的说法正确的是_______(填标号)。| A.加入少量硫酸,溶液的橙色加深 |
| B.加入少量水稀释,溶液中离子总数增加 |
C.入少量 溶液,平衡逆向移动 溶液,平衡逆向移动 |
D.加入少量 固体,平衡正向移动, 固体,平衡正向移动, 转化率变大 转化率变大 |
Ⅲ.
 可用作电讯器材元件材料。还可用作瓷釉、颜料及制造锰盐的原料。它在空气中加热易转化为不同价态锰的氧化物,其固体残留率(
可用作电讯器材元件材料。还可用作瓷釉、颜料及制造锰盐的原料。它在空气中加热易转化为不同价态锰的氧化物,其固体残留率( )随温度的变化如图所示。
)随温度的变化如图所示。
(5)
 时,剩余固体中
时,剩余固体中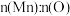 为
为(6)图中C点对应固体的成分为
您最近一年使用:0次
4 . 下列关于“化学反应速率和化学平衡”的说法正确的是
A. 恒压下充入 恒压下充入 ,化学反应速率不变 ,化学反应速率不变 |
B.已知 ,则该反应能在高温下自发进行 ,则该反应能在高温下自发进行 |
C.某温度下,在恒容密闭容器中加入一定量 ,发生反应 ,发生反应 ,一段时间后达到平衡,再加入一定量 ,一段时间后达到平衡,再加入一定量 ,达新平衡后 ,达新平衡后 的物质的量分数增大 的物质的量分数增大 |
D.对于反应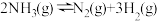 达平衡后,缩小容器体积, 达平衡后,缩小容器体积, 的浓度增大 的浓度增大 |
您最近一年使用:0次
5 . 已知: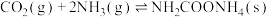
 。下列说法正确的是
。下列说法正确的是
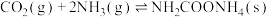
 。下列说法正确的是
。下列说法正确的是A.相同条件下,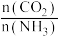 增大, 增大, 转化率增大 转化率增大 |
B.当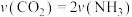 时,反应达到平衡状态 时,反应达到平衡状态 |
| C.该反应是放热反应,因此一定能自发进行 |
D.该反应的 |
您最近一年使用:0次
6 . 在一定温度下的密闭容器中发生反应:mA(g)+nB(g)⇌pC(g)+qD(s),平衡时测得C的浓度为 。保持温度不变,将容器的容积扩大到原来的二倍,再达平衡时,测得C的浓度为
。保持温度不变,将容器的容积扩大到原来的二倍,再达平衡时,测得C的浓度为 。下列有关判断正确的是
。下列有关判断正确的是
 。保持温度不变,将容器的容积扩大到原来的二倍,再达平衡时,测得C的浓度为
。保持温度不变,将容器的容积扩大到原来的二倍,再达平衡时,测得C的浓度为 。下列有关判断正确的是
。下列有关判断正确的是| A.B的转化率增大 | B.平衡向逆反应方向移动 |
| C.m+n>p+q | D.C的体积分数减小 |
您最近一年使用:0次
7 .  可用作有机合成的氯化剂。在体积为
可用作有机合成的氯化剂。在体积为 的密闭容器中充入
的密闭容器中充入 ,发生反应:
,发生反应: ,图中所示曲线分别表示反应在
,图中所示曲线分别表示反应在 时和平衡时
时和平衡时 的转化率
的转化率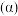 与温度
与温度 的关系。下列说法正确的是
的关系。下列说法正确的是

 可用作有机合成的氯化剂。在体积为
可用作有机合成的氯化剂。在体积为 的密闭容器中充入
的密闭容器中充入 ,发生反应:
,发生反应: ,图中所示曲线分别表示反应在
,图中所示曲线分别表示反应在 时和平衡时
时和平衡时 的转化率
的转化率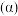 与温度
与温度 的关系。下列说法正确的是
的关系。下列说法正确的是 
A. 的 的 |
B. ,从 ,从 ,以 ,以 表示反应的平均速率为 表示反应的平均速率为 |
| C.当容器中混合气体的平均相对分子质量恒定不变时,反应达到平衡状态 |
D.82℃,若起始时在该密闭容器中充入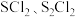 和 和 各 各 ,则此时v(逆)>v(正) ,则此时v(逆)>v(正) |
您最近一年使用:0次
2022-04-22更新
|
1229次组卷
|
11卷引用:辽宁省锦州市2022届高三第一次质量检测化学试题
辽宁省锦州市2022届高三第一次质量检测化学试题辽宁省锦州市2022届高三下学期质量检测化学试题湖南省隆回县第一中学2022届高三下学期第二次模拟考试化学试题(已下线)化学-2022年高考考前押题密卷(北京卷)(已下线)考点25 化学反应速率与平衡图象-备战2023年高考化学一轮复习考点帮(全国通用)重庆市西南大学附属中学校2022-2023学年高三上学期开学定时训练化学试题浙江省“山水联盟”2021届高三4月联考化学试题(已下线)押山东卷第14题 化学反应速率和平衡-备战2021年高考化学临考题号押题(山东卷)(已下线)考点19 化学平衡常数 化学反应进行的方向-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)题型23 平衡常数、平衡转化率图象(已下线)题型04 化学反应速率与平衡图像分析-2024年高考化学答题技巧与模板构建
8 . 在体积为2L的恒容绝热密闭容器中投入1molA和1molB,发生反应
 ,2min后达到平衡,此时容器内有0.3molC。下列说法
,2min后达到平衡,此时容器内有0.3molC。下列说法不正确 的是

 ,2min后达到平衡,此时容器内有0.3molC。下列说法
,2min后达到平衡,此时容器内有0.3molC。下列说法| A.若容器内混合气体压强不变,则反应达到平衡状态 |
B.单位时间内 生成时,则反应达到平衡状态 生成时,则反应达到平衡状态 |
| C.若开始时在该容器中投入1molA和2molB,则平衡时B的转化率小于30% |
| D.若将容器的体积压缩到原来的一半,正逆反应速率都增大 |
您最近一年使用:0次
2021-12-07更新
|
495次组卷
|
5卷引用:一轮巩固卷4-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(辽宁专用)
(已下线)一轮巩固卷4-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(辽宁专用)(已下线)解密09 化学反应速率与化学平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密09 化学反应速率与化学平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)解密09 化学反应速率与化学平衡(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)浙江省丽水市缙云中学等三校2021-2022学年高三12月份联考化学试题
名校
9 . 恒温条件下,某体积可变的密闭容器中发生反应:2A(g) B(?)+2C(g),且达到平衡。当压缩体积时,气体的平均分子质量增大,则下列叙述中正确的是
B(?)+2C(g),且达到平衡。当压缩体积时,气体的平均分子质量增大,则下列叙述中正确的是
 B(?)+2C(g),且达到平衡。当压缩体积时,气体的平均分子质量增大,则下列叙述中正确的是
B(?)+2C(g),且达到平衡。当压缩体积时,气体的平均分子质量增大,则下列叙述中正确的是| A.压缩体积,平衡逆向移动 |
| B.物质B为非气态 |
| C.若充入惰性气体,正、逆反应速率都会增大 |
| D.若往容器中加入更多的C物质,化学平衡常数会变大 |
您最近一年使用:0次
2020-12-19更新
|
241次组卷
|
5卷引用:辽宁省铁岭市六校协作体2021-2022学年高一下学期期末联考化学试题
名校
解题方法
10 . 下列事实不能用勒夏特列原理解释的是( )
| A.盛有2mL5%H2O2溶液的试管中加入MnO2作催化剂,试管中迅速产生大量气泡 |
| B.工业合成氨中,将氨气液化分离以提高氨气产率 |
| C.SO2氧化为SO3,使用过量的空气以提高SO2的利用率 |
| D.夏天,打开啤酒瓶时会从瓶口逸出泡沫 |
您最近一年使用:0次
2020-11-23更新
|
596次组卷
|
7卷引用:辽宁省协作校2022-2023学年高二上学期期中考试化学试题



