名校
解题方法
1 . 我国提出2060年达“碳中和”目标,通过反应CO2+H2 HCOOH将CO2转化为高附加值产品HCOOH是实现该目标的一种方式。回答下列问题:
HCOOH将CO2转化为高附加值产品HCOOH是实现该目标的一种方式。回答下列问题:
(1)向恒容密闭容器中充入1molCO2和lmolH2,发生反应:CO2(g)+H2(g) HCOOH(g) △H。测定不同温度下CO2的平衡转化率数据如表所示:
HCOOH(g) △H。测定不同温度下CO2的平衡转化率数据如表所示:
①该反应的△H_______ 0(填“>”或“<”)。已知:2H2(g)+O2(g)=2H2O(g)△H1,则反应2CO2(g)+2H2O(g)  2HCOOH(g)+O2(g)的△H2
2HCOOH(g)+O2(g)的△H2_______ (用△H和△H1表示)。
②下列有利于提高CO2的平衡转化率的措施有_______ (填标号)。
A.增大反应体系的压强 B.增大 C.降低反应温度 D.移出HCOOH
C.降低反应温度 D.移出HCOOH
③373K下,平衡时压强为P,用各物质的平衡分压(分压=总压×物质的量分数)表示该反应的平衡常数Kp=_________ (用含α和P的代数式表示)。
(2)浙江大学某国家实验室用水热法还原CO2转化为HCOOH,探究了不同条件下CO2的转化率,数据如图所示:
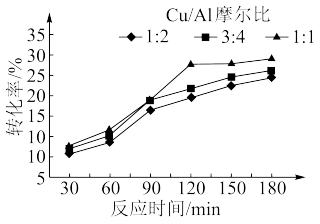
依据以上数据,最佳的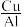 摩尔比和反应时间是
摩尔比和反应时间是______ 。
(3)中国科学院大学以Bi为电极材料,利用电化学催化还原法制备HCOOH。用计算机模拟CO2在电极材料表面发生还原反应的历程如图(*表示微粒与Bi的接触位点):
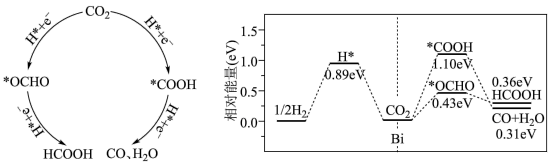
①HCOOH是________ (填“阴极”或“阳极”)产物,若在该电极消耗22gCO2,则转移电子数目为________ 。
②依据反应历程图中数据,你认为电催化还原CO2生成HCOOH的选择性______ (填“高于”或“低于”)生成CO的选择性,原因是________ 。
 HCOOH将CO2转化为高附加值产品HCOOH是实现该目标的一种方式。回答下列问题:
HCOOH将CO2转化为高附加值产品HCOOH是实现该目标的一种方式。回答下列问题:(1)向恒容密闭容器中充入1molCO2和lmolH2,发生反应:CO2(g)+H2(g)
 HCOOH(g) △H。测定不同温度下CO2的平衡转化率数据如表所示:
HCOOH(g) △H。测定不同温度下CO2的平衡转化率数据如表所示:| T/K | 373 | 473 | 573 | 673 |
| 平衡转化率 | α | 8.4α | 24.3α | 37.5α |
 2HCOOH(g)+O2(g)的△H2
2HCOOH(g)+O2(g)的△H2②下列有利于提高CO2的平衡转化率的措施有
A.增大反应体系的压强 B.增大
 C.降低反应温度 D.移出HCOOH
C.降低反应温度 D.移出HCOOH③373K下,平衡时压强为P,用各物质的平衡分压(分压=总压×物质的量分数)表示该反应的平衡常数Kp=
(2)浙江大学某国家实验室用水热法还原CO2转化为HCOOH,探究了不同条件下CO2的转化率,数据如图所示:

依据以上数据,最佳的
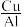 摩尔比和反应时间是
摩尔比和反应时间是(3)中国科学院大学以Bi为电极材料,利用电化学催化还原法制备HCOOH。用计算机模拟CO2在电极材料表面发生还原反应的历程如图(*表示微粒与Bi的接触位点):

①HCOOH是
②依据反应历程图中数据,你认为电催化还原CO2生成HCOOH的选择性
您最近一年使用:0次
2 . 下列事实不能用勒夏特列原理解释的是
| A.采用排饱和食盐水的方法收集氯气 |
B.红棕色的 ,加压后颜色先变深后变浅 ,加压后颜色先变深后变浅 |
| C.高压更有利于合成氨 |
D.盛有 溶液与稀硫酸混合液的试管浸入热水时迅速变浑浊 溶液与稀硫酸混合液的试管浸入热水时迅速变浑浊 |
您最近一年使用:0次
2023-05-01更新
|
270次组卷
|
7卷引用:四川省资阳中学2022-2023学年高二上学期期末考试化学试题
名校
解题方法
3 . 下列事实不能用勒夏特列原理解释的是
A. ,平衡后加压,颜色加深 ,平衡后加压,颜色加深 |
| B.夏天打开啤酒瓶,有许多气泡冒出 |
C.加压有利于 与 与 生成 生成 的反应 的反应 |
| D.浓硫酸的吸水性有利于酯化反应正向进行 |
您最近一年使用:0次
名校
4 . 下列说法正确的有几个
(1)强电解质溶液的导电能力不一定比弱电解质溶液强
(2)将氢氧化钠溶液和氨水各稀释一倍,氢氧根浓度均减小为原来的一半
(3)减少反应物的用量,平衡一定逆向移动
(4)加入催化剂可以降低活化能,活化分子百分比虽然没变,但可以加快反应速率
(5)电离常数大的酸溶液中的 一定比电离常数小的酸溶液中的
一定比电离常数小的酸溶液中的 大
大
(6)非电解质的水溶液一定不能导电
(7)常温下向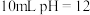 的氢氧化钠溶液中加入
的氢氧化钠溶液中加入 的
的 溶液至
溶液至 ,所得溶液的总体积≤20mL
,所得溶液的总体积≤20mL
(1)强电解质溶液的导电能力不一定比弱电解质溶液强
(2)将氢氧化钠溶液和氨水各稀释一倍,氢氧根浓度均减小为原来的一半
(3)减少反应物的用量,平衡一定逆向移动
(4)加入催化剂可以降低活化能,活化分子百分比虽然没变,但可以加快反应速率
(5)电离常数大的酸溶液中的
 一定比电离常数小的酸溶液中的
一定比电离常数小的酸溶液中的 大
大(6)非电解质的水溶液一定不能导电
(7)常温下向
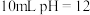 的氢氧化钠溶液中加入
的氢氧化钠溶液中加入 的
的 溶液至
溶液至 ,所得溶液的总体积≤20mL
,所得溶液的总体积≤20mL| A.1个 | B.2个 | C.3个 | D.4个 |
您最近一年使用:0次
5 . 甲为恒温恒容容器,乙为绝热恒容容器。在甲、乙两体积相同的密闭容器中均充入2mol  和6mol
和6mol  ,发生反应:
,发生反应:
 ,一段时间后均达到平衡。下列说法正确的是
,一段时间后均达到平衡。下列说法正确的是
 和6mol
和6mol  ,发生反应:
,发生反应:
 ,一段时间后均达到平衡。下列说法正确的是
,一段时间后均达到平衡。下列说法正确的是| A.平衡时,化学反应速率:甲=乙 |
B.平衡时, 的物质的量分数:甲<乙 的物质的量分数:甲<乙 |
| C.向甲容器中充入一定量的氦气,平衡向正反应方向移动 |
| D.平衡时,升高甲的温度,可达到与乙一样的平衡状态 |
您最近一年使用:0次
6 . 下列实验操作、现象及结论都正确的是
| 选项 | 实验操作 | 实验现象及结论 |
| A | 把水滴入盛有少量 固体的试管中,向反应后的溶液滴入3滴酚酞溶液 固体的试管中,向反应后的溶液滴入3滴酚酞溶液 | 溶液最终呈红色,说明反应后溶液呈碱性 |
| B | 将 球浸泡在热水中 球浸泡在热水中 | 球内气体颜色加深,说明 是放热反应 是放热反应 |
| C | 取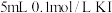 溶液于试管中,加入 溶液于试管中,加入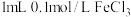 溶液,充分反应后滴入5滴 溶液,充分反应后滴入5滴 溶液 溶液 | 产生蓝色沉淀,说明 与 与 的反应有一定限度 的反应有一定限度 |
| D | 取 20%的蔗糖溶液于试管中,加入适量稀 20%的蔗糖溶液于试管中,加入适量稀 后水浴加热5min;再加入适量新制 后水浴加热5min;再加入适量新制 并加热 并加热 | 未产生砖红色沉淀,说明蔗糖在该条件下未发生水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 下列生产、生活等实际应用,不能用勒夏特列原理解释的是
| A.实验室中配制FeCl3溶液时,向其中加入少量浓盐酸 |
| B.工业合成氨选择高温和催化剂铁触媒 |
| C.Mg(OH)2沉淀可溶解于NH4Cl溶液中 |
| D.热的纯碱溶液去油污效果好 |
您最近一年使用:0次
名校
解题方法
8 . 某兴趣小组用铬铁矿(FeCr2O4,含Al、Si氧化物等杂质)为主要原料制备K2Cr2O7晶体,流程如下:
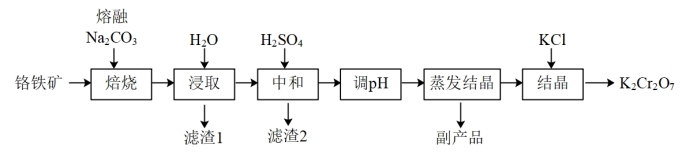
(1)焙烧的目的是将FeCr2O4转化为Na2CrO4,并将Al、Si氧化物转化为可溶性钠盐。焙烧时气体与矿料逆流而行,目的是___________ 。该步骤不能使用陶瓷容器,原因是___________ 。
(2)滤渣2的主要成份是Al(OH)3和___________ 。
(3)流程中调溶液的pH使之变___________ (填“大”或“小”),原因是___________ (用离子方程式表示)。
(4)蒸发结晶所产生的副产品是___________ 。
(5)为结晶得到杂质较少的K2Cr2O7粗产品,请结合下图从下列选项中选出合理的操作并排序___________ 。

a.50℃蒸发溶剂
b.100℃蒸发溶剂
c.抽滤
d.冷却至室温
e.蒸发至溶液出现晶膜,停止加热
f.蒸发至溶液出现大量晶体,停止加热
(6)该小组用m1kg铬铁矿(FeCr2O460%)制备K2Cr2O7,最终得到产品m2kg,产率为___________ (列出计算式)。

(1)焙烧的目的是将FeCr2O4转化为Na2CrO4,并将Al、Si氧化物转化为可溶性钠盐。焙烧时气体与矿料逆流而行,目的是
(2)滤渣2的主要成份是Al(OH)3和
(3)流程中调溶液的pH使之变
(4)蒸发结晶所产生的副产品是
(5)为结晶得到杂质较少的K2Cr2O7粗产品,请结合下图从下列选项中选出合理的操作并排序

a.50℃蒸发溶剂
b.100℃蒸发溶剂
c.抽滤
d.冷却至室温
e.蒸发至溶液出现晶膜,停止加热
f.蒸发至溶液出现大量晶体,停止加热
(6)该小组用m1kg铬铁矿(FeCr2O460%)制备K2Cr2O7,最终得到产品m2kg,产率为
您最近一年使用:0次
2022-03-27更新
|
1191次组卷
|
6卷引用:四川省南充市2022届高三 适应性考试(二模)理综化学试题
四川省南充市2022届高三 适应性考试(二模)理综化学试题(已下线)【奋进985】08-备战2022年高考化学名校进阶模拟卷(通用版)(已下线)微专题27 化学工艺流程题-----物质的分离与提纯-备战2023年高考化学一轮复习考点微专题四川省内江市第六中学2022-2023学年高二下学期第一次月考(创新班)化学试题2023届四川省绵阳东辰高级中学高三下学期大学预备部三诊模拟考试理综试题四川省泸县第五中学2023-2024学年高三上学期期末考试理综试题-高中化学
9 . 900°C时,将一 定质量的碳酸钙固体放入密闭容器中建立如下平衡:CaCO3(s)  CaO(s)+ CO2(g) ΔH> 0。下列说法错误的是
CaO(s)+ CO2(g) ΔH> 0。下列说法错误的是
 CaO(s)+ CO2(g) ΔH> 0。下列说法错误的是
CaO(s)+ CO2(g) ΔH> 0。下列说法错误的是| A.该反应高温下能自发进行 |
| B.达平衡后,再向容器中充入少量二氧化碳气体,达新平衡后c(CO2)不变 |
| C.达平衡后,再向容器中补充少量碳酸钙固体,反应速率加快,且平衡正向移动 |
| D.当容器中气体密度不再变化时,达到平衡状态 |
您最近一年使用:0次
名校
10 . 将等物质的量的X和Y投入某密闭容器中发生反应: ,达平衡后,改变某一条件,引起的变化正确的是
,达平衡后,改变某一条件,引起的变化正确的是
 ,达平衡后,改变某一条件,引起的变化正确的是
,达平衡后,改变某一条件,引起的变化正确的是| 条件改变 | 引发变化 | |
| A | 加入合适催化剂 | 活化分子百分数增大 |
| B | 缩小容器体积 | X的浓度不变 |
| C | 加入Y | 平衡正向移动 |
| D | 升高温度 | X的转化率增大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-01-27更新
|
165次组卷
|
2卷引用:四川省宜宾市2021-2022学年高二上学期理科期末考试化学试题



