名校
解题方法
1 . 表中实验操作、现象与结论对应关系均正确的
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 取2mL0.lmol/LAgNO3溶液,先后滴加3滴0.lmol/LNaCl溶液和6滴0.lmol/LKI溶液,观察沉淀情况 | 先产生白色沉淀,后产生黄色沉淀 | Ksp(AgCl)大于Ksp(AgI) |
| B | 等体积pH=2的两种酸HX和HY分别与足量的锌反应 | HX溶液中放出的H2多 | HX的酸性比HY弱 |
| C | 在KSCN与FeCl3的混合液中再加入KCl固体 | 溶液颜色变浅 | 增大生成物浓度,平衡逆向移动 |
| D | 用广泛pH试纸测定1mol/LNaHSO3溶液的酸碱性 | 测定pH=3.2 | NaHSO3溶液呈酸性,证明 在水中的电离程度大于水解程度 在水中的电离程度大于水解程度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
2 . 氨气和甲醇都是重要的工业产品,试运用必要的化学原理解决有关问题。
(1)在密闭容器中,使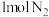 和
和 混合发生下列反应:
混合发生下列反应:
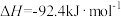 。
。
①反应进行一段时间后, 和
和 的转化率之比
的转化率之比______ 1(填“>”“<”或“=”)。
②当达到平衡时,充入氩气,并保持体积不变,平衡将______ (填“正向”“逆向”或“不”)移动。
③恒温下,压缩容器体积,混合气体的平均相对分子质量______ ,密度______ (填“变大”“变小”或“不变”)。
(2)水煤气在一定条件下可合成甲醇: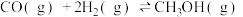
 。将1mol CO和
。将1mol CO和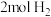 充入1L恒容密闭容器中,在一定条件下合成甲醇,相同时间(2min)内测得CO的转化率与温度的对应关系如图所示:
充入1L恒容密闭容器中,在一定条件下合成甲醇,相同时间(2min)内测得CO的转化率与温度的对应关系如图所示:
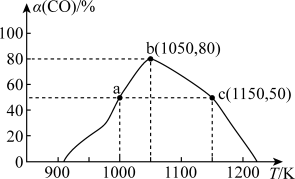
①试求温度为1000K条件下,反应开始至2min时,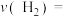
______ 。
②由图可知,从反应开始到b点之前,CO的转化率随温度升高而增大,原因是____________________ 。
③已知c点时容器内的压强为p,则在1150K温度下该反应的压强平衡常数 为
为______ (不用写单位, 是用各气体物质的分压替代浓度来计算的平衡常数)。
是用各气体物质的分压替代浓度来计算的平衡常数)。
(1)在密闭容器中,使
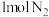 和
和 混合发生下列反应:
混合发生下列反应:
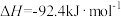 。
。①反应进行一段时间后,
 和
和 的转化率之比
的转化率之比②当达到平衡时,充入氩气,并保持体积不变,平衡将
③恒温下,压缩容器体积,混合气体的平均相对分子质量
(2)水煤气在一定条件下可合成甲醇:
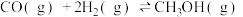
 。将1mol CO和
。将1mol CO和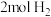 充入1L恒容密闭容器中,在一定条件下合成甲醇,相同时间(2min)内测得CO的转化率与温度的对应关系如图所示:
充入1L恒容密闭容器中,在一定条件下合成甲醇,相同时间(2min)内测得CO的转化率与温度的对应关系如图所示:
①试求温度为1000K条件下,反应开始至2min时,
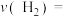
②由图可知,从反应开始到b点之前,CO的转化率随温度升高而增大,原因是
③已知c点时容器内的压强为p,则在1150K温度下该反应的压强平衡常数
 为
为 是用各气体物质的分压替代浓度来计算的平衡常数)。
是用各气体物质的分压替代浓度来计算的平衡常数)。
您最近一年使用:0次
3 . 钒具有广泛用途。黏土钒矿中,钒以 、
、 、
、 价的化合物存在,还包括钾、镁的铝硅酸盐,以及
价的化合物存在,还包括钾、镁的铝硅酸盐,以及 、
、 。采用以下工艺流程可由黏土钒矿制备
。采用以下工艺流程可由黏土钒矿制备 。
。
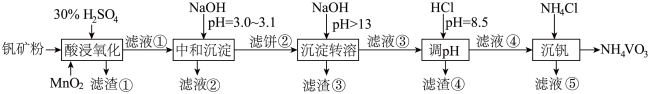
该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)“酸浸氧化”中, 和
和 被氧化成
被氧化成 ,同时还有
,同时还有_______ 离子被氧化。写出 转化为
转化为 反应的离子方程式
反应的离子方程式_______ 。
(2)“中和沉淀”中,钒水解并沉淀为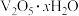 ,随滤液②可除去金属离子
,随滤液②可除去金属离子 、
、 、
、 、
、_______ ,以及部分的_______ 。
(3)“沉淀转溶”中,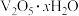 转化为钒酸盐溶解。滤渣③的主要成分是
转化为钒酸盐溶解。滤渣③的主要成分是_______ 。
(4)利用上述表格数据,计算 的
的
_______ ( 完全沉淀后其浓度应小于
完全沉淀后其浓度应小于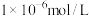 )。
)。
(5)“沉钒”中析出 晶体时,需要加入过量
晶体时,需要加入过量 ,其原因是
,其原因是_______ 。
 、
、 、
、 价的化合物存在,还包括钾、镁的铝硅酸盐,以及
价的化合物存在,还包括钾、镁的铝硅酸盐,以及 、
、 。采用以下工艺流程可由黏土钒矿制备
。采用以下工艺流程可由黏土钒矿制备 。
。
该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 |  |  |  |  |
| 开始沉淀pH | 1.9 | 7.0 | 3.0 | 8.1 |
| 完全沉淀pH | 3.0 | 9.0 | 4.7 | 10.1 |
(1)“酸浸氧化”中,
 和
和 被氧化成
被氧化成 ,同时还有
,同时还有 转化为
转化为 反应的离子方程式
反应的离子方程式(2)“中和沉淀”中,钒水解并沉淀为
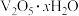 ,随滤液②可除去金属离子
,随滤液②可除去金属离子 、
、 、
、 、
、(3)“沉淀转溶”中,
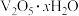 转化为钒酸盐溶解。滤渣③的主要成分是
转化为钒酸盐溶解。滤渣③的主要成分是(4)利用上述表格数据,计算
 的
的
 完全沉淀后其浓度应小于
完全沉淀后其浓度应小于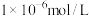 )。
)。(5)“沉钒”中析出
 晶体时,需要加入过量
晶体时,需要加入过量 ,其原因是
,其原因是
您最近一年使用:0次
名校
4 . 重铬酸钾(K2Cr2O7)又名红矾钾,是化学实验室中的一种重要分析试剂,在工业上用途广泛。已知K2Cr2O7溶液中存在平衡:
请回答下列问题:
(1)K2Cr2O7溶液中反应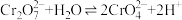 平衡常数的表达式为
平衡常数的表达式为
___________ 。
(2)复分解法制备重铬酸钾:以Na2CrO4溶液为原料,步骤如下:
①先向Na2CrO4溶液中加入酸调节溶液pH,其目的是___________ 。
②再向①的溶液中加入适量KCl,搅拌溶解、蒸发浓缩、冷却结晶,抽滤得到K2Cr2O7粗产品。则相同温度时的溶解度:Na2Cr2O7___________ K2Cr2O7(填“>”“<”或“=”)。
(3)K2Cr2O7溶液中存在的平衡又可分解为以下两步:
(ⅰ)

(ⅱ)

①下列有关K2Cr2O7溶液的说法正确的有_______ 。
A.加入少量硫酸,溶液颜色由橙色向黄色转变
B.加入少量水稀释,溶液中离子总数增加
C.加入少量NaOH溶液,反应(ⅰ)的平衡逆向移动
D.加入少量K2Cr2O7固体,平衡时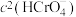 与
与 的比值保持不变
的比值保持不变
②在0.10 mol⋅L-1 K2Cr2O7溶液中设 、
、 、
、 的平衡浓度分别为x、y、z mol·L-1,则x、y、z之间的关系式为
的平衡浓度分别为x、y、z mol·L-1,则x、y、z之间的关系式为_______ =0.10。
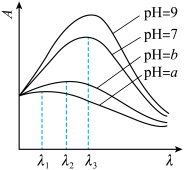
③已知在稀溶液中,一种物质对光的吸收程度(A)与其所吸收光的波长(λ)有关;在一定波长范围内,最大A对应的波长(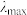 )取决于物质的结构特征;浓度越高,A越大。混合溶液在某一波长的A是各组分吸收程度之和。为研究对反应(ⅰ)和(ⅱ)平衡的影响,配制浓度相同、pH不同的K2Cr2O7稀溶液,测得其A随λ的变化曲线如右上图所示,波长λ1、λ2和λ3中,与
)取决于物质的结构特征;浓度越高,A越大。混合溶液在某一波长的A是各组分吸收程度之和。为研究对反应(ⅰ)和(ⅱ)平衡的影响,配制浓度相同、pH不同的K2Cr2O7稀溶液,测得其A随λ的变化曲线如右上图所示,波长λ1、λ2和λ3中,与 的
的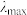 最接近的是
最接近的是_______ ;溶液pH从a变到b的过程中, 的值
的值_______ (填“增大”“减小”或“不变”)。

请回答下列问题:
(1)K2Cr2O7溶液中反应
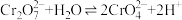 平衡常数的表达式为
平衡常数的表达式为
(2)复分解法制备重铬酸钾:以Na2CrO4溶液为原料,步骤如下:
①先向Na2CrO4溶液中加入酸调节溶液pH,其目的是
②再向①的溶液中加入适量KCl,搅拌溶解、蒸发浓缩、冷却结晶,抽滤得到K2Cr2O7粗产品。则相同温度时的溶解度:Na2Cr2O7
(3)K2Cr2O7溶液中存在的平衡又可分解为以下两步:
(ⅰ)


(ⅱ)



①下列有关K2Cr2O7溶液的说法正确的有
A.加入少量硫酸,溶液颜色由橙色向黄色转变
B.加入少量水稀释,溶液中离子总数增加
C.加入少量NaOH溶液,反应(ⅰ)的平衡逆向移动
D.加入少量K2Cr2O7固体,平衡时
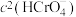 与
与 的比值保持不变
的比值保持不变②在0.10 mol⋅L-1 K2Cr2O7溶液中设
 、
、 、
、 的平衡浓度分别为x、y、z mol·L-1,则x、y、z之间的关系式为
的平衡浓度分别为x、y、z mol·L-1,则x、y、z之间的关系式为③已知在稀溶液中,一种物质对光的吸收程度(A)与其所吸收光的波长(λ)有关;在一定波长范围内,最大A对应的波长(
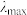 )取决于物质的结构特征;浓度越高,A越大。混合溶液在某一波长的A是各组分吸收程度之和。为研究对反应(ⅰ)和(ⅱ)平衡的影响,配制浓度相同、pH不同的K2Cr2O7稀溶液,测得其A随λ的变化曲线如右上图所示,波长λ1、λ2和λ3中,与
)取决于物质的结构特征;浓度越高,A越大。混合溶液在某一波长的A是各组分吸收程度之和。为研究对反应(ⅰ)和(ⅱ)平衡的影响,配制浓度相同、pH不同的K2Cr2O7稀溶液,测得其A随λ的变化曲线如右上图所示,波长λ1、λ2和λ3中,与 的
的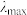 最接近的是
最接近的是 的值
的值
您最近一年使用:0次
5 . 重铬酸钾(K2Cr2O7)又名红矾钾,是化学实验室中的一种重要分析试剂,在工业上用途广泛。已知水溶液中存在平衡:( )。请回答下列问题:
)。请回答下列问题:
(1)复分解法制备重铬酸钾
以Na2CrO4溶液为原料,步骤如下:
①先向Na2CrO4溶液中加入酸调节溶液pH,其目的是___________ 。
②再向①的溶液中加入适量KCl,搅拌溶解、蒸发浓缩、冷却结晶,抽滤得到K2Cr2O7粗产品。则相同温度时的溶解度:Na2Cr2O7___________ K2Cr2O7 (填“﹥”“﹤”或“=”)。
(2)电化学法制备重铬酸钾
以净化后的铬酸钾(K2CrO4)为原料,用电化学法制备重铬酸钾的实验装置如图所示。
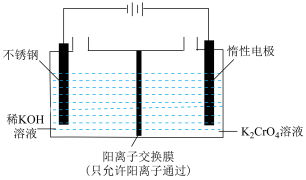
①不锈钢电极的电极反应式为___________ 。
②阳极区能得到重铬酸钾溶液的原因是___________ 。
(3)工业上常用钡盐沉淀法处理含有K2Cr2O7的废水,达到含铬废水达标排放、六价铬[Cr(Ⅵ)]回收利用、保护环境和节约资源的目的。已知 具体流程如下图所示:
具体流程如下图所示:

①从步骤i→Ⅱ生成沉淀2的总反应离子方程式为___________ 。
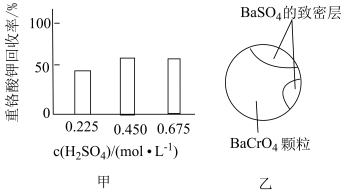
②向沉淀2中加入硫酸,回收Cr(Ⅵ)。加入不同浓度硫酸,每次均搅拌10小时,硫酸浓度对重铬酸的回收率如图甲所示。但当硫酸浓度高于 时,重铬酸的回收率没有明显变化,结合图乙分析其原因是
时,重铬酸的回收率没有明显变化,结合图乙分析其原因是___________ 。
 )。请回答下列问题:
)。请回答下列问题:(1)复分解法制备重铬酸钾
以Na2CrO4溶液为原料,步骤如下:
①先向Na2CrO4溶液中加入酸调节溶液pH,其目的是
②再向①的溶液中加入适量KCl,搅拌溶解、蒸发浓缩、冷却结晶,抽滤得到K2Cr2O7粗产品。则相同温度时的溶解度:Na2Cr2O7
(2)电化学法制备重铬酸钾
以净化后的铬酸钾(K2CrO4)为原料,用电化学法制备重铬酸钾的实验装置如图所示。

①不锈钢电极的电极反应式为
②阳极区能得到重铬酸钾溶液的原因是
(3)工业上常用钡盐沉淀法处理含有K2Cr2O7的废水,达到含铬废水达标排放、六价铬[Cr(Ⅵ)]回收利用、保护环境和节约资源的目的。已知
 具体流程如下图所示:
具体流程如下图所示:
①从步骤i→Ⅱ生成沉淀2的总反应离子方程式为
②向沉淀2中加入硫酸,回收Cr(Ⅵ)。加入不同浓度硫酸,每次均搅拌10小时,硫酸浓度对重铬酸的回收率如图甲所示。但当硫酸浓度高于
 时,重铬酸的回收率没有明显变化,结合图乙分析其原因是
时,重铬酸的回收率没有明显变化,结合图乙分析其原因是
您最近一年使用:0次
解题方法
6 . 工业上以铬铁矿(主要成分为 ,含Al、Si氧化物等杂质)为主要原料制备红矾钠
,含Al、Si氧化物等杂质)为主要原料制备红矾钠 的工艺流程如图。回答下列问题:
的工艺流程如图。回答下列问题:

(1) 中Fe元素的化合价
中Fe元素的化合价___________ ,焙烧的目的是将 转化为
转化为 并将Al、Si氧化物转化为可溶性钠盐,焙烧时气体与矿料逆流而行,目的是
并将Al、Si氧化物转化为可溶性钠盐,焙烧时气体与矿料逆流而行,目的是___________ 。
(2)滤渣2的成分___________ (填化学式)滤渣提纯后的用途___________ 。
(3)加入 酸化的作用是
酸化的作用是___________ (结合化学用语简述)。
(4)蒸发结晶时,过度蒸发将导致___________
(5)该小组用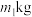 铬铁矿(
铬铁矿( 的质量分数60%)制备
的质量分数60%)制备 ,最终得到产品
,最终得到产品 ,产率为
,产率为___________ (列出计算式)
 ,含Al、Si氧化物等杂质)为主要原料制备红矾钠
,含Al、Si氧化物等杂质)为主要原料制备红矾钠 的工艺流程如图。回答下列问题:
的工艺流程如图。回答下列问题:
(1)
 中Fe元素的化合价
中Fe元素的化合价 转化为
转化为 并将Al、Si氧化物转化为可溶性钠盐,焙烧时气体与矿料逆流而行,目的是
并将Al、Si氧化物转化为可溶性钠盐,焙烧时气体与矿料逆流而行,目的是(2)滤渣2的成分
(3)加入
 酸化的作用是
酸化的作用是(4)蒸发结晶时,过度蒸发将导致
(5)该小组用
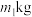 铬铁矿(
铬铁矿( 的质量分数60%)制备
的质量分数60%)制备 ,最终得到产品
,最终得到产品 ,产率为
,产率为
您最近一年使用:0次
解题方法
7 . 下列解释事实的离子方程式不正确的是
A.在重铬酸钾溶液中滴入氢氧化钠溶液,溶液变为黄色: |
B.牙齿表面薄层釉质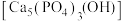 易被有机酸溶解从而导致龋齿,含氟牙膏能起到预防龋齿的作用的原理: 易被有机酸溶解从而导致龋齿,含氟牙膏能起到预防龋齿的作用的原理: |
C. 化学性质非常稳定,在工业上有着广泛用途,可用 化学性质非常稳定,在工业上有着广泛用途,可用 制备 制备 : : |
D.纯碱溶于水显碱性: |
您最近一年使用:0次
8 . 铬是硬度最高的金属,具有良好的抗腐蚀性的耐磨性,常用于制造不锈钢和仪器仪表的金属表面镀铬,用途十分广泛。
(1)铬的常见的氧化——三氧化二铬( ),既能与KOH溶液反应生成
),既能与KOH溶液反应生成 ,又能与硫酸反应生成
,又能与硫酸反应生成 。
。 是
是___________ (填“酸性”“碱性”或“两性”)氧化物, 与过量KOH溶液反应的离子方程式为
与过量KOH溶液反应的离子方程式为___________ 。
(2)已知: ,Cr(Ⅲ)体现还原性生成
,Cr(Ⅲ)体现还原性生成 或
或 。在碱性介质中Cr(Ⅲ)有较强的还原性,可使
。在碱性介质中Cr(Ⅲ)有较强的还原性,可使 —淀粉溶液褪色,反应过程中铬元素由
—淀粉溶液褪色,反应过程中铬元素由___________ 转化为___________ (填离子符号);在酸性介质中Cr(Ⅲ)还原性较差,可与强氧化剂反应,可将 还原为
还原为 ,其反应的离子方程式为
,其反应的离子方程式为___________ 。
(3) 中铬元素的化合价为
中铬元素的化合价为___________ ;将 溶液滴加到淀粉——KI溶液中,溶液变蓝;可使
溶液滴加到淀粉——KI溶液中,溶液变蓝;可使 、
、 和
和 在不同酸碱性条件下氧化性的大小关系是
在不同酸碱性条件下氧化性的大小关系是___________ 。
(1)铬的常见的氧化——三氧化二铬(
 ),既能与KOH溶液反应生成
),既能与KOH溶液反应生成 ,又能与硫酸反应生成
,又能与硫酸反应生成 。
。 是
是 与过量KOH溶液反应的离子方程式为
与过量KOH溶液反应的离子方程式为(2)已知:
 ,Cr(Ⅲ)体现还原性生成
,Cr(Ⅲ)体现还原性生成 或
或 。在碱性介质中Cr(Ⅲ)有较强的还原性,可使
。在碱性介质中Cr(Ⅲ)有较强的还原性,可使 —淀粉溶液褪色,反应过程中铬元素由
—淀粉溶液褪色,反应过程中铬元素由 还原为
还原为 ,其反应的离子方程式为
,其反应的离子方程式为(3)
 中铬元素的化合价为
中铬元素的化合价为 溶液滴加到淀粉——KI溶液中,溶液变蓝;可使
溶液滴加到淀粉——KI溶液中,溶液变蓝;可使 、
、 和
和 在不同酸碱性条件下氧化性的大小关系是
在不同酸碱性条件下氧化性的大小关系是
您最近一年使用:0次
9 . 重金属元素钒(V)性能优良,用途广泛,有金属“维生素”之称,以硅藻土为载体的五氧化二钒(V2O5)是接触法制备硫酸的催化剂。
废钒催化剂的主要成分为:
以下是一种废钒催化剂回收 工艺路线:
工艺路线:

回答下列问题:
(1)“酸浸”时V2O5转化为 ,V2O4转化为VO2+,写出V2O4转化为VO2+反应的离子方程式:
,V2O4转化为VO2+,写出V2O4转化为VO2+反应的离子方程式:_______ 。
(2)“氧化”中VO2+转变为 ,反应的离子方程式为
,反应的离子方程式为_______ 。
(3)V2O5能与盐酸反应产生VO2+和一种黄绿色气体,该气体能与Na2SO3溶液反应被吸收,则 、Cl-、VO2+还原性由小到大的顺序是
、Cl-、VO2+还原性由小到大的顺序是_______ 。
(4)“中和”作用之一是使钒以 形式存在于溶液中,“废渣2”中含有
形式存在于溶液中,“废渣2”中含有_______ 。
(5)“离子交换”和“洗脱”可简单表示为: (以ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈
(以ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈_______ 性(填“酸”“碱”“中”)。
(6)“煅烧”中使用的主要实验仪器名称为(写3种)_______ 。
废钒催化剂的主要成分为:
| 物质 |  |  | 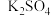 |  |  |  |
| 质量分数/% | 2.2~2.9 | 2.8~3.1 | 22~28 | 60~65 | 1~2 | <1 |
 工艺路线:
工艺路线:
回答下列问题:
(1)“酸浸”时V2O5转化为
 ,V2O4转化为VO2+,写出V2O4转化为VO2+反应的离子方程式:
,V2O4转化为VO2+,写出V2O4转化为VO2+反应的离子方程式:(2)“氧化”中VO2+转变为
 ,反应的离子方程式为
,反应的离子方程式为(3)V2O5能与盐酸反应产生VO2+和一种黄绿色气体,该气体能与Na2SO3溶液反应被吸收,则
 、Cl-、VO2+还原性由小到大的顺序是
、Cl-、VO2+还原性由小到大的顺序是(4)“中和”作用之一是使钒以
 形式存在于溶液中,“废渣2”中含有
形式存在于溶液中,“废渣2”中含有(5)“离子交换”和“洗脱”可简单表示为:
 (以ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈
(以ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈(6)“煅烧”中使用的主要实验仪器名称为(写3种)
您最近一年使用:0次
10 . 我国力争于2030年前做到碳达峰,2060年前实现碳中和。CH4与CO2重整是CO2利用的研究热点之一、该重整反应体系主要涉及以下反应:
a)

b)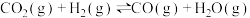

c)

d)

e)

(1)已知相关物质的燃烧热(25℃、101 kPa):
则△H1=___________ 。
(2)上述反应体系在一定条件下建立平衡后,下列说法正确的有___________。
(3)一定条件下,CH4分解形成碳的反应历程如图所示。该历程分___________ 步进行,其中,第___________ 步的正反应活化能最大。

(4)900℃下,将CH4和CO2的混合气体(投料比1:1)按一定流速通过盛有炭催化剂的反应器,测得CH4的转化率受炭催化剂颗粒大小的影响如图所示。(注:目数越大,表示炭催化剂颗粒越小)

由图可知,75 min后CH4转化率与炭催化剂目数的关系为___________ ,原因是___________ 。
(5)CO2用途广泛,写出基于其物理性质的一种用途:___________ 。
a)


b)
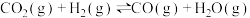

c)


d)


e)


(1)已知相关物质的燃烧热(25℃、101 kPa):
| 物质 | CH4(g) | CO(g) | H2(g) |
燃烧热(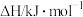 ) ) |  |  |  |
(2)上述反应体系在一定条件下建立平衡后,下列说法正确的有___________。
| A.移去部分C(s),反应c、d、e的平衡均向右移动 |
| B.增大CO2与CH4的浓度,反应a、b、c的正反应速率都增加 |
| C.加入反应a的催化剂,可提高CH4的平衡转化率 |
| D.降低反应温度,反应a~e的正、逆反应速率都减小 |

(4)900℃下,将CH4和CO2的混合气体(投料比1:1)按一定流速通过盛有炭催化剂的反应器,测得CH4的转化率受炭催化剂颗粒大小的影响如图所示。(注:目数越大,表示炭催化剂颗粒越小)

由图可知,75 min后CH4转化率与炭催化剂目数的关系为
(5)CO2用途广泛,写出基于其物理性质的一种用途:
您最近一年使用:0次



