名校
解题方法
1 . 缓冲和供氧是维持人体正常生理活动的两个重要平衡系统,回答下列问题:
Ⅰ.人体血液中存在平衡:H2CO3 (aq) H+(aq)+HCO3-(aq) ΔH,该平衡可使血液的pH维持在一定范围内。
H+(aq)+HCO3-(aq) ΔH,该平衡可使血液的pH维持在一定范围内。
(1)已知:CO2(g) CO2(aq) ΔH1=akJ·mol-l;
CO2(aq) ΔH1=akJ·mol-l;
CO2(aq)+H2O(l) H2CO3 (aq) ΔH2=bkJ·mol-1;
H2CO3 (aq) ΔH2=bkJ·mol-1;
HCO (aq)
(aq) H+(aq)+CO
H+(aq)+CO (aq) ΔH3=ckJ·mol-1;
(aq) ΔH3=ckJ·mol-1;
CO2(g)+H2O(l) 2H+(aq)+ CO
2H+(aq)+ CO (aq) ΔH4=dkJ·mol-1。
(aq) ΔH4=dkJ·mol-1。
则上述电离方程式中ΔH =_____________ (用含a、b、c、d的代数式表示)。
(2)若某人血液中c(HCO ):c(H2CO3) = 20:1,pKa1(H2CO3)=6.1,则该人血液的pH为
):c(H2CO3) = 20:1,pKa1(H2CO3)=6.1,则该人血液的pH为______________ 。(lg2=0.3)若pH升高,则c(H2CO3)/c(HCO )=
)=___________ (填“增大”“减小”或“不变”)。
(3)当有少量酸性物质进入血液后,血液的pH变化不大,用平衡移动原理解释上述现象:_____________ 。
Ⅱ.肌细胞石储存氧气和分配氧气时存在如下平衡

(4)经测定动物体温升高,氧气的结合度[α(MbO2),氧合肌红蛋白的浓度占肌红蛋白初始浓度的百分数]降低,则该反应的ΔH_______________ (填“>”或“<”)0。
(5)温度为37 ℃时,氧气的结合度[α(MbO2)与氧气的平衡分压[p(O2)]关系如下图所示:
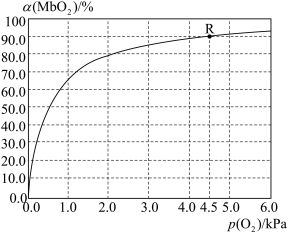
①利用R点所示数据,计算37 ℃时该反应的平衡常数K=_________________ (氧气的平衡浓度可用氧气的平衡分压代替求算)。
②已知37 ℃时,该反应的正反应速率v(正)=k1c(Mb)×p(O2),逆反应速率v(逆)=k2c(MbO2),若k2=60s-1,则k1=___________________ 。
Ⅰ.人体血液中存在平衡:H2CO3 (aq)
 H+(aq)+HCO3-(aq) ΔH,该平衡可使血液的pH维持在一定范围内。
H+(aq)+HCO3-(aq) ΔH,该平衡可使血液的pH维持在一定范围内。(1)已知:CO2(g)
 CO2(aq) ΔH1=akJ·mol-l;
CO2(aq) ΔH1=akJ·mol-l;CO2(aq)+H2O(l)
 H2CO3 (aq) ΔH2=bkJ·mol-1;
H2CO3 (aq) ΔH2=bkJ·mol-1;HCO
 (aq)
(aq) H+(aq)+CO
H+(aq)+CO (aq) ΔH3=ckJ·mol-1;
(aq) ΔH3=ckJ·mol-1;CO2(g)+H2O(l)
 2H+(aq)+ CO
2H+(aq)+ CO (aq) ΔH4=dkJ·mol-1。
(aq) ΔH4=dkJ·mol-1。则上述电离方程式中ΔH =
(2)若某人血液中c(HCO
 ):c(H2CO3) = 20:1,pKa1(H2CO3)=6.1,则该人血液的pH为
):c(H2CO3) = 20:1,pKa1(H2CO3)=6.1,则该人血液的pH为 )=
)=(3)当有少量酸性物质进入血液后,血液的pH变化不大,用平衡移动原理解释上述现象:
Ⅱ.肌细胞石储存氧气和分配氧气时存在如下平衡

(4)经测定动物体温升高,氧气的结合度[α(MbO2),氧合肌红蛋白的浓度占肌红蛋白初始浓度的百分数]降低,则该反应的ΔH
(5)温度为37 ℃时,氧气的结合度[α(MbO2)与氧气的平衡分压[p(O2)]关系如下图所示:

①利用R点所示数据,计算37 ℃时该反应的平衡常数K=
②已知37 ℃时,该反应的正反应速率v(正)=k1c(Mb)×p(O2),逆反应速率v(逆)=k2c(MbO2),若k2=60s-1,则k1=
您最近一年使用:0次
2018-03-19更新
|
477次组卷
|
3卷引用:山东省菏泽市2018届高三第一次模拟考试理综化学试题
名校
2 . 砷为VA族元素,金属冶炼过程产生的含砷有毒废水需处理与检测。
(1)I.已知:As(s)+ H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+ O2(g)=H2O(l) ΔH2
O2(g)=H2O(l) ΔH2
2As(s)+ O2(g) =As2O5(s) ΔH3
O2(g) =As2O5(s) ΔH3
则反应As2O5(s) +3H2O(l)= 2H3AsO4(s)的ΔH =_______________ 。
II.冶炼废水中砷元素主要以亚砷酸(H3AsO3)形式存在,可用化学沉降法处理酸性高浓度含砷废水,其工艺流程如下:

已知:①As2S3与过量的S2-存在以下反应:As2S3(s)+3S2-(aq) 2AsS
2AsS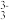 (aq);
(aq);
②亚砷酸盐的溶解性大于相应砷酸盐。
(1)亚砷酸中砷元素的化合价为______ ;砷酸的第一步电离方程式为_____________ 。
(2)“一级沉砷”中FeSO4的作用是_______________ ; “二级沉砷”中H2O2与含砷物质反应的化学方程式为_________ 。
III.去除水体中的砷,将As(Ⅲ)转化为As(Ⅴ),也可选用NaClO实现该转化。研究NaClO投加量对As(Ⅲ)氧化率的影响得到如下结果:
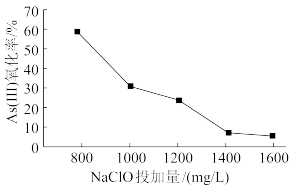
已知:投料前水样pH=5.81,0.1mol/LNaClO溶液pH=10.5,溶液中起氧化作用的物质是次氯酸。产生此结果的原因是_________________________________________ 。
(1)I.已知:As(s)+
 H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+2O2(g)=H3AsO4(s) ΔH1H2(g)+
 O2(g)=H2O(l) ΔH2
O2(g)=H2O(l) ΔH22As(s)+
 O2(g) =As2O5(s) ΔH3
O2(g) =As2O5(s) ΔH3则反应As2O5(s) +3H2O(l)= 2H3AsO4(s)的ΔH =
II.冶炼废水中砷元素主要以亚砷酸(H3AsO3)形式存在,可用化学沉降法处理酸性高浓度含砷废水,其工艺流程如下:

已知:①As2S3与过量的S2-存在以下反应:As2S3(s)+3S2-(aq)
 2AsS
2AsS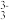 (aq);
(aq);②亚砷酸盐的溶解性大于相应砷酸盐。
(1)亚砷酸中砷元素的化合价为
(2)“一级沉砷”中FeSO4的作用是
III.去除水体中的砷,将As(Ⅲ)转化为As(Ⅴ),也可选用NaClO实现该转化。研究NaClO投加量对As(Ⅲ)氧化率的影响得到如下结果:

已知:投料前水样pH=5.81,0.1mol/LNaClO溶液pH=10.5,溶液中起氧化作用的物质是次氯酸。产生此结果的原因是
您最近一年使用:0次
3 . 某化学兴趣小组为验证SO2的还原性,特邀你参与以下探究活动。
I.理论预测
该兴趣小组实验实施前进行了充分的讨论交流,确定选择SO2和FeCl3溶液的反应来探究,并预测将SO2通入FeCl3溶液中的现象。小组同学想听听你的分析,你认为可能观察到的现象是:_____________ ,你预测的理论依据是(用离子方程式表示):________________________ 。
II.实验探究
(1)配制1mol/LFeCl3溶液(未用盐酸酸化)
①下面是小组四位同学在配制溶液时的“转移”操作,其中正确的是:_______________ 。
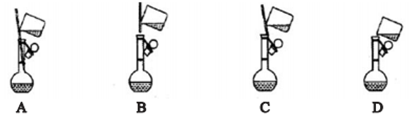
②测溶液的pH得知溶液呈酸性,其原因是:____________________ (用离子方程式表示)。
(2)SO2通入FeCl3溶液至饱和,观察到溶液由棕黄色变为红棕色,并没有观察到预期的现象。将反应后的溶液放置12小时后又出现了预期的结果。
查阅资料得知[Fe(HSO3)]2+为红棕色,生成[Fe(HSO3)]2+的反应为可逆反应。请你用化学方程式解释将SO2通入FeCl3溶液至饱和时观察到的现象:_______________ 。
(3)为了探究如何缩短红棕色变为预期颜色的时间,小组继续探究:另取少量FeCl3溶液,再通入SO2溶液变为红棕色,加浓HCl酸化,几分钟后变为预期颜色。
请你推测小组在实验方案设计中“加浓HCl酸化”的目的是:_______________ 。
III.感悟与分享
通过探究,小组同学深受启发、感悟良多。比如,有同学认为“实验才是化学的最高法庭”。请写出一种你的感悟与同学分享:______________________ 。
I.理论预测
该兴趣小组实验实施前进行了充分的讨论交流,确定选择SO2和FeCl3溶液的反应来探究,并预测将SO2通入FeCl3溶液中的现象。小组同学想听听你的分析,你认为可能观察到的现象是:
II.实验探究
(1)配制1mol/LFeCl3溶液(未用盐酸酸化)
①下面是小组四位同学在配制溶液时的“转移”操作,其中正确的是:

②测溶液的pH得知溶液呈酸性,其原因是:
(2)SO2通入FeCl3溶液至饱和,观察到溶液由棕黄色变为红棕色,并没有观察到预期的现象。将反应后的溶液放置12小时后又出现了预期的结果。
查阅资料得知[Fe(HSO3)]2+为红棕色,生成[Fe(HSO3)]2+的反应为可逆反应。请你用化学方程式解释将SO2通入FeCl3溶液至饱和时观察到的现象:
(3)为了探究如何缩短红棕色变为预期颜色的时间,小组继续探究:另取少量FeCl3溶液,再通入SO2溶液变为红棕色,加浓HCl酸化,几分钟后变为预期颜色。
请你推测小组在实验方案设计中“加浓HCl酸化”的目的是:
III.感悟与分享
通过探究,小组同学深受启发、感悟良多。比如,有同学认为“实验才是化学的最高法庭”。请写出一种你的感悟与同学分享:
您最近一年使用:0次
4 . 以下是关于“外界因素对化学平衡移动影响的实验研究”的课题,回答问题:
(1)影响化学平衡因素的界定:化学平衡发生移动的本质原因是________ ,所以影响化学平衡的因素可以从分析影响的因素入手.
a. v(正)≠v(逆) .v(正)和v(逆)都增大
.v(正)和v(逆)都增大 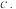 v(正)和v(逆)都减小
v(正)和v(逆)都减小
(2)研究的思路与方法
①研究对象的选择,现有以下可逆反应:
 .
.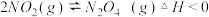
 .
.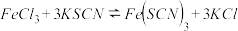
其中, 适合于研究
适合于研究_______ 对平衡的影响, 适合于研究
适合于研究_______ 对平衡的影响.
 .浓度
.浓度  .温度
.温度  .压强
.压强  .催化剂
.催化剂
②研究方法:采用控制其他因素不变,改变其中一个因素的方法,并进行对比实验.
(3)单一因素对化学平衡移动影响的实验研究:
 .浓度:将
.浓度:将 与
与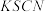 反应后所得的混合液分为
反应后所得的混合液分为 等份,分别加入浓
等份,分别加入浓 溶液、浓
溶液、浓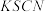 溶液和
溶液和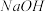 固体,观察现象.现象:加入浓
固体,观察现象.现象:加入浓 溶液后的混合溶液红色
溶液后的混合溶液红色________ ,加入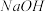 固体后,混合溶液红棕色
固体后,混合溶液红棕色________ .
 .温度:将密封并相互连通的盛有
.温度:将密封并相互连通的盛有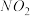 的两个玻璃球,一个放入热水中,另一个放入冷水中.
的两个玻璃球,一个放入热水中,另一个放入冷水中.
现象:放入热水中的球内红棕色________ ;放入冷水中的球内红棕色________ .
(4)综合(3)能得出的影响化学平衡移动的原因是________ .
(1)影响化学平衡因素的界定:化学平衡发生移动的本质原因是
a. v(正)≠v(逆)
 .v(正)和v(逆)都增大
.v(正)和v(逆)都增大 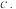 v(正)和v(逆)都减小
v(正)和v(逆)都减小(2)研究的思路与方法
①研究对象的选择,现有以下可逆反应:
 .
.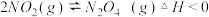
 .
.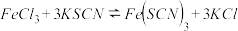
其中,
 适合于研究
适合于研究 适合于研究
适合于研究 .浓度
.浓度  .温度
.温度  .压强
.压强  .催化剂
.催化剂②研究方法:采用控制其他因素不变,改变其中一个因素的方法,并进行对比实验.
(3)单一因素对化学平衡移动影响的实验研究:
 .浓度:将
.浓度:将 与
与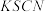 反应后所得的混合液分为
反应后所得的混合液分为 等份,分别加入浓
等份,分别加入浓 溶液、浓
溶液、浓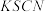 溶液和
溶液和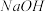 固体,观察现象.现象:加入浓
固体,观察现象.现象:加入浓 溶液后的混合溶液红色
溶液后的混合溶液红色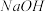 固体后,混合溶液红棕色
固体后,混合溶液红棕色 .温度:将密封并相互连通的盛有
.温度:将密封并相互连通的盛有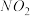 的两个玻璃球,一个放入热水中,另一个放入冷水中.
的两个玻璃球,一个放入热水中,另一个放入冷水中.现象:放入热水中的球内红棕色
(4)综合(3)能得出的影响化学平衡移动的原因是
您最近一年使用:0次
名校
5 . 重铬酸钾溶液中存在如下平衡:(1)Cr2O72-+H2O 2H++2CrO42-,向2mL0.1mol·L-1酸化的K2Cr2O7溶液中滴入适量(NH4)2Fe(SO4)2溶液,发生反应:Cr2O72-+14H++6Fe2+=2Cr3++6Fe3++7H2O。下列分析正确的是
2H++2CrO42-,向2mL0.1mol·L-1酸化的K2Cr2O7溶液中滴入适量(NH4)2Fe(SO4)2溶液,发生反应:Cr2O72-+14H++6Fe2+=2Cr3++6Fe3++7H2O。下列分析正确的是
 2H++2CrO42-,向2mL0.1mol·L-1酸化的K2Cr2O7溶液中滴入适量(NH4)2Fe(SO4)2溶液,发生反应:Cr2O72-+14H++6Fe2+=2Cr3++6Fe3++7H2O。下列分析正确的是
2H++2CrO42-,向2mL0.1mol·L-1酸化的K2Cr2O7溶液中滴入适量(NH4)2Fe(SO4)2溶液,发生反应:Cr2O72-+14H++6Fe2+=2Cr3++6Fe3++7H2O。下列分析正确的是| A.向K2Cr2O7溶液加入几滴浓NaOH溶液,溶液由黄色变成橙黄 |
| B.氧化性:Cr2O72->Fe3+ |
| C.CrO42-和Fe2+在酸性溶液中能大量共存 |
| D.向K2Cr2O7溶液中加水稀释,反应(1)平衡向左移动 |
您最近一年使用:0次
2017-11-29更新
|
266次组卷
|
2卷引用:湖北省华中师范大学第一附属中学2017-2018学年高二上学期期中考试化学试题
6 . 在温度T1 和T2 时,分别将0.50 mol CH4和1.2 mol NO2 充入体积为1L的恒容密闭容器中,发生如下反应:CH4(g) +2NO2(g)  N2(g) +CO2(g) +2H2O(g),测得n(CH4)随时间变化数据如下表,下列说法正确的是
N2(g) +CO2(g) +2H2O(g),测得n(CH4)随时间变化数据如下表,下列说法正确的是
 N2(g) +CO2(g) +2H2O(g),测得n(CH4)随时间变化数据如下表,下列说法正确的是
N2(g) +CO2(g) +2H2O(g),测得n(CH4)随时间变化数据如下表,下列说法正确的是| 温度 | 时间/min | 0 | 10 | 20 | 40 | 50 |
| T1 | n( CH4) /mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| T2 | n( CH4) /mol | 0.50 | 0.30 | 0.18 | …… | 0.15 |
| A.该反应的正反应为放热反应 |
| B.T1时,0~10 min NO2 的平均反应速率为0.15 mol·L-1·min -1 |
| C.保持其他条件不变,T2 时向平衡体系中再充入0.50 mol CH4和1.20 mol NO2,与原平衡相比,达新平衡时N2 的浓度增大、体积分数减小 |
| D.保持其他条件不变,T1 时向平衡体系中再充入0.30 mol CH4和0.80 mol H2O( g),平衡向正反应方向移动 |
您最近一年使用:0次
7 . 某温度下,在2L的密闭容器中,加入1molX和3molY发生反应:X(s)+mY(g) 3Z(g),平衡时,Y、Z的体积分数分别为60%、40%,在此平衡体系中加入2mol Z(g),再次达到平衡后,Y、Z的体积分数不变。下列叙述不正确的是
3Z(g),平衡时,Y、Z的体积分数分别为60%、40%,在此平衡体系中加入2mol Z(g),再次达到平衡后,Y、Z的体积分数不变。下列叙述不正确的是
 3Z(g),平衡时,Y、Z的体积分数分别为60%、40%,在此平衡体系中加入2mol Z(g),再次达到平衡后,Y、Z的体积分数不变。下列叙述不正确的是
3Z(g),平衡时,Y、Z的体积分数分别为60%、40%,在此平衡体系中加入2mol Z(g),再次达到平衡后,Y、Z的体积分数不变。下列叙述不正确的是 | A.从向平衡体系中加入2mol Z(g)到重新达到平衡始终存在v(逆)>v(正) |
| B.两次平衡的平衡常数相同 |
| C.第二次平衡时,Z的浓度为2mol·L-1 |
| D.m=3 |
您最近一年使用:0次
名校
8 . 将BaO2放入密闭真空容器中,反应2BaO2(s) 2BaO(s)+O2(g)达到平衡。下列哪些改变可使平衡移动,且新平衡时氧气的浓度与原平衡不同
2BaO(s)+O2(g)达到平衡。下列哪些改变可使平衡移动,且新平衡时氧气的浓度与原平衡不同
 2BaO(s)+O2(g)达到平衡。下列哪些改变可使平衡移动,且新平衡时氧气的浓度与原平衡不同
2BaO(s)+O2(g)达到平衡。下列哪些改变可使平衡移动,且新平衡时氧气的浓度与原平衡不同 | A.保持体积和温度不变,充入一定量的氧气 | B.保持温度不变,缩小容器的体积 |
| C.保持体积不变,升高温度 | D.保持体积和温度不变,加入BaO2 |
您最近一年使用:0次
2017-10-22更新
|
351次组卷
|
6卷引用:河南省八市2017-2018学年高二上学期第一次质量检测化学试题
名校
9 . 下列说法中,能说明化学平衡一定向逆反应方向移动的是
A.N2O4(g) 2NO2(g),改变某一条件后,气体颜色变浅 2NO2(g),改变某一条件后,气体颜色变浅 |
B.N2(g)+3H2(g) 2NH3(g),改变某一条件后,NH3的体积分数减少 2NH3(g),改变某一条件后,NH3的体积分数减少 |
C.H2(g)+I2(g) 2HI(g),单位时间内消耗H2和HI的物质的量之比等于1∶2 2HI(g),单位时间内消耗H2和HI的物质的量之比等于1∶2 |
D.2SO2(g)+O2(g) 2SO3(g),恒温恒压条件下,充入He 2SO3(g),恒温恒压条件下,充入He |
您最近一年使用:0次
名校
10 . —定条件下,在容积为10L的密闭容器中,将2molX和1molY进行如下反应:2X(g)+Y(g) Z(s),经1min达到平衡生成0.3mol的Z,下列说法正确的是
Z(s),经1min达到平衡生成0.3mol的Z,下列说法正确的是
 Z(s),经1min达到平衡生成0.3mol的Z,下列说法正确的是
Z(s),经1min达到平衡生成0.3mol的Z,下列说法正确的是| A.1min内,用Z表示平均反应速率为0.03mol·L-1·min-1 |
| B.将容器容积变为20L,Z的新平衡浓度将等于原平衡浓度的一半 |
| C.当X的体积分数不变时,则说明该反应达到平衡状态 |
| D.若温度和体积不变,往容器内增加1molX,Y的转化率将增大 |
您最近一年使用:0次
2017-10-11更新
|
412次组卷
|
2卷引用:安徽省六安市第一中学2017-2018学年高二9月月考化学试题



