名校
1 . 下列事实能用勒夏特列原理来解释的是
A. 被氧化为 被氧化为 ,往往需要使用催化剂: ,往往需要使用催化剂: |
B.500℃温度比室温更有利于合成氨反应:  |
C. 、 、 、 、 平衡混合气体加压后颜色加深: 平衡混合气体加压后颜色加深: |
D.实验室采用排饱和食盐水的方法收集氯气: |
您最近半年使用:0次
名校
解题方法
2 . 氟碳铈矿(主要成分为 )是提取稀土化合物、冶炼铈的重要矿物原料,以氟碳铈矿为原料提取铈的工艺流程如图:
)是提取稀土化合物、冶炼铈的重要矿物原料,以氟碳铈矿为原料提取铈的工艺流程如图:

(1) 中
中 的化合价为
的化合价为___________ ;氧化焙烧时不能使用陶瓷容器的原因是产物 会腐蚀
会腐蚀 生成
生成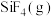 ,该反应的化学方程式为
,该反应的化学方程式为___________ 。
(2)氧化焙烧后的产物之一为 ,则酸浸时发生反应的离子方程式为
,则酸浸时发生反应的离子方程式为___________ 。
(3)操作I的名称为___________ ;有机物 能将
能将 从水溶液中提取出来,该过程可表示为
从水溶液中提取出来,该过程可表示为 。向
。向 中加入稀硫酸能获得较纯的含
中加入稀硫酸能获得较纯的含 水溶液,从平衡移动角度解释其原因
水溶液,从平衡移动角度解释其原因___________ 。
(4)写出向 悬浊液中通入氧气得到产品
悬浊液中通入氧气得到产品 的化学方程式
的化学方程式___________ 。
 )是提取稀土化合物、冶炼铈的重要矿物原料,以氟碳铈矿为原料提取铈的工艺流程如图:
)是提取稀土化合物、冶炼铈的重要矿物原料,以氟碳铈矿为原料提取铈的工艺流程如图:
(1)
 中
中 的化合价为
的化合价为 会腐蚀
会腐蚀 生成
生成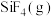 ,该反应的化学方程式为
,该反应的化学方程式为(2)氧化焙烧后的产物之一为
 ,则酸浸时发生反应的离子方程式为
,则酸浸时发生反应的离子方程式为(3)操作I的名称为
 能将
能将 从水溶液中提取出来,该过程可表示为
从水溶液中提取出来,该过程可表示为 。向
。向 中加入稀硫酸能获得较纯的含
中加入稀硫酸能获得较纯的含 水溶液,从平衡移动角度解释其原因
水溶液,从平衡移动角度解释其原因(4)写出向
 悬浊液中通入氧气得到产品
悬浊液中通入氧气得到产品 的化学方程式
的化学方程式
您最近半年使用:0次
名校
3 . 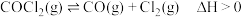 .当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加
.当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加 的浓度 ④减压 ⑤恒压通入惰性气体 ⑥加催化剂,能提高
的浓度 ④减压 ⑤恒压通入惰性气体 ⑥加催化剂,能提高 转化率的是
转化率的是
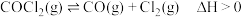 .当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加
.当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加 的浓度 ④减压 ⑤恒压通入惰性气体 ⑥加催化剂,能提高
的浓度 ④减压 ⑤恒压通入惰性气体 ⑥加催化剂,能提高 转化率的是
转化率的是| A.①②④ | B.③⑤⑥ | C.②③⑤ | D.①④⑤ |
您最近半年使用:0次
名校
4 . 根据下列实验操作与现象所得出的结论正确的是
| 选项 | 实验操作与现象 | 结论 |
| A | 向Fe(NO3)2溶液中滴入硫酸酸化的H2O2溶液,溶液由浅绿色变为黄色 | 氧化性:H2O2>>Fe2+ |
| B | 向4mL0.1mol/LK2CrO4溶液中缓慢滴加1molL稀硫酸,溶液由黄色变为橙色 | 增大c(H+)有利于 转化为 转化为 |
| C | 等体积pH=2的HX和HY两种酸溶液分别与足量的锌粒反应,用排水法收集气体,HX溶液放出的氢气多且反应速率快 | 证明HX的酸性比HY强 |
| D | 室温下,向浓度均为0.05mol/L的NaI和NaCl的混合溶液中滴加少量AgNO3溶液,有黄色沉淀生成 | Ksp(AgI)>Ksp(AgCI) |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
5 . 下列事实不能用勒夏特列原理(化学平衡移动原理)解释的是
| A.合成氨时,选定温度为400~500℃,而不是常温 |
| B.人体血液的pH稳定在7.4±0.05范围内 |
| C.氯气在水中的溶解度大于在饱和食盐水中的溶解度 |
| D.生活中,可用热的纯碱溶液除油污 |
您最近半年使用:0次
2024-01-18更新
|
78次组卷
|
3卷引用:四川省雅安市多校联考2023-2024学年高二上学期12月月考化学试题
名校
6 . 下列变化不能用勒夏特列原理解释的是
| A.开启可乐瓶盖后,马上泛起大量泡沫 |
B. 溶液加热蒸干最终得不到 溶液加热蒸干最终得不到 固体 固体 |
C.合成氨工厂通常加入过量的 ,以提高 ,以提高 的转化率 的转化率 |
D.缩小平衡体系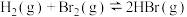 的体积,体系颜色变深 的体积,体系颜色变深 |
您最近半年使用:0次
名校
7 . 下列事实可用勒夏特列原理解释的是
A.光照新制氯水,一段时间后溶液 减小 减小 |
B. 比室温更有利于工业合成氨的反应 比室温更有利于工业合成氨的反应 |
C.由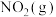 和 和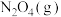 组成的平衡体系,加压后颜色变深 组成的平衡体系,加压后颜色变深 |
D.向盛有双氧水的试管中加入少量 ,立即产生大量气泡 ,立即产生大量气泡 |
您最近半年使用:0次
名校
解题方法
8 . 探究甲醇对丙烷制丙烯的影响。丙烷制烯烃过程主要发生的反应有
ⅰ.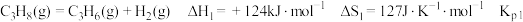
ⅱ.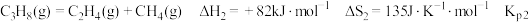
ⅲ.
已知: 为用气体分压表示的平衡常数,分压=物质的量分数×总压。在
为用气体分压表示的平衡常数,分压=物质的量分数×总压。在 下,丙烷单独进料时,平衡体系中各组分的体积分数
下,丙烷单独进料时,平衡体系中各组分的体积分数 见下表。
见下表。
(1)比较反应自发进行(∆G=∆H-T∆S<0)的最低温度,反应ⅰ_____ 反应 ⅱ(填“>”或“<”)。
(2)①从初始投料到达到平衡,反应 ⅰ、ⅱ、ⅲ 的丙烷消耗的平均速率从大到小的顺序为:_____ 。
②平衡体系中检测不到 ,可认为存在反应:
,可认为存在反应: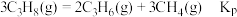 ,下列相关说法正确的是
,下列相关说法正确的是_____ (填标号)。
a.
b.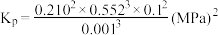
c.使用催化剂,可提高丙烯的平衡产率
d.平衡后再通入少量丙烷,可提高丙烯的体积分数
③由表中数据推算:丙烯选择性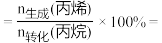
_____ (列出计算式)。
(3)丙烷甲醇共进料时,还发生反应:ⅳ.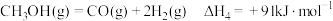 ,在
,在 下,平衡体系中各组分体积分数与进料比的关系如图所示。
下,平衡体系中各组分体积分数与进料比的关系如图所示。
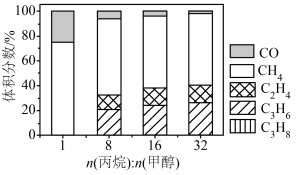
①进料比n(丙烷):n(甲醇) 时,体系总反应:
时,体系总反应: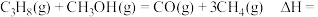
______  。
。
②随着甲醇投料增加,平衡体系中丙烯的体积分数降低的原因是______ 。
ⅰ.
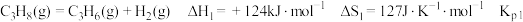
ⅱ.
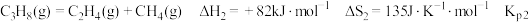
ⅲ.

已知:
 为用气体分压表示的平衡常数,分压=物质的量分数×总压。在
为用气体分压表示的平衡常数,分压=物质的量分数×总压。在 下,丙烷单独进料时,平衡体系中各组分的体积分数
下,丙烷单独进料时,平衡体系中各组分的体积分数 见下表。
见下表。| 物质 | 丙烯 | 乙烯 | 甲烷 | 丙烷 | 氢气 |
| 体积分数(%) | 21 | 23.7 | 55.2 | 0.1 | 0 |
(1)比较反应自发进行(∆G=∆H-T∆S<0)的最低温度,反应ⅰ
(2)①从初始投料到达到平衡,反应 ⅰ、ⅱ、ⅲ 的丙烷消耗的平均速率从大到小的顺序为:
②平衡体系中检测不到
 ,可认为存在反应:
,可认为存在反应: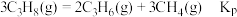 ,下列相关说法正确的是
,下列相关说法正确的是a.

b.
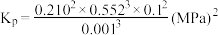
c.使用催化剂,可提高丙烯的平衡产率
d.平衡后再通入少量丙烷,可提高丙烯的体积分数
③由表中数据推算:丙烯选择性
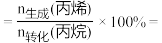
(3)丙烷甲醇共进料时,还发生反应:ⅳ.
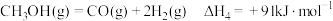 ,在
,在 下,平衡体系中各组分体积分数与进料比的关系如图所示。
下,平衡体系中各组分体积分数与进料比的关系如图所示。
①进料比n(丙烷):n(甲醇)
 时,体系总反应:
时,体系总反应: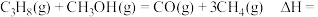
 。
。②随着甲醇投料增加,平衡体系中丙烯的体积分数降低的原因是
您最近半年使用:0次
名校
9 . 在373K时,把0.5molN2O4气体通入体积为5L 的恒容密闭容器中,发生反应: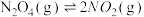 立即出现红棕色。在60秒时,体系已达平衡,此时容器内压强为开始时的1.6倍。下列说法正确的是
立即出现红棕色。在60秒时,体系已达平衡,此时容器内压强为开始时的1.6倍。下列说法正确的是
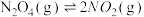 立即出现红棕色。在60秒时,体系已达平衡,此时容器内压强为开始时的1.6倍。下列说法正确的是
立即出现红棕色。在60秒时,体系已达平衡,此时容器内压强为开始时的1.6倍。下列说法正确的是| A.前60秒,以N2O4的浓度变化表示的平均反应速率为0.01mol/(L·s) |
B.在 60秒时,  物质的量为0.2mol 物质的量为0.2mol |
| C.在平衡时体系内含N2O4的物质的量为0.2mol |
| D.60秒时,再充入一定量N2O4则可提高N2O4的转化率 |
您最近半年使用:0次
名校
10 . 下列实验中,能达到实验目的是
| A | B | C | D |
| 实现将反应Cu+2Fe3+=Cu2++2Fe2+的化学能转变为电能 | 验证非金属性强弱:Cl>C>Si | 证明:相同温度下的溶解度:Mg(OH)2>Fe(OH)3 | 探究浓度对化学平衡的影响规律: +H2O +H2O 2 2 +2H+ +2H+ |
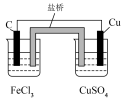 |  | 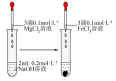 | 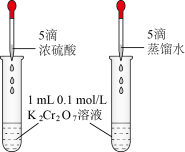 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次



