名校
1 . 可逆反应A(?)+aB(g) C(g)+2D(g)(a为正整数) ΔH。反应过程中,当其他条件不变时,C的百分含量与温度(T)和压强(p)的关系如图所示。下列说法正确的是
C(g)+2D(g)(a为正整数) ΔH。反应过程中,当其他条件不变时,C的百分含量与温度(T)和压强(p)的关系如图所示。下列说法正确的是
 C(g)+2D(g)(a为正整数) ΔH。反应过程中,当其他条件不变时,C的百分含量与温度(T)和压强(p)的关系如图所示。下列说法正确的是
C(g)+2D(g)(a为正整数) ΔH。反应过程中,当其他条件不变时,C的百分含量与温度(T)和压强(p)的关系如图所示。下列说法正确的是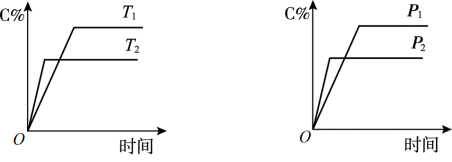
| A.T1>T2、p1>p2 | B.a不可能大于3 |
| C.该反应的ΔH>0 | D.反应过程中,始终有v(C)=2v(D) |
您最近半年使用:0次
2024-03-26更新
|
101次组卷
|
2卷引用:安徽省滁州市明光市第三中学2023-2024学年高二上学期11月月考化学试题
名校
2 . NH3是世界上产量最多的无机化合物之一,具有广泛的用途。工业上通常用N2和H2来合成NH3。
(1)已知:i.H2的燃烧热为-285.8kJ•mol-1
ii.N2(g)+O2(g)=2NO(g)△H=+180kJ•mol-1
iii.4NH3(g)+5O2(g)=4NO(g)+6H2O(l)△H=-1170kJ•mol-1
工业合成氨的热化学方程式为______ ;在恒温恒容密闭容器中进行合成氨的反应,下列不能说明反应已达到平衡状态的是______ 。
A.容器内N2、H2、NH3的浓度之比为1:3:2
B.N2百分含量保持不变
C.容器内压强保持不变
D.混合气体的密度保持不变
(2)某科研小组研究:在其他条件不变的情况下,不同温度时,固定氮气的投入量,起始氢气的物质的量与平衡时氨气的百分含量关系如图:______ T2(填“>,<或=”)。
②a、b、c、d四点所处的平衡状态中,反应物N2的转化率最高的是:_______ 。
③合成氨工业中,为提高氨气的平衡产率,除适当控制反应的温度和压强外,还可采取的措施是______ 。
(3)恒温下,向一个4L的恒容密闭容器中充入1.8molN2和4.2molH2,反应过程中对NH3的浓度进行检测。
①20min后,反应达平衡,氨气的浓度为0.3mol•L-1,用N2表示的平均反应速率为______ mol•L-1•min-1。且此时,混合气体的总压强为p,则该反应的化学平衡常数Kp=_______ (对于气相反应,用某组分B的平衡压强p(B)代替物质的量浓度c(B)也可表示平衡常数,记作Kp,如p(B)=p•x(B),p为平衡总压强,x(B)为平衡系统中B的物质的量分数)。
②若维持容器的体积不变,温度不变,向原平衡体系中再加入1.8molN2和4.2molH2,再次达平衡后,氨气的浓度_______ 0.6mol/L(填“大于”或“小于”或“等于”)。
(1)已知:i.H2的燃烧热为-285.8kJ•mol-1
ii.N2(g)+O2(g)=2NO(g)△H=+180kJ•mol-1
iii.4NH3(g)+5O2(g)=4NO(g)+6H2O(l)△H=-1170kJ•mol-1
工业合成氨的热化学方程式为
A.容器内N2、H2、NH3的浓度之比为1:3:2
B.N2百分含量保持不变
C.容器内压强保持不变
D.混合气体的密度保持不变
(2)某科研小组研究:在其他条件不变的情况下,不同温度时,固定氮气的投入量,起始氢气的物质的量与平衡时氨气的百分含量关系如图:

②a、b、c、d四点所处的平衡状态中,反应物N2的转化率最高的是:
③合成氨工业中,为提高氨气的平衡产率,除适当控制反应的温度和压强外,还可采取的措施是
(3)恒温下,向一个4L的恒容密闭容器中充入1.8molN2和4.2molH2,反应过程中对NH3的浓度进行检测。
①20min后,反应达平衡,氨气的浓度为0.3mol•L-1,用N2表示的平均反应速率为
②若维持容器的体积不变,温度不变,向原平衡体系中再加入1.8molN2和4.2molH2,再次达平衡后,氨气的浓度
您最近半年使用:0次
名校
解题方法
3 . 在恒温恒压下,向密闭容器中充入4mol  和2mol
和2mol  ,发生如下反应:
,发生如下反应: △H<0,2min后,反应达到平衡,生成
△H<0,2min后,反应达到平衡,生成 为1.4mol,同时放出热量Q kJ。则下列分析正确的是
为1.4mol,同时放出热量Q kJ。则下列分析正确的是
 和2mol
和2mol  ,发生如下反应:
,发生如下反应: △H<0,2min后,反应达到平衡,生成
△H<0,2min后,反应达到平衡,生成 为1.4mol,同时放出热量Q kJ。则下列分析正确的是
为1.4mol,同时放出热量Q kJ。则下列分析正确的是A.若反应开始时容器体积为2L,则 |
B.若把条件“恒温恒压”改为“恒压恒容”,则平衡后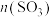 大于1.4mol 大于1.4mol |
C.2min后,向容器中再通入一定量的 气体,重新达到平衡时 气体,重新达到平衡时 的含量变小 的含量变小 |
| D.若把条件“恒温恒压”改为“恒温恒容”,则平衡时放出热量小于Q kJ |
您最近半年使用:0次
解题方法
4 . 在一密闭容器中反应aA(g)  bB(g)达平衡后,测得c(B)为1mol/L。如保持温度不变,将容器体积变为原来的2倍,重新达到新的平衡时,c(B)变为0.4mol/L,则下列说法正确的是
bB(g)达平衡后,测得c(B)为1mol/L。如保持温度不变,将容器体积变为原来的2倍,重新达到新的平衡时,c(B)变为0.4mol/L,则下列说法正确的是
 bB(g)达平衡后,测得c(B)为1mol/L。如保持温度不变,将容器体积变为原来的2倍,重新达到新的平衡时,c(B)变为0.4mol/L,则下列说法正确的是
bB(g)达平衡后,测得c(B)为1mol/L。如保持温度不变,将容器体积变为原来的2倍,重新达到新的平衡时,c(B)变为0.4mol/L,则下列说法正确的是| A.平衡向正反应方向移动 | B.物质A的转化率增大 |
| C.物质B的质量分数增大 | D.a>b |
您最近半年使用:0次
名校
5 . 一定量的气体在密闭容器中发生反应:xA(g)+yB(g)⇌zC(g),平衡时测得A的浓度为1.0mol/L,保持温度不变,将容器的容积扩大到原来的2倍,达到新平衡后,测得A的浓度为0.60mol/L。下列有关判断不正确的是
| A.平衡向正反应方向移动 | B.x+y>z |
| C.物质B的转化率减小 | D.物质C的质量分数减小 |
您最近半年使用:0次
2022-09-15更新
|
360次组卷
|
4卷引用:北京市第四十四中学2021-2022学年高二上学期期中考试化学试题
6 . 在一密闭容器中,反应aA(g) bB(g)达平衡后,保持温度不变,将容器体积压缩至一半,当达到新的平衡时,B的浓度是原来的180%,则正确的是
bB(g)达平衡后,保持温度不变,将容器体积压缩至一半,当达到新的平衡时,B的浓度是原来的180%,则正确的是
 bB(g)达平衡后,保持温度不变,将容器体积压缩至一半,当达到新的平衡时,B的浓度是原来的180%,则正确的是
bB(g)达平衡后,保持温度不变,将容器体积压缩至一半,当达到新的平衡时,B的浓度是原来的180%,则正确的是| A.a>b | B.物质A的转化率增大了 |
| C.物质A的质量分数减小了 | D.平衡向逆反应方向移动了 |
您最近半年使用:0次
2022-09-15更新
|
156次组卷
|
3卷引用:北京市第一五六中学2021-2022学年高二上学期期中考试化学试题
名校
解题方法
7 . 科学家研究了乙醇催化合成乙酸乙酯的新方法: ,在常压下反应,冷凝收集,测得常温下液态收集物中主要产物的质量分数如图所示。关于该方法,下列推测不合理的是
,在常压下反应,冷凝收集,测得常温下液态收集物中主要产物的质量分数如图所示。关于该方法,下列推测不合理的是
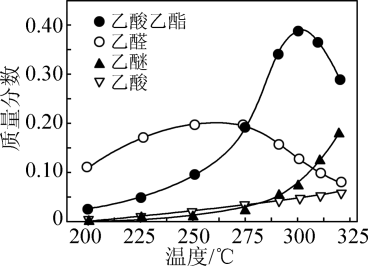
 ,在常压下反应,冷凝收集,测得常温下液态收集物中主要产物的质量分数如图所示。关于该方法,下列推测不合理的是
,在常压下反应,冷凝收集,测得常温下液态收集物中主要产物的质量分数如图所示。关于该方法,下列推测不合理的是
| A.反应温度不宜超过300℃ |
| B.适当减小体系压强,有利于提高乙醇平衡转化率 |
| C.在催化剂作用下,乙酸是反应历程中的中间产物 |
| D.提高催化剂的活性和选择性,减少乙醚、乙烯等副产物是工艺的关键 |
您最近半年使用:0次
名校
解题方法
8 . 在一密闭容器中发生如下反应:aA(g)+bB(g) xC(g) ΔH=Q kJ/mol,某化学小组根据不同条件下的实验数据作出如图所示曲线( C%表示平衡混合气中产物C的百分含量,T表示温度,p表示压强,t表示反应时间)。其他条件不变时,下列分析正确的是
xC(g) ΔH=Q kJ/mol,某化学小组根据不同条件下的实验数据作出如图所示曲线( C%表示平衡混合气中产物C的百分含量,T表示温度,p表示压强,t表示反应时间)。其他条件不变时,下列分析正确的是
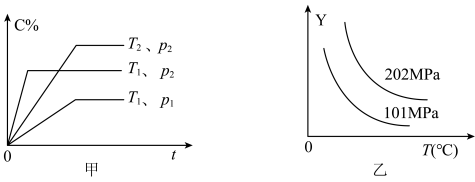
 xC(g) ΔH=Q kJ/mol,某化学小组根据不同条件下的实验数据作出如图所示曲线( C%表示平衡混合气中产物C的百分含量,T表示温度,p表示压强,t表示反应时间)。其他条件不变时,下列分析正确的是
xC(g) ΔH=Q kJ/mol,某化学小组根据不同条件下的实验数据作出如图所示曲线( C%表示平衡混合气中产物C的百分含量,T表示温度,p表示压强,t表示反应时间)。其他条件不变时,下列分析正确的是
| A.p2>p1,a+b<x |
| B.T2>T1,Q<0 |
| C.Y可能表示平衡混合气的平均相对分子质量 |
| D.升高温度,A的转化率增大 |
您最近半年使用:0次
9 . 向相同容积的甲、乙两容器中分别充入4 mol SO2和2 mol O2,发生如下反应:2SO2(g)+O2(g)=2SO3(g) △H<0。若甲容器保持恒温恒容,乙容器保持恒温恒压,分别达到平衡。乙容器中平衡时生成SO3为1.6 mol,同时放出热量Q kJ。下列说法正确的是
| A.平衡时,反应放出的热量:甲>乙 |
| B.平衡时,O2的质量:甲<乙 |
| C.乙容器若把条件“恒温恒压”改为“恒压绝热”,则平衡后n(SO2)大于2.4 mol |
| D.平衡时,向乙容器中再通入一定量的SO3气体,重新达到平衡时,SO2的百分含量升高 |
您最近半年使用:0次
2023高三·全国·专题练习
10 . 肼( )是一种应用广泛的化工原料。工业上先合成氨气:
)是一种应用广泛的化工原料。工业上先合成氨气:
 ,再进一步制备肼。完成下列填空:
,再进一步制备肼。完成下列填空:
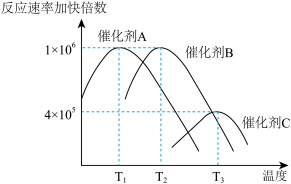
(1)合成氨需要选择合适的催化剂,分别选用A、B、C三种催化剂进行试验,所得结果如图所示(其他条件相同),则生产中适宜选择的催化剂是___________ (填“A”或“B”或“C”)
(2)一定条件下,对在密闭容器中进行的合成氨反应达平衡后,其他条件不变时,若同时压缩容器的体积和升高温度达新平衡后,与原平衡相比,请将有关物理量的变化的情况填入下表中(填“增大”、“减小”或“无法确定”)
(3)氨主要用于生产化肥和硝酸。“十三五”期间,预计我国合成氨产量将保持稳中略增。下图是不同温度和不同压强下,反应达到平衡后,混合物中 含量(体积%)的变化情况,已知初始时
含量(体积%)的变化情况,已知初始时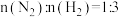 。判断
。判断 、
、 压强的大小关系,
压强的大小关系,
___________  (选填“>”、“<”或“=”)。
(选填“>”、“<”或“=”)。
 )是一种应用广泛的化工原料。工业上先合成氨气:
)是一种应用广泛的化工原料。工业上先合成氨气:
 ,再进一步制备肼。完成下列填空:
,再进一步制备肼。完成下列填空:(1)合成氨需要选择合适的催化剂,分别选用A、B、C三种催化剂进行试验,所得结果如图所示(其他条件相同),则生产中适宜选择的催化剂是

(2)一定条件下,对在密闭容器中进行的合成氨反应达平衡后,其他条件不变时,若同时压缩容器的体积和升高温度达新平衡后,与原平衡相比,请将有关物理量的变化的情况填入下表中(填“增大”、“减小”或“无法确定”)
| 反应速率 | 平衡常数K | |
| 变化情况 |
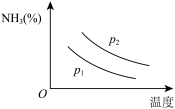
(3)氨主要用于生产化肥和硝酸。“十三五”期间,预计我国合成氨产量将保持稳中略增。下图是不同温度和不同压强下,反应达到平衡后,混合物中
 含量(体积%)的变化情况,已知初始时
含量(体积%)的变化情况,已知初始时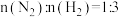 。判断
。判断 、
、 压强的大小关系,
压强的大小关系,
 (选填“>”、“<”或“=”)。
(选填“>”、“<”或“=”)。
您最近半年使用:0次



