名校
解题方法
1 . 在容积恒为1 L的密闭容器中通入一定量N2O4,发生反应 △H>0。假设温度不变,体系中各组分浓度随时间(t)的变化如下表。下列说法错误的是
△H>0。假设温度不变,体系中各组分浓度随时间(t)的变化如下表。下列说法错误的是
 △H>0。假设温度不变,体系中各组分浓度随时间(t)的变化如下表。下列说法错误的是
△H>0。假设温度不变,体系中各组分浓度随时间(t)的变化如下表。下列说法错误的是| t/s | 0 | 20 | 40 | 60 | 80 |
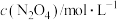 | 0.100 | 0.062 | 0.048 | 0.040 | 0.040 |
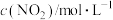 | 0 | 0.076 | 0.104 | 0.120 | 0.120 |
A.0~40 s,N2O4的平均反应速率为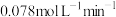 |
| B.80 s时,再充入N2O4、NO2各0.12 mol,平衡移动 |
| C.升高温度,反应的化学平衡常数值增大 |
| D.若压缩容器,达新平衡后,混合气颜色比原平衡时深 |
您最近一年使用:0次
2021-09-12更新
|
402次组卷
|
2卷引用:山东省济南市历城第二中学2021-2022学年(2022届)高三上学期开学考试(B)化学试题
名校
2 . 一定量的 与足量的碳在体积可变的恒压密闭容器中反应:
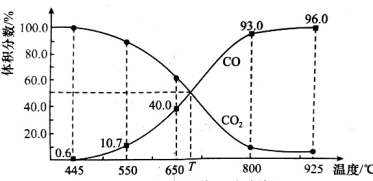
与足量的碳在体积可变的恒压密闭容器中反应: 。平衡时,体系中气体体积分数与温度的关系如图所示,已知:气体分压
。平衡时,体系中气体体积分数与温度的关系如图所示,已知:气体分压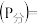 气体总压
气体总压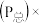 体积分数。下列说法不正确的是
体积分数。下列说法不正确的是
 与足量的碳在体积可变的恒压密闭容器中反应:
与足量的碳在体积可变的恒压密闭容器中反应: 。平衡时,体系中气体体积分数与温度的关系如图所示,已知:气体分压
。平衡时,体系中气体体积分数与温度的关系如图所示,已知:气体分压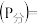 气体总压
气体总压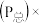 体积分数。下列说法不正确的是
体积分数。下列说法不正确的是
A.该反应 , , |
B.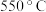 时,若充入惰性气体, 时,若充入惰性气体, , , 均减小,平衡向正反应方向移动 均减小,平衡向正反应方向移动 |
C. 时,若充入等体积的 时,若充入等体积的 和 和 ,平衡向逆反应方向移动 ,平衡向逆反应方向移动 |
D.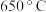 时,反应达平衡后 时,反应达平衡后 的转化率为 的转化率为 |
您最近一年使用:0次
2021-09-10更新
|
263次组卷
|
3卷引用:山西省运城市2022届高三上学期入学摸底测试化学试题
名校
3 . 如图表示合成氨反应过程中的能量变化。关于合成氨反应 ,下列说法
,下列说法不 正确的是
 ,下列说法
,下列说法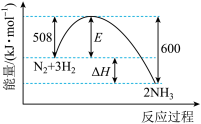
A.升高温度有利于提高 的平衡转化率 的平衡转化率 |
B.提高 与 与 的投料比可增大 的投料比可增大 的转化率 的转化率 |
C.增大压强能提高 的反应速率和转化率 的反应速率和转化率 |
| D.使用催化剂能缩短该反应到达平衡的时间 |
您最近一年使用:0次
2022-11-18更新
|
305次组卷
|
8卷引用:江苏省扬州市2020-2021学年高二下学期期末考试化学(选修)试题
江苏省扬州市2020-2021学年高二下学期期末考试化学(选修)试题(已下线)第二章 第三节化学平衡(第2课时 化学平衡的影响因素)(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版选修4)(原卷版)(已下线)第2章 化学反应速率和化学平衡(提分小卷)-【单元测试】2021-2022学年高二化学尖子生选拔卷(人教版选修4)云南昆明师范专科学校附属中学2021-2022学年高二上学期期中考试化学试题(已下线)2.4 化学反应的调控(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)(已下线)第二章 化学反应速率与化学平衡(B卷·能力提升练)【单元测试】2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修1)江苏省马坝高级中学2022-2023学年高二上学期期中考试化学试题江苏省南京市五校(秦淮中学,溧水二高,江浦文昌)2023-2024学年高二下学期期中联考化学试题
4 . 下列有关化学平衡的说法正确的是
A.对于恒温密闭容器中进行的反应N2(g)+3H2(g) 2NH3(g),若N2的体积分数保持不变,则一定说明反应已达到平衡状态 2NH3(g),若N2的体积分数保持不变,则一定说明反应已达到平衡状态 |
| B.一定温度下,将2.0g CaCO3固体置于1L恒容密闭容器中充分反应后,c(CO2)=0.0125mol/L,若保持温度不变,将容器体积扩大至2L,达到新平衡后c(CO2)=0.01mol/L |
C.反应:CH4(g)+H2O(g) CO(g)+3H2(g) ∆H>0,在其它条件不变的情况下,升高温度、减小容器体积、增大水蒸气的浓度均能提高CH4的平衡转化率 CO(g)+3H2(g) ∆H>0,在其它条件不变的情况下,升高温度、减小容器体积、增大水蒸气的浓度均能提高CH4的平衡转化率 |
D.一定温度下,恒容密闭容器中充入一定量NO2发生反应:2NO2 N2O4达到平衡后,再向容器中充入一定量的NO2并达到新的平衡,则NO2体积分数先增大后减小,但比原平衡小 N2O4达到平衡后,再向容器中充入一定量的NO2并达到新的平衡,则NO2体积分数先增大后减小,但比原平衡小 |
您最近一年使用:0次
名校
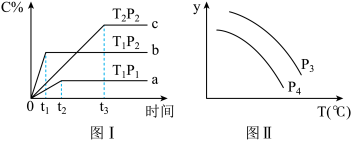
5 . 在某容积一定的密闭容器中,可逆反应:A(g)+B(g) xC(g),有图Ⅰ所示的反应曲线,试判断对图Ⅱ的说法中正确的是(T表示温度,p表示压强,C%表示C的体积分数)
xC(g),有图Ⅰ所示的反应曲线,试判断对图Ⅱ的说法中正确的是(T表示温度,p表示压强,C%表示C的体积分数)
 xC(g),有图Ⅰ所示的反应曲线,试判断对图Ⅱ的说法中正确的是(T表示温度,p表示压强,C%表示C的体积分数)
xC(g),有图Ⅰ所示的反应曲线,试判断对图Ⅱ的说法中正确的是(T表示温度,p表示压强,C%表示C的体积分数)
| A.p3>p4,y轴表示A的物质的量 |
| B.p3<p4,y轴表示C的体积分数 |
| C.p3<p4,y轴表示混合气体的密度 |
| D.p3>p4,y轴表示混合气体的平均相对分子质量 |
您最近一年使用:0次
2022-09-17更新
|
517次组卷
|
8卷引用:山西省吕梁市2020-2021学年高二上学期期末考试化学试题
6 . 当今,世界多国相继规划了碳达峰、碳中和的时间节点,我国提出争取2030年“碳达峰”,2060年“碳中和”。因此,研发二氧化碳利用技术、降低空气中二氧化碳含量成为热点。
(1)甲醇是一种可再生能源,由CO2制备甲醇的过程可能涉及的反应如下:
反应Ⅰ:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1=-49.58kJ·mol-1
CH3OH(g)+H2O(g) △H1=-49.58kJ·mol-1
反应Ⅱ:CO2(g)+H2(g) CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2
反应Ⅲ:CO(g)+2H2(g) CH3OH(g) △H3=-90.77kJ·mol-1
CH3OH(g) △H3=-90.77kJ·mol-1
则:反应Ⅱ的ΔH2=___________ kJ·mol-1
(2)若反应II在一绝热恒容密闭容器中进行,下面能说明反应已达到平衡状态的是___________ ;
a、v(CO)=v(H2O) b、总压强不变
c、平衡常数不变 d、容器内n(CO2)/n(H2O)的值保持不变
(3)①对于反应Ⅰ,不同温度对CO2的转化率及催化剂的催化效率影响如图所示,下列有关说法正确的是___________ 。
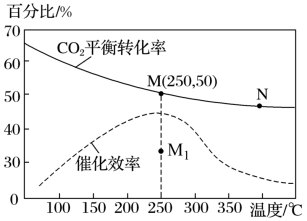
A.其他条件不变,若不使用催化剂,则250℃时CO2的平衡转化率可能位于M1
B.温度低于250℃时,随温度升高甲醇的平衡产率增大
C.M点时平衡常数比N点时平衡常数大
D.若反应在较低的温度下进行,可以提高CO2的平衡转化率,符合勒沙特列原理
②若在2L密闭容器中充入3molH2和1molCO2只发生反应Ⅰ,250℃时反应的平衡常数K=___________ L2/mol2,若要进一步提高甲醇的体积分数,可采取的措施有___________ (写一条即可)。
(4)我国科学家研究Li-CO2电池,取得了重大科研成果。回答下列问题:
①Li-CO2电池中,研究表明该电池反应产物为碳酸锂和单质碳,正极CO2电还原后与锂离子结合形成碳酸锂按以下4个步骤进行,写出步骤Ⅲ的离子方程式。
I、2CO2+2e‑=C2O
II、C2O =CO2+CO
=CO2+CO
III、___________
IV、 +2Li+=Li2CO3
+2Li+=Li2CO3
②研究表明,在电解质水溶液中,CO2气体可被电化学还原。写出CO2在碱性介质中电还原为正丙醇(CH3CH2CH2OH)的电极反应方程式为___________ 。
(1)甲醇是一种可再生能源,由CO2制备甲醇的过程可能涉及的反应如下:
反应Ⅰ:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H1=-49.58kJ·mol-1
CH3OH(g)+H2O(g) △H1=-49.58kJ·mol-1反应Ⅱ:CO2(g)+H2(g)
 CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2反应Ⅲ:CO(g)+2H2(g)
 CH3OH(g) △H3=-90.77kJ·mol-1
CH3OH(g) △H3=-90.77kJ·mol-1则:反应Ⅱ的ΔH2=
(2)若反应II在一绝热恒容密闭容器中进行,下面能说明反应已达到平衡状态的是
a、v(CO)=v(H2O) b、总压强不变
c、平衡常数不变 d、容器内n(CO2)/n(H2O)的值保持不变
(3)①对于反应Ⅰ,不同温度对CO2的转化率及催化剂的催化效率影响如图所示,下列有关说法正确的是

A.其他条件不变,若不使用催化剂,则250℃时CO2的平衡转化率可能位于M1
B.温度低于250℃时,随温度升高甲醇的平衡产率增大
C.M点时平衡常数比N点时平衡常数大
D.若反应在较低的温度下进行,可以提高CO2的平衡转化率,符合勒沙特列原理
②若在2L密闭容器中充入3molH2和1molCO2只发生反应Ⅰ,250℃时反应的平衡常数K=
(4)我国科学家研究Li-CO2电池,取得了重大科研成果。回答下列问题:
①Li-CO2电池中,研究表明该电池反应产物为碳酸锂和单质碳,正极CO2电还原后与锂离子结合形成碳酸锂按以下4个步骤进行,写出步骤Ⅲ的离子方程式。
I、2CO2+2e‑=C2O

II、C2O
 =CO2+CO
=CO2+CO
III、
IV、
 +2Li+=Li2CO3
+2Li+=Li2CO3②研究表明,在电解质水溶液中,CO2气体可被电化学还原。写出CO2在碱性介质中电还原为正丙醇(CH3CH2CH2OH)的电极反应方程式为
您最近一年使用:0次
名校
解题方法
7 . 通过下列反应合成CO和CH4,可实现CO2的再转化:
①CO2(g)+4H2(g) CH4(g)+2H2O(g) △H<0
CH4(g)+2H2O(g) △H<0
②CO2(g)+H2(g) CO(g)+H2O(g) △H>0
CO(g)+H2O(g) △H>0
在密闭容器中通入3 mol的H2和1 mol的CO2,分别在压强为1 MPa 和10 MPa下进行反应。实验中对平衡体系的三种物质(CO2、CO、CH4)进行分析,其中温度对CO和CH4在三种物质中的体积分数影响如图所示。
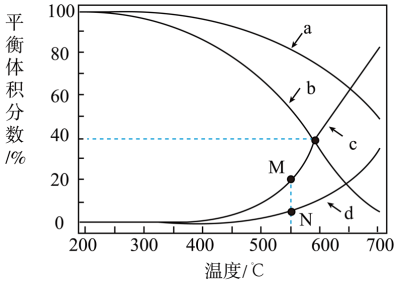
下列说法不正确的是
①CO2(g)+4H2(g)
 CH4(g)+2H2O(g) △H<0
CH4(g)+2H2O(g) △H<0②CO2(g)+H2(g)
 CO(g)+H2O(g) △H>0
CO(g)+H2O(g) △H>0在密闭容器中通入3 mol的H2和1 mol的CO2,分别在压强为1 MPa 和10 MPa下进行反应。实验中对平衡体系的三种物质(CO2、CO、CH4)进行分析,其中温度对CO和CH4在三种物质中的体积分数影响如图所示。

下列说法不正确的是
| A.曲线a表示10 MPa条件下CH4的体积分数随温度的变化 |
| B.曲线a、d交点纵坐标可能为40% |
| C.550°C时M点位于N点上方是由于压强降低时,平衡①逆向移动导致平衡②正向移动 |
| D.由曲线b、c的交点可计算该温度下反应②的平衡常数为2.4 |
您最近一年使用:0次
2022-09-02更新
|
214次组卷
|
2卷引用:江苏省南师附中、天一中学、海安中学、海门中学四校2021-2022学年高三12月联考化学试题
名校
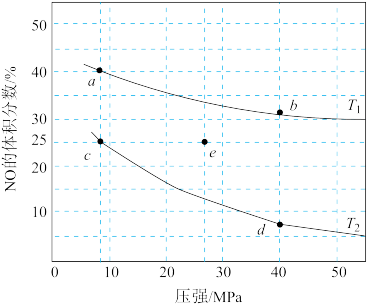
8 . 反应2NO(g) + 2CO(g) N2(g) + 2CO2(g)+Q(Q>0)可用于消除汽车尾气中的有害气体。在密闭容器中充入4 mol NO和5 mol CO,平衡时NO的体积分数随温度、压强的变化关系如图。下列说法错误的是
N2(g) + 2CO2(g)+Q(Q>0)可用于消除汽车尾气中的有害气体。在密闭容器中充入4 mol NO和5 mol CO,平衡时NO的体积分数随温度、压强的变化关系如图。下列说法错误的是
 N2(g) + 2CO2(g)+Q(Q>0)可用于消除汽车尾气中的有害气体。在密闭容器中充入4 mol NO和5 mol CO,平衡时NO的体积分数随温度、压强的变化关系如图。下列说法错误的是
N2(g) + 2CO2(g)+Q(Q>0)可用于消除汽车尾气中的有害气体。在密闭容器中充入4 mol NO和5 mol CO,平衡时NO的体积分数随温度、压强的变化关系如图。下列说法错误的是
| A.温度:T1>T2 |
| B.a点达到平衡所需时间比c点短 |
| C.c点NO的平衡转化率:50% |
| D.若在e点对反应容器升温的同时扩大体积使体系压强减小,重新达到的平衡状态可能是图中的c点 |
您最近一年使用:0次
2022-10-13更新
|
305次组卷
|
10卷引用:黑龙江省嫩江市高级中学2021届高三上学期模拟考试化学试题
黑龙江省嫩江市高级中学2021届高三上学期模拟考试化学试题北京市朝阳区2020届高三学业水平等级性考试练习化学试题(已下线)北京市2019-2020学年高三各区一模化学考试分类汇编 选择题:化学平衡 离子平衡上海市复旦大学附属中学2021届高三上学期第一次教学质量检测化学试题上海行知中学2022-2023学年高三上学期第一次月考化学试题甘肃省张掖市高台县第一中学2022-2023学年高二上学期期中考试化学试题河南省鹤壁市高中2022-2023学年高三上学期第三次模拟考试化学试题河南省汝州市第一高级中学2022-2023学年高二上学期11月月考化学试题甘肃省张掖市高台县第一中学2023-2024学年高二上学期开学(暑假学习效果)检测化学试题河南省南阳市第一中学校2023-2024学年高二上学期第一次月考化学试题
9 . 某温度下,在甲、乙、丙三个恒容密闭容器中进行反应CO2(g)+H2(g) CO(g)+H2O(g),起始时投料如下表,达到平衡状态时K=4.
CO(g)+H2O(g),起始时投料如下表,达到平衡状态时K=4.
下列有关说法正确的是
 CO(g)+H2O(g),起始时投料如下表,达到平衡状态时K=4.
CO(g)+H2O(g),起始时投料如下表,达到平衡状态时K=4. 起始浓度(mol·L-1) | 甲 | 乙 | 丙 |
c(CO2) | 0.01 | 0.02 | 0.02 |
c(H2) | 0.01 | 0.01 | 0.02 |
A.反应CO(g)+H2O(g) CO2(g)+H2(g)的平衡常数为0.25 CO2(g)+H2(g)的平衡常数为0.25 |
| B.平衡的时间:t丙>t乙>t甲 |
| C.平衡时,CO2的转化率:乙<甲<丙 |
| D.平衡时,H2的转化率:甲=丙<乙 |
您最近一年使用:0次
2021-05-13更新
|
186次组卷
|
2卷引用:山东省淄博市沂源县第二中学2020-2021学年高二下学期期中考试化学试题
10 . 如图,I是恒压密闭容器,II是恒容密闭容器。其它条件相同时,在I、II中分别加入2molX和2molY,起始时容器体积均为VL,发生如下反应并达到平衡(X、Y状态未知):2X(?)+Y(?) aZ(g)。此时I中X、Y、Z的物质的量之比为1∶3∶2,则下列说法一定正确的是
aZ(g)。此时I中X、Y、Z的物质的量之比为1∶3∶2,则下列说法一定正确的是

 aZ(g)。此时I中X、Y、Z的物质的量之比为1∶3∶2,则下列说法一定正确的是
aZ(g)。此时I中X、Y、Z的物质的量之比为1∶3∶2,则下列说法一定正确的是
| A.若X、Y均为气态,则平衡时气体平均摩尔质量:II>I |
| B.a值为2 |
| C.若X为固态,Y为气态,则I、II中从起始到平衡所需时间相同 |
| D.平衡时I容器的体积小于VL |
您最近一年使用:0次



