名校
解题方法
1 . 我国的能源消费结构以燃煤为主,将煤气化可减少环境污染。
(1)将煤与水蒸气在恒容密闭容器中反应,可制合成气。制备过程中的主要反应(a)、(b)的 (
( 为以分压表示的平衡常数)与温度T的关系如图所示。回答下列问题:
为以分压表示的平衡常数)与温度T的关系如图所示。回答下列问题:
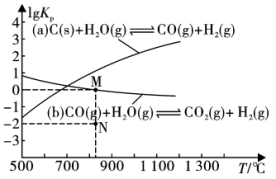
①下列能说明反应(a)
 已达到平衡状态的是
已达到平衡状态的是___________ (填字母)。
A. B.混合气体的总压强不再变化
B.混合气体的总压强不再变化
C. 不再变化 D.混合气体的密度不再变化
不再变化 D.混合气体的密度不再变化
②在容积为1L的密闭容器中充入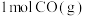 、
、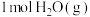 只发生反应(b),反应5 min到达图中M点,请计算0~5 min内,平均反应速率
只发生反应(b),反应5 min到达图中M点,请计算0~5 min内,平均反应速率
___________  ;已知反应速率
;已知反应速率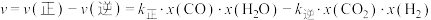 ,
, 、
、 分别为正、逆反应速率常数,x为物质的量分数,N处的
分别为正、逆反应速率常数,x为物质的量分数,N处的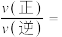
___________ 。
(2)一种新型煤气化燃烧集成制氢发生的主要反应如下:
Ⅰ.

Ⅱ.

Ⅲ.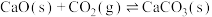

Ⅳ.
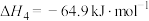
副反应:
Ⅴ.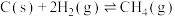
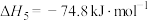
Ⅵ.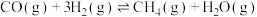
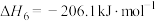
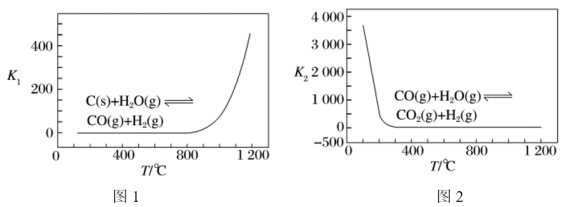
已知反应Ⅰ、Ⅱ的平衡常数 ,
, 随温度的变化如图1、图2所示。
随温度的变化如图1、图2所示。
①由反应Ⅴ和反应Ⅵ可知,
___________  ;反应Ⅰ的
;反应Ⅰ的
___________ (填“>”或“<”)0。
②温度小于800℃时, ,原因是
,原因是___________ 。
③为提高反应Ⅱ中CO的转化率,可采取的措施是___________ (写一条)。
④ 时,向密闭容器中充入
时,向密闭容器中充入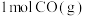 和
和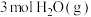 ,只发生反应Ⅱ,此时该反应的平衡常数
,只发生反应Ⅱ,此时该反应的平衡常数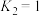 ,CO的平衡转化率为
,CO的平衡转化率为___________ 。
⑤从环境保护角度分析,该制氢工艺中设计反应Ⅲ的优点是___________ 。
(1)将煤与水蒸气在恒容密闭容器中反应,可制合成气。制备过程中的主要反应(a)、(b)的
 (
( 为以分压表示的平衡常数)与温度T的关系如图所示。回答下列问题:
为以分压表示的平衡常数)与温度T的关系如图所示。回答下列问题:
①下列能说明反应(a)

 已达到平衡状态的是
已达到平衡状态的是A.
 B.混合气体的总压强不再变化
B.混合气体的总压强不再变化C.
 不再变化 D.混合气体的密度不再变化
不再变化 D.混合气体的密度不再变化②在容积为1L的密闭容器中充入
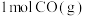 、
、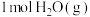 只发生反应(b),反应5 min到达图中M点,请计算0~5 min内,平均反应速率
只发生反应(b),反应5 min到达图中M点,请计算0~5 min内,平均反应速率
 ;已知反应速率
;已知反应速率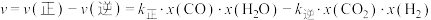 ,
, 、
、 分别为正、逆反应速率常数,x为物质的量分数,N处的
分别为正、逆反应速率常数,x为物质的量分数,N处的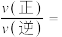
(2)一种新型煤气化燃烧集成制氢发生的主要反应如下:
Ⅰ.


Ⅱ.


Ⅲ.
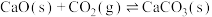

Ⅳ.

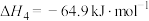
副反应:
Ⅴ.
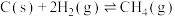
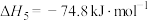
Ⅵ.
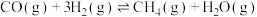
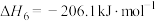
已知反应Ⅰ、Ⅱ的平衡常数
 ,
, 随温度的变化如图1、图2所示。
随温度的变化如图1、图2所示。
①由反应Ⅴ和反应Ⅵ可知,

 ;反应Ⅰ的
;反应Ⅰ的
②温度小于800℃时,
 ,原因是
,原因是③为提高反应Ⅱ中CO的转化率,可采取的措施是
④
 时,向密闭容器中充入
时,向密闭容器中充入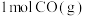 和
和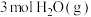 ,只发生反应Ⅱ,此时该反应的平衡常数
,只发生反应Ⅱ,此时该反应的平衡常数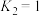 ,CO的平衡转化率为
,CO的平衡转化率为⑤从环境保护角度分析,该制氢工艺中设计反应Ⅲ的优点是
您最近一年使用:0次
名校
2 . 煤的气化是一种重要的制氢途径。一定条件下,在容积固定的密闭容器中发生反应: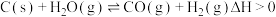 。下列说法不正确的是
。下列说法不正确的是
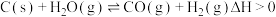 。下列说法不正确的是
。下列说法不正确的是| A.该反应的逆方向高温自发 |
| B.将炭块粉碎,可提高反应速率 |
C.增大 的量,可以增大活化分子浓度 的量,可以增大活化分子浓度 |
D.升高温度,可以提高 的转化率 的转化率 |
您最近一年使用:0次
2024-02-16更新
|
142次组卷
|
3卷引用:湖北省襄阳市第一中学2023-2024学年高二下学期3月月考化学试题
名校
3 . 下列过程属于熵减的是
| A.-10℃的液态水自动结冰成为固态 | B.常温下,H2O2分解成H2O和O2 |
| C.NaCl晶体溶于水 | D.一盒粉笔无序散落一地 |
您最近一年使用:0次
名校
4 . 合成氨反应为:N2(g)+3H2(g)  2NH3(g) ΔH= -92.4kJ·mol-1,下列说法正确的是
2NH3(g) ΔH= -92.4kJ·mol-1,下列说法正确的是
 2NH3(g) ΔH= -92.4kJ·mol-1,下列说法正确的是
2NH3(g) ΔH= -92.4kJ·mol-1,下列说法正确的是| A.合成氨反应在任何温度下都能自发 | B.将混合气体进行循环利用符合绿色化学思想 |
| C.合成氨实际生产中选择高压和低温 | D.将氨液化分离,可促进平衡正移,加快反应速率 |
您最近一年使用:0次
5 . 判断化学反应进行的方向是一个比较复杂的问题。下列有关说法正确的是
A.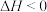 或 或 的反应一定能自发进行 的反应一定能自发进行 |
B.反应 能否自发进行与温度有关 能否自发进行与温度有关 |
C. 在不同状态时的熵值: 在不同状态时的熵值: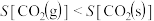 |
D.反应 的 的 |
您最近一年使用:0次
2024-02-13更新
|
68次组卷
|
2卷引用:安徽省六安市裕安区新安中学2023-2024学年高二下学期第一次月考化学试题
名校
解题方法
6 . 下列说法正确的是
A.常温下,2H2O 2H2↑+O2↑,所以常温下水的分解反应是自发反应 2H2↑+O2↑,所以常温下水的分解反应是自发反应 |
| B.化学平衡常数大于1×105的反应一定能迅速发生 |
| C.能自发进行的反应一定能实际发生 |
| D.ΔH<0且ΔS<0的反应不一定能自发进行 |
您最近一年使用:0次
名校
7 . 甲醇是重要的化工原料,利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,相关反应的热化学方程式为:
ⅰ.CO(g)+2H2(g) CH3OH(g) ΔH=a kJ/mol;
CH3OH(g) ΔH=a kJ/mol;
ⅱ.CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=b kJ/mol;
CH3OH(g)+H2O(g) ΔH=b kJ/mol;
ⅲ.CO2(g)+H2(g) CO(g)+H2O(g) ΔH=−c kJ/mol。
CO(g)+H2O(g) ΔH=−c kJ/mol。
回答下列问题:
(1)a=______ (用b、c表示),已知反应ⅱ在一定条件下可自发进行,则b______ (填“>”“<”或“=”)0。
(2)在一定温度下,向体积为1L的恒容密闭容器中通入等物质的量的CO2与H2,在催化剂的作用下仅发生反应ⅲ。该反应达到平衡时,其他条件不变,通入CO2时,则v(正)___ (填“>”“<”或“=”)v(逆),平衡常数_______ (填“变大”“变小”或“不变”)。
(3)一定温度下,向体积为2L的恒容密闭容器中通入CO、H2、CH3OH,发生反应ⅰ,其中X、Y的物质的量与时间的关系如图所示,反应进行1min时三种物质的体积分数均相等。
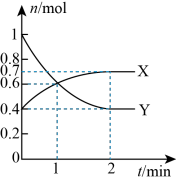
①Y为_____ (填化学式)。
②0~1min时v(CO)为_____ mol/(L·min)。
③该温度下,该反应的平衡常数Kc=______ 。
(4)工业上以 和
和 为原料可制备合成气(CO、H2),已知
为原料可制备合成气(CO、H2),已知 、
、 、CO的燃烧热分别为890 kJ/mol、285kJ/mol、283kJ/mol,则反应
、CO的燃烧热分别为890 kJ/mol、285kJ/mol、283kJ/mol,则反应

______ 。若该反应的 ,
, (
(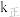 、
、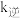 为速率常数,只与温度有关),平衡后降低温度,则
为速率常数,只与温度有关),平衡后降低温度,则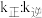
_______ (填“增大”“不变”或“减小”)。
(5)化学反应常伴随热效应。某些反应(如中和反应)的热量变化,其数值Q可通过量热装置测量反应前后体系温度变化,用公式Q=cm△T计算获得。
①热量的测定:取0.5000mol/LNaOH溶液和0.5500mol/L盐酸各50mL进行反应,测得反应前后体系的温度值(℃)分别为T0、T1,(c和 分别取
分别取 和
和 ,忽略水以外各物质吸收的热量,后同),则该实验测得中和热
,忽略水以外各物质吸收的热量,后同),则该实验测得中和热
_____  。
。
②下列操作会使所测得的焓变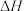 偏小的是
偏小的是______ 。
a.用等物质的量浓度的醋酸代替盐酸实验 b.量热装置绝热效果欠佳 c.NaOH溶液量多了
ⅰ.CO(g)+2H2(g)
 CH3OH(g) ΔH=a kJ/mol;
CH3OH(g) ΔH=a kJ/mol;ⅱ.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH=b kJ/mol;
CH3OH(g)+H2O(g) ΔH=b kJ/mol;ⅲ.CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH=−c kJ/mol。
CO(g)+H2O(g) ΔH=−c kJ/mol。回答下列问题:
(1)a=
(2)在一定温度下,向体积为1L的恒容密闭容器中通入等物质的量的CO2与H2,在催化剂的作用下仅发生反应ⅲ。该反应达到平衡时,其他条件不变,通入CO2时,则v(正)
(3)一定温度下,向体积为2L的恒容密闭容器中通入CO、H2、CH3OH,发生反应ⅰ,其中X、Y的物质的量与时间的关系如图所示,反应进行1min时三种物质的体积分数均相等。
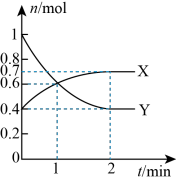
①Y为
②0~1min时v(CO)为
③该温度下,该反应的平衡常数Kc=
(4)工业上以
 和
和 为原料可制备合成气(CO、H2),已知
为原料可制备合成气(CO、H2),已知 、
、 、CO的燃烧热分别为890 kJ/mol、285kJ/mol、283kJ/mol,则反应
、CO的燃烧热分别为890 kJ/mol、285kJ/mol、283kJ/mol,则反应

 ,
, (
(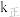 、
、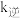 为速率常数,只与温度有关),平衡后降低温度,则
为速率常数,只与温度有关),平衡后降低温度,则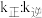
(5)化学反应常伴随热效应。某些反应(如中和反应)的热量变化,其数值Q可通过量热装置测量反应前后体系温度变化,用公式Q=cm△T计算获得。
①热量的测定:取0.5000mol/LNaOH溶液和0.5500mol/L盐酸各50mL进行反应,测得反应前后体系的温度值(℃)分别为T0、T1,(c和
 分别取
分别取 和
和 ,忽略水以外各物质吸收的热量,后同),则该实验测得中和热
,忽略水以外各物质吸收的热量,后同),则该实验测得中和热
 。
。②下列操作会使所测得的焓变
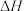 偏小的是
偏小的是a.用等物质的量浓度的醋酸代替盐酸实验 b.量热装置绝热效果欠佳 c.NaOH溶液量多了
您最近一年使用:0次
名校
8 . 氯化硫酰(SO2Cl2)常用作氧化剂,它是一种无色液体,熔点:-54.1℃,沸点:69.1℃,可用干燥的SO2和Cl2在活性炭作催化剂的条件下制取:SO2(g)+Cl2(g)⇌SO2Cl2(l) ΔH=-97.3kJ·mol-1。下列有关SO2Cl2制取的说法正确的是
| A.该反应在高温下能自发进行 |
| B.使用活性炭作催化剂能缩短该反应达平衡的时间 |
| C.化学平衡发生移动,该反应平衡常数必发生变化 |
| D.使SO2Cl2液化从平衡体系中分离,能加快正反应速率,增大Cl2转化率 |
您最近一年使用:0次
名校
解题方法
9 . 下列说法正确的是
| A.非自发进行的反应在任何条件下都不能发生 |
B. |
C.反应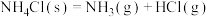 在室温下不可自发进行,则该反应的 在室温下不可自发进行,则该反应的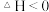 |
| D.“酒香不怕巷子深”“花香四溢”都体现了生活中的“熵增”原理 |
您最近一年使用:0次
10 . Ⅰ.铁触媒催化合成氨经历下图所示①至⑥步基元反应(从状态Ⅰ至状态Ⅶ):
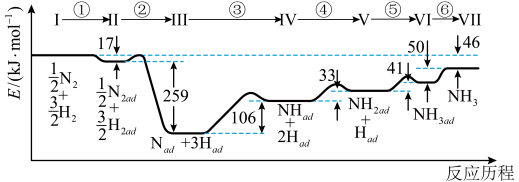
上图中“ad”表示吸附在催化剂表面的物质。
回答下列问题:
(1)根据上图计算合成氨反应的焓变:N2(g)+3H2(g) 2NH3(g) ΔH=
2NH3(g) ΔH=___________ 。
(2)上述反应的ΔS___ 0(填“>”“<”或“=”)。已知:反应N2(g)+3H2(g) 2NH3(g)的|ΔS|=199J/(mol·K),则下列温度中,合成氨反应能自发进行的是
2NH3(g)的|ΔS|=199J/(mol·K),则下列温度中,合成氨反应能自发进行的是____ (填标号)。
A.25℃ B.125℃ C.225℃ D.325℃
Ⅱ.高锰酸钾是一种常用的消毒剂和氧化剂。回答下列问题:
实验(一):电解法制备KMnO4。
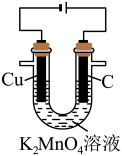
以石墨、铜为电极,电解K2MnO4溶液制备KMnO4溶液,装置如图所示。
(3)电解过程中,Cu极附近电解质溶液的pH______ (填“升高”“降低”或“不变”)。
(4)铜极、石墨极能否互换并简述理由:___________ 。
实验(二):探究K2FeO4和KMnO4氧化性强弱。装置如图所示。

关闭开关K,观察到左烧杯中紫红色溶液变为浅黄色,右烧杯中无色溶液变为紫红色。
(5)关闭K,盐桥中_______ (填离子符号)向左烧杯迁移。
(6)石墨极的电极反应式为_______ 。实验结论是氧化性:
___  (填>”“<”或“=”)。
(填>”“<”或“=”)。

上图中“ad”表示吸附在催化剂表面的物质。
回答下列问题:
(1)根据上图计算合成氨反应的焓变:N2(g)+3H2(g)
 2NH3(g) ΔH=
2NH3(g) ΔH=(2)上述反应的ΔS
 2NH3(g)的|ΔS|=199J/(mol·K),则下列温度中,合成氨反应能自发进行的是
2NH3(g)的|ΔS|=199J/(mol·K),则下列温度中,合成氨反应能自发进行的是A.25℃ B.125℃ C.225℃ D.325℃
Ⅱ.高锰酸钾是一种常用的消毒剂和氧化剂。回答下列问题:
实验(一):电解法制备KMnO4。

以石墨、铜为电极,电解K2MnO4溶液制备KMnO4溶液,装置如图所示。
(3)电解过程中,Cu极附近电解质溶液的pH
(4)铜极、石墨极能否互换并简述理由:
实验(二):探究K2FeO4和KMnO4氧化性强弱。装置如图所示。

关闭开关K,观察到左烧杯中紫红色溶液变为浅黄色,右烧杯中无色溶液变为紫红色。
(5)关闭K,盐桥中
(6)石墨极的电极反应式为

 (填>”“<”或“=”)。
(填>”“<”或“=”)。
您最近一年使用:0次
2024-02-02更新
|
152次组卷
|
2卷引用:湖南省长沙市长郡中学2023-2024学年高二上学期12月阶段性检测化学试题



