名校
解题方法
1 . 下列说法错误的是
A.反应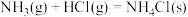 在室温下可自发进行,则该反应的 在室温下可自发进行,则该反应的 |
B.常温下,若反应 不能自发进行,则该反应的 不能自发进行,则该反应的 |
C.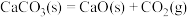 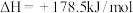 ,该反应高温才能自发 ,该反应高温才能自发 |
D.一定温度下,反应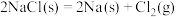 的 的 , , |
您最近一年使用:0次
2024-01-21更新
|
75次组卷
|
2卷引用:云南省昆明市云南师范大学附属中学2023-2024学年高二上学期12月月考化学试题
名校
2 . 依据图示关系,下列说法正确的是
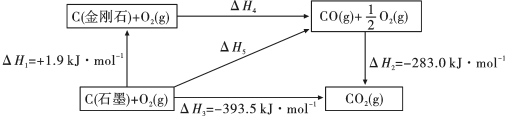

A.石墨的燃烧热 |
B.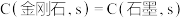  ,则金刚石比石墨稳定 ,则金刚石比石墨稳定 |
C. 石墨或 石墨或 金刚石分别完全燃烧,金刚石放出热量多 金刚石分别完全燃烧,金刚石放出热量多 |
D.反应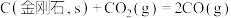 在任何温度下均能自发进行 在任何温度下均能自发进行 |
您最近一年使用:0次
名校
3 . 下列有关说法正确的是
A.恒容绝热容器中,发生反应 ,当压强不变时反应达到平衡状态 ,当压强不变时反应达到平衡状态 |
B.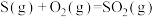  , ,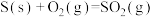  ,则 ,则 |
C.室温下,反应 不能自发进行,说明该反应的 不能自发进行,说明该反应的 |
D.一定温度下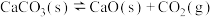 ,压缩容器体积,再次达到新平衡后, ,压缩容器体积,再次达到新平衡后, 浓度增大 浓度增大 |
您最近一年使用:0次
名校
解题方法
4 . 中华传统文化蕴含着丰富的化学知识,下列说法错误的是
| A.“青蒿一握,以水二升渍,绞取汁”,这种提取青蒿素的方法属于物理变化 |
| B.“投泥泼水愈光明,烁玉流金见精悍”,所指高温时碳与水蒸气的反应为放热反应 |
| C.“爝火燃回春浩浩,烘炉照破夜沉沉”,这里的能量变化是化学能转化为热能和光能 |
| D.“千锤万凿出深山,烈火焚烧若等闲”,涉及的反应在高温下自发进行 |
您最近一年使用:0次
名校
解题方法
5 . 硫酸有着广泛的用途。硫酸工业在国民经济中占有重要地位。
(1)实验室可用铜与浓硫酸反应制备少量 :
: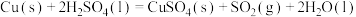
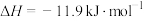 。判断该反应的自发性并说明理由
。判断该反应的自发性并说明理由___________ 。
(2)我国古籍记载了硫酸的制备方法—“炼石胆( )取精华法”。
)取精华法”。
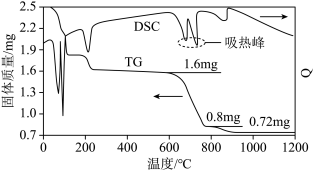
①借助现代仪器分析,该制备过程中 分解的TG曲线(热重曲线,即受热分解过程中固体质量变化曲线)及DSC曲线(反映体系热量变化情况,数值已省略)如图所示。700℃左右有两个吸热峰,则此时分解生成的氧化物有
分解的TG曲线(热重曲线,即受热分解过程中固体质量变化曲线)及DSC曲线(反映体系热量变化情况,数值已省略)如图所示。700℃左右有两个吸热峰,则此时分解生成的氧化物有___________ 、___________ (填化学式)和 。
。
②已知下列热化学方程式:
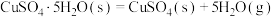



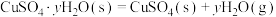

则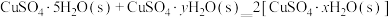 的△H=
的△H=__________  。
。
(3)接触法制硫酸的关键反应为 的催化氧化:
的催化氧化: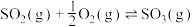
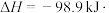

①为寻求固定投料比下不同反应阶段的最佳生产温度,绘制不同转化率( )下反应速率(数值已略去)与温度的关系如图,下列说法正确的是
)下反应速率(数值已略去)与温度的关系如图,下列说法正确的是__________ 。
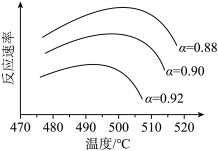
A.温度越高,反应速率越大 B.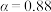 的曲线代表平衡转化率
的曲线代表平衡转化率
C. 越大,反应速率最大值对应温度越低 D.可根据不同
越大,反应速率最大值对应温度越低 D.可根据不同 下的最大速率,选择最佳生产温度
下的最大速率,选择最佳生产温度
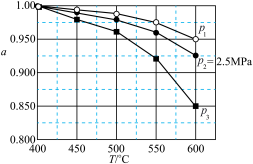
②固定投料比,在压强分别为0.5MPa、2.5MPa和5.0MPa下,得到 的平衡转化率随温度的变化如图所示。则在5.0MPa、550℃时,该反应的平衡转化率=
的平衡转化率随温度的变化如图所示。则在5.0MPa、550℃时,该反应的平衡转化率=__________ 。
③对于气体参与的反应,可用气体组分(B)的平衡压强p(B)代替该气体物质的量浓度c(B)来表示平衡常数 。设
。设 的平衡分压为p,
的平衡分压为p, 的平衡转化率为
的平衡转化率为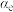 ,则上述催化氧化反应
,则上述催化氧化反应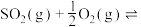
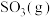 的
的
_____________ (用含p和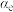 的代数式表示)。
的代数式表示)。
(1)实验室可用铜与浓硫酸反应制备少量
 :
: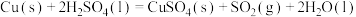
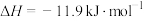 。判断该反应的自发性并说明理由
。判断该反应的自发性并说明理由(2)我国古籍记载了硫酸的制备方法—“炼石胆(
 )取精华法”。
)取精华法”。①借助现代仪器分析,该制备过程中
 分解的TG曲线(热重曲线,即受热分解过程中固体质量变化曲线)及DSC曲线(反映体系热量变化情况,数值已省略)如图所示。700℃左右有两个吸热峰,则此时分解生成的氧化物有
分解的TG曲线(热重曲线,即受热分解过程中固体质量变化曲线)及DSC曲线(反映体系热量变化情况,数值已省略)如图所示。700℃左右有两个吸热峰,则此时分解生成的氧化物有 。
。
②已知下列热化学方程式:
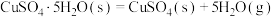



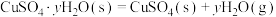

则
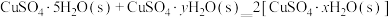 的△H=
的△H= 。
。(3)接触法制硫酸的关键反应为
 的催化氧化:
的催化氧化: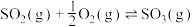
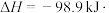

①为寻求固定投料比下不同反应阶段的最佳生产温度,绘制不同转化率(
 )下反应速率(数值已略去)与温度的关系如图,下列说法正确的是
)下反应速率(数值已略去)与温度的关系如图,下列说法正确的是
A.温度越高,反应速率越大 B.
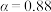 的曲线代表平衡转化率
的曲线代表平衡转化率C.
 越大,反应速率最大值对应温度越低 D.可根据不同
越大,反应速率最大值对应温度越低 D.可根据不同 下的最大速率,选择最佳生产温度
下的最大速率,选择最佳生产温度②固定投料比,在压强分别为0.5MPa、2.5MPa和5.0MPa下,得到
 的平衡转化率随温度的变化如图所示。则在5.0MPa、550℃时,该反应的平衡转化率=
的平衡转化率随温度的变化如图所示。则在5.0MPa、550℃时,该反应的平衡转化率=
③对于气体参与的反应,可用气体组分(B)的平衡压强p(B)代替该气体物质的量浓度c(B)来表示平衡常数
 。设
。设 的平衡分压为p,
的平衡分压为p, 的平衡转化率为
的平衡转化率为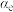 ,则上述催化氧化反应
,则上述催化氧化反应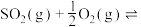
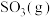 的
的
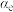 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
名校
6 . 甲烷是重要的气体燃料和化工原料,由 制取合成气(
制取合成气( 、
、 )的反应原理为
)的反应原理为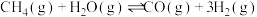
 。回答下列问题:
。回答下列问题:
(1)若生成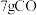 ,吸收热量akJ,相关化学键的键能(断裂1mol化学键所吸收的能量),如表所示。
,吸收热量akJ,相关化学键的键能(断裂1mol化学键所吸收的能量),如表所示。
①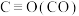 的键能为
的键能为___________ (用含a的式子表示) 。
。
②当体系温度等于TK时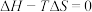 ,温度大于T时
,温度大于T时
___________ (填“>”“<”或“=”)0。
③在一定温度下,恒容密闭容器中发生上述反应,下列状态表示反应一定达到平衡状态的有___________ (填标号)。
A.
B.气体压强不再变化
C.单位时间每消耗 ,同时产生
,同时产生
D. 与
与 的物质的量之比为
的物质的量之比为
(2)在体积为 的恒容密闭容器中通入
的恒容密闭容器中通入 和
和 ,在不同条件下发生反应
,在不同条件下发生反应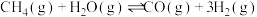 ,测得平衡时
,测得平衡时 的体积分数与温度、压强的关系如图所示。
的体积分数与温度、压强的关系如图所示。

①X表示___________ (填“温度”或“压强”),m、n、q点的平衡常数由大到小的顺序为___________ 。
②若q点对应的纵坐标为30,此时甲烷的转化率为___________ ,该条件下平衡常数
___________ (保留两位有效数字)。
 制取合成气(
制取合成气( 、
、 )的反应原理为
)的反应原理为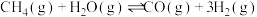
 。回答下列问题:
。回答下列问题:(1)若生成
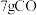 ,吸收热量akJ,相关化学键的键能(断裂1mol化学键所吸收的能量),如表所示。
,吸收热量akJ,相关化学键的键能(断裂1mol化学键所吸收的能量),如表所示。| 化学键 |  |  |  |
键能 | 414 | 436 | 467 |
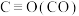 的键能为
的键能为 。
。②当体系温度等于TK时
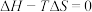 ,温度大于T时
,温度大于T时
③在一定温度下,恒容密闭容器中发生上述反应,下列状态表示反应一定达到平衡状态的有
A.

B.气体压强不再变化
C.单位时间每消耗
 ,同时产生
,同时产生
D.
 与
与 的物质的量之比为
的物质的量之比为
(2)在体积为
 的恒容密闭容器中通入
的恒容密闭容器中通入 和
和 ,在不同条件下发生反应
,在不同条件下发生反应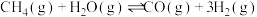 ,测得平衡时
,测得平衡时 的体积分数与温度、压强的关系如图所示。
的体积分数与温度、压强的关系如图所示。
①X表示
②若q点对应的纵坐标为30,此时甲烷的转化率为

您最近一年使用:0次
名校
7 . 按要求回答下列问题。
(1)汽车尾气是城市主要空气污染物,汽车内燃机工作时发生反应N2(g)+O2(g)⇌2NO(g)是导致汽车尾气中含有NO的原因之一、已知H2可以催化还原NO达到消除污染的目的。
N2(g)+O2(g)⇌2NO(g) △H=+180.5kJ∙mol-1
2H2(g)+O2(g)⇌2H2O(l) △H=-571.6kJ∙mol-1
写出H2(g)与NO(g)反应生成N2(g)和H2O(l)的热化学方程式是___________ ,判断该反应自发进行的条件:___________ 。(填“高温自发”或“低温自发”)
(2)已知H2S为二元弱酸,欲使0.1mol•L-1的H2S溶液中 的比值变大,下列措施可行的是
的比值变大,下列措施可行的是___________
a.加入H2O b.通入少量H2S c.通入少量HCl d.加入少量NaOH固体
(3)有下列物质:①Zn②KAl(SO4)2∙12H2O③Ba(OH)2④乙醇⑤冰醋酸⑥盐酸⑦Cu(NO3)2溶液⑧熔融态AlCl3⑨NH3∙H2O⑩熔融态CH3COONa⑪NaHCO3。其中属于能导电的电解质的是___________ (填编号)属于弱电解质的是___________ (填编号)
(4)若向0.1mol∙L-1的弱碱MOH溶液中逐滴加入0.1mol∙L-1的弱酸HB至恰好反应,溶液的导电性变化规律是___________ (填“逐渐变强”、“逐渐变弱”、“先变强后变弱”、“先变弱后变强”和“几乎不变”)
(1)汽车尾气是城市主要空气污染物,汽车内燃机工作时发生反应N2(g)+O2(g)⇌2NO(g)是导致汽车尾气中含有NO的原因之一、已知H2可以催化还原NO达到消除污染的目的。
N2(g)+O2(g)⇌2NO(g) △H=+180.5kJ∙mol-1
2H2(g)+O2(g)⇌2H2O(l) △H=-571.6kJ∙mol-1
写出H2(g)与NO(g)反应生成N2(g)和H2O(l)的热化学方程式是
(2)已知H2S为二元弱酸,欲使0.1mol•L-1的H2S溶液中
 的比值变大,下列措施可行的是
的比值变大,下列措施可行的是a.加入H2O b.通入少量H2S c.通入少量HCl d.加入少量NaOH固体
(3)有下列物质:①Zn②KAl(SO4)2∙12H2O③Ba(OH)2④乙醇⑤冰醋酸⑥盐酸⑦Cu(NO3)2溶液⑧熔融态AlCl3⑨NH3∙H2O⑩熔融态CH3COONa⑪NaHCO3。其中属于能导电的电解质的是
(4)若向0.1mol∙L-1的弱碱MOH溶液中逐滴加入0.1mol∙L-1的弱酸HB至恰好反应,溶液的导电性变化规律是
您最近一年使用:0次
名校
解题方法
8 . 下列叙述中,正确的是
A.甲烷的标准燃烧热为 ,则甲烷燃烧的热化学方程式可表示为: ,则甲烷燃烧的热化学方程式可表示为: |
B.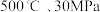 下,将 下,将 和 和 置于密闭的容器中充分反应生成 置于密闭的容器中充分反应生成 ,放热 ,放热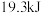 ,其热化学方程式为: ,其热化学方程式为: |
C.相同条件下, 氢原子所具有的能量小于 氢原子所具有的能量小于 氢分子所具有的能量 氢分子所具有的能量 |
D.常温下,反应 不能自发进行,则该反应的 不能自发进行,则该反应的 |
您最近一年使用:0次
名校
9 . 下列反应及其自由能与温度的关系如下图所示:
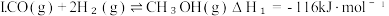
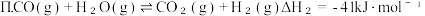
Ⅲ.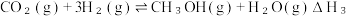
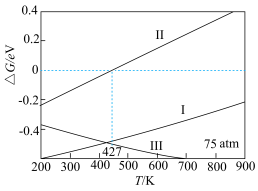
下列说法错误的是
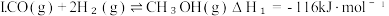
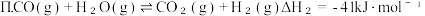
Ⅲ.
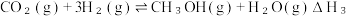

下列说法错误的是
A.反应 在 在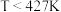 时, 能自发进行 时, 能自发进行 |
B.相同温度下, 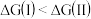 的主要原因可能是 的主要原因可能是  |
C. |
D.400K时,平衡常数 |
您最近一年使用:0次
2024-01-18更新
|
183次组卷
|
3卷引用:辽宁省沈阳市第二中学2023-2024学年高二上学期10月阶段考试化学试题
名校
解题方法
10 . 二甲醚是一种重要的清洁燃料,工业上可以通过 、合成气(主要成分是一氧化碳和氢气)制得。
、合成气(主要成分是一氧化碳和氢气)制得。
I. 分子间脱水制二甲醚
分子间脱水制二甲醚

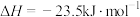 。在
。在 ℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。
℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。
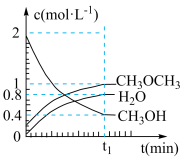
(1) 时刻反应达平衡后,其他条件不变,升高温度,平衡
时刻反应达平衡后,其他条件不变,升高温度,平衡___________ (填“向右”、“向左”或“不发生”)移动, 将
将___________ (填“增大”或“减小”)
(2)相同条件下,若改变起始浓度,某时刻各组分浓度依次为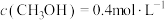 、
、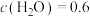
 、
、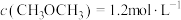 ,此时
,此时
___________  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
Ⅱ.合成气制取二甲醚的原理如下:
反应1:
反应2:
(3)500K时,在2L密闭容器中充入4
 和8
和8
 ,4min达到平衡,平衡时
,4min达到平衡,平衡时 的转化率为80%,且
的转化率为80%,且 ,则反应2中
,则反应2中 的转化率
的转化率
___________ ,反应1的平衡常数
___________ (结果需化成最简比)。
 、合成气(主要成分是一氧化碳和氢气)制得。
、合成气(主要成分是一氧化碳和氢气)制得。I.
 分子间脱水制二甲醚
分子间脱水制二甲醚
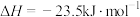 。在
。在 ℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。
℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。
(1)
 时刻反应达平衡后,其他条件不变,升高温度,平衡
时刻反应达平衡后,其他条件不变,升高温度,平衡 将
将(2)相同条件下,若改变起始浓度,某时刻各组分浓度依次为
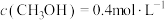 、
、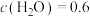
 、
、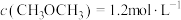 ,此时
,此时
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。Ⅱ.合成气制取二甲醚的原理如下:
反应1:

反应2:

(3)500K时,在2L密闭容器中充入4

 和8
和8
 ,4min达到平衡,平衡时
,4min达到平衡,平衡时 的转化率为80%,且
的转化率为80%,且 ,则反应2中
,则反应2中 的转化率
的转化率

您最近一年使用:0次



