名校
解题方法
1 . 在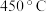 下
下 催化
催化 和
和 反应时的反应机理如下。
反应时的反应机理如下。
反应①: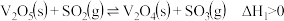
反应②: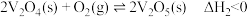 ,下列说法正确的是
,下列说法正确的是
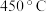 下
下 催化
催化 和
和 反应时的反应机理如下。
反应时的反应机理如下。反应①:
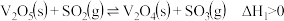
反应②:
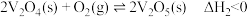 ,下列说法正确的是
,下列说法正确的是A.反应①的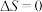 |
B. 在高温条件下能自发进行、低温条件下不能自发进行 在高温条件下能自发进行、低温条件下不能自发进行 |
C. |
D.使用 降低反应的焓变,氯碱工业使用阴离子交换膜可防止 降低反应的焓变,氯碱工业使用阴离子交换膜可防止 与 与 反应 反应 |
您最近一年使用:0次
2024-02-03更新
|
119次组卷
|
2卷引用:辽宁省葫芦岛市第一高级中学2023-2024学年高二上学期化学期末复习提升卷
名校
2 . 一定条件下,反应2N2O5(g)⇌4NO2(g)+O2(g) ΔH=+56.76kJ/mol能自发进行,下列关于该反应的说法中正确的是
| A.是熵减少的反应 |
| B.反应能自发进行的原因是熵增大效应大于能量效应 |
| C.反应在任何温度下都能自发进行 |
| D.反应能自发进行,所以反应速率一定很快 |
您最近一年使用:0次
名校
3 . 下列说法中,正确的是
| A.冰在室温下自动熔化成水,这是熵增的过程 | B.能够自发进行的反应一定是放热反应 |
| C.ΔH > 0的反应均不能自发进行 | D.能够自发进行的反应一定是熵增的过程 |
您最近一年使用:0次
2024-02-02更新
|
106次组卷
|
2卷引用:黑龙江省哈尔滨师范大学附属中学2023-2024学年高二上学期期末考试 化学试卷
4 . Ⅰ.铁触媒催化合成氨经历下图所示①至⑥步基元反应(从状态Ⅰ至状态Ⅶ):
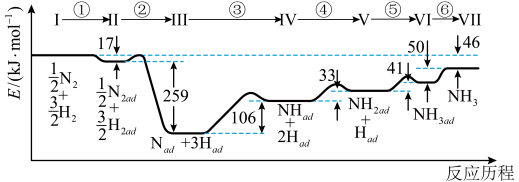
上图中“ad”表示吸附在催化剂表面的物质。
回答下列问题:
(1)根据上图计算合成氨反应的焓变:N2(g)+3H2(g) 2NH3(g) ΔH=
2NH3(g) ΔH=___________ 。
(2)上述反应的ΔS___ 0(填“>”“<”或“=”)。已知:反应N2(g)+3H2(g) 2NH3(g)的|ΔS|=199J/(mol·K),则下列温度中,合成氨反应能自发进行的是
2NH3(g)的|ΔS|=199J/(mol·K),则下列温度中,合成氨反应能自发进行的是____ (填标号)。
A.25℃ B.125℃ C.225℃ D.325℃
Ⅱ.高锰酸钾是一种常用的消毒剂和氧化剂。回答下列问题:
实验(一):电解法制备KMnO4。
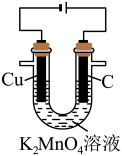
以石墨、铜为电极,电解K2MnO4溶液制备KMnO4溶液,装置如图所示。
(3)电解过程中,Cu极附近电解质溶液的pH______ (填“升高”“降低”或“不变”)。
(4)铜极、石墨极能否互换并简述理由:___________ 。
实验(二):探究K2FeO4和KMnO4氧化性强弱。装置如图所示。

关闭开关K,观察到左烧杯中紫红色溶液变为浅黄色,右烧杯中无色溶液变为紫红色。
(5)关闭K,盐桥中_______ (填离子符号)向左烧杯迁移。
(6)石墨极的电极反应式为_______ 。实验结论是氧化性:
___  (填>”“<”或“=”)。
(填>”“<”或“=”)。

上图中“ad”表示吸附在催化剂表面的物质。
回答下列问题:
(1)根据上图计算合成氨反应的焓变:N2(g)+3H2(g)
 2NH3(g) ΔH=
2NH3(g) ΔH=(2)上述反应的ΔS
 2NH3(g)的|ΔS|=199J/(mol·K),则下列温度中,合成氨反应能自发进行的是
2NH3(g)的|ΔS|=199J/(mol·K),则下列温度中,合成氨反应能自发进行的是A.25℃ B.125℃ C.225℃ D.325℃
Ⅱ.高锰酸钾是一种常用的消毒剂和氧化剂。回答下列问题:
实验(一):电解法制备KMnO4。

以石墨、铜为电极,电解K2MnO4溶液制备KMnO4溶液,装置如图所示。
(3)电解过程中,Cu极附近电解质溶液的pH
(4)铜极、石墨极能否互换并简述理由:
实验(二):探究K2FeO4和KMnO4氧化性强弱。装置如图所示。

关闭开关K,观察到左烧杯中紫红色溶液变为浅黄色,右烧杯中无色溶液变为紫红色。
(5)关闭K,盐桥中
(6)石墨极的电极反应式为

 (填>”“<”或“=”)。
(填>”“<”或“=”)。
您最近一年使用:0次
2024-02-02更新
|
153次组卷
|
2卷引用:湖南省长沙市长郡中学2023-2024学年高二上学期12月阶段性检测化学试题
名校
5 . 研究碳、氮等元素化合物的性质或转化对体会化学与生活有重要意义。
Ⅰ.以CO2和NH3为原料合成尿素总反应为:CO2 (g)+ 2NH3 (g) CO (NH2) (s) + H2O (g) ΔH该反应的具体过程分两步完成,ⅰ.CO2和NH3生成H2NCOONH4;ⅱ.H2NCOONH4分解生成尿素,反应过程能量变化如图。
CO (NH2) (s) + H2O (g) ΔH该反应的具体过程分两步完成,ⅰ.CO2和NH3生成H2NCOONH4;ⅱ.H2NCOONH4分解生成尿素,反应过程能量变化如图。
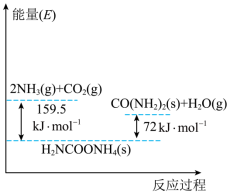
(1)总反应的
______  ,该反应在
,该反应在______ (填“高温”或“低温”或“任何条件都不”)可以自发进行。
(2)若该反应在恒容密闭容器中进行,判断该反应达到化学平衡状态的依据是________ (填字母序号)。
(3)在恒温、体积为1L的恒容装置中通入CO2和NH3各1mol 、1.5mol,达平衡时CO2的转化率为50%,平衡常数的值为_______ 。
Ⅱ.亚硝酸钠(NaNO2)是肉制品生产中常使用的一种食品添加剂,外观与食盐极为相似,具有较强毒性,误食可能造成死亡。已知常温下 Ka(HNO2)=1.75×10-4,Ka(CH3COOH)=1.8×10-5。
(4)常温下,pH=4的HNO2溶液中,由水电离出的c(H+)约为______ mol·L-1,浓度均为 0.1mol/L 的 NaNO2和 CH3COONa 的混合溶液中各离子浓度由大到小的关系为__________ 。
(5)高锰酸钾常用于亚硝酸盐的测定。欲测定某样品中NaNO2的含量,某同学设计如下实验:
①称取样品a g,加水溶解,配制成100 mL溶液。
②取25.00 mL溶液于锥形瓶中,用0.02000 mol·L-1 KMnO4标准溶液(酸性)进行滴定,反应离子方程式是: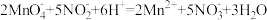 ,滴定结束后消耗KMnO4溶液VmL。
,滴定结束后消耗KMnO4溶液VmL。
进行滴定操作时无需另加指示剂,达到滴定终点时的现象是_______ ,测得该样品中NaNO2的质量分数为_______ 。(写出计算式)
Ⅰ.以CO2和NH3为原料合成尿素总反应为:CO2 (g)+ 2NH3 (g)
 CO (NH2) (s) + H2O (g) ΔH该反应的具体过程分两步完成,ⅰ.CO2和NH3生成H2NCOONH4;ⅱ.H2NCOONH4分解生成尿素,反应过程能量变化如图。
CO (NH2) (s) + H2O (g) ΔH该反应的具体过程分两步完成,ⅰ.CO2和NH3生成H2NCOONH4;ⅱ.H2NCOONH4分解生成尿素,反应过程能量变化如图。
(1)总反应的

 ,该反应在
,该反应在(2)若该反应在恒容密闭容器中进行,判断该反应达到化学平衡状态的依据是________ (填字母序号)。
| A.反应速率2 v(CO2) = v(NH3) | B.混合气体中 CO2的浓度保持不变 |
| C.混合气体密度不变 | D.消耗2 mol NH3的同时生成 1 mol H2O |
(3)在恒温、体积为1L的恒容装置中通入CO2和NH3各1mol 、1.5mol,达平衡时CO2的转化率为50%,平衡常数的值为
Ⅱ.亚硝酸钠(NaNO2)是肉制品生产中常使用的一种食品添加剂,外观与食盐极为相似,具有较强毒性,误食可能造成死亡。已知常温下 Ka(HNO2)=1.75×10-4,Ka(CH3COOH)=1.8×10-5。
(4)常温下,pH=4的HNO2溶液中,由水电离出的c(H+)约为
(5)高锰酸钾常用于亚硝酸盐的测定。欲测定某样品中NaNO2的含量,某同学设计如下实验:
①称取样品a g,加水溶解,配制成100 mL溶液。
②取25.00 mL溶液于锥形瓶中,用0.02000 mol·L-1 KMnO4标准溶液(酸性)进行滴定,反应离子方程式是:
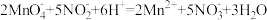 ,滴定结束后消耗KMnO4溶液VmL。
,滴定结束后消耗KMnO4溶液VmL。进行滴定操作时无需另加指示剂,达到滴定终点时的现象是
您最近一年使用:0次
6 . 下列关于化学反应方向的说法正确的是
| A.水结冰的过程不能自发进行的原因是熵减的过程,改变条件也不可能自发进行 |
| B.一定条件下,使用催化剂可以使非自发反应变成自发反应 |
| C.反应NH3(g) + HCl(g)=NH4Cl(s)在低温下能自发进行,说明该反应的ΔH<0 |
| D.能自发进行的反应一定能迅速发生 |
您最近一年使用:0次
7 . 以下过程在常温下都可以自发进行,可利用焓判据来解释的是
| A.2N2O5(g)=4N2O4(g)+O2(g) ΔH=+56.7kJ·mol-1 |
| B.2H2(g)+O2(g)=2H2O(l) ΔH=-571.6kJ·mol-1 |
| C.硝酸铵自发地溶于水 |
| D.湿衣服经过晾晒变干 |
您最近一年使用:0次
2024-01-28更新
|
40次组卷
|
2卷引用:四川省成都市成华区某校2023-2024学年高二上学期12月月考化学试题
名校
解题方法
8 . 下列推论正确的是
| A.S(g)+O2(g)=SO2(g)ΔH1,S(s)+O2(g)=SO2(g) ΔH2,则:ΔH1>ΔH2 |
| B.石墨燃烧热为393.5kJ·mol-1,则有2C(s)+O2(g)=2CO(g)ΔH=-393.5kJ·mol-1 |
| C.中和热为57.4kJ/mol,则有Ba(OH)2(aq)+H2SO4(aq)=BaSO4(s)+2H2O(l) ΔH<-114.8kJ/mol |
| D.已知CaCO3(s)=CaO(s)+CO2(g)ΔH>0,该反应任何温度下都能自发进行 |
您最近一年使用:0次
2024-01-28更新
|
37次组卷
|
3卷引用:四川省成都市成华区某校2023-2024学年高二上学期12月月考化学试题
9 . 2022北京冬奥会采用氢气作为火炬燃料,选择氢能汽车作为赛事交通服务用车,充分体现了绿色奥运的理念。已知:
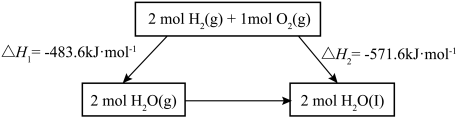
下列说法不正确的是

下列说法不正确的是
| A.氢气既可以通过燃烧反应提供热能,也可以设计成燃料电池提供电能 |
| B.H2O(g)=H2O(l)的过程中,ΔH<0、ΔS<0 |
| C.断裂2mol H2和1mol O2中化学键所需能量大于断裂2mol H2O中化学键所需能量 |
| D.化学反应的ΔH与反应体系中的物质类别及其聚集状态均有关系 |
您最近一年使用:0次
名校
10 . 反应SiCl4(g)+2H2(g)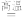 Si(s)+4HCl(g)用于纯硅的制备。下列有关该反应的说法不正确的是
Si(s)+4HCl(g)用于纯硅的制备。下列有关该反应的说法不正确的是
 Si(s)+4HCl(g)用于纯硅的制备。下列有关该反应的说法不正确的是
Si(s)+4HCl(g)用于纯硅的制备。下列有关该反应的说法不正确的是| A.该反应ΔH>0,ΔS>0 |
| B.高温下反应每生成1molSi需消耗2×22.4LH2 |
C.该反应的逆反应平衡常数K=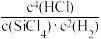 |
| D.用E表示键能,该反应ΔH═4E(Si-Cl)+2E(H-H)-4E(H-Cl)-2E(Si-Si) |
您最近一年使用:0次



