名校
解题方法
1 . 工业上,利用异丙醇制备丙烯。已知:
①
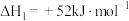
②

③

已知几种共价键键能如下表所示:
下列叙述正确的是
①

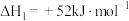
②


③


已知几种共价键键能如下表所示:
| 共价键 |  |  |  |  |  |  |
键能/( ) ) | 413 | 347 |  | 799 | 467 | 498 |
| A.反应①和②在任何温度下都能自发进行 |
B.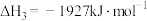 |
C. 的键能为 的键能为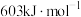 |
| D.在恒温恒容容器进行反应①②③,平衡时总压减小 |
您最近一年使用:0次
名校
2 . 亚硝酰氯( )是有机合成的氯化剂。合成原理:
)是有机合成的氯化剂。合成原理:
 ,在密闭反应器中投入
,在密闭反应器中投入 和
和 合成
合成 ,测得
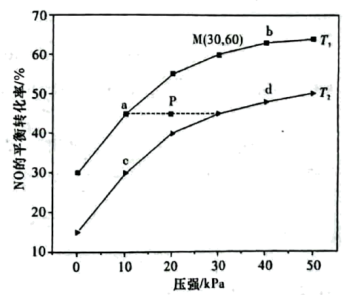
,测得 的平衡转化率与温度、压强关系如图所示,下列叙述错误的是
的平衡转化率与温度、压强关系如图所示,下列叙述错误的是
 )是有机合成的氯化剂。合成原理:
)是有机合成的氯化剂。合成原理:
 ,在密闭反应器中投入
,在密闭反应器中投入 和
和 合成
合成 ,测得
,测得 的平衡转化率与温度、压强关系如图所示,下列叙述错误的是
的平衡转化率与温度、压强关系如图所示,下列叙述错误的是
| A.该反应在较低温度下能自发进行 |
B. 的体积分数: 的体积分数: |
C. 点时反应器中气体的平均摩尔质量约为 点时反应器中气体的平均摩尔质量约为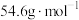 |
D. 点时同时减压和升温, 点时同时减压和升温, 的平衡转化率由 的平衡转化率由 点向 点向 点迁移 点迁移 |
您最近一年使用:0次
名校
解题方法
3 . 乙醇是一种绿色能源,也是一种化工原料。
(1)已知几种热化学方程式如下:
①
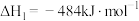
②
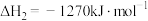
③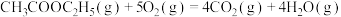

(ⅰ)上述反应中,在任意温度下都能自发进行的是___________ (填序号)。
(ⅱ)我国科学家开发新型催化剂利用乙醇直接制备乙酸乙酯: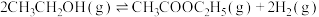

___________  。
。
(2)乙醇是一种储氢材料。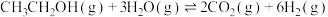
 ,Akande对其动力学机理的研究(*代表物种吸附在催化剂表面上)如图所示:
,Akande对其动力学机理的研究(*代表物种吸附在催化剂表面上)如图所示:
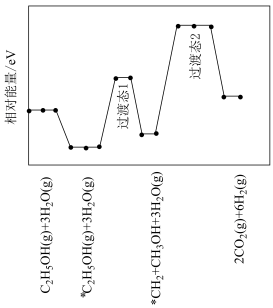
①
___________ 0(填“>”“<”或“=”),总反应分___________ 步反应进行。
②速控反应的方程式为___________ 。
(3)一定温度下,向恒容密闭容器中充入适量乙醇蒸气,发生反应: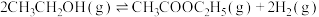 ,下列叙述正确的是___________(填标号)。
,下列叙述正确的是___________(填标号)。
(4)保持总压为 ,向反应器中充入乙醇
,向反应器中充入乙醇 和氮气(不参与反应),发生反应:
和氮气(不参与反应),发生反应: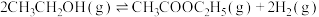 ,测得乙醇的平衡转化率与投料比
,测得乙醇的平衡转化率与投料比 、温度
、温度 的关系如图所示:
的关系如图所示:
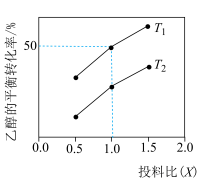
①其他条件不变时,随着 增大,乙醇的平衡转化率增大的原因是
增大,乙醇的平衡转化率增大的原因是_______ ,
_____  (填“>”或“<”)。
(填“>”或“<”)。
② 温度下,投料比为1.0时,平衡常数
温度下,投料比为1.0时,平衡常数 为
为________  (提示:用分压计算的平衡常数为
(提示:用分压计算的平衡常数为 ,分压
,分压 总压
总压 物质的显分数)。
物质的显分数)。
(5)我国科学家开发复合催化剂,实现了在酸性条件下电还原 制备乙醇,阴极反应式为
制备乙醇,阴极反应式为___________ 。
(1)已知几种热化学方程式如下:
①

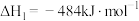
②

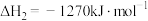
③
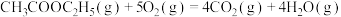

(ⅰ)上述反应中,在任意温度下都能自发进行的是
(ⅱ)我国科学家开发新型催化剂利用乙醇直接制备乙酸乙酯:
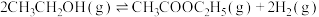

 。
。(2)乙醇是一种储氢材料。
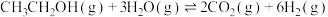
 ,Akande对其动力学机理的研究(*代表物种吸附在催化剂表面上)如图所示:
,Akande对其动力学机理的研究(*代表物种吸附在催化剂表面上)如图所示:
①

②速控反应的方程式为
(3)一定温度下,向恒容密闭容器中充入适量乙醇蒸气,发生反应:
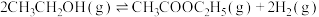 ,下列叙述正确的是___________(填标号)。
,下列叙述正确的是___________(填标号)。| A.当气体总压强不变时,达到平衡状态 |
| B.平衡时升温,正反应速率大于逆反应速率 |
| C.平衡时,充入氩气,平衡向左移动 |
D.平衡时,充入少量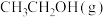 ,其平衡转化率减小 ,其平衡转化率减小 |
(4)保持总压为
 ,向反应器中充入乙醇
,向反应器中充入乙醇 和氮气(不参与反应),发生反应:
和氮气(不参与反应),发生反应: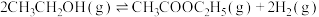 ,测得乙醇的平衡转化率与投料比
,测得乙醇的平衡转化率与投料比 、温度
、温度 的关系如图所示:
的关系如图所示:
①其他条件不变时,随着
 增大,乙醇的平衡转化率增大的原因是
增大,乙醇的平衡转化率增大的原因是
 (填“>”或“<”)。
(填“>”或“<”)。②
 温度下,投料比为1.0时,平衡常数
温度下,投料比为1.0时,平衡常数 为
为 (提示:用分压计算的平衡常数为
(提示:用分压计算的平衡常数为 ,分压
,分压 总压
总压 物质的显分数)。
物质的显分数)。(5)我国科学家开发复合催化剂,实现了在酸性条件下电还原
 制备乙醇,阴极反应式为
制备乙醇,阴极反应式为
您最近一年使用:0次
名校
4 . 下列有关说法正确的是
A.常温下,向 溶液中加入少量盐酸,溶液中 溶液中加入少量盐酸,溶液中 的值增大 的值增大 |
B.反应 常温下能自发进行,则该反应的 常温下能自发进行,则该反应的 |
C.一定条件下, 碘蒸气和 碘蒸气和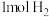 充分混合反应生成HI并放热 充分混合反应生成HI并放热 ,则该反应的热化学方程式为: ,则该反应的热化学方程式为: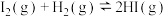 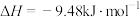 |
D.同温同压下, 在光照和点燃条件下的 在光照和点燃条件下的 不同 不同 |
您最近一年使用:0次
名校
解题方法
5 . 下列说法错误的是
A.反应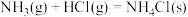 在室温下可自发进行,则该反应的 在室温下可自发进行,则该反应的 |
B.常温下,若反应 不能自发进行,则该反应的 不能自发进行,则该反应的 |
C.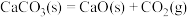 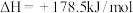 ,该反应高温才能自发 ,该反应高温才能自发 |
D.一定温度下,反应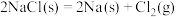 的 的 , , |
您最近一年使用:0次
2024-01-21更新
|
75次组卷
|
2卷引用:云南省昆明市云南师范大学附属中学2023-2024学年高二上学期12月月考化学试题
名校
6 . 下列有关说法正确的是
A.恒容绝热容器中,发生反应 ,当压强不变时反应达到平衡状态 ,当压强不变时反应达到平衡状态 |
B.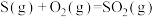  , ,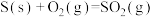  ,则 ,则 |
C.室温下,反应 不能自发进行,说明该反应的 不能自发进行,说明该反应的 |
D.一定温度下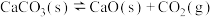 ,压缩容器体积,再次达到新平衡后, ,压缩容器体积,再次达到新平衡后, 浓度增大 浓度增大 |
您最近一年使用:0次
解题方法
7 . 下列关于化学反应方向的说法正确的是
| A.凡是放热反应都是自发反应 | B.非自发反应任何条件都不能发生 |
| C.凡是熵增大的反应都是自发反应 | D.反应是否自发与熵变和焓变都有关 |
您最近一年使用:0次
2024-01-20更新
|
63次组卷
|
2卷引用:北京市石景山区2023-2024学年高二上学期期末考试化学试卷
名校
解题方法
8 . 硫酸有着广泛的用途。硫酸工业在国民经济中占有重要地位。
(1)实验室可用铜与浓硫酸反应制备少量 :
: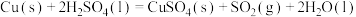
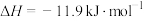 。判断该反应的自发性并说明理由
。判断该反应的自发性并说明理由___________ 。
(2)我国古籍记载了硫酸的制备方法—“炼石胆( )取精华法”。
)取精华法”。
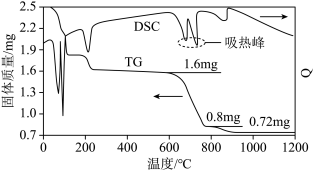
①借助现代仪器分析,该制备过程中 分解的TG曲线(热重曲线,即受热分解过程中固体质量变化曲线)及DSC曲线(反映体系热量变化情况,数值已省略)如图所示。700℃左右有两个吸热峰,则此时分解生成的氧化物有
分解的TG曲线(热重曲线,即受热分解过程中固体质量变化曲线)及DSC曲线(反映体系热量变化情况,数值已省略)如图所示。700℃左右有两个吸热峰,则此时分解生成的氧化物有___________ 、___________ (填化学式)和 。
。
②已知下列热化学方程式:
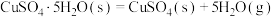



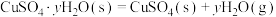

则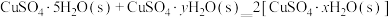 的△H=
的△H=__________  。
。
(3)接触法制硫酸的关键反应为 的催化氧化:
的催化氧化: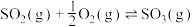
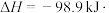

①为寻求固定投料比下不同反应阶段的最佳生产温度,绘制不同转化率( )下反应速率(数值已略去)与温度的关系如图,下列说法正确的是
)下反应速率(数值已略去)与温度的关系如图,下列说法正确的是__________ 。
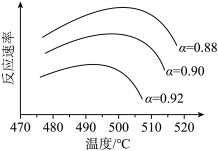
A.温度越高,反应速率越大 B.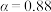 的曲线代表平衡转化率
的曲线代表平衡转化率
C. 越大,反应速率最大值对应温度越低 D.可根据不同
越大,反应速率最大值对应温度越低 D.可根据不同 下的最大速率,选择最佳生产温度
下的最大速率,选择最佳生产温度
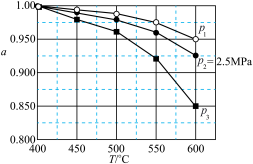
②固定投料比,在压强分别为0.5MPa、2.5MPa和5.0MPa下,得到 的平衡转化率随温度的变化如图所示。则在5.0MPa、550℃时,该反应的平衡转化率=
的平衡转化率随温度的变化如图所示。则在5.0MPa、550℃时,该反应的平衡转化率=__________ 。
③对于气体参与的反应,可用气体组分(B)的平衡压强p(B)代替该气体物质的量浓度c(B)来表示平衡常数 。设
。设 的平衡分压为p,
的平衡分压为p, 的平衡转化率为
的平衡转化率为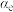 ,则上述催化氧化反应
,则上述催化氧化反应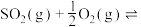
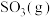 的
的
_____________ (用含p和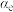 的代数式表示)。
的代数式表示)。
(1)实验室可用铜与浓硫酸反应制备少量
 :
: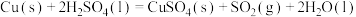
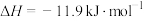 。判断该反应的自发性并说明理由
。判断该反应的自发性并说明理由(2)我国古籍记载了硫酸的制备方法—“炼石胆(
 )取精华法”。
)取精华法”。①借助现代仪器分析,该制备过程中
 分解的TG曲线(热重曲线,即受热分解过程中固体质量变化曲线)及DSC曲线(反映体系热量变化情况,数值已省略)如图所示。700℃左右有两个吸热峰,则此时分解生成的氧化物有
分解的TG曲线(热重曲线,即受热分解过程中固体质量变化曲线)及DSC曲线(反映体系热量变化情况,数值已省略)如图所示。700℃左右有两个吸热峰,则此时分解生成的氧化物有 。
。
②已知下列热化学方程式:
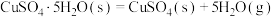



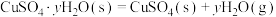

则
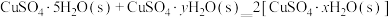 的△H=
的△H= 。
。(3)接触法制硫酸的关键反应为
 的催化氧化:
的催化氧化: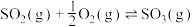
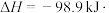

①为寻求固定投料比下不同反应阶段的最佳生产温度,绘制不同转化率(
 )下反应速率(数值已略去)与温度的关系如图,下列说法正确的是
)下反应速率(数值已略去)与温度的关系如图,下列说法正确的是
A.温度越高,反应速率越大 B.
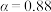 的曲线代表平衡转化率
的曲线代表平衡转化率C.
 越大,反应速率最大值对应温度越低 D.可根据不同
越大,反应速率最大值对应温度越低 D.可根据不同 下的最大速率,选择最佳生产温度
下的最大速率,选择最佳生产温度②固定投料比,在压强分别为0.5MPa、2.5MPa和5.0MPa下,得到
 的平衡转化率随温度的变化如图所示。则在5.0MPa、550℃时,该反应的平衡转化率=
的平衡转化率随温度的变化如图所示。则在5.0MPa、550℃时,该反应的平衡转化率=
③对于气体参与的反应,可用气体组分(B)的平衡压强p(B)代替该气体物质的量浓度c(B)来表示平衡常数
 。设
。设 的平衡分压为p,
的平衡分压为p, 的平衡转化率为
的平衡转化率为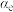 ,则上述催化氧化反应
,则上述催化氧化反应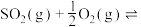
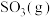 的
的
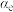 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
名校
9 . 甲烷是重要的气体燃料和化工原料,由 制取合成气(
制取合成气( 、
、 )的反应原理为
)的反应原理为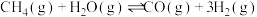
 。回答下列问题:
。回答下列问题:
(1)若生成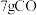 ,吸收热量akJ,相关化学键的键能(断裂1mol化学键所吸收的能量),如表所示。
,吸收热量akJ,相关化学键的键能(断裂1mol化学键所吸收的能量),如表所示。
①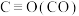 的键能为
的键能为___________ (用含a的式子表示) 。
。
②当体系温度等于TK时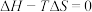 ,温度大于T时
,温度大于T时
___________ (填“>”“<”或“=”)0。
③在一定温度下,恒容密闭容器中发生上述反应,下列状态表示反应一定达到平衡状态的有___________ (填标号)。
A.
B.气体压强不再变化
C.单位时间每消耗 ,同时产生
,同时产生
D. 与
与 的物质的量之比为
的物质的量之比为
(2)在体积为 的恒容密闭容器中通入
的恒容密闭容器中通入 和
和 ,在不同条件下发生反应
,在不同条件下发生反应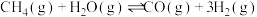 ,测得平衡时
,测得平衡时 的体积分数与温度、压强的关系如图所示。
的体积分数与温度、压强的关系如图所示。

①X表示___________ (填“温度”或“压强”),m、n、q点的平衡常数由大到小的顺序为___________ 。
②若q点对应的纵坐标为30,此时甲烷的转化率为___________ ,该条件下平衡常数
___________ (保留两位有效数字)。
 制取合成气(
制取合成气( 、
、 )的反应原理为
)的反应原理为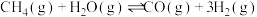
 。回答下列问题:
。回答下列问题:(1)若生成
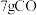 ,吸收热量akJ,相关化学键的键能(断裂1mol化学键所吸收的能量),如表所示。
,吸收热量akJ,相关化学键的键能(断裂1mol化学键所吸收的能量),如表所示。| 化学键 |  |  |  |
键能 | 414 | 436 | 467 |
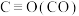 的键能为
的键能为 。
。②当体系温度等于TK时
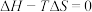 ,温度大于T时
,温度大于T时
③在一定温度下,恒容密闭容器中发生上述反应,下列状态表示反应一定达到平衡状态的有
A.

B.气体压强不再变化
C.单位时间每消耗
 ,同时产生
,同时产生
D.
 与
与 的物质的量之比为
的物质的量之比为
(2)在体积为
 的恒容密闭容器中通入
的恒容密闭容器中通入 和
和 ,在不同条件下发生反应
,在不同条件下发生反应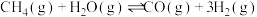 ,测得平衡时
,测得平衡时 的体积分数与温度、压强的关系如图所示。
的体积分数与温度、压强的关系如图所示。
①X表示
②若q点对应的纵坐标为30,此时甲烷的转化率为

您最近一年使用:0次
解题方法
10 . 下列反应可以自发进行但不能利用熵判据解释的是
| A.NaHCO3(s)+HCl(aq)=NaCl(aq)+CO2(g)+H2O(l) |
| B.Zn(s)+H2SO4(aq)=ZnSO4(aq)+H2(g) |
| C.4Fe(OH)2(s)+O2(g)+2H2O(l)=4Fe(OH)3(s) |
| D.2KClO3(s)=2KCl(s)+3O2(g) |
您最近一年使用:0次



