1 . 镁是一种重要的金属资源,在工业上用途广泛。回答下列问题:
(1)已知某温度下Mg(OH)2的Ksp = 6.4×l0-12,当溶液中c(Mg2+) ≤1.0×10-5mol/L可视为沉淀完全,则此温度下应保持溶液中c(OH-) ≥______ mol·L-1。
(2)已知常温下CH3COOH的电离常数为:Ka = l.75×10-5mol/L;NH3·H2O的电离常数为,Kb =1.76×l0-5mol/L。A.NH4Cl溶液显酸性,原因是_________________________ (用离子方程式表示),NH4Cl溶液中所有离子的浓度由大到小的顺序为___________ ;
B.CH3COONH4溶液显___________ (填“酸”、“碱”或“中”)性。
C.将饱和NH4Cl溶液滴入少量的Mg(OH)2悬浊液中,可看到白色沉淀溶解。产生这种现象的原因存在以下两种观点。
观点①:2NH4+ + Mg(OH)2= 2NH3·H2O+ Mg2+ ;
观点②的离子方程式为_________________________ 。
要验证①和②谁是Mg(OH)2溶解的主要原因,可选取______________ (填序号)代替NH4Cl溶液作对照实验。
a. NH4NO3 b. (NH4)2SO4 c. CH3COONH4 d. NH4HSO4
(1)已知某温度下Mg(OH)2的Ksp = 6.4×l0-12,当溶液中c(Mg2+) ≤1.0×10-5mol/L可视为沉淀完全,则此温度下应保持溶液中c(OH-) ≥
(2)已知常温下CH3COOH的电离常数为:Ka = l.75×10-5mol/L;NH3·H2O的电离常数为,Kb =1.76×l0-5mol/L。A.NH4Cl溶液显酸性,原因是
B.CH3COONH4溶液显
C.将饱和NH4Cl溶液滴入少量的Mg(OH)2悬浊液中,可看到白色沉淀溶解。产生这种现象的原因存在以下两种观点。
观点①:2NH4+ + Mg(OH)2= 2NH3·H2O+ Mg2+ ;
观点②的离子方程式为
要验证①和②谁是Mg(OH)2溶解的主要原因,可选取
a. NH4NO3 b. (NH4)2SO4 c. CH3COONH4 d. NH4HSO4
您最近一年使用:0次
2 . (1)在室温时,NaHSO4溶液中c(H+)______ c(OH-)+ c(SO42-)(填 “>”、“=”或“<”),硫酸氢钠溶液与氢氧化钡溶液反应,若溶液中SO42-完全沉淀,则反应后溶液的pH_____ 7(填 “>”、“=”或“<”)。
(2)将20mLpH=2的NaHSO4溶液逐滴加入到20mL 0.1 mol·L-1Na2CO3溶液中,溶液中发生反应的离子方程式为:____________________________________ ;向此反应后的溶液中滴加0.01 mol·L-1BaCl2溶液,首先析出的沉淀是______________ 。[KSP(BaSO4)=1.1×10-10mol2·L-2;KSP(BaCO3)=5.1×10-9mol2·L-2]
(2)将20mLpH=2的NaHSO4溶液逐滴加入到20mL 0.1 mol·L-1Na2CO3溶液中,溶液中发生反应的离子方程式为:
您最近一年使用:0次
3 . 已知:25 ℃时,Ksp(BaSO4)=1×10-10,Ksp(BaCO3)=1×10-9。
Ba2+对人体有毒,医学上进行消化系统X射线透视时,常用BaSO4作内服造影剂。胃酸酸性很强(pH约为1),但服用大量BaSO4仍然是安全的,BaSO4不溶于酸的原因是:
__________________________________________________________ 。
万一误服了少量BaCO3,应尽快用大量0.5 mol/L Na2SO4溶液给患者洗胃,如果忽略洗胃过程中Na2SO4溶液浓度的变化,残留在胃液中的Ba2+浓度仅为__________ mol/L。
Ba2+对人体有毒,医学上进行消化系统X射线透视时,常用BaSO4作内服造影剂。胃酸酸性很强(pH约为1),但服用大量BaSO4仍然是安全的,BaSO4不溶于酸的原因是:
万一误服了少量BaCO3,应尽快用大量0.5 mol/L Na2SO4溶液给患者洗胃,如果忽略洗胃过程中Na2SO4溶液浓度的变化,残留在胃液中的Ba2+浓度仅为
您最近一年使用:0次
4 . I.某温度下,Kw = 10-12。
(1)若保持温度不变,向少量水中加入_________ g的NaOH固体,并加水至1 L,才能使溶液中水电离产生的H+、OH-的浓度乘积即:c(H+)·c(OH-) = 10-22
(2)若保持温度不变,某溶液中c(H+)为1×10-7 mol/L,则该溶液显________ 性(选填“酸”、“碱”或“中”)。
II.(3)实验室中常用NaOH进行洗气和提纯,当600 mL 1 mol/L NaOH溶液吸收标准状况下8.96 L CO2气体时所得溶液中各离子浓度由大到小的顺序是___________________ 。
(4)已知常温下Kw[Fe(OH)3] = 4.0×10-38,在FeCl3溶液中加入NaHCO3溶液,发生反应的离子方程式为_____________ 。若所得悬浊液的pH调整为4,则溶液中Fe3+的浓度为__________ mol/L。
(5)试利用平衡移动原理解释下列事实:FeS不溶于水,但能溶于稀盐酸中_________________ 。
(1)若保持温度不变,向少量水中加入
(2)若保持温度不变,某溶液中c(H+)为1×10-7 mol/L,则该溶液显
II.(3)实验室中常用NaOH进行洗气和提纯,当600 mL 1 mol/L NaOH溶液吸收标准状况下8.96 L CO2气体时所得溶液中各离子浓度由大到小的顺序是
(4)已知常温下Kw[Fe(OH)3] = 4.0×10-38,在FeCl3溶液中加入NaHCO3溶液,发生反应的离子方程式为
(5)试利用平衡移动原理解释下列事实:FeS不溶于水,但能溶于稀盐酸中
您最近一年使用:0次
名校
5 . 弱电解质的电离平衡、盐类的水解平衡和难溶物的溶解平衡均属于化学平衡。根据要求回答问题。
(1)生活中明矾常作净水剂,其净水的原理是_____________ (用离子方程式表示)。
(2)常温下,取0.2 mol/L HCl溶液与0.2mol/L MOH溶液等体积混合,测得混合后溶液的pH=5。写出MOH的电离方程式:__________________ 。
(3)0.1mol/L的NaHA溶液,测得溶液显碱性。则
①该溶液中c(H2A)_______________ c(A2-)(填“>”、“<”或“=”)
②作出上述判断的依据是_____________ (用文字解释)。
(4)含Cr2O72-的废水毒性较大,某工厂废水中含5.0×10-3mol/L的Cr2O72-。为了使废水的排放达标,进行如下处理:
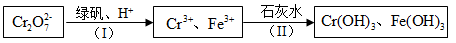
绿矾为FeSO4• 7H2O。反应(I)中Cr2O72-与FeSO4的物质的量之比为___________ 。
常温下若处理后的废水中c(Cr3+)=6.0×10-7mol/L,则处理后的废水的pH=___________ 。{Ksp[Cr(OH)3]=6.0×10-31}
(1)生活中明矾常作净水剂,其净水的原理是
(2)常温下,取0.2 mol/L HCl溶液与0.2mol/L MOH溶液等体积混合,测得混合后溶液的pH=5。写出MOH的电离方程式:
(3)0.1mol/L的NaHA溶液,测得溶液显碱性。则
①该溶液中c(H2A)
②作出上述判断的依据是
(4)含Cr2O72-的废水毒性较大,某工厂废水中含5.0×10-3mol/L的Cr2O72-。为了使废水的排放达标,进行如下处理:
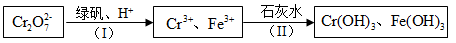
绿矾为FeSO4• 7H2O。反应(I)中Cr2O72-与FeSO4的物质的量之比为
常温下若处理后的废水中c(Cr3+)=6.0×10-7mol/L,则处理后的废水的pH=
您最近一年使用:0次
2016-12-09更新
|
561次组卷
|
4卷引用:2016-2017学年湖南省长沙一中高二上期中化学卷
6 . 以下是某实验小组用工业硫酸铜(含硫酸亚铁等杂质)进行提纯实验,得到纯净硫酸铜晶体的流程:(已知数据:lg2=0.3;lg5=0.7)
工业CuSO4
 CuSO4溶液
CuSO4溶液 CuSO4·5H2O
CuSO4·5H2O
请回答下列问题:
(1)①步骤I的目的是除不溶性杂质。操作是_________________________ 。
②步骤Ⅱ是为了除去Fe2+,常加入氧化剂使Fe2+氧化为Fe3+,下列物质最适合的是________ 。
A.KMnO4 B.H2O2 C.Cl2水 D.HNO3
然后再加入适当物质调整至溶液pH=4,使Fe3+转化为Fe(OH)3,可以达到除去Fe3+而不损失CuSO4的目的,调整溶液pH可选用下列中的________ 。
A.NaOH B.NH3·H2O C.CuO D.Cu
(2)已知常温下Fe(OH)3的溶度积Ksp=8.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol·L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0 mol·L-1,分别写出Cu(OH)2开始沉淀时溶液的pH=________ 并写出步骤Ⅱ调节溶液pH的合理范围______ 。
工业CuSO4

 CuSO4溶液
CuSO4溶液 CuSO4·5H2O
CuSO4·5H2O请回答下列问题:
(1)①步骤I的目的是除不溶性杂质。操作是
②步骤Ⅱ是为了除去Fe2+,常加入氧化剂使Fe2+氧化为Fe3+,下列物质最适合的是
A.KMnO4 B.H2O2 C.Cl2水 D.HNO3
然后再加入适当物质调整至溶液pH=4,使Fe3+转化为Fe(OH)3,可以达到除去Fe3+而不损失CuSO4的目的,调整溶液pH可选用下列中的
A.NaOH B.NH3·H2O C.CuO D.Cu
(2)已知常温下Fe(OH)3的溶度积Ksp=8.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol·L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0 mol·L-1,分别写出Cu(OH)2开始沉淀时溶液的pH=
您最近一年使用:0次
7 . 绿矾(FeSO4·7H2O)是治疗缺铁性贫血药品的重要成分。下面是以市售铁屑(含少量锡、氧化铁等杂质)为原料生产纯净绿矾的一种方法:

查询资料,得有关物质的数据如下表:
(1)检验制得的绿矾晶体中是否含有Fe3+,最好选用的试剂为 。
A.KSCN溶液 B.NaOH溶液 C.KMnO4溶液
(2)操作II中,通入硫化氢至饱和的目的是 。
(3)操作IV的顺序依次为 、冷却结晶、过滤。
(4)操作IV得到的绿矾晶体用少量冰水洗涤,其目的是:①除去晶体表面附着的硫酸等杂质;② 。
(5)测定绿矾产品中Fe2+含量的方法是:A.称取一定量的绿矾产品,溶解,在250mL容量瓶中定容;量取一定量的待测溶液于锥形瓶中;再用硫酸酸化的KMnO4溶液滴定至终点。
①滴定时盛放KMnO4溶液的仪器为 (填仪器名称)。
②判断此滴定实验达到终点的方法是 。

查询资料,得有关物质的数据如下表:
| 25℃时 | pH值 |
| 饱和H2S溶液 | 3.9 |
| SnS沉淀完全 | 1.6 |
| FeS开始沉淀 | 3.0 |
| FeS沉淀完全 | 5.5 |
(1)检验制得的绿矾晶体中是否含有Fe3+,最好选用的试剂为 。
A.KSCN溶液 B.NaOH溶液 C.KMnO4溶液
(2)操作II中,通入硫化氢至饱和的目的是 。
(3)操作IV的顺序依次为 、冷却结晶、过滤。
(4)操作IV得到的绿矾晶体用少量冰水洗涤,其目的是:①除去晶体表面附着的硫酸等杂质;② 。
(5)测定绿矾产品中Fe2+含量的方法是:A.称取一定量的绿矾产品,溶解,在250mL容量瓶中定容;量取一定量的待测溶液于锥形瓶中;再用硫酸酸化的KMnO4溶液滴定至终点。
①滴定时盛放KMnO4溶液的仪器为 (填仪器名称)。
②判断此滴定实验达到终点的方法是 。
您最近一年使用:0次
12-13高二上·黑龙江·期末
名校
8 . 以下是25℃时几种难溶电解质的溶解度:
在无机化合物的提纯中,常利用难溶电解质的溶解平衡原理除去某些离子,例如:
①为了除去氯化铵中的杂质Fe3+,先将混合物溶于水,再加入一定量的试剂反应,过滤结晶即可;
②为了除去氯化镁晶体中的杂质Fe3+,现将混合物溶于水,再加入足量的氢氧化镁,充分反应,过滤结晶即可;
③为了除去硫酸铜晶体中的杂质Fe2+,先将混合物溶于水,再加入一定量的H2O2,将Fe2+氧化成Fe3+,调节溶液的pH=4,过滤结晶即可;
请回答下列问题:
(1).上述三个除杂方案都能够达到很好的效果,Fe3+、Fe2+都被转化为__________ (填名称)而除去
(2).①中加入的试剂应该选择__________ 为宜。
(3).②中除去Fe3+时所发生的总反应的离子方程式为__________
(4).下列与方案③相关的叙述中,正确的是( )
A.H2O2是绿色氧化剂,在氧化过程中不引进杂质,不产生污染
B.将Fe2+氧化为Fe3+的主要原因是Fe(OH)2沉淀比Fe(OH)3沉淀难过滤
C.调节溶液pH=4可选择的试剂是氢氧化铜或碱式碳酸铜
D.Cu2+可以大量存在于pH=4的溶液中
E.在pH>4的溶液中Fe3+—定不能大量存在
| 难溶电解质 | Mg(OH)2 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 溶解度/g | 9×10-4 | 1.7×10-6 | 1.5×10-4 | 3.0×10-9 |
在无机化合物的提纯中,常利用难溶电解质的溶解平衡原理除去某些离子,例如:
①为了除去氯化铵中的杂质Fe3+,先将混合物溶于水,再加入一定量的试剂反应,过滤结晶即可;
②为了除去氯化镁晶体中的杂质Fe3+,现将混合物溶于水,再加入足量的氢氧化镁,充分反应,过滤结晶即可;
③为了除去硫酸铜晶体中的杂质Fe2+,先将混合物溶于水,再加入一定量的H2O2,将Fe2+氧化成Fe3+,调节溶液的pH=4,过滤结晶即可;
请回答下列问题:
(1).上述三个除杂方案都能够达到很好的效果,Fe3+、Fe2+都被转化为
(2).①中加入的试剂应该选择
(3).②中除去Fe3+时所发生的总反应的离子方程式为
(4).下列与方案③相关的叙述中,正确的是
A.H2O2是绿色氧化剂,在氧化过程中不引进杂质,不产生污染
B.将Fe2+氧化为Fe3+的主要原因是Fe(OH)2沉淀比Fe(OH)3沉淀难过滤
C.调节溶液pH=4可选择的试剂是氢氧化铜或碱式碳酸铜
D.Cu2+可以大量存在于pH=4的溶液中
E.在pH>4的溶液中Fe3+—定不能大量存在
您最近一年使用:0次
2016-12-09更新
|
285次组卷
|
11卷引用:2015-2016学年湖南省衡阳八中高二上第二次月考化学试卷
2015-2016学年湖南省衡阳八中高二上第二次月考化学试卷(已下线)2011-2012学年黑龙江省哈六中高二上学期期末考试化学试卷(已下线)2014届江西省宜春市上高二中高二第六次月考化学试卷(已下线)2013届辽宁省鞍山一中上学期期中考试高二年级化学试卷 (已下线)2015安徽望江中学同步课时练(人教选修4)第三章检测试卷2014-2015黑龙江省大庆市铁人中学高二上期末化学试卷2014-2015陕西省西安市一中高二上学期期末化学试卷陕西省西安市第一中学2015-2016学年高二上12月月考化学试卷2015-2016学年内蒙古赤峰市宁城县高二上学期期末考试化学试卷吉林省白城一中2018-2019学年高二上学期期中考试化学试题河北省石家庄市辛集市第一中学2020-2021学年高二月考第四次考试(一)化学试题
12-13高二·山东聊城·期末
名校
9 . 水体中重金属铅的污染问题备受关注。水溶液中铅的存在形态主要有Pb2+、Pb(OH)+、Pb(OH)2、Pb(OH)  、Pb(OH)
、Pb(OH)  ,各形态的浓度分数α随溶液pH变化的关系如下图所示:
,各形态的浓度分数α随溶液pH变化的关系如下图所示:
___________ 2(填“>”“=”或“<”);往该溶液中滴入氯化铵溶液后, 增加,可能的原因是
增加,可能的原因是___________ 。
(2)往Pb(NO3)2溶液中滴入稀NaOH溶液,pH=8时溶液中存在的阳离子(Na+除外)有___________ ,pH=9时主要反应的离子方程式为___________ 。
(3)某课题组制备了一种新型脱铅剂,能有效去除水中的痕量铅,实验结果如下表:
上表中除Pb2+外,该脱铅剂对其他离子的去除效果最好的是___________ 。
(4)如果该脱铅剂(用EH表示)脱铅过程中主要发生的反应为:2EH(s)+Pb2+ E2Pb(s)+2H+则脱铅的最合适pH范围为
E2Pb(s)+2H+则脱铅的最合适pH范围为( )
A.4~5 B.6~7 C.9~10 D.11~12
 、Pb(OH)
、Pb(OH)  ,各形态的浓度分数α随溶液pH变化的关系如下图所示:
,各形态的浓度分数α随溶液pH变化的关系如下图所示: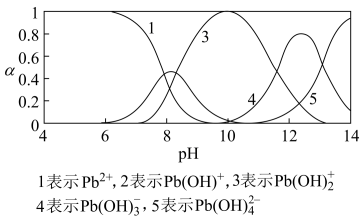

 增加,可能的原因是
增加,可能的原因是(2)往Pb(NO3)2溶液中滴入稀NaOH溶液,pH=8时溶液中存在的阳离子(Na+除外)有
(3)某课题组制备了一种新型脱铅剂,能有效去除水中的痕量铅,实验结果如下表:
| 离子 | Pb2+ | Ca2+ | Fe3+ | Mn2+ | Cl- |
| 处理前浓度/(mg·L-1) | 0.100 | 29.8 | 0.120 | 0.087 | 51.9 |
| 处理后浓度/(mg·L-1) | 0.004 | 22.6 | 0.040 | 0.053 | 49.8 |
(4)如果该脱铅剂(用EH表示)脱铅过程中主要发生的反应为:2EH(s)+Pb2+
 E2Pb(s)+2H+则脱铅的最合适pH范围为
E2Pb(s)+2H+则脱铅的最合适pH范围为A.4~5 B.6~7 C.9~10 D.11~12
您最近一年使用:0次
2016-12-09更新
|
1048次组卷
|
4卷引用:湖南省长沙市南雅中学2018-2019学年高二上学期期中考试化学试题
湖南省长沙市南雅中学2018-2019学年高二上学期期中考试化学试题(已下线)2012-2013学年山东省聊城市某重点中学高二第四次模块检测化学试卷(已下线)2012-2013学年山东省聊城市四县六校高二下学期期末联考化学试卷山西省运城市芮城中学2021-2022学年高二下学期开学摸底考试化学试题
10 . 二氧化氯(ClO2)是一种高效、广谱、安全的杀菌、消毒剂。
(1)氯化钠电解法是一种可靠的工业生产ClO2方法。
①用于电解的食盐水需先除去其中的Ca2+、Mg2+、SO42-等杂质。其次除杂操作时,往粗盐水中先加入过量的________ (填化学式),至沉淀不再产生后,再加入过量的Na2CO3和NaOH,充分反应后将沉淀一并滤去。经检测发现滤液中仍含有一定量的SO42-,其原因是___________ 【已知:Ksp(BaSO4)= 1.1 ×10-10 Ksp(BaCO3)= 5.1 ×10-9】
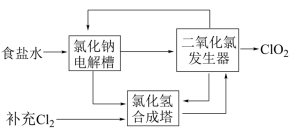
②该法工艺原理如右。其过程是将食盐水在特定条件下电解得到的氯酸钠(NaClO3)与盐酸反应生成ClO2。
工艺中可以利用的单质有____________ (填化学式),发生器中生成ClO2的化学方程式为___________ 。
(2)纤维素还原法制ClO2是一种新方法,其原理是:纤维素水解得到的最终产物D与NaClO3反应生成ClO2。完成反应的化学方程式:
□ (D) +24NaClO3+12H2SO4=□ClO2↑+□CO2↑+18H2O+□_________
(3)ClO2和Cl2均能将电镀废水中的CN-氧化为无毒的物质,自身被还原为Cl-。处理含CN-相同量得电镀废水,所需Cl2的物质的量是ClO2的_______ 倍
(1)氯化钠电解法是一种可靠的工业生产ClO2方法。
①用于电解的食盐水需先除去其中的Ca2+、Mg2+、SO42-等杂质。其次除杂操作时,往粗盐水中先加入过量的

②该法工艺原理如右。其过程是将食盐水在特定条件下电解得到的氯酸钠(NaClO3)与盐酸反应生成ClO2。
工艺中可以利用的单质有
(2)纤维素还原法制ClO2是一种新方法,其原理是:纤维素水解得到的最终产物D与NaClO3反应生成ClO2。完成反应的化学方程式:
□ (D) +24NaClO3+12H2SO4=□ClO2↑+□CO2↑+18H2O+□
(3)ClO2和Cl2均能将电镀废水中的CN-氧化为无毒的物质,自身被还原为Cl-。处理含CN-相同量得电镀废水,所需Cl2的物质的量是ClO2的
您最近一年使用:0次
2016-12-09更新
|
1354次组卷
|
3卷引用:湖南省邵阳市第二中学2022-2023学年高三上学期第五次月考化学试题
湖南省邵阳市第二中学2022-2023学年高三上学期第五次月考化学试题2013年全国普通高等学校招生统一考试理科综合能力测试化学(福建卷)(已下线)练习9 电解池-2020-2021学年【补习教材·寒假作业】高二化学(人教版2019)



