名校
1 . 已知部分弱酸的电离平衡常数如表,根据表中数据回答下列问题。
(1)已知某浓度的 水溶液
水溶液 ,原因是
,原因是_______ (用离子方程式表示), 的
的 溶液中,由水电离出的
溶液中,由水电离出的 浓度为
浓度为_______ 。
(2)同浓度 这4种溶液中碱性由强到弱的顺序是
这4种溶液中碱性由强到弱的顺序是_______ ; 溶液中各离子浓度由大到小的顺序是
溶液中各离子浓度由大到小的顺序是_______ 。
(3)体积相同、 相同的三种酸溶液a.
相同的三种酸溶液a. ;b.
;b. ;c.
;c. 分别与同浓度的
分别与同浓度的 溶液完全中和,消耗
溶液完全中和,消耗 溶液的体积由大到小的排列顺序是(填字母)
溶液的体积由大到小的排列顺序是(填字母)_______ 。
| 弱酸 |  |  |  |
电离平衡常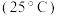 | 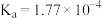 |  | 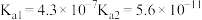 |
 水溶液
水溶液 ,原因是
,原因是 的
的 溶液中,由水电离出的
溶液中,由水电离出的 浓度为
浓度为(2)同浓度
 这4种溶液中碱性由强到弱的顺序是
这4种溶液中碱性由强到弱的顺序是 溶液中各离子浓度由大到小的顺序是
溶液中各离子浓度由大到小的顺序是(3)体积相同、
 相同的三种酸溶液a.
相同的三种酸溶液a. ;b.
;b. ;c.
;c. 分别与同浓度的
分别与同浓度的 溶液完全中和,消耗
溶液完全中和,消耗 溶液的体积由大到小的排列顺序是(填字母)
溶液的体积由大到小的排列顺序是(填字母)
您最近一年使用:0次
2022-04-04更新
|
79次组卷
|
2卷引用:新疆乌鲁木齐市第四中学2021-2022学年高二上学期期末考试化学试题
20-21高二·浙江·期中
解题方法
2 . 下列各组离子在指定溶液中一定能大量共存的是
A.由水电离出来的氢离子浓度为10-13mol/L的溶液中:CH3COO-、K+、 、Cl- 、Cl- |
B.能使甲基橙变红的溶液中:K+、Mg2+、 、 、 |
C.c(H+)/c(OH-)=107的溶液:Fe2+、Al3+、 、C1- 、C1- |
D.含有大量Fe3+的溶液: Na+、 Cl-、 、 、 |
您最近一年使用:0次
名校
解题方法
3 . 一定温度下,水溶液中 和
和 的浓度变化曲线如图,下列说法不正确的是
的浓度变化曲线如图,下列说法不正确的是
 和
和 的浓度变化曲线如图,下列说法不正确的是
的浓度变化曲线如图,下列说法不正确的是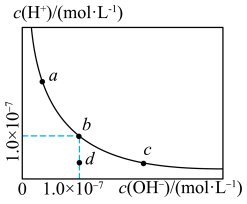
| A.升高温度,可能引起由c向a的变化 |
B.该温度下,水的离子积常数为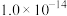 |
C.该温度下,加入 可能引起由b向α的变化 可能引起由b向α的变化 |
| D.该温度下,稀释溶液可能引起由c向d的变化 |
您最近一年使用:0次
名校
解题方法
4 . 已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
(1)下列离子中,最容易结合H+的是___________ (用编号填写)
a.CH3COO- b. c.CN- d.
c.CN- d.
(2)常温下,0.1 mol·L-1 CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是___________ (填字母)
A.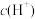 B.
B. C.
C.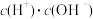 D.
D.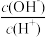 E.
E.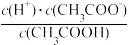
(3)写出向NaCN溶液中通入少量二氧化碳的离子方程式:___________
(4)25℃时,CH3COOH与CH3COONa混合溶液,若测得混合液pH=6,则溶液中c(CH3COO-)-c(Na+)=___________ (填准确数值)。
(5)标准状况下,将1.12 L CO2通入100 mL 1 mol·L-1的NaOH溶液中,用溶液中微粒的浓度符号完成下列等式:c(OH-)=2c(H2CO3)+___________ 。
| 化学式 | CH3COOH | H2CO3 | HCN |
| 电离平衡常数 | 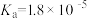 | 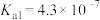  | K=4.9×10-10 |
(1)下列离子中,最容易结合H+的是
a.CH3COO- b.
 c.CN- d.
c.CN- d.
(2)常温下,0.1 mol·L-1 CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是
A.
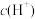 B.
B. C.
C.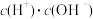 D.
D.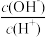 E.
E.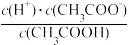
(3)写出向NaCN溶液中通入少量二氧化碳的离子方程式:
(4)25℃时,CH3COOH与CH3COONa混合溶液,若测得混合液pH=6,则溶液中c(CH3COO-)-c(Na+)=
(5)标准状况下,将1.12 L CO2通入100 mL 1 mol·L-1的NaOH溶液中,用溶液中微粒的浓度符号完成下列等式:c(OH-)=2c(H2CO3)+
您最近一年使用:0次
名校
解题方法
5 . 物质在水中可能存在电离平衡、水解平衡和沉淀溶解平衡,请根据所学知识回答:
I.常温下,一定浓度的 溶液的
溶液的 ,已知
,已知 的电离平衡常数
的电离平衡常数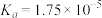 。
。
(1)乙酸钠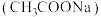 溶液呈碱性的原因是
溶液呈碱性的原因是_______ (用离子方程式表示)。 的
的 溶液中:
溶液中: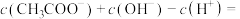
_______  。
。
Ⅱ.常温下向某氨水中缓缓通入 气体,溶液中
气体,溶液中 与
与 关系如图所示。
关系如图所示。

(2)在常温下 的电离平衡常数
的电离平衡常数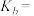
_______ (用含有a的代数式表示)。
Ⅲ. 时,向
时,向 溶液中滴加
溶液中滴加 溶液(一种酸,酸性强弱未知)时,溶液中由水电离的
溶液(一种酸,酸性强弱未知)时,溶液中由水电离的 浓度随加入的HA体积的变化如图所示:
浓度随加入的HA体积的变化如图所示:

(3)根据该图判断HA为_______ (填“强酸”或“弱酸”),理由是_______ 。
(4)若稀释a点溶液,则与稀释前相比,稀释后的溶液中水的电离程度会_______ (填“增大”、“减小”或“不变”)。
(5)d点溶液中溶质成分是_______ ,溶液中离子浓度大小关系_______ 。
I.常温下,一定浓度的
 溶液的
溶液的 ,已知
,已知 的电离平衡常数
的电离平衡常数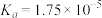 。
。(1)乙酸钠
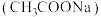 溶液呈碱性的原因是
溶液呈碱性的原因是 的
的 溶液中:
溶液中: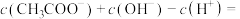
 。
。Ⅱ.常温下向某氨水中缓缓通入
 气体,溶液中
气体,溶液中 与
与 关系如图所示。
关系如图所示。
(2)在常温下
 的电离平衡常数
的电离平衡常数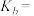
Ⅲ.
 时,向
时,向 溶液中滴加
溶液中滴加 溶液(一种酸,酸性强弱未知)时,溶液中由水电离的
溶液(一种酸,酸性强弱未知)时,溶液中由水电离的 浓度随加入的HA体积的变化如图所示:
浓度随加入的HA体积的变化如图所示:
(3)根据该图判断HA为
(4)若稀释a点溶液,则与稀释前相比,稀释后的溶液中水的电离程度会
(5)d点溶液中溶质成分是
您最近一年使用:0次
名校
6 . 常温下,分别取未知浓度的 和
和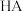 溶液,加水稀释至原体积的
溶液,加水稀释至原体积的 倍,稀释过程中,两溶液
倍,稀释过程中,两溶液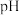 的变化如图所示。下列叙述正确的是
的变化如图所示。下列叙述正确的是

 和
和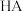 溶液,加水稀释至原体积的
溶液,加水稀释至原体积的 倍,稀释过程中,两溶液
倍,稀释过程中,两溶液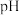 的变化如图所示。下列叙述正确的是
的变化如图所示。下列叙述正确的是
A. 为弱碱, 为弱碱,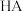 为强酸 为强酸 |
| B.将X点溶液与Z点溶液等体积混合,所得溶液呈碱性 |
C.若升高温度,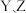 点对应溶液的 点对应溶液的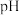 均不变 均不变 |
D.水的电离程度: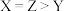 |
您最近一年使用:0次
2024-04-08更新
|
53次组卷
|
2卷引用:山东省济南市历城第一中学2023-2024学年高二上学期期中考试化学试题
名校
解题方法
7 . 向1000 mL 3mol/LNaOH中通入适量CO2气体,溶液中有关阴离子的物质的量变化曲线如图所示:
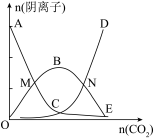
下列说法正确的是

下列说法正确的是
A.CD段反应的离子方程式为OH-+CO2=HCO |
| B.水的电离程度先增大后减小 |
| C.溶液的pH先减小后增大 |
| D.M、N两点对应的溶液中离子种类不同 |
您最近一年使用:0次
解题方法
8 . 298 K时,向20 mL 0.1 mol/L某酸HA溶液中逐滴加入0.1 mol/L NaOH溶液,混合溶液的pH变化曲线如图所示。下列说法错误的是
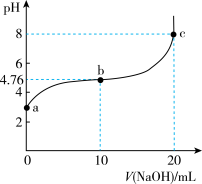

| A.a点溶液的pH为2.88 |
| B.b点溶液中:c(Na+)>c(A-)>c(HA) |
| C.b、c之间一定存在c(Na+)=c(A-)的点 |
| D.a、b、c三点中,c点水的电离程度最大 |
您最近一年使用:0次
名校
解题方法
9 . 常温下,下列关于电解质溶液的正确判断是
A.在pH=12的溶液中,Al3+、Cl-、CO 、Na+可以大量共存 、Na+可以大量共存 |
B.在pH=0的溶液中,Na+、NO 、SO 、SO 、K+可以大量共存 、K+可以大量共存 |
C.由水电离出的氢离子浓度为1.0×10-12mol•L-1溶液中,K+、Cl-、HCO 、Na+可以大量共存 、Na+可以大量共存 |
| D.由0.1mol•L-1一元酸HA溶液的pH=3,可推知NaA溶液存在A-+H2O⇌HA+OH- |
您最近一年使用:0次
名校
解题方法
10 . 常温下,向20mL0.2mol·L-1H2X溶液中滴加0.2mol·L-1NaOH溶液,在不同pH环境下不同形态的粒子组成分数如图所示,下列说法正确的是
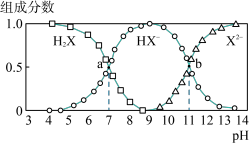

| A.水的电离程度:b点小于点a |
| B.将等物质的量的NaHX、Na2X溶于水中,所得溶液pH恰好为11 |
| C.常温下的Ka(HY)=1.1×10-10,将少量H2X溶液加入到足量NaY溶液中,发生的反应为:H2X+Y-=HY+HX- |
| D.常温下,反应X2-+H2O⇌HX-+OH-的平衡常数对数值1gK=-11 |
您最近一年使用:0次
2020-06-22更新
|
180次组卷
|
2卷引用:安徽师范大学附属中学2020届高三6月第九次模拟考试理综化学试题



