1 . 要除去CuCl2溶液中的Fe3+ ,甲同学不知道调整溶液pH=4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计算确定,他查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp = 1×10-38,Cu(OH)2的溶度积Ksp=3×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol•L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0mol•L-1,通过调节溶液pH除去Fe3+而不损失Cu2+,调节pH的取值范围
| A.3≤pH<4 | B.3≤pH≤4 |
| C.2<pH≤3 | D.2≤pH<3 |
您最近半年使用:0次
解题方法
2 . 在不同温度下的水溶液中离子浓度曲线如图所示。

(1)图中
_______  (填写“>”,“<”或“=”)
(填写“>”,“<”或“=”)
(2)C点溶液的性质_______ 。(填写“酸性”、“碱性”或“中性”)
(3)将D点变为E点,采取的措施是_______ 。
(4)在48 mL 0.1 mol/L 液中加入12 mL 0.4 mol/L KOH溶液,所得溶液呈_______。
液中加入12 mL 0.4 mol/L KOH溶液,所得溶液呈_______。
(5)用已知浓度HCl溶液滴定未知浓度NaOH溶液,选用酚酞做指示剂。

①滴定时,将酸性HCl标准液装在图中的_______ (填“甲”或“乙”)滴定管中。
②判断滴定终点到达时的现象为_______ 。
③若出现下列情况,测定结果偏高的是_______ (选填字母序号)
a.滴定前用蒸馏水冲洗锥形瓶
b.滴定过程中振荡锥形瓶时不慎将瓶内溶液溅出
c.滴定过程中不慎将数滴酸液滴在锥形瓶外
d.酸式滴定管在滴定前有气泡,滴定后气泡消失

(1)图中

 (填写“>”,“<”或“=”)
(填写“>”,“<”或“=”)(2)C点溶液的性质
(3)将D点变为E点,采取的措施是
(4)在48 mL 0.1 mol/L
 液中加入12 mL 0.4 mol/L KOH溶液,所得溶液呈_______。
液中加入12 mL 0.4 mol/L KOH溶液,所得溶液呈_______。| A.弱酸性 | B.强酸性 | C.碱性 | D.中性 |
(5)用已知浓度HCl溶液滴定未知浓度NaOH溶液,选用酚酞做指示剂。

①滴定时,将酸性HCl标准液装在图中的
②判断滴定终点到达时的现象为
③若出现下列情况,测定结果偏高的是
a.滴定前用蒸馏水冲洗锥形瓶
b.滴定过程中振荡锥形瓶时不慎将瓶内溶液溅出
c.滴定过程中不慎将数滴酸液滴在锥形瓶外
d.酸式滴定管在滴定前有气泡,滴定后气泡消失
您最近半年使用:0次
名校
解题方法
3 . 下列有关水的电离情况的说法正确的是
A.100℃时,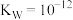 ,此温度下 ,此温度下 的溶液一定呈中性 的溶液一定呈中性 |
B. 、 、 、 、 、 、 溶于水,对水的电离都有促进作用 溶于水,对水的电离都有促进作用 |
C.25℃时, 的烧碱溶液与纯碱溶液,水的电离程度前者等于后者 的烧碱溶液与纯碱溶液,水的电离程度前者等于后者 |
D.常温下,由水电离出的 的溶液可能呈碱性 的溶液可能呈碱性 |
您最近半年使用:0次
名校
解题方法
4 . 设NA为阿伏加德罗常数的值。下列说法正确的是
| A.99℃时,1LpH=7的NaOH溶液中,OH-的数目为10-7NA |
B.25℃时,1mol·L-1的NH4NO3溶液中含有 、NH3、NH3·H2O的总数目为0.1NA 、NH3、NH3·H2O的总数目为0.1NA |
| C.25℃时,1LpH=3的H2SO3溶液中,H+的数目为0.001NA |
| D.25℃时,1LpH=11的Na2CO3溶液中,水电离出的H+的数目为10-11NA |
您最近半年使用:0次
名校
解题方法
5 . 河水是主要的饮用水源,污染物通过饮用水可直接毒害人体,也可通过食物链和农田灌溉间接危及人体健康。请回答下列问题。
已知在25℃和T℃时,水的电离平衡曲线如图所示:。

(1)由图可知,则该温度T___________ (填“>”“<”“=”)25℃,原因___________ 。
(2)图中四点 间的大小关系:
间的大小关系:___________ (用A、B、C、D表示)。
(3)在新制氯水中加入少量 固体,水的电离平衡移动
固体,水的电离平衡移动___________ (填“向左”“向右”或“不”)。
(4)25℃时, 浓度的
浓度的 溶液与
溶液与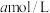 醋酸溶液等体积混合后
醋酸溶液等体积混合后 ,醋酸的电离常数为
,醋酸的电离常数为___________ (用含a的式子表示)。
(5)T℃时,将 的
的 溶液与
溶液与 的
的 溶液混合,若所得混合溶液的
溶液混合,若所得混合溶液的 (忽略溶液混合时的体积变化),则
(忽略溶液混合时的体积变化),则 溶液与
溶液与 溶液的体积比为
溶液的体积比为___________ 。
(6) ,25℃时,
,25℃时, 溶液的pH约等于
溶液的pH约等于___________ (已知 )。将浓度相等的HF与
)。将浓度相等的HF与 溶液等体积混合,判断溶液呈
溶液等体积混合,判断溶液呈___________ (填“酸”、“碱”或“中”性,并结合有关数据解释原因:___________ 。
已知在25℃和T℃时,水的电离平衡曲线如图所示:。

(1)由图可知,则该温度T
(2)图中四点
 间的大小关系:
间的大小关系:(3)在新制氯水中加入少量
 固体,水的电离平衡移动
固体,水的电离平衡移动(4)25℃时,
 浓度的
浓度的 溶液与
溶液与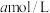 醋酸溶液等体积混合后
醋酸溶液等体积混合后 ,醋酸的电离常数为
,醋酸的电离常数为(5)T℃时,将
 的
的 溶液与
溶液与 的
的 溶液混合,若所得混合溶液的
溶液混合,若所得混合溶液的 (忽略溶液混合时的体积变化),则
(忽略溶液混合时的体积变化),则 溶液与
溶液与 溶液的体积比为
溶液的体积比为(6)
 ,25℃时,
,25℃时, 溶液的pH约等于
溶液的pH约等于 )。将浓度相等的HF与
)。将浓度相等的HF与 溶液等体积混合,判断溶液呈
溶液等体积混合,判断溶液呈
您最近半年使用:0次
名校
6 . T℃时,水溶液中c(H+)、c(OH-)的关系如图所示,请回答下列问题:

(1)x表示___________ (填“H+”或“OH-”)浓度;T℃时,水的离子积Kw=___________ ;T___________ (填“>”、“<”或“=”)25。
(2)在T℃下,向Ba(OH)2溶液中逐滴加入pH=4的盐酸,测得加入盐酸前后溶液的pH如下表所示:
①Ba(OH)2溶液的浓度是___________ mol·L-1。
②忽略溶液混合前后的体积变化,则α=___________ 。
(3)T℃下,100mLpH=9的Na2CO3溶液中,水电离出的OH-的物质的量为___________ mol;c(OH-)___________ (填“>”、“<”或“=”)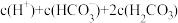 。
。

(1)x表示
(2)在T℃下,向Ba(OH)2溶液中逐滴加入pH=4的盐酸,测得加入盐酸前后溶液的pH如下表所示:
| Ba(OH)2溶液的体积/mL | 盐酸的体积/mL | 溶液的pH |
| 22.00 | 0.00 | 8 |
| 22.00 | 18.00 | a |
②忽略溶液混合前后的体积变化,则α=
(3)T℃下,100mLpH=9的Na2CO3溶液中,水电离出的OH-的物质的量为
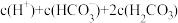 。
。
您最近半年使用:0次
名校
7 . 水是生命之源,水溶液中pH和pOH【pOH=-1gc(OH-)】的关系如图所示,下列判断正确的是

| A.a点溶液呈酸性 |
| B.a→c可表示稀硫酸稀释时pH的变化 |
| C.升高NaCl溶液的温度,可使溶液由b点移动到a点 |
D.温度为T2时,pH=2的盐酸中,由水电离产生的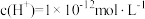 |
您最近半年使用:0次
2023-12-05更新
|
375次组卷
|
4卷引用:吉林省松原市前郭县第五高级中学2023~2024学年高二上学期期中考试化学试题
吉林省松原市前郭县第五高级中学2023~2024学年高二上学期期中考试化学试题江西省上饶市清源学校2023-2024学年高二上学期12月考试化学试题(已下线)题型14 电解质溶液-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)通关练10 盘点溶液中的“四大”平衡-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)
名校
8 . 25℃时,下列各组离子在指定条件下一定不能大量共存的是
A.含有大量Fe3+的溶液中:H+、Na+、Cl-、NO |
B.能使酚酞变红的溶液中:Na+、Mg2+、HCO 、Cl- 、Cl- |
C.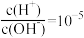 的溶液中:Na+、K+、OH-、NO 的溶液中:Na+、K+、OH-、NO |
D.pH<7的溶液中:Al3+、Ca2+、NO 、Cl- 、Cl- |
您最近半年使用:0次
2023-12-05更新
|
171次组卷
|
3卷引用:吉林省松原市前郭县第五高级中学2023~2024学年高二上学期期中考试化学试题
9 . 25℃时,水的电离达到平衡:
 ,下列叙述正确的
,下列叙述正确的

 ,下列叙述正确的
,下列叙述正确的A.将水加热, 增大,pH变小 增大,pH变小 |
B.向水中加入稀氨水,平衡逆向移动, 减小, 减小, 减小 减小 |
C.向水中加入少量 气体,平衡逆向移动, 气体,平衡逆向移动, 减小, 减小, 减小 减小 |
D.向水中加入少量固体碳酸氢钠, 增大, 增大, 变大 变大 |
您最近半年使用:0次
2023-11-30更新
|
93次组卷
|
2卷引用:吉林省长春市农安县2023-2024学年高二上学期期中考试化学试题
名校
解题方法
10 . 中国在国际上首次拍摄到水分子内部结构照片(如图),下列关于水的叙述不正确的是

| A.水的电离是吸热过程 |
B.相同条件下海水的 和纯水的 和纯水的 相同 相同 |
C.纯水的 改变时,水仍然呈中性 改变时,水仍然呈中性 |
D. 只适用于纯水体系 只适用于纯水体系 |
您最近半年使用:0次



