1 . 常温下,向浓度均为01mol·L-1、体积均为100mL的两种一元酸HX、HY溶液中,分别加入NaOH的稀溶液,lg 随加入NaOH的物质的量的变化如图所示。下列说法正确的是
随加入NaOH的物质的量的变化如图所示。下列说法正确的是

 随加入NaOH的物质的量的变化如图所示。下列说法正确的是
随加入NaOH的物质的量的变化如图所示。下列说法正确的是
| A.a点溶液的ph=2 |
| B.水的电离程度:a<b<c |
| C.b点溶液中:c(Yˉ)+c(HY)=c(Na+) |
| D.c点溶液中:c(Yˉ)>C(Na+)>c(HY)>c(H+)>c(OHˉ) |
您最近一年使用:0次
名校
2 . 常温下,分别取未知浓度的MOH和HA溶液,加水稀释至原体积的n倍。稀释过程中,两溶液pH的变化如下图所示。下列叙述正确的是
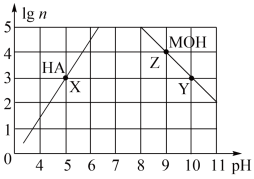

| A.MOH为弱碱,HA为强酸 |
| B.水的电离程度:X=Z>Y |
| C.若升高温度,Y、Z点对应溶液的pH均不变 |
| D.将X点溶液与Z点溶液等体积混合,所得溶液呈碱性 |
您最近一年使用:0次
2018-04-14更新
|
1515次组卷
|
15卷引用:宁夏银川市2018届高三4月高中教学质量检测理科综合化学试题
宁夏银川市2018届高三4月高中教学质量检测理科综合化学试题【百强校】天津市静海区第一中学2020届高三下学期第七周周末训练化学试题天津市海河中学2020届高三第二学期化学测试(二)试卷云南省腾冲市第八中学2022-2023学年高二下学期第三次月考化学试题(已下线)专题12 水溶液中离子平衡(攻克各种图像问题)-2021年高考化学必做热点专题广东省佛山市第一中学2021-2022学年高二上学期期中考试化学(选考) 试题湖南省怀化市沅陵县第一中学2021-2022学年高三下学期期中考试化学试题新疆乌鲁木齐市第八中学2021-2022学年高二上学期第三次月考化学试题(已下线)押新高考卷13题 水溶液中的离子平衡-备战2022年高考化学临考题号押题(新高考通版)宁夏回族自治区银川一中2022-2023学年高二上学期期中考试化学试题(已下线)【2022】【高二上】【期中考】【高中化学】59(已下线)专题21 电解质溶液图像分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)专题11 水溶液中的离子平衡图像(选择题)-2023年高考化学毕业班二轮热点题型归纳与变式演练(已下线)专题四 电解质溶液图象(讲)广东省广州市第二中学2023-2024学年高二上学期期中考试化学试题
名校
3 . 表1是元素周期表的一部分:

25℃时,用浓度为0.1000 mol•L-1的氢氧化钠溶液分别滴定20.00mL浓度均为0.1000 mol•L-1 的两种酸HX、HZ(忽略体积变化),实验数据如表2,下列判断正确的是

25℃时,用浓度为0.1000 mol•L-1的氢氧化钠溶液分别滴定20.00mL浓度均为0.1000 mol•L-1 的两种酸HX、HZ(忽略体积变化),实验数据如表2,下列判断正确的是
| A.通过分析可得表格中a <7,b=7 |
| B.将上述的HZ溶液稀释100倍后pH比HX溶液的pH大 |
| C.由于Z元素的非金属性比Y强,所以Z氢化物的酸性较强 |
| D.0.1000 mol•L-1 Na2Y的水溶液中:c(Y2-) + c(HY-) + c(H2Y) = 0.1000 mol•L-1 |
您最近一年使用:0次
名校
4 . 化学上常用AG表示溶液的lg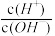 。25℃时,用0.100mol·L-1的NaOH溶液滴定20.00mL0.1mol·L-1的HNO2溶液。AG与所加NaOH溶液的体积(V)的关系如图所示,下列说法不正确的是
。25℃时,用0.100mol·L-1的NaOH溶液滴定20.00mL0.1mol·L-1的HNO2溶液。AG与所加NaOH溶液的体积(V)的关系如图所示,下列说法不正确的是

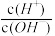 。25℃时,用0.100mol·L-1的NaOH溶液滴定20.00mL0.1mol·L-1的HNO2溶液。AG与所加NaOH溶液的体积(V)的关系如图所示,下列说法不正确的是
。25℃时,用0.100mol·L-1的NaOH溶液滴定20.00mL0.1mol·L-1的HNO2溶液。AG与所加NaOH溶液的体积(V)的关系如图所示,下列说法不正确的是
| A.C点时,加入NaOH溶液的体积不为20mL |
| B.D点溶液的pH=11.25 |
| C.B点溶液中存在2c(H+)-2c(OH-)=c(NO2-)-c(HNO2) |
| D.25℃时,HNO2的电离常数Ka=1.0×10-5.5 |
您最近一年使用:0次
2018-01-16更新
|
473次组卷
|
2卷引用:云南省师范大学附属中学2018届高三高考适应性月考卷(六)理综化学试题
5 . 实验题
(一)实验室中有一瓶含有一定量杂质的烧碱样品,某学生用中和滴定法测定烧碱的纯度,若烧碱中所含杂质与酸不反应,请根据实验回答:
(1)将准确称取的5g烧碱样品配成100 mL待测液,需要的主要仪器除量筒、烧杯、玻璃棒、托盘天平外,还必须用到的玻璃仪器有:____________ 、_____________ 。
(2)取10.00 mL待测液,选择右图中_________ (填A或B)来移取。

(3)用0.5000mol/L标准盐酸滴定待测烧碱溶液,以酚酞为指示剂。滴定时左手旋转滴定管玻璃活塞,右手不停地摇动锥形瓶,两眼注视___________ ,直到滴定终点。滴定达到终点的标志是:_________ 。
(4)根据下列数据,烧碱的纯度为:_______________________ (纯度=纯物质的质量/样品的质量×100%)
(二)氧化还原滴定实验与酸碱中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。测血钙的含量时,进行如下实验:
①可将2mL血液用蒸馏水稀释后,向其中加入足量草酸铵(NH4)2C2O4晶体,反应生成 CaC2O4沉淀,将沉淀用稀硫酸处理得H2C2O4溶液。
②将①得到的H2C2O4溶液,再用酸性KMnO4溶液滴定,氧化产物为CO2,还原产物为Mn2+。
③终点时用去20mL l.0×l0﹣4 mol/L的KMnO4溶液。
(1)写出用KMnO4滴定H2C2O4的离子方程式_____________________ 。
(2)滴定时,将KMnO4溶液装在________ (填“酸式”或“碱式”)滴定管中。
(3)计算:血液中含钙离子的浓度为_____ mol·L-1。
(一)实验室中有一瓶含有一定量杂质的烧碱样品,某学生用中和滴定法测定烧碱的纯度,若烧碱中所含杂质与酸不反应,请根据实验回答:
(1)将准确称取的5g烧碱样品配成100 mL待测液,需要的主要仪器除量筒、烧杯、玻璃棒、托盘天平外,还必须用到的玻璃仪器有:
(2)取10.00 mL待测液,选择右图中

(3)用0.5000mol/L标准盐酸滴定待测烧碱溶液,以酚酞为指示剂。滴定时左手旋转滴定管玻璃活塞,右手不停地摇动锥形瓶,两眼注视
(4)根据下列数据,烧碱的纯度为:
| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 10.00 | 0.50 | 20.40 |
| 第二次 | 10.00 | 4.00 | 24.10 |
①可将2mL血液用蒸馏水稀释后,向其中加入足量草酸铵(NH4)2C2O4晶体,反应生成 CaC2O4沉淀,将沉淀用稀硫酸处理得H2C2O4溶液。
②将①得到的H2C2O4溶液,再用酸性KMnO4溶液滴定,氧化产物为CO2,还原产物为Mn2+。
③终点时用去20mL l.0×l0﹣4 mol/L的KMnO4溶液。
(1)写出用KMnO4滴定H2C2O4的离子方程式
(2)滴定时,将KMnO4溶液装在
(3)计算:血液中含钙离子的浓度为
您最近一年使用:0次
名校
6 . 用标准浓度的NaOH溶液滴定未知浓度的盐酸时下列情况会使盐酸物质的量浓度偏低的是( )
| A.碱式滴定管用蒸馏水洗净后,直接注入标准浓度的NaOH溶液 |
| B.碱式滴定管尖端有气泡,滴定后气泡消失 |
| C.记录消耗的碱液,滴定前平视,滴定后俯视凹液面 |
| D.锥形瓶用蒸馏水洗净后,直接装入未知浓度的盐酸 |
您最近一年使用:0次
2017-11-17更新
|
861次组卷
|
14卷引用:云南省永德县第一中学2019-2020学年高二12月月考化学试题
云南省永德县第一中学2019-2020学年高二12月月考化学试题宁夏育才中学2017-2018学年高二上学期期中化学试题宁夏育才中学2017-2018学年高二上学期期中考试化学试题甘肃省岷县二中2018-2019学年高二上学期第三次月考化学试题河南省洛阳市栾川县实验高中2019-2020学年高二9月月考化学试题贵州省龙里中学2019-2020学年高二上学期期末考试化学试题内蒙古包钢第一中学2019-2020学年高二上学期10月月考化学试题人教版(2019)高二化学选择性必修1第三章 水溶液中的离子反应与平衡 第二节 水的电离和溶液的pH 课时3 酸碱中和滴定四川省成都新津为明学校2020-2021学年高二上学期期中测试化学试题云南省凤庆县第一中学2021-2022学年高二下学期3月份考试化学试题(已下线)3.2.2 pH计算和酸碱中和滴定-同步学习必备知识广东省深圳市龙华高级中学2022-2023学年高二上学期第二次段考化学试题广东省广州市第三中学2022-2023学年高二上学期期末测试化学试题江苏省无锡市江阴市两校联考2023-2024学年高二下学期3月月考化学试题
名校
7 . 下列说法正确的是
| A.0.1 mol·L-1pH为4的NaHB溶液中:c (HB-)>c(H2B)>c(B2-) |
B.如下图表示25℃时,用0.1mol·L-1盐酸滴定20mL 0.1mol·L-1 NaOH溶液时,溶液的pH随加入酸体积的变化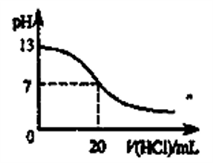 |
| C.在pH=2的NaHSO4溶液中c(H+)=c(OH-)+ c(SO42-) |
D.pH=2的两种一元酸x和y,体积均为100 mL,稀释过程中pH与溶液体积的关系如下图所示,分别滴加NaOH溶液(c=0.1mol·L-1)至pH=3,消耗NaOH溶液的体积为Vx、Vy,则x为强酸,y为弱酸且Vx>Vy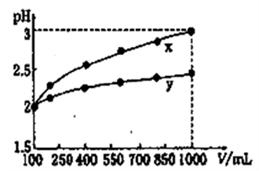 |
您最近一年使用:0次
2017-10-28更新
|
956次组卷
|
7卷引用:云南省峨山彝族自治县第一中学2018届高三第四次模拟考试化学试题
名校
解题方法
8 . 一定物质的量浓度溶液的配制和酸碱中和滴定是中学化学中两个典型的定量实验。若要配制1 mol·L-1的稀硫酸标准溶液,用其滴定某未知浓度的NaOH溶液。下列有关说法错误的是( )
| A.实验中用到的滴定管和容量瓶使用前都需要检漏 |
| B.如果实验需用85 mL的稀硫酸标准溶液,配制时可选用100 mL容量瓶 |
| C.用甲基橙作指示剂,滴定终点时,溶液颜色从红色变为橙色 |
| D.酸式滴定管用蒸馏水洗涤后,即装入标准浓度的稀硫酸滴定,会导致测定的NaOH溶液浓度偏大 |
您最近一年使用:0次
2017-08-20更新
|
967次组卷
|
5卷引用:云南省临沧市第一中学2018届高三上学期期末考试化学试题
名校
解题方法
9 . 某化学小组设计了如图1所示的数字化实验装置,研究常温下,向1L 0.1mol/L H2A溶液中逐滴加入等浓度NaOH溶液时的pH变化情况,并绘制出溶液中含A元素的微粒的物质的量分数与溶液pH的关系如图2所示,则下列说法中不正确的是
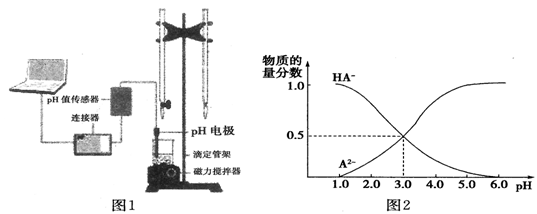

| A.pH=4.0时,图中n(HA-)约为0.0091mol |
| B.该实验应将左边的酸式滴定管换成右边碱式滴定管并加酚酞作指示剂 |
| C.常温下,等物质的量浓度的NaHA与Na2A溶液等体积混合后溶液pH=3.0 |
| D.0.1mol/LNaHA溶液中存在c(A2-)+c(HA-)+c(H2A)=0.1mol/L |
您最近一年使用:0次
2016-12-09更新
|
299次组卷
|
7卷引用:2016届湖北省武昌实验中学高三高考前模拟理综化学试卷
10 . (1)锌锰干电池是一种一次电池,外壳为金属锌,中间是碳棒,其周围有碳粉,二氧化锰,氯化锌和氯化铵等组成的填充物,该电池在放电过程产生MnOOH(难溶于水),回收处理该废电池可以得到多种化工原料,有关数据下图所示:
溶解度/(g/100g水)
回答下列问题:
①普通锌锰电池放电时发生的主要反应为:Zn+2NH4Cl+2MnO2=Zn(NH3)2Cl2+2MnOOH。该电池中,负极材料主要是________,正极发生的主要反应式是 。
②用废电池的锌皮制作七水合硫酸锌,需去除少量杂质铁,其方法是:加入稀硫酸和双氧水,溶解,
加碱调节溶液pH,使溶液中氢氧根离子浓度达到 mol/L,铁刚好完全沉淀(离子浓度小于1×10-5mol/L时,即可认为该离子沉淀完全)。继续加碱调节pH为 ,锌开始沉淀(假定Zn2+浓度为0.1mol/L)。
(2)在分析化学中常用Na2C2O4晶体(溶液无色)作为基准物质测定KMnO4溶液的浓度。在H2SO4溶液中,反应如下:2MnO+5C2O+16H+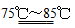 2Mn2+(溶液无色)+10CO2↑+8H2O。
2Mn2+(溶液无色)+10CO2↑+8H2O。
①若将W g Na2C2O4配成100 mL标准溶液,移取20.00 mL置于锥形瓶中,则酸性KMnO4溶液应装在__________(填“酸式”或“碱式”)滴定管中。本次滴定 选择指示剂(填“需要”、“不需要”)。判断滴定达终点的现象是____ ___。
②若滴定管起始读数和终点读数如图所示,则酸性KMnO4的物质的量浓度为_ (填表达式)。

③若滴定完毕立即读数,测定的KMnO4溶液的浓度___(填“偏高”、“偏低”或“不变”)。
溶解度/(g/100g水)
| 温度/℃ 化合物 | 0 | 20 | 40 | 60 | 80 | 100 |
| NH4Cl | 29.3 | 37.2 | 45.8 | 55.3 | 65.6 | 77.3 |
| ZnCl2 | 343 | 395 | 452 | 488 | 541 | 614 |
| 化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
| Ksp近似值 | 10-17 | 10-17 | 10-39 |
回答下列问题:
①普通锌锰电池放电时发生的主要反应为:Zn+2NH4Cl+2MnO2=Zn(NH3)2Cl2+2MnOOH。该电池中,负极材料主要是________,正极发生的主要反应式是 。
②用废电池的锌皮制作七水合硫酸锌,需去除少量杂质铁,其方法是:加入稀硫酸和双氧水,溶解,
加碱调节溶液pH,使溶液中氢氧根离子浓度达到 mol/L,铁刚好完全沉淀(离子浓度小于1×10-5mol/L时,即可认为该离子沉淀完全)。继续加碱调节pH为 ,锌开始沉淀(假定Zn2+浓度为0.1mol/L)。
(2)在分析化学中常用Na2C2O4晶体(溶液无色)作为基准物质测定KMnO4溶液的浓度。在H2SO4溶液中,反应如下:2MnO+5C2O+16H+
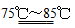 2Mn2+(溶液无色)+10CO2↑+8H2O。
2Mn2+(溶液无色)+10CO2↑+8H2O。①若将W g Na2C2O4配成100 mL标准溶液,移取20.00 mL置于锥形瓶中,则酸性KMnO4溶液应装在__________(填“酸式”或“碱式”)滴定管中。本次滴定 选择指示剂(填“需要”、“不需要”)。判断滴定达终点的现象是____ ___。
②若滴定管起始读数和终点读数如图所示,则酸性KMnO4的物质的量浓度为_ (填表达式)。

③若滴定完毕立即读数,测定的KMnO4溶液的浓度___(填“偏高”、“偏低”或“不变”)。
您最近一年使用:0次



