1 . 常温下,向浓度相等的甲酸( )和醋酸(
)和醋酸( )的混合溶液中滴加氨水,溶液中
)的混合溶液中滴加氨水,溶液中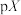 [
[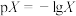 ,
, 、
、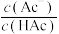 、
、 ]与
]与 的关系如图所示。下列叙述错误的是
的关系如图所示。下列叙述错误的是
 )和醋酸(
)和醋酸( )的混合溶液中滴加氨水,溶液中
)的混合溶液中滴加氨水,溶液中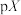 [
[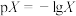 ,
, 、
、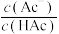 、
、 ]与
]与 的关系如图所示。下列叙述错误的是
的关系如图所示。下列叙述错误的是
A. 代表 代表 与 与 的变化关系 的变化关系 |
B.常温下, |
C.向 溶液中滴加氨水至Q点: 溶液中滴加氨水至Q点: |
D.上述反应中,最先生成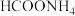 和 和 |
您最近一年使用:0次
2024-06-01更新
|
152次组卷
|
3卷引用:2024届河北省邯郸市高三下学期第四次调研检测化学试卷
2 . 饱和 溶液中,
溶液中,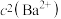 随
随 而变化,在
而变化,在 温度下,
温度下,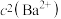 与
与 关系如右图所示。下列说法错误的是
关系如右图所示。下列说法错误的是
 溶液中,
溶液中,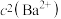 随
随 而变化,在
而变化,在 温度下,
温度下,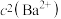 与
与 关系如右图所示。下列说法错误的是
关系如右图所示。下列说法错误的是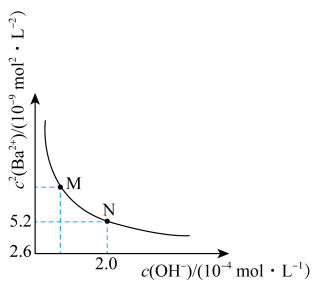
A. 的溶度积 的溶度积 |
B.若忽略 的第二步水解, 的第二步水解,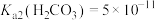 |
C.饱和 溶液中 溶液中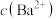 随 随 增大而减小 增大而减小 |
D. 点溶液中: 点溶液中: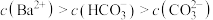 |
您最近一年使用:0次
3 . 室温下,调节MgCl2溶液、HF溶液、HA溶液[已知 ]的pH,测得溶液中pX[
]的pH,测得溶液中pX[ ;X代表
;X代表 、
、 ,
, ]随溶液pH的变化如图所示[已知
]随溶液pH的变化如图所示[已知 ]。下列叙述正确的是
]。下列叙述正确的是
 ]的pH,测得溶液中pX[
]的pH,测得溶液中pX[ ;X代表
;X代表 、
、 ,
, ]随溶液pH的变化如图所示[已知
]随溶液pH的变化如图所示[已知 ]。下列叙述正确的是
]。下列叙述正确的是 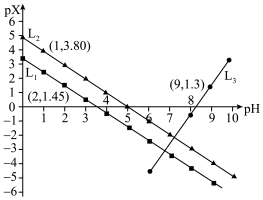
A. 代表溶液中 代表溶液中 随溶液pH的变化 随溶液pH的变化 |
B.浓度均为0.1 mol·L NaF、NaA的混合溶液中: NaF、NaA的混合溶液中: |
C.NaF、NaA的混合溶液中: |
D.由于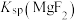 、 、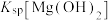 很接近,故 很接近,故 很难转化为 很难转化为 |
您最近一年使用:0次
2024-03-24更新
|
406次组卷
|
3卷引用:河北省邯郸市2024年高三下学期一模(第三次调研)考试化学试题
名校
解题方法
4 . 常温下,已知 溶液中含A元素的粒子浓度之和为
溶液中含A元素的粒子浓度之和为 ,溶液中各含A元素的粒子的pc-pOH关系所示。图中pc表示各含A粒子浓度的负对数(
,溶液中各含A元素的粒子的pc-pOH关系所示。图中pc表示各含A粒子浓度的负对数( ),pOH表示
),pOH表示 浓度的负对数[
浓度的负对数[ ];x、y、z三点的坐标:x(7.3,1.3),y(10.0,3.6),z(12.6,1.3)。下列说法正确的是
];x、y、z三点的坐标:x(7.3,1.3),y(10.0,3.6),z(12.6,1.3)。下列说法正确的是

 溶液中含A元素的粒子浓度之和为
溶液中含A元素的粒子浓度之和为 ,溶液中各含A元素的粒子的pc-pOH关系所示。图中pc表示各含A粒子浓度的负对数(
,溶液中各含A元素的粒子的pc-pOH关系所示。图中pc表示各含A粒子浓度的负对数( ),pOH表示
),pOH表示 浓度的负对数[
浓度的负对数[ ];x、y、z三点的坐标:x(7.3,1.3),y(10.0,3.6),z(12.6,1.3)。下列说法正确的是
];x、y、z三点的坐标:x(7.3,1.3),y(10.0,3.6),z(12.6,1.3)。下列说法正确的是
A.曲线①表示 随pOH的变化 随pOH的变化 |
| B.x点到z点对应的变化过程中,溶液中水的电离程度先减小再增大 |
C.pH=4的溶液中: |
D.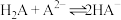 的平衡常数的数量级为 的平衡常数的数量级为 |
您最近一年使用:0次
2024-02-23更新
|
314次组卷
|
3卷引用:河北省邯郸市2024届高三第二次调研监测化学试题
11-12高二上·辽宁沈阳·期中
5 . 高氯酸、硫酸、硝酸和盐酸都是强酸,其酸性在水溶液中差别不大。以下是某温度下这四种酸在冰醋酸中的电离常数:
由以上表格中数据判断以下说法不正确的是
| 酸 | HClO4 | H2SO4 | HCl | HNO3 |
| Ka | 1.6× 10-5mol·L-1 | 6.3× 10-9mol·L-1 | 1.6× 10-9mol·L-1 | 4.2× 10-10mol·L-1 |
| A.在冰醋酸中这四种酸都没有完全电离 |
| B.在冰醋酸中高氯酸是这四种酸中酸性最强的酸 |
C.在冰醋酸中硫酸的电离方程式为H2SO4=2H++SO |
| D.水对这四种酸的强弱没有区分能力,但冰醋酸可以区分这四种酸的强弱 |
您最近一年使用:0次
2023-08-27更新
|
801次组卷
|
52卷引用:河北省邯郸市大名县第一中学2020-2021学年高二上学期10月月考化学试题(普通版)
河北省邯郸市大名县第一中学2020-2021学年高二上学期10月月考化学试题(普通版)(已下线)2011-2012学年辽宁省沈阳四校协作体高二上学期期中考试化学试卷(已下线)2012-2013学年江西省赣州市十一县(市)高二上学期期中联考化学试卷(已下线)2015安徽望江中学同步课时练(人教选修4)3.1弱电解质的电离试卷(已下线)2014秋湖北省武汉市部分重点中学高二上学期期中联考化学试卷2014-2015湖南省益阳市箴言中学高二1月月考化学试卷2015-2016学年河北省冀州中学高二上第二次月考化学试卷2015-2016学年吉林实验中学高二上学期期中考试化学试卷12015-2016学年吉林实验中学高二上学期期中考试化学试卷22015-2016学年内蒙古赤峰二中高二上第二次月考化学试卷2015-2016学年福建晨曦、冷曦、正曦、岐滨四校高二上联考化学卷2015-2016学年江西省丰城中学高二上学期期中考试化学试卷江西省南康中学2017-2018学年高二上学期第一次月考化学试题湖南省祁阳四中2018届高三第四次月考化学试题(已下线)2018年10月28日 《每日一题》人教选修4--每周一测江西省上高县第二中学2019-2020学年高二上学期第一次月考化学试题河北省承德第一中学2020届高三10月月考化学试题江苏省南京师大苏州实验学校2019-2020学年高二9月月考化学试题(已下线)上海市徐汇区2010届高三上学期期末学习能力诊断化学试题人教版(2019)高二选择性必修第一册 第三章 水溶液中的离子反应与平衡 第一节 电离平衡 教材帮湖南省临澧县第一中学2020-2021学年高二上学期期中考试化学试题(选考)重庆市凤鸣山中学2020-2021学年高二上学期期中考试化学试题(已下线)第03章 水溶液中的离子反应与平衡(A卷基础强化篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材人教版)湖南省临澧县第一中学2020-2021学年高二下学期阶段性考试(二)化学试题福建省莆田第十五中学2019-2020学年高二下学期期末考试化学试题河北正定中学2020-2021学年高二上学期第一次半月考化学试题吉林省长春外国语学校2021-2022学年高二上学期第一次月考化学试题湖北省黄冈市浠水县实验高级中学2021-2022学年高二上学期九月月考化学试题(已下线)专题3.1 电离平衡(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)(已下线)3.1.2 电离平衡常数-2021-2022学年高二化学课后培优练(人教版选修4)山东省济南市第一中学2021-2022学年高二上学期期中考试化学试题(已下线)必考点05 电离平衡-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版选择性必修1)广东省高州市校际2021-2022学年高二11月联考化学试题陕西省西安市第一中学2021-2022学年高二上学期期中考试化学试题河北省唐山市第十一中学2021-2022学年高二上学期期中考试化学试题安徽省马鞍山市第二中学2021-2022学年高二上学期期中考试化学试题陕西省西安中学2021-2022学年高二上学期期末考试化学试题新疆生产建设兵团第二师八一中学2021-2022学年高二上学期期中考试化学试题河南省濮阳市第一高级中学2021-2022学年高二下学期期中考试化学试题海南省琼海市嘉积第二中学2021-2022学年高二下学期教学质量监测(段考)化学科试题 四川省广安市第二中学校2022-2023学年高二上学期11月期中考试化学试题江苏省宿迁市北大附属宿迁实验学校2022-2023学年高二上学期11月期中化学试题广东番禺中学2022-2023学年高二下学期科开学考试化学试题作业(十八) 弱电解质的电离平衡河北省新乐市第一中学2022-2023学年高二上学期11月期中考试化学试题浙江省浙南名校联盟2023-2024学年高二上学期10月联考化学试题【精品卷】3.1.3电离平衡常数课堂例题-人教版2023-2024学年选择性必修1(已下线)BBWYhjhx1106.pdf(已下线)选择题16-20广东省清远市阳山县南阳中学2023-2024学年高二上学期第二次月考(期中)化学试题湖南省郴州市明星高级中学2023-2024学年高二上学期期中考试化学试题甘肃省白银市会宁县第三中学2023-2024学年高二上学期期中考试化学试题
6 . 某酸 溶液中含X粒子的物质的量分数与pH的关系如图所示。下列说法正确的是
溶液中含X粒子的物质的量分数与pH的关系如图所示。下列说法正确的是

 溶液中含X粒子的物质的量分数与pH的关系如图所示。下列说法正确的是
溶液中含X粒子的物质的量分数与pH的关系如图所示。下列说法正确的是
A.已知亚磷酸的结构为 ,则X可能为P ,则X可能为P |
B.在 溶液中滴加少量 溶液中滴加少量 溶液,发生反应的离子方程式为 溶液,发生反应的离子方程式为 |
C. 溶液中有 溶液中有 |
D. 溶液中有 溶液中有 |
您最近一年使用:0次
2023-04-19更新
|
677次组卷
|
2卷引用:河北省邯郸市2023届高三二模化学试题
7 . 常温下,向100 mL0.1 mol·L-1的某二元酸H2A溶液中滴加0.1 mol·L-1的NaOH溶液,溶液中含A微粒的物质的量浓度随溶液pH的变化如图所示,下列说法正确的是


| A.该二元酸的第一步电离是完全的 |
| B.H2A的第二步电离平衡常数的数量级为10-5 |
| C.pH=3时,c(HA- )>c(H2A)>c(A2- ) |
| D.当加入100mLNaOH溶液时,溶液显碱性 |
您最近一年使用:0次
2023-02-11更新
|
151次组卷
|
2卷引用:河北省邯郸市2022-2023学年高二上学期期末考试化学试题
名校
8 . 根据下列图示得出的结论正确的是。


A.图甲表示常温下稀释 的 的 溶液和氨水时溶液 溶液和氨水时溶液 的变化,曲线II表示氨水 的变化,曲线II表示氨水 |
B.图乙表示反应 在其他条件不变的情况下,改变起始 在其他条件不变的情况下,改变起始 的物质的量,平衡时 的物质的量,平衡时 的体积分数变化情况,由图可知 的体积分数变化情况,由图可知 的转化率: 的转化率: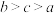 |
C.图丙表示相同浓度的 溶液与 溶液与 溶液中分子浓度的分数[ 溶液中分子浓度的分数[ 或 或 ]随 ]随 的变化曲线,可得出 的变化曲线,可得出 酸性较强 酸性较强 |
D.图丁是用 溶液滴定等浓度 溶液滴定等浓度 的滴定曲线 的滴定曲线 ,图中 ,图中 |
您最近一年使用:0次
2023-01-14更新
|
495次组卷
|
7卷引用:河北省邯郸市魏县2022-2023学年高二上学期期末考试化学试题
河北省邯郸市魏县2022-2023学年高二上学期期末考试化学试题江苏省南通市海安市2022-2023学年高二上学期1月期末考试化学试题 山东省青岛第二中学2022-2023学年高二下学期期初考试化学试题(已下线)专题09 水溶液中的离子平衡-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(江苏专用)(已下线)专题08 化学反应速率与化学平衡-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(江苏专用)江苏省扬州中学2023-2024学年高二上学期12月月考化学试题江苏省苏州市昆山中学2023-2024学年高二上学期期中考试化学试卷
10-11高二下·江苏南京·期中
名校
9 . 常温下,体积相同、pH相同的盐酸和醋酸两种溶液中,下列两者的量相同的是
| A.与Zn反应开始时的反应速率 | B.酸的物质的量浓度 |
| C.电离程度 | D.与足量的Zn反应产生H2的量 |
您最近一年使用:0次
2022-12-11更新
|
313次组卷
|
6卷引用:2015-2016学年河北省成安县第一中学高二12月月考化学试卷
名校
解题方法
10 . 甘油硼酸是一种一元有机弱酸,可简写为HM。常温下,向20 mL 0.2 mol·L-1HM溶液中逐滴加入浓度为0.2 mol·L-1的NaOH溶液,溶液中 、pH、中和率(中和率=
、pH、中和率(中和率= )的变化如图所示。
)的变化如图所示。

下列说法正确的是
 、pH、中和率(中和率=
、pH、中和率(中和率= )的变化如图所示。
)的变化如图所示。
下列说法正确的是
| A.HM的电离常数数量级为10-5 |
| B.a点时,c(HM)+c(M- )= 2c(Na+ ) |
| C.b点时,c(M- )>c(Na +)>c(H+ )>c(OH- ) |
| D.溶液中水的电离程度: c点<b点 |
您最近一年使用:0次
2022-05-26更新
|
371次组卷
|
2卷引用:河北省邯郸市大名县第一中学2022-2023学年高三上学期第一次月考化学试题



