1 . 根据表格中电离常数判断下列反应可以发生的是
| 化学式 | HClO | H2CO3 | H2SO3 |
| 电离平衡常数(25℃) | 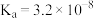 | 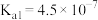 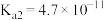 | 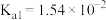 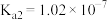 |
A.NaClO溶液中通入少量CO2: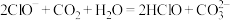 |
B.Na2SO3溶液中通入足量CO2: |
C.Na2CO3溶液中通入少量SO2: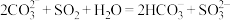 |
D.NaClO溶液中通入足量SO2: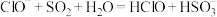 |
您最近一年使用:0次
2 . 已知:25℃时, 、HClO、
、HClO、 ,
, 的电离平衡常数如表所示,
的电离平衡常数如表所示, 。请回答下列问题。
。请回答下列问题。
(1)等浓度的四种酸溶液的酸性由强到弱的顺序是_________ 。
(2)写出HClO在水中的电离方程式:_________ 。
(3)将10 mL 0.1 mol⋅L
 溶液逐滴滴入50 mL 0.1 mol⋅L
溶液逐滴滴入50 mL 0.1 mol⋅L
 溶液中,现象为
溶液中,现象为_________ ,写出反应的离子方程式_________ 。
(4)若将少量的 气体通入NaClO溶液中,反应的离子方程式为
气体通入NaClO溶液中,反应的离子方程式为_________ 。
(5)25℃时,取50 mL 0.1 mol⋅L
 溶液,将其稀释100倍。
溶液,将其稀释100倍。
①稀释前 的电离度(
的电离度(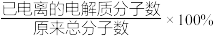 )约为
)约为_________ (保留三位有效数字)%。
②在稀释过程中,随着 浓度的降低,
浓度的降低, 逐渐
逐渐_________ (填“增大”、“减小”或“不变”)。
 、HClO、
、HClO、 ,
, 的电离平衡常数如表所示,
的电离平衡常数如表所示, 。请回答下列问题。
。请回答下列问题。| 物质 |  | HClO |  |  |
| 电离平衡常数 |  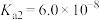 | 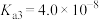 |   |  |
(2)写出HClO在水中的电离方程式:
(3)将10 mL 0.1 mol⋅L

 溶液逐滴滴入50 mL 0.1 mol⋅L
溶液逐滴滴入50 mL 0.1 mol⋅L
 溶液中,现象为
溶液中,现象为(4)若将少量的
 气体通入NaClO溶液中,反应的离子方程式为
气体通入NaClO溶液中,反应的离子方程式为(5)25℃时,取50 mL 0.1 mol⋅L

 溶液,将其稀释100倍。
溶液,将其稀释100倍。①稀释前
 的电离度(
的电离度(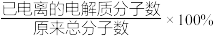 )约为
)约为②在稀释过程中,随着
 浓度的降低,
浓度的降低, 逐渐
逐渐
您最近一年使用:0次
2022-11-11更新
|
254次组卷
|
3卷引用:贵州省遵义市2022-2023学年高二上学期期中考试化学试题
3 . 硫化钠( )是一种重要的化工原料,生产方法有:硫化氢(
)是一种重要的化工原料,生产方法有:硫化氢( )吸收法,该方法是用NaOH溶液或
)吸收法,该方法是用NaOH溶液或 溶液吸收
溶液吸收 ,已知酸性:
,已知酸性: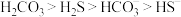 ;下列化学反应表示正确的是
;下列化学反应表示正确的是
 )是一种重要的化工原料,生产方法有:硫化氢(
)是一种重要的化工原料,生产方法有:硫化氢( )吸收法,该方法是用NaOH溶液或
)吸收法,该方法是用NaOH溶液或 溶液吸收
溶液吸收 ,已知酸性:
,已知酸性: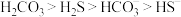 ;下列化学反应表示正确的是
;下列化学反应表示正确的是A. 溶液呈碱性: 溶液呈碱性: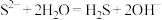 |
B. 与NaOH溶液反应: 与NaOH溶液反应: |
C. 与 与 溶液反应: 溶液反应: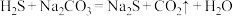 |
D.用足量炭还原硫酸钡制取硫化钡: |
您最近一年使用:0次
2022-11-11更新
|
198次组卷
|
3卷引用:江苏省连云港市2022-2023学年高三上学期期中调研考试化学试题
4 . 已知25℃时,几种弱酸的电离平衡常数如下:HCOOH(甲酸):K=1.77×10-4,HCN(氢氰酸):K=4.9×10-10,H2CO3:Ka1=4.4×10-7, Ka2=4.7×10-11,则下列说法不正确的是
| A.25℃时,相同浓度的HCOOH和 HCN溶液的pH:HCOOH<HCN |
| B.一定条件下,反应 Na2CO3 + HCN = NaHCO3 + NaCN可以发生 |
C.一定条件下,反应CO2 + H2O + 2CN- =  + 2HCN可以发生 + 2HCN可以发生 |
| D.向碳酸氢钠溶液中加入甲酸溶液有气泡产生 |
您最近一年使用:0次
解题方法
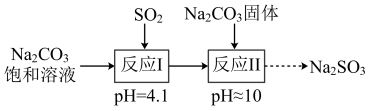
5 . 实验室制备亚硫酸钠的过程如下:将饱和碳酸钠溶液加热到40°C,通入二氧化硫至饱和后,再加入碳酸钠固体,在避免与空气接触的情况下结晶而制得。
(已知:H2SO3:Ka1=1.5×10-2;Ka2=6.3×10-8;H2CO3:Ka1=4.4×10-7;Ka2=4.7×10-11)
下列说法正确的是
(已知:H2SO3:Ka1=1.5×10-2;Ka2=6.3×10-8;H2CO3:Ka1=4.4×10-7;Ka2=4.7×10-11)
下列说法正确的是

A.饱和Na2CO3溶液中存在c(Na+)+c(H+)=c(H2CO3)+c(HCO )+c(CO )+c(CO ) ) |
B.“反应I”的离子方程式为2CO +SO2+H2O=2HCO +SO2+H2O=2HCO +SO +SO |
C.“反应I”得到的溶液中有c(HSO )>c(SO )>c(SO ) ) |
| D.“反应II”中有大量气体产生 |
您最近一年使用:0次
名校
6 . 氧化铋( )俗称铋黄,是制作防火纸的材料之一。以白色难溶物氯氧化铋(
)俗称铋黄,是制作防火纸的材料之一。以白色难溶物氯氧化铋( )为原料转型脱氯制备氧化铋的方法如下:
)为原料转型脱氯制备氧化铋的方法如下:
步骤1:准确称取3.0g ,先与25mL3
,先与25mL3 脱氯剂
脱氯剂 溶液混合,加入氨水至
溶液混合,加入氨水至 ,50℃下搅拌40min可得前驱体
,50℃下搅拌40min可得前驱体 (难溶于水),反应装置如图所示(加热装置已略去);
(难溶于水),反应装置如图所示(加热装置已略去);

步骤2:将前驱体干燥后灼烧,可得 。
。
回答下列问题:
(1) 的原子序数为83,则
的原子序数为83,则 在元素周期表中的位置是
在元素周期表中的位置是_______ 。
(2)试剂X的目的为防止挥发的氨气进入空气中,试剂X可选用_______ (填化学式)。
(3) 溶液过量的原因是
溶液过量的原因是_______ (用平衡移动原理解释),步骤1中生成 的化学方程式为
的化学方程式为_______ 。
(4)反应后,分离出三颈烧瓶的前驱体,用蒸馏水洗涤前驱体2~3次,将滤液和洗涤液合并,稀释至100 ,取25.00
,取25.00 于锥形瓶中,滴入2滴
于锥形瓶中,滴入2滴 溶液作指示剂,再用0.1
溶液作指示剂,再用0.1 标准
标准 溶液滴定,平行测定三组。
溶液滴定,平行测定三组。
①分离前驱体的操作名称是_______ ;盛装标准 溶液应选用
溶液应选用_______ (填“酸式”或“碱式”)滴定管。
②若消耗 标准液的平均体积为a
标准液的平均体积为a ,则脱氯率为
,则脱氯率为_______ %(用含a的代数式表示)。
(5)灼烧 时用到的硅酸盐制品有
时用到的硅酸盐制品有_______ 、酒精灯、玻璃棒、泥三角。
 )俗称铋黄,是制作防火纸的材料之一。以白色难溶物氯氧化铋(
)俗称铋黄,是制作防火纸的材料之一。以白色难溶物氯氧化铋( )为原料转型脱氯制备氧化铋的方法如下:
)为原料转型脱氯制备氧化铋的方法如下:步骤1:准确称取3.0g
 ,先与25mL3
,先与25mL3 脱氯剂
脱氯剂 溶液混合,加入氨水至
溶液混合,加入氨水至 ,50℃下搅拌40min可得前驱体
,50℃下搅拌40min可得前驱体 (难溶于水),反应装置如图所示(加热装置已略去);
(难溶于水),反应装置如图所示(加热装置已略去);
步骤2:将前驱体干燥后灼烧,可得
 。
。回答下列问题:
(1)
 的原子序数为83,则
的原子序数为83,则 在元素周期表中的位置是
在元素周期表中的位置是(2)试剂X的目的为防止挥发的氨气进入空气中,试剂X可选用
(3)
 溶液过量的原因是
溶液过量的原因是 的化学方程式为
的化学方程式为(4)反应后,分离出三颈烧瓶的前驱体,用蒸馏水洗涤前驱体2~3次,将滤液和洗涤液合并,稀释至100
 ,取25.00
,取25.00 于锥形瓶中,滴入2滴
于锥形瓶中,滴入2滴 溶液作指示剂,再用0.1
溶液作指示剂,再用0.1 标准
标准 溶液滴定,平行测定三组。
溶液滴定,平行测定三组。①分离前驱体的操作名称是
 溶液应选用
溶液应选用②若消耗
 标准液的平均体积为a
标准液的平均体积为a ,则脱氯率为
,则脱氯率为(5)灼烧
 时用到的硅酸盐制品有
时用到的硅酸盐制品有
您最近一年使用:0次
2022-09-01更新
|
188次组卷
|
2卷引用:河北省省级联测2022-2023学年高三上学期第一次月考化学试题
7 . 已知下面三个数据:7.2×10−4、4.6×10−4、4.9×10−10分别是下列有关的三种酸的电离平衡常数,若已知下列反应可以发生:NaCN+HNO2=HCN+NaNO2; NaNO2+HF=HNO2+NaF,由此可判断下列叙述不正确的是
| A.相同浓度的三种酸中, c(H+)最小的是HF |
| B.K(HF)=7.2×10−4 |
| C.HF和NaCN可以生成HCN |
| D.相同温度下, K(HCN)<K(HNO2)<K(HF) |
您最近一年使用:0次
2022-08-18更新
|
450次组卷
|
2卷引用:黑龙江省齐齐哈尔市恒昌中学校2021-2022学年高二上学期期中考试化学试题
2021高三·全国·专题练习
解题方法
8 . 电离平衡右移,电解质分子的浓度一定减小,离子浓度一定增大。( )
您最近一年使用:0次
2022-07-10更新
|
264次组卷
|
7卷引用:考点23 弱电解质的电离-备战2022年高考化学一轮复习考点帮(全国通用)
(已下线)考点23 弱电解质的电离-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点26 弱电解质的电离-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第八章 水溶液中的离子反应与平衡 第46讲 弱电解质的电离平衡(已下线)考点26 弱电解质的电离(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)专题12 水溶液中的离子反应与平衡-2023年高考化学真题题源解密(全国通用)第三章 水溶液中的离子反应与平衡 第一节 电离平衡第1讲 弱电解质的电离平衡
名校
解题方法
9 . 下列离子方程式错误的是
A.向饱和碳酸钠溶液中通入过量二氧化碳:2Na++CO +CO2+H2O=2NaHCO3↓ +CO2+H2O=2NaHCO3↓ |
B.氢氧化钠溶液吸收处理SO2尾气:2OH-+SO2=SO +H2O +H2O |
C.漂白液中通入少量CO2:2ClO-+CO2+H2O=CO +2HClO +2HClO |
| D.将过量氯气通入FeI2溶液中:2Fe2++4I-+3Cl2=2I2+2Fe3++6Cl- |
您最近一年使用:0次
2022-05-14更新
|
1418次组卷
|
4卷引用:湖南省株洲市攸县第一中学2021-2022学年高三下学期期中考试化学试题
名校
10 . 根据表中提供的数据,判断下列离子方程式或化学方程式书写正确的是
| 化学式 | HClO | H2CO3 |
| 电离常数/mol·L-1 | K=3×10-8 | K1=4×10-7 K2=4×10-11 |
A.向Na2CO3溶液中滴加少量氯水:CO +Cl2+H2O=HCO +Cl2+H2O=HCO +Cl-+HClO +Cl-+HClO |
B.向NaHCO3溶液中滴加少量氯水:2HCO +Cl2=Cl-+ClO-+2CO2↑+H2O +Cl2=Cl-+ClO-+2CO2↑+H2O |
C.向Na2CO3溶液中滴加过量HClO:CO +2HClO=2ClO-+H2O+CO2↑ +2HClO=2ClO-+H2O+CO2↑ |
| D.向NaClO溶液中通入过量CO2:CO2+NaClO+H2O=NaHCO3+HClO |
您最近一年使用:0次
2022-03-29更新
|
330次组卷
|
2卷引用:江西省宜春市铜鼓中学2021-2022学年高二下学期开学考化学试题



