名校
1 . 已知联氨( )为二元弱碱,常温下将盐酸滴加到联氨(
)为二元弱碱,常温下将盐酸滴加到联氨( )的水溶液中,混合溶液中微粒的物质的量分数
)的水溶液中,混合溶液中微粒的物质的量分数 随
随 变化的关系如图所示。下列叙述错误的是
变化的关系如图所示。下列叙述错误的是
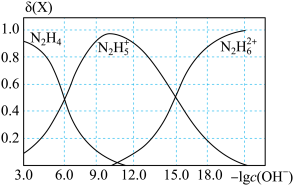
 )为二元弱碱,常温下将盐酸滴加到联氨(
)为二元弱碱,常温下将盐酸滴加到联氨( )的水溶液中,混合溶液中微粒的物质的量分数
)的水溶液中,混合溶液中微粒的物质的量分数 随
随 变化的关系如图所示。下列叙述错误的是
变化的关系如图所示。下列叙述错误的是
A. |
B.反应 的 的 (已知 (已知 ) ) |
C.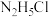 浴液中存在: 浴液中存在: |
D.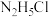 溶液中: 溶液中: |
您最近一年使用:0次
名校
2 . 某二元酸(用H2X表示)在水中的电离方程式是:H2X=H++HX-,HX- H++X2-。25℃时,向20.00mL 0.1molL H2X溶液中滴入0.1mol/L NaOH溶液,pOH水表示溶液中由水电离出的c(OH-)水的负对数[-lgc(OH-)水],pOH水与所加NaOH溶液体积的关系如图所示。下列说法错误的是
H++X2-。25℃时,向20.00mL 0.1molL H2X溶液中滴入0.1mol/L NaOH溶液,pOH水表示溶液中由水电离出的c(OH-)水的负对数[-lgc(OH-)水],pOH水与所加NaOH溶液体积的关系如图所示。下列说法错误的是

 H++X2-。25℃时,向20.00mL 0.1molL H2X溶液中滴入0.1mol/L NaOH溶液,pOH水表示溶液中由水电离出的c(OH-)水的负对数[-lgc(OH-)水],pOH水与所加NaOH溶液体积的关系如图所示。下列说法错误的是
H++X2-。25℃时,向20.00mL 0.1molL H2X溶液中滴入0.1mol/L NaOH溶液,pOH水表示溶液中由水电离出的c(OH-)水的负对数[-lgc(OH-)水],pOH水与所加NaOH溶液体积的关系如图所示。下列说法错误的是
| A.C、E两点溶液:C点显中性,E点显碱性 |
| B.B点溶液中:c(X2-)>c(H+)-c(OH-) |
| C.D点溶液中:c(Na+)+c(HX-)+c(X2-)=0.10 mo/L |
D.图中C点至D点对应溶液中: 逐渐减小 逐渐减小 |
您最近一年使用:0次
3 . 常温下,用 氢氧化钠溶液滴定一定浓度的
氢氧化钠溶液滴定一定浓度的 溶液,溶液的
溶液,溶液的 与加入氢氧化钠溶液的体积
与加入氢氧化钠溶液的体积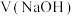 、
、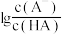 的关系如图.下列说法错误的是
的关系如图.下列说法错误的是

 氢氧化钠溶液滴定一定浓度的
氢氧化钠溶液滴定一定浓度的 溶液,溶液的
溶液,溶液的 与加入氢氧化钠溶液的体积
与加入氢氧化钠溶液的体积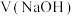 、
、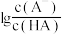 的关系如图.下列说法错误的是
的关系如图.下列说法错误的是
| A.从N点到P点,水的电离程度先增大后减小 |
B.M点对应的溶液中 |
C. 数量级为 数量级为 |
| D.滴定过程可采用酚酞作为指示剂 |
您最近一年使用:0次
4 . 阿伏加德罗常数符号为NA。关于100mL1mol/L的Fe2(SO4)3溶液,下列说法正确的是
| A.加NaOH溶液可制得Fe(OH)3胶粒数目为0.2NA |
| B.溶液中阳离子数目为0.2NA |
C.加Na2CO3溶液发生的反应为3 +2Fe3+=Fe2(CO3)3↓ +2Fe3+=Fe2(CO3)3↓ |
| D.Fe2(SO4)3溶液可用于止血 |
您最近一年使用:0次
解题方法
5 . 常温下,下列各组离子在指定溶液中能大量共存的是
| A.无色透明的溶液中:Fe3+、Mg2+、SCN-、Cl- |
B.pH=12的溶液中:K+、Na+、 、 、 |
C.c(Fe2+)=1mol/L的溶液中:K+、 、 、 、 、 |
D.能使甲基橙变红的溶液中:Na+、 、 、 、 、 |
您最近一年使用:0次
名校
解题方法
6 . 已知25 ℃时某些酸碱的电离常数见下表,回答下列问题:
(1)25℃将pH=4醋酸和pH=10氨水等体积混合,所得溶液pH___________ 7(填“>”、“<”或“=”);将pH=4醋酸和pH=4氢氟酸混合,则HF的电离程度___________ (填“增大”、“减小”或“不变”)。
(2)将2mol/LCH3COONa溶液与1mol/L盐酸等体积混合,该溶液中各离子浓度由大到小顺序为___________ 。
(3)(NH4)2CO3溶液显___________ 性(填“中”、“酸”或“碱”),写出(NH4)2CO3溶液的质子守恒表达式___________ 。
(4)向TiCl4中加大量水同时加热可制备TiO2·xH2O,写出该反应的化学方程式___________ 。
(5)已知100℃时,0.01 mol/L的NaHSO4溶液中水电离的c(H+)=10-10mol/L,该温度下将pH=5的NaHSO4溶液V1L与pH=8的Ba(OH)2溶液V2L混合,所得溶液pH=7,则V1:V2为___________ (忽略溶液混合时的体积变化)。
| 化学式 | CH3COOH | H2CO3 | HF | NH3·H2O |
| 电离常数 | 1.8×10-5 | Ka1:4.5×10-7、Ka2:4.7×10-11 | 6.3×10-4 | 1.8×10-5 |
(2)将2mol/LCH3COONa溶液与1mol/L盐酸等体积混合,该溶液中各离子浓度由大到小顺序为
(3)(NH4)2CO3溶液显
(4)向TiCl4中加大量水同时加热可制备TiO2·xH2O,写出该反应的化学方程式
(5)已知100℃时,0.01 mol/L的NaHSO4溶液中水电离的c(H+)=10-10mol/L,该温度下将pH=5的NaHSO4溶液V1L与pH=8的Ba(OH)2溶液V2L混合,所得溶液pH=7,则V1:V2为
您最近一年使用:0次
名校
解题方法
7 . 下表是25℃时弱酸的电离平衡常数和某些盐的溶度积常数。下列说法正确的是
| 化学式 | CH3COOH | HClO | FePO4 | Fe(OH)3 | AgCl |
| Ka或Ksp | Ka=1.8×10-5 | Ka=3.0×10-8 | Ksp=1.3×10-22 | Ksp=1.0×10-38 | Ksp=1.8×10-10 |
| A.AgCl在盐酸中的Ksp小于其在水中的Ksp |
| B.向饱和氯水中滴加NaOH溶液至溶液刚好呈中性时,c(Na+)=c(ClO-)+2c(HClO) |
| C.pH相同的①CH3COOK、②KOH、③KClO三种溶液中的c(K+):①>③>② |
| D.向浓度均为0.01mol/L的FeCl3两溶液中分别缓慢滴加浓度均为0.01 mol/LNa3PO4溶液和NaOH溶液,先生成Fe(OH)3沉淀 |
您最近一年使用:0次
名校
解题方法
8 . 下列有关电极方程式或离子方程式错误的是
A.碱性锌锰电池的正极反应: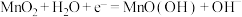 |
B.铅酸蓄电池充电时的阳极反应: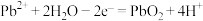 |
C. 悬浊液中加入浓 悬浊液中加入浓 溶液变澄清: 溶液变澄清: |
D. 加入水中: 加入水中: |
您最近一年使用:0次
9 . 设NA为阿伏加德罗常数的值,下列说法正确的是
| A.1 L0.1 mol·L-1AlCl3溶液中,N(Cl-)+N(Al3+)=0.4NA |
B.1 L0.2 mol·L-1NaHCO3溶液中,N( )+N( )+N( )+N(H2CO3)>0.2NA )+N(H2CO3)>0.2NA |
| C.常温下,1 LpH=1的硫酸溶液中,所含的H+总数为0.2NA |
| D.1 L0.1 mol·L-1NH4Cl溶液中,所含阳离子总数大于0.1NA |
您最近一年使用:0次
名校
解题方法
10 . 常温下,下列有关溶液的说法一定正确的是
A.NaHCO3溶液加水稀释,c(Na+)与c(HCO )的比值将减小 )的比值将减小 |
| B.pH=1的一元酸和pH=13的一元碱等体积混合后:c(OH-)=c(H+) |
C.0.1 mol·L-1硫酸铵溶液中:c(NH ) > c(SO ) > c(SO ) >c(H+)>c(OH-) ) >c(H+)>c(OH-) |
| D.0.1 mol·L-1硫化钠溶液中:c(OH-)=c(H+)+c(HS-)+c(H2S) |
您最近一年使用:0次



