1 . 完成下列问题。
(1) 水溶液呈酸性的原因是(用离子方程式表示):
水溶液呈酸性的原因是(用离子方程式表示):________ 。
(2)室温时, 的
的 溶液中由水电离出的
溶液中由水电离出的
______  。
。
(3)室温时, 的Ba(OH)2溶液,
的Ba(OH)2溶液,
________ 。
(4)室温下pH=3的 水溶液水电离的c(H+)
水溶液水电离的c(H+)______  。
。
(5)常温下pH=13的 溶液与pH=11
溶液与pH=11 溶液等体积混合,混合溶液pH=
溶液等体积混合,混合溶液pH=______ 。
(6)常温下0.1 的NH3·H2O,pH=11,则Kb=
的NH3·H2O,pH=11,则Kb=_______ ,常温下0.1 的CH3COOH溶液pH=3 ,则Ka=
的CH3COOH溶液pH=3 ,则Ka=_______ 。
(1)
 水溶液呈酸性的原因是(用离子方程式表示):
水溶液呈酸性的原因是(用离子方程式表示):(2)室温时,
 的
的 溶液中由水电离出的
溶液中由水电离出的
 。
。(3)室温时,
 的Ba(OH)2溶液,
的Ba(OH)2溶液,
(4)室温下pH=3的
 水溶液水电离的c(H+)
水溶液水电离的c(H+) 。
。(5)常温下pH=13的
 溶液与pH=11
溶液与pH=11 溶液等体积混合,混合溶液pH=
溶液等体积混合,混合溶液pH=(6)常温下0.1
 的NH3·H2O,pH=11,则Kb=
的NH3·H2O,pH=11,则Kb= 的CH3COOH溶液pH=3 ,则Ka=
的CH3COOH溶液pH=3 ,则Ka=
您最近一年使用:0次
2 . 部分弱电解质的电离常数如表所示。
下列说法错误的是
| 弱电解质 | HCOOH | HCN | H2CO3 |
| 电离常数(25℃) | Ka=1.8×10-4 | Ka=6.2×10-10 |  =4.5×10-7 =4.5×10-7 =4.7×10-11 =4.7×10-11 |
A.结合H+的能力: >CN-> >CN-> >HCOO- >HCOO- |
B.反应2CN-+H2O+CO2=2HCN+C 能发生 能发生 |
| C.中和等体积、等c(H+)的HCOOH和HCN,消耗NaOH的量前者小于后者 |
D.25℃时,反应HCOOH+CN- HCN+HCOO-的化学平衡常数约为2.9×105 HCN+HCOO-的化学平衡常数约为2.9×105 |
您最近一年使用:0次
3 . 常温下,取三份浓度均为 体积均为20mL的醋酸钠溶液,分别向其中滴加浓度均为
体积均为20mL的醋酸钠溶液,分别向其中滴加浓度均为 的氯化铵溶液、醋酸铵溶液和盐酸,滴加过程中溶液的pOH变化曲线如图所示
的氯化铵溶液、醋酸铵溶液和盐酸,滴加过程中溶液的pOH变化曲线如图所示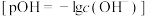 。
。
 体积均为20mL的醋酸钠溶液,分别向其中滴加浓度均为
体积均为20mL的醋酸钠溶液,分别向其中滴加浓度均为 的氯化铵溶液、醋酸铵溶液和盐酸,滴加过程中溶液的pOH变化曲线如图所示
的氯化铵溶液、醋酸铵溶液和盐酸,滴加过程中溶液的pOH变化曲线如图所示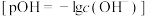 。
。
| A.曲线Ⅰ、Ⅱ、Ⅲ分别代表盐酸、氯化铵溶液和醋酸铵溶液 |
B.常温下 |
C.水的电离程度: |
D.d点存在: |
您最近一年使用:0次
解题方法
4 . 川西地区盐卤浓度较低,为了降低成本,侯德榜对原有的制碱方法——氨碱法(以食盐、氨气、二氧化碳为原料制取碳酸钠)进行改进。下列说法正确的是

| A.二氧化碳为含极性共价键的非极性分子 |
B.实验室可采用如图所示装置来制取 |
| C.工业上常采用电解饱和食盐水的方法来获得金属钠 |
D. 的 的 溶液中, 溶液中, |
您最近一年使用:0次
5 . 据图所示,下列说法正确的是
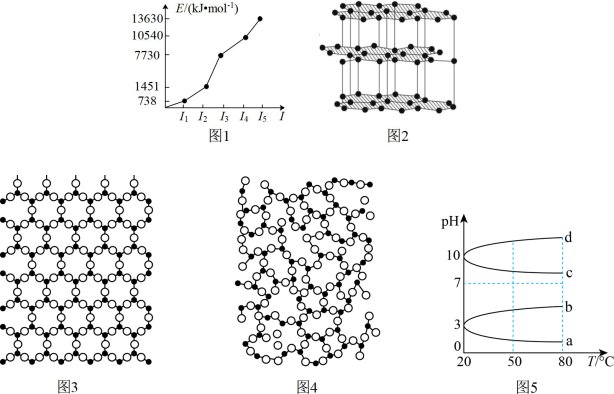
| A.短周期某元素的前5个电子的电离能如图1所示,则该元素是Be |
| B.图2表示石墨的层状结构,石墨为混合型晶体,其片层之间存在范德华力,因此具有导电性 |
C.已知图3、图4为 结构图,则可以用红外光谱法区别图3和图4 结构图,则可以用红外光谱法区别图3和图4 |
D.0.1mol/L 溶液的pH随温度变化的曲线如图5中a所示 溶液的pH随温度变化的曲线如图5中a所示 |
您最近一年使用:0次
名校
6 . 室温下,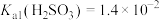 ,通过下列实验探究
,通过下列实验探究 、
、 溶液的性质:
溶液的性质:
实验1:用pH试纸测定0.1mol⋅L
 溶液的pH,测得pH约为10。
溶液的pH,测得pH约为10。
实验2:向0.1mol⋅L
 溶液中通入过量的
溶液中通入过量的 ,再滴入2滴紫色石蕊试剂,溶液呈红色。
,再滴入2滴紫色石蕊试剂,溶液呈红色。
实验3:向实验2溶液中逐滴滴加一定体积的盐酸,测得溶液pH为3。
实验4:向0.1mol⋅L
 溶液中加入等体积、等浓度的
溶液中加入等体积、等浓度的 溶液,产生白色沉淀。
溶液,产生白色沉淀。
下列说法正确的是
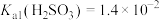 ,通过下列实验探究
,通过下列实验探究 、
、 溶液的性质:
溶液的性质:实验1:用pH试纸测定0.1mol⋅L

 溶液的pH,测得pH约为10。
溶液的pH,测得pH约为10。实验2:向0.1mol⋅L

 溶液中通入过量的
溶液中通入过量的 ,再滴入2滴紫色石蕊试剂,溶液呈红色。
,再滴入2滴紫色石蕊试剂,溶液呈红色。实验3:向实验2溶液中逐滴滴加一定体积的盐酸,测得溶液pH为3。
实验4:向0.1mol⋅L

 溶液中加入等体积、等浓度的
溶液中加入等体积、等浓度的 溶液,产生白色沉淀。
溶液,产生白色沉淀。下列说法正确的是
A.0.1mol⋅L 的 的 溶液中存在: 溶液中存在: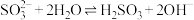 |
B.实验2可以得出: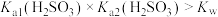 |
C.实验3得到的溶液中存在: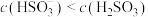 |
D.实验4中可推测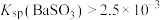 |
您最近一年使用:0次
解题方法
7 . 常温下,向0.1mol∙L-1二元弱酸H2A溶液中逐滴加入NaOH溶液,H2A、HA-、A2-的物质的量分数[已知 ]。随pH的变化如图所示。下列叙述正确的是
]。随pH的变化如图所示。下列叙述正确的是
 ]。随pH的变化如图所示。下列叙述正确的是
]。随pH的变化如图所示。下列叙述正确的是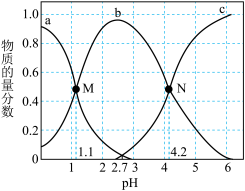
| A.a曲线代表A2-的物质的量分数随pH的变化 |
| B.溶液pH=1时的导电能力强于pH=6时的导电能力 |
| C.H2A第二步电离常数Ka2=10-4.2 |
| D.N点pH=4.2时,c(A2-)=c(HA-),溶液中不存在H2A分子 |
您最近一年使用:0次
8 . 常温下0.2mol•L-1NaHCO3溶液与0.1mol•L-1Na2CO3溶液等体积混合后,下列关于说法不正确 的是
A.NaHCO3=Na++ | B.c(Na+)>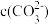 > > >c(OH-) >c(OH-) |
C.c(H+)+c(Na+)=c(OH-)+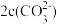 + + | D.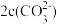 + + + +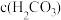 <c(Na+) <c(Na+) |
您最近一年使用:0次
9 . 在一定条件下,Na2S溶液存在水解平衡;S2-+H2O HS-+OH-。下列说法正确的是
HS-+OH-。下列说法正确的是
 HS-+OH-。下列说法正确的是
HS-+OH-。下列说法正确的是| A.加水稀释,平衡正移,HS-浓度增大 | B.升高温度, 减少 减少 |
| C.稀释溶液,水解平衡常数不变 | D.加入NaOH固体,溶液pH减小 |
您最近一年使用:0次
10 . 物质的量浓度相同的NaX、NaY和NaZ溶液,其pH依次为9、11、10,则HX、HY、HZ的电离平衡常数由大到小的顺序是
| A.HX,HZ, HY | B.HX,HY,HZ |
| C.HZ,HY,HX | D.HY,HZ,HX |
您最近一年使用:0次



