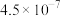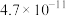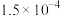名校
1 . 锑(Sb)可用作阻燃剂、电极材料、催化剂等物质的原材料。一种以辉锑矿(主要成分为 ,还含有
,还含有 、
、 、MgO、
、MgO、 等)为原料提取锑的工艺如下:
等)为原料提取锑的工艺如下:
回答下列问题:
(1)“溶浸”时氧化产物是S, 被氧化的化学方程式为
被氧化的化学方程式为________ 。
(2)“还原”时加入Sb的目的是将________ 还原,提高产物的纯度。
(3)“水解”时需控制溶液pH=2.5。
① 发生水解的离子方程式为
发生水解的离子方程式为________ 。
②下列能促进该水解反应的措施有________ (填字母)。
A.升高温度 B.增大 C.增大
C.增大 D.加入
D.加入 粉末
粉末
③为避免水解产物中混入 ,
, 浓度应小于
浓度应小于________  (已知
(已知 )。
)。
(4)向“滤液”中通入足量 ,再将滤液pH调至3.5,可析出
,再将滤液pH调至3.5,可析出 沉淀。将沉淀溶于浓盐酸后,产物可返回
沉淀。将沉淀溶于浓盐酸后,产物可返回________ 工序循环使用。
(5)Sb可由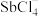 电解制得,阴极的电极反应式为
电解制得,阴极的电极反应式为________ 。
 ,还含有
,还含有 、
、 、MgO、
、MgO、 等)为原料提取锑的工艺如下:
等)为原料提取锑的工艺如下: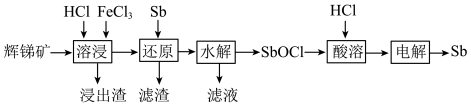
| 金属离子 |
|
|
|
|
开始沉淀时( )的pH )的pH | 2.2 | 3.7 | 7.5 | 9.6 |
完全沉淀时( )的pH )的pH | 3.2 | 4.7 | 9.0 | 11.1 |
(1)“溶浸”时氧化产物是S,
 被氧化的化学方程式为
被氧化的化学方程式为(2)“还原”时加入Sb的目的是将
(3)“水解”时需控制溶液pH=2.5。
①
 发生水解的离子方程式为
发生水解的离子方程式为②下列能促进该水解反应的措施有
A.升高温度 B.增大
 C.增大
C.增大 D.加入
D.加入 粉末
粉末③为避免水解产物中混入
 ,
, 浓度应小于
浓度应小于 (已知
(已知 )。
)。(4)向“滤液”中通入足量
 ,再将滤液pH调至3.5,可析出
,再将滤液pH调至3.5,可析出 沉淀。将沉淀溶于浓盐酸后,产物可返回
沉淀。将沉淀溶于浓盐酸后,产物可返回(5)Sb可由
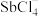 电解制得,阴极的电极反应式为
电解制得,阴极的电极反应式为
您最近一年使用:0次
名校
2 . 2023年杭州亚运会主火炬使用了零碳甲醇燃料,其制备共消耗了16万吨 。该甲醇的制备反应及副反应如下:
。该甲醇的制备反应及副反应如下:
i.

ii.
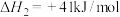
(1)研究表明,CO与 也能生成
也能生成 ,写出该反应的热化学方程式:
,写出该反应的热化学方程式:________ 。
(2)其他条件相同,当仅改变容器体积时,实验测得CO的平衡产率随着压强的增加而________ 。(填“增大”、“减小”或“不变”)
(3)在催化剂作用下,将 、
、 投入容积为1L的反应器,反应温度对
投入容积为1L的反应器,反应温度对 平衡转化率
平衡转化率 、
、 选择性Y(
选择性Y( )的影响如下。
)的影响如下。
240℃体系达到平衡时用时为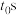 ,则
,则
________  。
。
240℃时反应i的化学平衡常数为________ (列出计算式即可,数据用小数表示)
(4)已知25℃时, 、
、 、HCN的电离平衡常数如下表。
、HCN的电离平衡常数如下表。
①25℃时,某 溶液的pH=8,关于此溶液中的微粒浓度,下列说法正确的是
溶液的pH=8,关于此溶液中的微粒浓度,下列说法正确的是________ 。
A.
B.
C.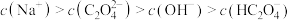
②将少量 溶液加入KCN溶液中,发生反应的离子方程式为
溶液加入KCN溶液中,发生反应的离子方程式为________ 。
(5) 电池可以实现对
电池可以实现对 的利用,该类电池放电的反应方程式为:
的利用,该类电池放电的反应方程式为: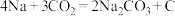 。其工作原理如图所示(固体沉积物中含两种固体)。请写出正极的反应方程式
。其工作原理如图所示(固体沉积物中含两种固体)。请写出正极的反应方程式________ 。
 。该甲醇的制备反应及副反应如下:
。该甲醇的制备反应及副反应如下:i.


ii.

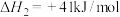
(1)研究表明,CO与
 也能生成
也能生成 ,写出该反应的热化学方程式:
,写出该反应的热化学方程式:(2)其他条件相同,当仅改变容器体积时,实验测得CO的平衡产率随着压强的增加而
(3)在催化剂作用下,将
 、
、 投入容积为1L的反应器,反应温度对
投入容积为1L的反应器,反应温度对 平衡转化率
平衡转化率 、
、 选择性Y(
选择性Y( )的影响如下。
)的影响如下。

240℃体系达到平衡时用时为
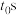 ,则
,则
 。
。240℃时反应i的化学平衡常数为
(4)已知25℃时,
 、
、 、HCN的电离平衡常数如下表。
、HCN的电离平衡常数如下表。
|
| HCN | |
|
|
|
|
|
|
| — |
 溶液的pH=8,关于此溶液中的微粒浓度,下列说法正确的是
溶液的pH=8,关于此溶液中的微粒浓度,下列说法正确的是A.

B.

C.
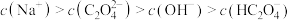
②将少量
 溶液加入KCN溶液中,发生反应的离子方程式为
溶液加入KCN溶液中,发生反应的离子方程式为(5)
 电池可以实现对
电池可以实现对 的利用,该类电池放电的反应方程式为:
的利用,该类电池放电的反应方程式为: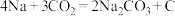 。其工作原理如图所示(固体沉积物中含两种固体)。请写出正极的反应方程式
。其工作原理如图所示(固体沉积物中含两种固体)。请写出正极的反应方程式
您最近一年使用:0次
名校
解题方法
3 . 室温下,通过下列实验探究某些碳酸盐溶液及碳酸氢盐溶液的性质。
已知: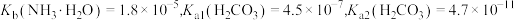 。
。
下列有关说法正确的是
已知:
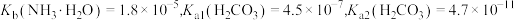 。
。| 实验 | 实验操作和现象 |
| 1 | 测量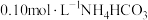 溶液的 溶液的 ,测得 ,测得 为 为 |
| 2 | 测量某浓度的 溶液的 溶液的 ,测得 ,测得 约为9.4 约为9.4 |
| 3 | 将两种浓度均为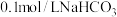 和 和 溶液等体积混合,测量其 溶液等体积混合,测量其 |
A.实验1溶液中: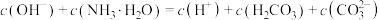 |
B.实验1测得的 值 值 |
C.实验2溶液中: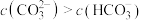 |
D.实验3所得溶液中: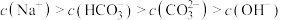 |
您最近一年使用:0次
4 . 在菠菜等植物中含有丰富的草酸,草酸对生命活动有重要影响。
 溶液的pH,溶液中的
溶液的pH,溶液中的 、
、 、
、 的物质的量分数
的物质的量分数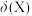 随pH的变化如图所示:
随pH的变化如图所示: )在水中的电离方程式:
)在水中的电离方程式:___________ 。
(2)要使溶液中草酸的电离程度增大,采取的措施为___________ 。(写两点)
(3)草酸溶液中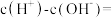
___________ 。(用含碳微粒表示)
(4)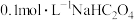 溶液中
溶液中
___________  。(填“<”“>”“=”)
。(填“<”“>”“=”)
(5) 时,
时,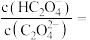
___________ 。

 溶液的pH,溶液中的
溶液的pH,溶液中的 、
、 、
、 的物质的量分数
的物质的量分数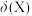 随pH的变化如图所示:
随pH的变化如图所示: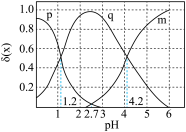
 )在水中的电离方程式:
)在水中的电离方程式:(2)要使溶液中草酸的电离程度增大,采取的措施为
(3)草酸溶液中
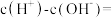
(4)
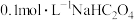 溶液中
溶液中
 。(填“<”“>”“=”)
。(填“<”“>”“=”)(5)
 时,
时,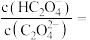
您最近一年使用:0次
5 . 研究水溶液中的粒子行为在研究中具有重要价值。
根据下表所列三种溶液在25℃时的相关数据,按要求填空:
(1)用离子方程式表示CH3COOH溶液显酸性的原因 ___________ 。
(2)比较溶液(Ⅱ)、(Ⅲ)中 的大小关系是(Ⅱ)
的大小关系是(Ⅱ)___________ (Ⅲ)(填“>”、“<”或“=”)。
(3)溶液(Ⅱ)中各离子浓度由大到小的顺序是___________ 。
(4)溶液(Ⅰ)和(Ⅱ)中由水电离出的 之比是
之比是 ___________ 。
根据下表所列三种溶液在25℃时的相关数据,按要求填空:
| 溶液 | 物质的量浓度 | pH | 用离子方程式表示溶液显酸性的原因 |
| (Ⅰ)CH3COOH | 0.1mol/L | 3 | _______ |
| (Ⅱ)NH4Cl | 0.1mol/L | 6 | / |
| (Ⅲ)NH4HSO4 | 0.1mol/L | 1 | / |
(2)比较溶液(Ⅱ)、(Ⅲ)中
 的大小关系是(Ⅱ)
的大小关系是(Ⅱ)(3)溶液(Ⅱ)中各离子浓度由大到小的顺序是
(4)溶液(Ⅰ)和(Ⅱ)中由水电离出的
 之比是
之比是
您最近一年使用:0次
6 . 已知25℃时,醋酸、碳酸、氢氰酸的电离平衡常数如表:
(1)写出碳酸的第一步电离方程式 ___________ 。
(2) 的盐酸与醋酸溶液分别加蒸馏水稀释至
的盐酸与醋酸溶液分别加蒸馏水稀释至 ,稀释后溶液的
,稀释后溶液的 ,前者
,前者 ___________ 后者(填“>”、“<”或“=”)。
(3)25℃时,等浓度的三种溶液a.NaCN溶液、b.Na2CO3溶液、c.CH3COONa溶液, 由大到小的顺序为
由大到小的顺序为 ___________  填序号
填序号 。
。
(4)25℃时,向 溶液中通入少量
溶液中通入少量 ,反应的离子方程式为
,反应的离子方程式为 ___________ 。
| 醋酸 | 碳酸 | 氢氰酸 |
 |  、 、 |  |
(2)
 的盐酸与醋酸溶液分别加蒸馏水稀释至
的盐酸与醋酸溶液分别加蒸馏水稀释至 ,稀释后溶液的
,稀释后溶液的 ,前者
,前者 (3)25℃时,等浓度的三种溶液a.NaCN溶液、b.Na2CO3溶液、c.CH3COONa溶液,
 由大到小的顺序为
由大到小的顺序为  填序号
填序号 。
。(4)25℃时,向
 溶液中通入少量
溶液中通入少量 ,反应的离子方程式为
,反应的离子方程式为
您最近一年使用:0次
7 . 写出下列离子方程式:
(1)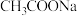 溶液呈碱性的原因:
溶液呈碱性的原因:___________ 。
(2) 溶液呈酸性的原因:
溶液呈酸性的原因:___________ 。
(3)泡沫灭火器(碳酸氢钠和硫酸铝)的原理:___________ 。
(1)
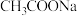 溶液呈碱性的原因:
溶液呈碱性的原因:(2)
 溶液呈酸性的原因:
溶液呈酸性的原因:(3)泡沫灭火器(碳酸氢钠和硫酸铝)的原理:
您最近一年使用:0次
名校
8 . 下列说法正确的是
A. 溶液: 溶液: |
B.常温下 溶液的 溶液的 ,该溶液中 ,该溶液中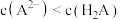 |
C.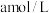 的 的 溶液与 溶液与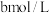 的 的 溶液等体积混合,所得溶液中 溶液等体积混合,所得溶液中 ,则a一定小于b ,则a一定小于b |
D.将pH均为a的氢氧化钠溶液和氨水分别加水稀释100倍,pH变为b和c,则a、b、c的大小关系是: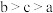 |
您最近一年使用:0次
解题方法
9 . 金属钛( )广泛应用于航空、军工、医疗等领域。某火电厂粉煤灰(主要成分为
)广泛应用于航空、军工、医疗等领域。某火电厂粉煤灰(主要成分为 、
、 、
、 、
、 、
、 、
、 等)的综合利用具有重要的经济价值和社会效益。工艺流程如下:
等)的综合利用具有重要的经济价值和社会效益。工艺流程如下: 形式存在,易水解;
形式存在,易水解;
②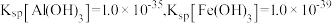 。
。
回答下列问题:
(1)基态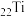 原子有
原子有_______ 个未成对电子,有_______ 个运动状态不同的电子。
(2)“酸浸”时,若要提高浸取速率,可采取的措施是_______ (任写一条)
(3)操作Ⅱ中加热将 水解得
水解得 ,写出其反应的离子方程式:
,写出其反应的离子方程式:_______ 。
(4)由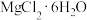 晶体得到无水
晶体得到无水 ,需要
,需要_______ 氛围中加热。
(5)为了使滤渣2沉淀完全(离子浓度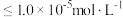 时认为沉淀完全),需“调
时认为沉淀完全),需“调 ”最小为
”最小为_______ 。
 )广泛应用于航空、军工、医疗等领域。某火电厂粉煤灰(主要成分为
)广泛应用于航空、军工、医疗等领域。某火电厂粉煤灰(主要成分为 、
、 、
、 、
、 、
、 、
、 等)的综合利用具有重要的经济价值和社会效益。工艺流程如下:
等)的综合利用具有重要的经济价值和社会效益。工艺流程如下: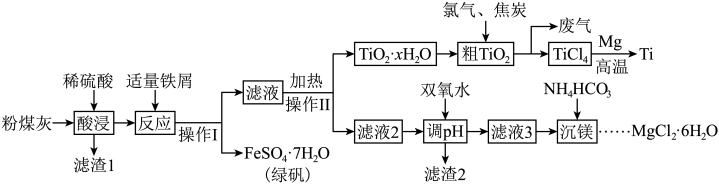
 形式存在,易水解;
形式存在,易水解;②
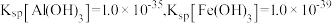 。
。回答下列问题:
(1)基态
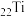 原子有
原子有(2)“酸浸”时,若要提高浸取速率,可采取的措施是
(3)操作Ⅱ中加热将
 水解得
水解得 ,写出其反应的离子方程式:
,写出其反应的离子方程式:(4)由
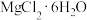 晶体得到无水
晶体得到无水 ,需要
,需要(5)为了使滤渣2沉淀完全(离子浓度
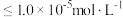 时认为沉淀完全),需“调
时认为沉淀完全),需“调 ”最小为
”最小为
您最近一年使用:0次
解题方法
10 . I. 溶液可用于多种气体的处理。
溶液可用于多种气体的处理。
(1) 是温室气体,可用
是温室气体,可用 溶液吸收得到
溶液吸收得到 或
或 。
。
① 俗称纯碱,已知25℃时,
俗称纯碱,已知25℃时, 第一步水解的平衡常数
第一步水解的平衡常数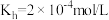 ,当溶液中
,当溶液中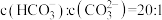 时,溶液的
时,溶液的
_______ 。
②泡沫灭火器中通常装有 溶液和
溶液和 溶液,请写出这两种溶液混合反应时的离子方程式
溶液,请写出这两种溶液混合反应时的离子方程式_______ 。
(2)金属与浓硝酸反应产生的 可用
可用 溶液吸收,反应方程式为:
溶液吸收,反应方程式为: ,含
,含 的水溶液与
的水溶液与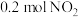 恰好完全反应得
恰好完全反应得 溶液A,溶液B为
溶液A,溶液B为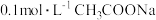 溶液,则两份溶液中
溶液,则两份溶液中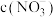 、
、 和
和 由大到小的顺序为
由大到小的顺序为_______ 。(已知 的电离常数
的电离常数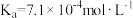 ,
, 的电离常数
的电离常数 )。
)。
(3)直接排放含 的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的
的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的 。吸收液吸收
。吸收液吸收 的过程中,
的过程中, 随
随 变化关系如下表所示:
变化关系如下表所示:
 溶液中溶液离子浓度关系正确的是(选填字母)
溶液中溶液离子浓度关系正确的是(选填字母)_______ 。
a.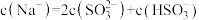
b.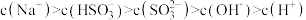
c.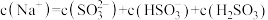
d.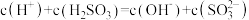
Ⅱ.滴定是一种重要的定量实验方法:某实验小组为测定碱式碳酸铜的纯度,取制得的碱式碳酸铜产品5.0g,加适量硫酸,再加 水,加热溶解,冷却后配成
水,加热溶解,冷却后配成 溶液,量取配成的
溶液,量取配成的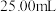 溶液于碘量瓶中,加入适量缓冲溶液控制溶液的
溶液于碘量瓶中,加入适量缓冲溶液控制溶液的 在3~4之间,以及过量的碘化钾,摇匀,于暗处放置5分钟。用
在3~4之间,以及过量的碘化钾,摇匀,于暗处放置5分钟。用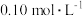 的
的 溶液进行滴定,至临近滴定终点时再加入
溶液进行滴定,至临近滴定终点时再加入 淀粉溶液做指示剂,继续滴入
淀粉溶液做指示剂,继续滴入 溶液至滴定终点。平行测定3次,实验数据如下表所示。
溶液至滴定终点。平行测定3次,实验数据如下表所示。
已知: ,
, 。
。
(4)判断滴定到达终 溶液点的现象是
溶液点的现象是_______ 。
(5)经数据处理可得该实验中滴定所用标准溶液的体积为_______  。
。
(6)下列操作会导致测定结果偏高的是_______ 。
a.装Na2S2O3溶液的滴定管,滴定前尖嘴处有气泡,滴定后气泡消失
b.锥形瓶未用待测液润洗
c.读 溶液体积时,若滴定前仰视,滴定后俯视
溶液体积时,若滴定前仰视,滴定后俯视
d.滴定过程中使用的碱式滴定管未润洗就装标准液滴定
 溶液可用于多种气体的处理。
溶液可用于多种气体的处理。(1)
 是温室气体,可用
是温室气体,可用 溶液吸收得到
溶液吸收得到 或
或 。
。①
 俗称纯碱,已知25℃时,
俗称纯碱,已知25℃时, 第一步水解的平衡常数
第一步水解的平衡常数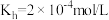 ,当溶液中
,当溶液中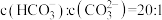 时,溶液的
时,溶液的
②泡沫灭火器中通常装有
 溶液和
溶液和 溶液,请写出这两种溶液混合反应时的离子方程式
溶液,请写出这两种溶液混合反应时的离子方程式(2)金属与浓硝酸反应产生的
 可用
可用 溶液吸收,反应方程式为:
溶液吸收,反应方程式为: ,含
,含 的水溶液与
的水溶液与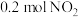 恰好完全反应得
恰好完全反应得 溶液A,溶液B为
溶液A,溶液B为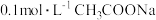 溶液,则两份溶液中
溶液,则两份溶液中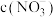 、
、 和
和 由大到小的顺序为
由大到小的顺序为 的电离常数
的电离常数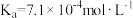 ,
, 的电离常数
的电离常数 )。
)。(3)直接排放含
 的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的
的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的 。吸收液吸收
。吸收液吸收 的过程中,
的过程中, 随
随 变化关系如下表所示:
变化关系如下表所示: | 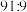 |  |  |
 | 8.2 | 7.2 | 6.2 |
 溶液中溶液离子浓度关系正确的是(选填字母)
溶液中溶液离子浓度关系正确的是(选填字母)a.
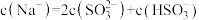
b.
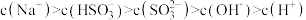
c.
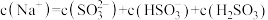
d.
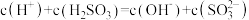
Ⅱ.滴定是一种重要的定量实验方法:某实验小组为测定碱式碳酸铜的纯度,取制得的碱式碳酸铜产品5.0g,加适量硫酸,再加
 水,加热溶解,冷却后配成
水,加热溶解,冷却后配成 溶液,量取配成的
溶液,量取配成的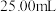 溶液于碘量瓶中,加入适量缓冲溶液控制溶液的
溶液于碘量瓶中,加入适量缓冲溶液控制溶液的 在3~4之间,以及过量的碘化钾,摇匀,于暗处放置5分钟。用
在3~4之间,以及过量的碘化钾,摇匀,于暗处放置5分钟。用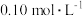 的
的 溶液进行滴定,至临近滴定终点时再加入
溶液进行滴定,至临近滴定终点时再加入 淀粉溶液做指示剂,继续滴入
淀粉溶液做指示剂,继续滴入 溶液至滴定终点。平行测定3次,实验数据如下表所示。
溶液至滴定终点。平行测定3次,实验数据如下表所示。已知:
 ,
, 。
。| 实验编号 | 滴定前 溶液的体积读数/ 溶液的体积读数/ | 滴定后 溶液的体积读数/ 溶液的体积读数/ |
| 1 | 0.10 | 20.12 |
| 2 | 1.20 | 23.21 |
| 3 | 1.50 | 21.48 |
 溶液点的现象是
溶液点的现象是(5)经数据处理可得该实验中滴定所用标准溶液的体积为
 。
。(6)下列操作会导致测定结果偏高的是
a.装Na2S2O3溶液的滴定管,滴定前尖嘴处有气泡,滴定后气泡消失
b.锥形瓶未用待测液润洗
c.读
 溶液体积时,若滴定前仰视,滴定后俯视
溶液体积时,若滴定前仰视,滴定后俯视d.滴定过程中使用的碱式滴定管未润洗就装标准液滴定
您最近一年使用:0次