解题方法
1 . 亚砷酸 在溶液中存在多种微粒形态,KOH溶液滴入亚砷酸溶液,各种微粒物质的量分数与溶液pH关系如图所示。下列说法
在溶液中存在多种微粒形态,KOH溶液滴入亚砷酸溶液,各种微粒物质的量分数与溶液pH关系如图所示。下列说法不正确 的是
 在溶液中存在多种微粒形态,KOH溶液滴入亚砷酸溶液,各种微粒物质的量分数与溶液pH关系如图所示。下列说法
在溶液中存在多种微粒形态,KOH溶液滴入亚砷酸溶液,各种微粒物质的量分数与溶液pH关系如图所示。下列说法
A. 的 的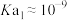 |
B.由图像信息可知 为三元弱酸 为三元弱酸 |
C.当pH调至8~11时,主要反应的离子方程式为 |
D. 时溶液中: 时溶液中: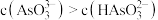 |
您最近一年使用:0次
解题方法
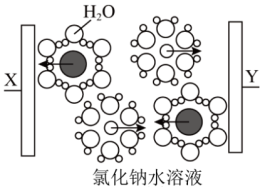
2 . 水溶液广泛存在于生命体及其赖以生存的环境中,电解质在水溶液中发生的离子反应以及电离平衡等,都与生命活动、日常生活、工农业生产和环境保护等息息相关。回答下列问题:
①图中黑球代表___________ 。(填微粒符号)
②写出Y电极的电极反应式:___________ 。
(2)A、B、C、D四种物质分别是NaOH、 、
、 、HCl中的一种。
、HCl中的一种。
① 的A溶液
的A溶液 ,则A是
,则A是___________ 。
②B溶液和D溶液显碱性,等浓度时两者的pH关系: ,则D溶液是
,则D溶液是___________ 。
(3)用水稀释 的氨水时,溶液中随着水量的增加而减小的是
的氨水时,溶液中随着水量的增加而减小的是___________ 。(填字母,下同)。
a. b.
b. c.
c. 与
与 的乘积 d.
的乘积 d. 的物质的量
的物质的量
(4)pH相同、等体积的盐酸和醋酸两份溶液,则下列说法正确的是___________ 。
a.
b.分别与过量的锌粉反应,醋酸产生的气体比较多
c.稀释相同倍数时,醋酸的pH比较小
d.恰好中和时消耗NaOH的物质的量相同
(5)碳酸钠的水溶液呈___________ 性,用离子方程式表示:___________ 。
①图中黑球代表
②写出Y电极的电极反应式:
(2)A、B、C、D四种物质分别是NaOH、
 、
、 、HCl中的一种。
、HCl中的一种。①
 的A溶液
的A溶液 ,则A是
,则A是②B溶液和D溶液显碱性,等浓度时两者的pH关系:
 ,则D溶液是
,则D溶液是(3)用水稀释
 的氨水时,溶液中随着水量的增加而减小的是
的氨水时,溶液中随着水量的增加而减小的是a.
 b.
b. c.
c. 与
与 的乘积 d.
的乘积 d. 的物质的量
的物质的量(4)pH相同、等体积的盐酸和醋酸两份溶液,则下列说法正确的是
a.

b.分别与过量的锌粉反应,醋酸产生的气体比较多
c.稀释相同倍数时,醋酸的pH比较小
d.恰好中和时消耗NaOH的物质的量相同
(5)碳酸钠的水溶液呈
您最近一年使用:0次
3 . 下列实验事实不能证明醋酸是弱电解质的是
| A.用醋酸溶液做导电实验时,灯泡很暗 |
B.常温下,测得 醋酸溶液的 醋酸溶液的 |
C.常温下,将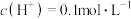 的醋酸溶液稀释1000倍测得 的醋酸溶液稀释1000倍测得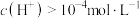 |
D.常温下测得 溶液的 溶液的 |
您最近一年使用:0次
名校
4 . 现有下列电解质溶液:
①Na2CO3 ②NaHCO3 ③NaClO ④CH3COONH4 ⑤NH4HCO3 ⑥NH4Cl ⑦NH3·H2O
(1)Na2CO3溶液呈___________ (填“酸性”“碱性”或“中性”),其原因是___________ (用离子方程式表示)。
(2)上述六种电解质溶液中,既能与盐酸反应又能与烧碱溶液反应的是___________ (填序号)。
(3)写出⑤与足量NaOH溶液混合加热的离子方程式:___________ 。
(4)常温下,物质的量浓度均为0.1mol•L−1的④、⑥、⑦四种溶液,溶液中c(NH )由大到小的顺序为:
)由大到小的顺序为:
___________ >___________ >___________ >(填序号)。
(5)已知:Ka(CH3COOH)=1.75×10−10,Kb(NH3·H2O)=1.76×10−10。常温下CH3COONH4溶液中的pH___________ 7(填“>”“=”或“<”),理由是___________ 。
(6)已知H2S能定量完成反应:R−(足量)+H2S=HR+HS−,2Z−+H2S(少量)=2HZ+S2−。相同温度下,相同物质的量浓度的①NaR ②Na2S ③NaHS ④NaZ 四种溶液的pH由大到小的顺序为:___________ (填序号)。
①Na2CO3 ②NaHCO3 ③NaClO ④CH3COONH4 ⑤NH4HCO3 ⑥NH4Cl ⑦NH3·H2O
(1)Na2CO3溶液呈
(2)上述六种电解质溶液中,既能与盐酸反应又能与烧碱溶液反应的是
(3)写出⑤与足量NaOH溶液混合加热的离子方程式:
(4)常温下,物质的量浓度均为0.1mol•L−1的④、⑥、⑦四种溶液,溶液中c(NH
 )由大到小的顺序为:
)由大到小的顺序为: (5)已知:Ka(CH3COOH)=1.75×10−10,Kb(NH3·H2O)=1.76×10−10。常温下CH3COONH4溶液中的pH
(6)已知H2S能定量完成反应:R−(足量)+H2S=HR+HS−,2Z−+H2S(少量)=2HZ+S2−。相同温度下,相同物质的量浓度的①NaR ②Na2S ③NaHS ④NaZ 四种溶液的pH由大到小的顺序为:
您最近一年使用:0次
名校
5 . 设NA为阿伏加德罗常数的值,下列说法正确的是
A.0.1mol香草醛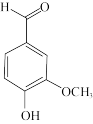 分了中 分了中 键的数目为1.6NA 键的数目为1.6NA |
| B.常温下1mol H2O中,中心原子的孤电子对数为2NA |
| C.标准状况下,0.1mol HF的体积约为2.24L |
D.1L 0.1mol•L-1的(NH4)2SO3溶液中,含有NH 的数目为0.2NA 的数目为0.2NA |
您最近一年使用:0次
名校
解题方法
6 . 科学研究人员在金星大气中探测到了只属于 的光谱特征,据此推断金星大气层或存在生命。已知
的光谱特征,据此推断金星大气层或存在生命。已知 与足量
与足量 溶液发生反应
溶液发生反应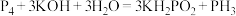 。
。 为弱电解质,下列说法正确的是
为弱电解质,下列说法正确的是
 的光谱特征,据此推断金星大气层或存在生命。已知
的光谱特征,据此推断金星大气层或存在生命。已知 与足量
与足量 溶液发生反应
溶液发生反应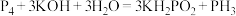 。
。 为弱电解质,下列说法正确的是
为弱电解质,下列说法正确的是A.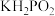 溶液中存在 溶液中存在 的电离平衡和水解平衡,以及水的电离平衡 的电离平衡和水解平衡,以及水的电离平衡 |
B.用 表示基态 表示基态 原子最外层电子排布违反能量最低原理 原子最外层电子排布违反能量最低原理 |
C.基态 原子核外电子有10种空间运动状态 原子核外电子有10种空间运动状态 |
D.加水稀释 溶液,溶液中所有离子浓度均减少 溶液,溶液中所有离子浓度均减少 |
您最近一年使用:0次
2024-03-25更新
|
146次组卷
|
2卷引用:福建省漳州市华安县第一中学2023-2024学年高二下学期3月月考化学试题
名校
7 . 室温下,向 溶液中滴加
溶液中滴加 溶液,溶液的pH随NaOH溶液体积的变化如图所示。下列说法正确的是
溶液,溶液的pH随NaOH溶液体积的变化如图所示。下列说法正确的是

 溶液中滴加
溶液中滴加 溶液,溶液的pH随NaOH溶液体积的变化如图所示。下列说法正确的是
溶液,溶液的pH随NaOH溶液体积的变化如图所示。下列说法正确的是
A.室温下, |
B.D点溶液中: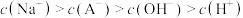 |
C.C点溶液中溶质为NaA,且 |
| D.溶液中水的电离程度:D>A>B |
您最近一年使用:0次
名校
8 . 常温常压下,有关下列各溶液的描述中正确的是
A.等浓度的 溶液和 溶液和 溶液, 溶液, 的水解程度一样 的水解程度一样 |
B.等浓度的醋酸钠和醋酸溶液混合后溶液显酸性,溶液中微粒的浓度关系为: |
C.浓度均为 的 的 、 、 混合溶液中: 混合溶液中: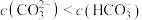 ,且 ,且 |
D.一定浓度的氨水加水稀释, 的比值和 的比值和 的比值均增大 的比值均增大 |
您最近一年使用:0次
名校
9 . 下列有关化学用语表示正确的是
A. 水解: 水解: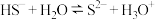 |
B. 电离: 电离: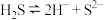 |
C. 的沉淀溶解平衡: 的沉淀溶解平衡: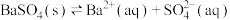 |
D.钢铁发生电化学腐蚀的负极反应式: |
您最近一年使用:0次
名校
10 . 根据下列实验操作和现象所得到的实验结论正确的是
| 选项 | 实验操作和现象 | 实验结论 |
| A | 向 溶液中加入 溶液中加入 溶液,有白色沉淀生成 溶液,有白色沉淀生成 |  与 与 发生了双水解反应 发生了双水解反应 |
| B | 向NaOH固体中加入少量稀盐酸,测得温度高于室温 | 盐酸与NaOH反应为放热反应 |
| C | 室温下,测得相同浓度的NaX和NaY溶液的pH分别为8和9 | 酸性: |
| D | 向等浓度的NaCl、KI的混合溶液中滴加少量 溶液,得到黄色沉淀 溶液,得到黄色沉淀 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-17更新
|
126次组卷
|
3卷引用:福建省福州市二中2023-2024学年高二上学期段考试化学试题



