名校
1 . 不能正确表示下列变化的离子方程式的是
A. 溶于盐酸: 溶于盐酸: |
B. 溶液腐蚀铜板: 溶液腐蚀铜板: |
C.苯酚钠溶液中通入少量CO2:2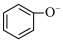 +CO2+H2O→2 +CO2+H2O→2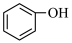 + + |
D.醋酸钠水解: |
您最近一年使用:0次
名校
解题方法
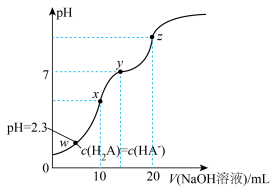
2 . 常温下向 溶液中滴加等浓度的
溶液中滴加等浓度的 溶液,滴定过程中溶液
溶液,滴定过程中溶液 随加入的
随加入的 溶液体积的变化曲线如图所示。下列说法正确的是
溶液体积的变化曲线如图所示。下列说法正确的是
 溶液中滴加等浓度的
溶液中滴加等浓度的 溶液,滴定过程中溶液
溶液,滴定过程中溶液 随加入的
随加入的 溶液体积的变化曲线如图所示。下列说法正确的是
溶液体积的变化曲线如图所示。下列说法正确的是
A.常温下, 的数量级为 的数量级为 |
| B.从w点至z点,水的电离程度逐渐增大 |
C.z点的离子浓度关系: |
D.在滴加 溶液过程中, 溶液过程中, |
您最近一年使用:0次
2024-03-19更新
|
150次组卷
|
2卷引用:云南省开远市第一中学校2023-2024学年高二下学期3月月考化学试题
名校
解题方法
3 .  时,向
时,向 溶液中滴加
溶液中滴加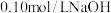 溶液,滴定曲线如图所示。下列说法不正确的是
溶液,滴定曲线如图所示。下列说法不正确的是

 时,向
时,向 溶液中滴加
溶液中滴加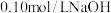 溶液,滴定曲线如图所示。下列说法不正确的是
溶液,滴定曲线如图所示。下列说法不正确的是
| A.该滴定过程应该选择石蕊溶液作指示剂 |
B.X点到Z点发生的主要反应的离子方程式为 |
C.Y点对应的溶液中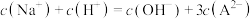 |
D.反应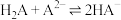 的平衡常数 的平衡常数 |
您最近一年使用:0次
2024-03-09更新
|
139次组卷
|
2卷引用:云南省昆明市云南师范大学实验中学2023-2024学年高二下学期3月月考化学试题
名校
4 . 在日常生产生活中,经常涉及化学反应原理,下列过程或现象与盐类水解无关的是
| A.加热氯化铁溶液,颜色变深 |
B. 与 与 溶液可用作焊接金属时的除锈剂 溶液可用作焊接金属时的除锈剂 |
| C.氯化钙溶液中滴加甲基橙,溶液显黄色 |
D.实验室中盛放 溶液的试剂瓶不能用磨口玻璃塞 溶液的试剂瓶不能用磨口玻璃塞 |
您最近一年使用:0次
2024-03-09更新
|
185次组卷
|
2卷引用:云南省昆明市云南师范大学实验中学2023-2024学年高二下学期3月月考化学试题
5 . Ⅰ:现有以下几种物质①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸钠、⑥亚硫酸氢钠、⑦氨水。请回答下列问题:
(1)以上物质属于弱电解质的是______ (填序号);
(2)常温下④的溶液pH______ 7(填>“<”或“=”),原因______ (用离子方程式表示);
(3)⑥的水溶液中呈酸性,原因是______ 。
(4)常温下,将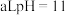 的
的 溶液与
溶液与 的
的 溶液混合(忽略混合后溶液体积的变化),若所得混合溶液的
溶液混合(忽略混合后溶液体积的变化),若所得混合溶液的 ,则
,则
______ 。
(5)已知:
a.常温下,醋酸和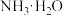 的电离平衡常数均为
的电离平衡常数均为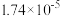 ;
;
b.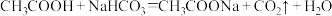
则 溶液呈
溶液呈______ 性(填“酸”、“碱”或“中”,下同), 溶液呈
溶液呈______ 性。
(6)对于醋酸溶液和醋酸钠溶液的下列说法正确的是______;
(1)以上物质属于弱电解质的是
(2)常温下④的溶液pH
(3)⑥的水溶液中呈酸性,原因是
(4)常温下,将
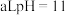 的
的 溶液与
溶液与 的
的 溶液混合(忽略混合后溶液体积的变化),若所得混合溶液的
溶液混合(忽略混合后溶液体积的变化),若所得混合溶液的 ,则
,则
(5)已知:
a.常温下,醋酸和
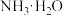 的电离平衡常数均为
的电离平衡常数均为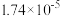 ;
;b.
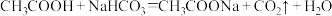
则
 溶液呈
溶液呈 溶液呈
溶液呈(6)对于醋酸溶液和醋酸钠溶液的下列说法正确的是______;
| A.稀释醋酸溶液,醋酸的电离程度增大,而稀释醋酸钠溶液则醋酸钠的水解程度减小。 |
| B.升高温度可以促进醋酸电离,也可以促进醋酸钠水解。 |
| C.醋酸和醋酸钠混合液中,醋酸抑制醋酸钠的水解、醋酸钠也抑制醋酸的电离。 |
| D.常温下,醋酸和醋酸钠等体积等浓度混合,溶液呈碱性。 |
您最近一年使用:0次
名校
解题方法
6 . 在下列溶液中,一定能大量共存的离子组是
A.室温时, 的溶液中: 的溶液中: |
B.能使甲基橙试液变红的溶液: |
C.无色透明溶液中: |
D.由水电离出的 的溶液中: 的溶液中: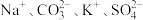 |
您最近一年使用:0次
名校
7 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.常温下,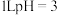 的 的 溶液中,发生电离的水分子数目为 溶液中,发生电离的水分子数目为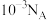 |
B.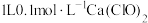 溶液中含 溶液中含 的数目为 的数目为 |
C.常温常压下, 和 和 混合得到的气体中含有的分子数小于 混合得到的气体中含有的分子数小于 |
D.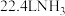 发生反应 发生反应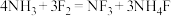 ,转移的电子数为 ,转移的电子数为 |
您最近一年使用:0次
名校
解题方法
8 . 下列物质加入水中对水的电离平衡没有影响的是
A. | B. | C. | D. |
您最近一年使用:0次
名校
9 . 常温下,有浓度均为 的下列4种溶液: ①NaCN溶液②NaOH溶液③
的下列4种溶液: ①NaCN溶液②NaOH溶液③ 溶液④
溶液④ 溶液
溶液
(1)这4种溶液中②由水电离出的 浓度为
浓度为___________ 。
(2)①中各离子浓度由大到小的顺序是___________ 。
(3)④中 的水解平衡常数
的水解平衡常数
___________ (保留2位有效数字)。
(4)若向等体积的③和④中滴加等浓度的盐酸至溶液呈中性,则消耗盐酸的体积③___________ ④(填“>”“<”或“=”)。
(5)25℃时,测得HCN和NaCN的混合溶液的 ,则
,则 约为
约为___________ (保留1位有效数字)。向NaCN溶液中通入少量 ,发生反应的离子方程式为
,发生反应的离子方程式为___________ 。
(6) 溶液显酸性的原因:
溶液显酸性的原因:___________ (用离子方程式表示), 是一种液态化合物,遇水剧烈反应,产生白雾,同时生成能使品红溶液褪色的气体,其水解反应的化学方程式为
是一种液态化合物,遇水剧烈反应,产生白雾,同时生成能使品红溶液褪色的气体,其水解反应的化学方程式为___________ 。用 水解制备
水解制备 的化学方程式为:
的化学方程式为:___________ 。
 的下列4种溶液: ①NaCN溶液②NaOH溶液③
的下列4种溶液: ①NaCN溶液②NaOH溶液③ 溶液④
溶液④ 溶液
溶液| HCN |  |  |
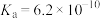 |   |  |
 浓度为
浓度为(2)①中各离子浓度由大到小的顺序是
(3)④中
 的水解平衡常数
的水解平衡常数
(4)若向等体积的③和④中滴加等浓度的盐酸至溶液呈中性,则消耗盐酸的体积③
(5)25℃时,测得HCN和NaCN的混合溶液的
 ,则
,则 约为
约为 ,发生反应的离子方程式为
,发生反应的离子方程式为(6)
 溶液显酸性的原因:
溶液显酸性的原因: 是一种液态化合物,遇水剧烈反应,产生白雾,同时生成能使品红溶液褪色的气体,其水解反应的化学方程式为
是一种液态化合物,遇水剧烈反应,产生白雾,同时生成能使品红溶液褪色的气体,其水解反应的化学方程式为 水解制备
水解制备 的化学方程式为:
的化学方程式为:
您最近一年使用:0次
名校
10 . 下列有关电解质溶液的说法正确的是


A.某温度下, 溶液显中性,所以 溶液显中性,所以 不水解 不水解 |
B.在常温下稀释两种酸溶液时pH变化如图,其中HX为较弱酸,且a点与b点的 数值相同 数值相同 |
C.25℃时,等体积 的HA和HB两种酸溶液分别与足量的锌充分反应,HA溶液与Zn反应生成的氢气更多,HA是较弱酸 的HA和HB两种酸溶液分别与足量的锌充分反应,HA溶液与Zn反应生成的氢气更多,HA是较弱酸 |
D.常温下, 的HA溶液中由水电离出的 的HA溶液中由水电离出的 为 为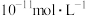 ,则能证明HA为弱酸 ,则能证明HA为弱酸 |
您最近一年使用:0次



