名校
1 . 已知常温下某二元弱酸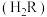 电离常数为
电离常数为 电离常数为
电离常数为 的
的 的
的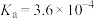 ,回答下列问题:
,回答下列问题:
(1)常温下向Na2R溶液加入少量的SO2气体发生反应的离子方程式为___________ 。
(2)常温下2mol/L的H2R溶液的pH约为___________ ;等浓度的H2R和Na2R溶液中HR-离子浓度的大小关系为前者___________ 后者(填“>”、“<”或“=”)。
(3)常温下0.1mol/L的NaHR溶液pOH___________ 7(填“>”、“<”或“=”)。
(4)等浓度等体积的NaCl和NaF溶液中离子总数的大小关系为前者___________ 后者(填“>”、“<”或“=”)。
(5)现有含有Fe3+和Ni2+混合溶液,若溶液中c(Ni2+)=35mol·L-1,加入碳酸钠调节溶液的pH为___________ 可使Fe3+恰好沉淀完全(离子浓度 ),此时
),此时___________ (填“有”或“无”)Ni(OH)2沉淀生成。(假设溶液体积不变,1g6=0.8;Ksp[Fe(OH)3]=2.16×10-39,Ksp[Ni(OH)2]=2×10-15)
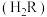 电离常数为
电离常数为 电离常数为
电离常数为 的
的 的
的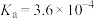 ,回答下列问题:
,回答下列问题:(1)常温下向Na2R溶液加入少量的SO2气体发生反应的离子方程式为
(2)常温下2mol/L的H2R溶液的pH约为
(3)常温下0.1mol/L的NaHR溶液pOH
(4)等浓度等体积的NaCl和NaF溶液中离子总数的大小关系为前者
(5)现有含有Fe3+和Ni2+混合溶液,若溶液中c(Ni2+)=35mol·L-1,加入碳酸钠调节溶液的pH为
 ),此时
),此时
您最近一年使用:0次
名校
解题方法
2 . 常温下,下列所述的量关系中不正确的是
A.将等浓度等体积的 溶液和盐酸混合后,测得pH为6.8,此时溶液中存在: 溶液和盐酸混合后,测得pH为6.8,此时溶液中存在: |
B.pH相同的① ② ② ③ ③ 三种溶液中, 三种溶液中, 大小关系是①=②=③ 大小关系是①=②=③ |
C.将 的 的 溶液加水稀释10倍,溶液中 溶液加水稀释10倍,溶液中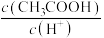 减小 减小 |
D.向体积为10 mL pH均为2的醋酸溶液与HCl溶液中分别加入相同表面积的Mg片,初始反应速率为 |
您最近一年使用:0次
名校
3 . 下列由实验现象所得结论正确的是
A.取补铁口服液的上层清液,滴加酸性 溶液,溶液紫色褪去,证明口服液中一定含有 溶液,溶液紫色褪去,证明口服液中一定含有 |
B.向盛有0.01 mol/L的 溶液的小试管中滴加酚酞溶液,溶液变红,再加入少量 溶液的小试管中滴加酚酞溶液,溶液变红,再加入少量 固体,溶液红色加深,证明 固体,溶液红色加深,证明 水解程度增大 水解程度增大 |
C.相同温度下,用pH试纸测定等浓度的 和NaClO溶液的PH,前者pH更小说明 和NaClO溶液的PH,前者pH更小说明 |
D.对 溶液进行加热,溶液由蓝色变为黄绿色,说明 溶液进行加热,溶液由蓝色变为黄绿色,说明 的正反应吸热 的正反应吸热 |
您最近一年使用:0次
名校
解题方法
4 . 钾的化合物对调节体内循环有重要用途,一定温度下,下列溶液中的离子浓度关系式正确的是
A.0.1 mol⋅L 的 的 溶液中: 溶液中: |
B. 溶液中: 溶液中: |
C.常温下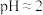 的0.1 mol/L的 的0.1 mol/L的 的溶液中: 的溶液中: |
D.pH相同的① 、②KOH、③KClO三种溶液中的 、②KOH、③KClO三种溶液中的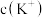 :③>①>②(已知: :③>①>②(已知: 的 的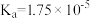 ,HClO的 ,HClO的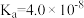 ) ) |
您最近一年使用:0次
名校
解题方法
5 .  为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.常温下, 的 的 溶液中由水电离出的 溶液中由水电离出的 数为 数为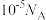 |
B.标准状况下将22.4 L  溶于水配成1 mol/L的溶液,则 溶于水配成1 mol/L的溶液,则 mol/L mol/L |
C.电解 溶液,阴极生成2.24 L气体(标况),外电路中通过电子的数目为 溶液,阴极生成2.24 L气体(标况),外电路中通过电子的数目为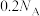 |
D. 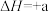 kJ⋅mol kJ⋅mol ,若参加反应的 ,若参加反应的 数目为 数目为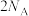 ,反应会吸收a kJ热量 ,反应会吸收a kJ热量 |
您最近一年使用:0次
名校
6 . 用 代表阿伏加德罗常数的值,下列说法正确的是
代表阿伏加德罗常数的值,下列说法正确的是
 代表阿伏加德罗常数的值,下列说法正确的是
代表阿伏加德罗常数的值,下列说法正确的是A.常温下,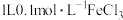 溶液中,所含 溶液中,所含 总数为 总数为 |
B. 溶液中含有的 溶液中含有的 数为 数为 |
C.向 溶液中滴入适量氨水至中性,此时溶液中所含 溶液中滴入适量氨水至中性,此时溶液中所含 的数目为 的数目为 |
D.在钢铁吸氧腐蚀中,若生成 ,被还原的 ,被还原的 分子数为 分子数为 |
您最近一年使用:0次
名校
7 . 我们的日常生产、生活与化学有着紧密的联系。
Ⅰ.已知次磷酸( )是一元中强酸,请回答:
)是一元中强酸,请回答:
(1)写出其正盐在水溶液中水解的离子方程式:__________ 。
Ⅱ.现有常温下 的盐酸溶液和
的盐酸溶液和 的醋酸溶液,请根据下列操作回答问题:
的醋酸溶液,请根据下列操作回答问题:
(2)①常温下, 溶液加水稀释,下列数值增大的是
溶液加水稀释,下列数值增大的是__________ (填字母)。
A. B.
B. C.
C. D.
D.
②取10mL醋酸溶液,加入少量无水 固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中
固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中 的值将
的值将__________ (填“增大”“减小”或“不变”)。
③相同条件下,取等体积的盐酸溶液和醋酸溶液,分别与0.1mol/LNaOH溶液恰好反应,消耗NaOH溶液的体积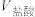
__________ (填“>”“<”或“=”)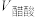 。
。
(3)某温度下,测得 的HCl溶液中,水电离出的氢离子的浓度
的HCl溶液中,水电离出的氢离子的浓度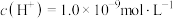 ,此温度下,将
,此温度下,将 盐酸溶液和
盐酸溶液和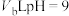 的
的 溶液混合均匀,测得溶液的
溶液混合均匀,测得溶液的 ,则
,则
__________ 。(忽略混合后溶液体积变化)
Ⅲ.25℃时,有浓度均为0.10mol/L的下列4种溶液及几种酸的电离平衡常数:
①NaCN溶液②NaOH溶液③ 溶液④
溶液④ 溶液
溶液
(4)这4种溶液的pH由大到小的顺序是__________ (填序号)。
(5)向NaCN溶液中通入少量 ,则发生反应的离子方程式为
,则发生反应的离子方程式为__________ 。
(6)测得HCN和NaCN的混合溶液的 ,则
,则 约为
约为__________ (保留1位有效数字)。
(7) 和
和 混合溶液中,若溶液
混合溶液中,若溶液 ,则溶液中
,则溶液中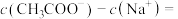
__________ (填精确值)mol/L。
Ⅰ.已知次磷酸(
 )是一元中强酸,请回答:
)是一元中强酸,请回答:(1)写出其正盐在水溶液中水解的离子方程式:
Ⅱ.现有常温下
 的盐酸溶液和
的盐酸溶液和 的醋酸溶液,请根据下列操作回答问题:
的醋酸溶液,请根据下列操作回答问题:(2)①常温下,
 溶液加水稀释,下列数值增大的是
溶液加水稀释,下列数值增大的是A.
 B.
B. C.
C. D.
D.
②取10mL醋酸溶液,加入少量无水
 固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中
固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中 的值将
的值将③相同条件下,取等体积的盐酸溶液和醋酸溶液,分别与0.1mol/LNaOH溶液恰好反应,消耗NaOH溶液的体积
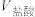
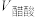 。
。(3)某温度下,测得
 的HCl溶液中,水电离出的氢离子的浓度
的HCl溶液中,水电离出的氢离子的浓度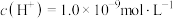 ,此温度下,将
,此温度下,将 盐酸溶液和
盐酸溶液和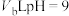 的
的 溶液混合均匀,测得溶液的
溶液混合均匀,测得溶液的 ,则
,则
Ⅲ.25℃时,有浓度均为0.10mol/L的下列4种溶液及几种酸的电离平衡常数:
①NaCN溶液②NaOH溶液③
 溶液④
溶液④ 溶液
溶液HCN |
|
|
|
|
|
(5)向NaCN溶液中通入少量
 ,则发生反应的离子方程式为
,则发生反应的离子方程式为(6)测得HCN和NaCN的混合溶液的
 ,则
,则 约为
约为(7)
 和
和 混合溶液中,若溶液
混合溶液中,若溶液 ,则溶液中
,则溶液中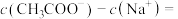
您最近一年使用:0次
名校
解题方法
8 . 下列实验操作不能达到实验目的的是
选项 | 实验目的 | 实验操作 |
A | 证明 溶液中存在 溶液中存在 的水解平衡 的水解平衡 | 向含有酚酞的 |
B | 制得 | 将 |
C | 比较盐酸和醋酸的酸性强弱 | 相同温度下,用pH计分别测定 盐酸溶液和 盐酸溶液和 醋酸溶液的pH 醋酸溶液的pH |
D | 探究温度对反应速率的影响 | 向2支试管中各加入相同体积、相同浓度的 溶液,再分别加入相同体积、相同浓度的稀硫酸,分别放入冷水和热水中 溶液,再分别加入相同体积、相同浓度的稀硫酸,分别放入冷水和热水中 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
9 . Ⅰ.已知某温度下CH3COOH的电离常数Ka=1.6×10-5。该温度下,向20mL0.01mol/LCH3COOH溶液中逐滴加入0.01mol/LKOH溶液,其pH变化曲线如图所示(忽略温度变化)。请回答下列问题(已知lg4≈0.6)。

(1)a点溶液中c(H+)为___________ ,pH约为___________ 。
(2)a、b、c、d四点中水的电离程度最大的是___________ 点
Ⅱ.完成下列问题
(3)若向20mL稀氨水中逐滴加入等浓度的盐酸,则下列变化趋势正确的是___________(填字母)。
Ⅲ.完成下列问题
(4)已知25℃,NH3·H2O的Kb=1.8×10-5,H2SO3的Ka1=1.3×10-2,Ka2=6.2×10-8,0.1mol/L的(NH4)2SO3溶液显___________ (填“酸性”、“碱性”或“中性”)。
(5)0.1mol/LNa2CO3溶液中c(OH-)-c(H+)=___________ [用含c(HCO )、c(H2CO3)的关系式表示]。
)、c(H2CO3)的关系式表示]。
(6)向Na2CO3溶液中加入明矾,请写出相关的离子方程式:___________ 。

(1)a点溶液中c(H+)为
(2)a、b、c、d四点中水的电离程度最大的是
Ⅱ.完成下列问题
(3)若向20mL稀氨水中逐滴加入等浓度的盐酸,则下列变化趋势正确的是___________(填字母)。
A. | B. |
C. | D. |
Ⅲ.完成下列问题
(4)已知25℃,NH3·H2O的Kb=1.8×10-5,H2SO3的Ka1=1.3×10-2,Ka2=6.2×10-8,0.1mol/L的(NH4)2SO3溶液显
(5)0.1mol/LNa2CO3溶液中c(OH-)-c(H+)=
 )、c(H2CO3)的关系式表示]。
)、c(H2CO3)的关系式表示]。(6)向Na2CO3溶液中加入明矾,请写出相关的离子方程式:
您最近一年使用:0次
名校
10 . 常温条件下,下列有关电解质溶液的说法正确的是
| A.加水稀释盐酸时,溶液中所有离子的浓度均减小 |
| B.将10mL0.01mol/LNaOH溶液与同浓度的HA溶液混合,若混合后溶液呈中性,则消耗的HA的体积V≤10mL |
C.等浓度的①NH4Cl溶液②NH4HSO4溶液③NH4HCO3溶液中,②中的c( )最小 )最小 |
D.室温下,向0.1mol/L氨水中加少量NH4Cl固体,溶液中 减小 减小 |
您最近一年使用:0次



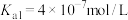
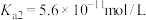
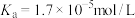
 溶液,观察溶液颜色的变化
溶液,观察溶液颜色的变化 固体
固体

