1 . 常温下,下列关于 的
的 溶液说法正确的是
溶液说法正确的是
 的
的 溶液说法正确的是
溶液说法正确的是A.将 的 的 溶液稀释10倍,溶液的 溶液稀释10倍,溶液的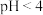 |
B.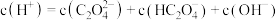 |
C.与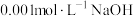 溶液等体积混合后,溶液呈碱性 溶液等体积混合后,溶液呈碱性 |
D.加水稀释时,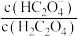 逐渐减小 逐渐减小 |
您最近一年使用:0次
2 . 为证明某可溶性一元酸(HX)是弱酸,设计如下实验得出的结论:HX是弱酸。其中不合理的是
A.室温下,测得 溶液的 溶液的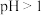 |
B.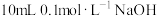 溶液与 溶液与 溶液恰好中和 溶液恰好中和 |
C.室温下,测得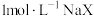 溶液的 溶液的 |
D.在相同条件下,对 的盐酸和 的盐酸和 的HX溶液进行导电性实验,HX溶液灯泡较暗 的HX溶液进行导电性实验,HX溶液灯泡较暗 |
您最近一年使用:0次
3 . 盐在化学工业中有重要的应用,请回答下列问题。
(1)用离子方程式表示 FeCl3 可作净水剂的原因 :_______ 。
(2)常温下,在 pH=3 的硫酸与 pH =11 的 Na 2 S 溶液中,水电离出来的 c(OH- ) 之比为______
(3)物质的量浓度相等的下列溶液溶液 ①NH4Cl、②NH4HSO4、③(NH4)2SO4、④CH3COONH4 ⑤NH3·H2O ,溶液中c( ) 由大到小的顺是
) 由大到小的顺是 _______ ( 用序号表示)。
(4)已知 25 ℃ 时 Ksp[Mg(OH) 2 ]=1.8×10 -11 , Ksp[Cu(OH) 2 ] =2.2 ×10 -20 。25 ℃ 时,向浓度均为 0.1 mol/L 的 MgCl 2 和 CuCl 2 混合溶液中逐滴加入氨水,先生成_______ ( 填化学式)沉淀 ; 当体系中两种沉淀共存时,  =
= _______ 。
(1)用离子方程式表示 FeCl3 可作净水剂的原因 :
(2)常温下,在 pH=3 的硫酸与 pH =11 的 Na 2 S 溶液中,水电离出来的 c(OH- ) 之比为
(3)物质的量浓度相等的下列溶液溶液 ①NH4Cl、②NH4HSO4、③(NH4)2SO4、④CH3COONH4 ⑤NH3·H2O ,溶液中c(
 ) 由大到小的顺是
) 由大到小的顺是 (4)已知 25 ℃ 时 Ksp[Mg(OH) 2 ]=1.8×10 -11 , Ksp[Cu(OH) 2 ] =2.2 ×10 -20 。25 ℃ 时,向浓度均为 0.1 mol/L 的 MgCl 2 和 CuCl 2 混合溶液中逐滴加入氨水,先生成
 =
=
您最近一年使用:0次
4 . 现有等体积、等浓度的① 、②
、② 、③
、③ 三种溶液,回答下列问题。
三种溶液,回答下列问题。
(1)三种溶液中铵根离子浓度由大到小的顺序为___________ (用序号表示,用>连接)。
(2)写出溶液①显酸性的原因___________ (用离子方程式表示)。
(3)写出溶液①的电荷守恒___________ (用离子浓度表示);该溶液中离子浓度由大到小的顺序为___________ (用离子浓度表示,用>连接)
(4)写出溶液③的物料守恒___________ (用离子浓度表示)。
 、②
、② 、③
、③ 三种溶液,回答下列问题。
三种溶液,回答下列问题。(1)三种溶液中铵根离子浓度由大到小的顺序为
(2)写出溶液①显酸性的原因
(3)写出溶液①的电荷守恒
(4)写出溶液③的物料守恒
您最近一年使用:0次
解题方法
5 . 常温下,下列各组离子在指定条件下可能大量共存的是
A.含有Al3+的溶液中: |
B. 的溶液中: 的溶液中: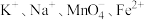 |
C.澄清透明的溶液中: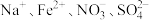 |
D.水电离出的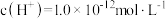 的溶液中: 的溶液中: |
您最近一年使用:0次
名校
6 . 回答下列问题
(1)盐碱地(含较多 、NaCl)不利于植物生长,盐碱地呈碱性的原因:
、NaCl)不利于植物生长,盐碱地呈碱性的原因:___________ (用离子方程式表示)。
(2)D元素的正三价离子的3d轨道为半充满,其基态原子的价层电子排布式为___________ 。
(3)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,其基态原子的简化电子排布式为___________ ,在元素周期表中的位置是___________ 。
(4) 是离子化合物,各原子均满足8电子稳定结构,
是离子化合物,各原子均满足8电子稳定结构, 的电子式是
的电子式是___________ 。
(5)Xe是第五周期的稀有气体元素,与F形成的 室温下易升华。下列对
室温下易升华。下列对 中心原子杂化方式推断合理的是
中心原子杂化方式推断合理的是___________ (填字母)。
(6)为测定某 消毒剂样品中含氯量,用
消毒剂样品中含氯量,用 溶液滴定该样品溶液,操作如下:
溶液滴定该样品溶液,操作如下:
a.取样:取20.00 mL样品溶液置于锥形瓶,加入稀硫酸酸化,发生反应: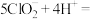
 (
( 极易溶于水);
极易溶于水);
b.氧化:加入足量碘化钾溶液,振荡充分反应;
c.滴定:加入淀粉作指示剂,在锥形瓶下垫一张白纸,用0.1000 mol/L 标准溶液滴定碘单质(已知:
标准溶液滴定碘单质(已知: );
);
d.重复上述操作三次。
滴定终点现象为:加入最后半滴 溶液后,溶液
溶液后,溶液___________ ,即到终点。
测得的实验数据如下表:
由以上数据计算该样品溶液的含氯量(以 计)
计)___________ g/L(保留三位有效数字)。滴定时,有一组数据出现了明显异常,所测含氯量偏大,原因可能有___________ (填字母序号)。
A.取样时用25.00 mL的滴定管液面在5.00 mL处放出所有溶液
B.滴定终点读数时仰视刻度线
C.达终点时滴定管尖嘴有标准液悬挂
D.盛装待测液的锥形瓶未润洗
E.摇动锥形瓶时有液体溅出
(1)盐碱地(含较多
 、NaCl)不利于植物生长,盐碱地呈碱性的原因:
、NaCl)不利于植物生长,盐碱地呈碱性的原因:(2)D元素的正三价离子的3d轨道为半充满,其基态原子的价层电子排布式为
(3)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,其基态原子的简化电子排布式为
(4)
 是离子化合物,各原子均满足8电子稳定结构,
是离子化合物,各原子均满足8电子稳定结构, 的电子式是
的电子式是(5)Xe是第五周期的稀有气体元素,与F形成的
 室温下易升华。下列对
室温下易升华。下列对 中心原子杂化方式推断合理的是
中心原子杂化方式推断合理的是| A.sp | B. | C. | D. |
 消毒剂样品中含氯量,用
消毒剂样品中含氯量,用 溶液滴定该样品溶液,操作如下:
溶液滴定该样品溶液,操作如下:a.取样:取20.00 mL样品溶液置于锥形瓶,加入稀硫酸酸化,发生反应:
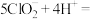
 (
( 极易溶于水);
极易溶于水);b.氧化:加入足量碘化钾溶液,振荡充分反应;
c.滴定:加入淀粉作指示剂,在锥形瓶下垫一张白纸,用0.1000 mol/L
 标准溶液滴定碘单质(已知:
标准溶液滴定碘单质(已知: );
);d.重复上述操作三次。
滴定终点现象为:加入最后半滴
 溶液后,溶液
溶液后,溶液测得的实验数据如下表:
| 实验序号 | 待测液体积(mL) |  标准溶液 标准溶液 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 20.00 | 0.06 | 20.60 |
| 2 | 20.00 | 6.00 | 25.95 |
| 3 | 20.00 | 1.40 | 23.20 |
| 4 | 20.00 | 1.00 | 21.05 |
 计)
计)A.取样时用25.00 mL的滴定管液面在5.00 mL处放出所有溶液
B.滴定终点读数时仰视刻度线
C.达终点时滴定管尖嘴有标准液悬挂
D.盛装待测液的锥形瓶未润洗
E.摇动锥形瓶时有液体溅出
您最近一年使用:0次
名校
解题方法
7 . 已知25℃时,几种弱酸的电离常数如下:
25℃时,下列说法正确的是
| 弱酸的化学式 | CH3COOH | HCN | H2S |
| 电离常数 |  |  | 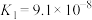 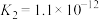 |
| A.某浓度的NaCN溶液的pH=d,则其中由水电离出的c(OH-)=10-d mol/L |
| B.用0.1 mol/L的NaOH溶液滴定pH相等的CH3COOH和HCN溶液,CH3COOH消耗的NaOH溶液体积更大 |
C.NaHS和Na2S的混合溶液中,一定存在 |
| D.常温下,pH=4的CH3COOH和pH=10的NaOH溶液等体积混合后,溶液中离子浓度由大到小的顺序为:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
您最近一年使用:0次
8 . 已知 H2O2、KMnO4、NaClO、K2Cr2O7均具有强氧化性。将溶液中的Cu2+、Fe2+、Fe3+沉淀为氢氧化物,需溶液的pH分别为6.4、9.6、3.7。现有含FeCl2杂质的氯化铜晶体(CuCl2∙2H2O),为制取纯净的CuCl2∙2H2O,首先将其制成水溶液,然后按图示步骤进行提纯:
(1)本实验最适合的氧化剂X是___________(填序号)。
(2)物质Y可以选择以下___________。
(3)本实验用加碱沉淀法能不能达到目的?___________ (填“能”或“不能”)。
(4)加氧化剂的目的是___________ 。
(5)最后蒸发结晶要想得到CuCl2∙2H2O晶体,应如何操作?___________ 。
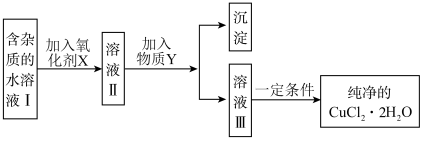
(1)本实验最适合的氧化剂X是___________(填序号)。
| A.K2Cr2O7 | B.NaClO | C. H2O2 | D.KMnO4 |
(2)物质Y可以选择以下___________。
| A.CuO | B.CuSO4 | C.Cu(OH)2 | D.KOH |
(3)本实验用加碱沉淀法能不能达到目的?
(4)加氧化剂的目的是
(5)最后蒸发结晶要想得到CuCl2∙2H2O晶体,应如何操作?
您最近一年使用:0次
解题方法
9 . 常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
请回答:
(1)从①组情况分析,HA是___________ (填“强酸”或“弱酸”)。
(2)②组情况表明,c___________ (填“大于”、“小于”或“等于”)0.2mol/L。混合液中离子浓度c(A-)与c(Na+)的大小关系是:c(A-)___________ c(Na+) (“大于”、“小于”或“等于”)。
(3)从③组实验结果分析,说明HA的电离程度___________ (填“大于”、“小于”或“等于”)NaA的水解程度。
(4)①组实验所得混合溶液中由水电离出的c(OH-)=___________ mol∙L-1。
| 实验编号 | HA物质的量浓度(mol/L) | NaOH物质的量浓度(mol/L) | 混合溶液的 pH |
| ① | 0.1 | 0.1 | pH=9 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.2 | 0.1 | pH<7 |
(1)从①组情况分析,HA是
(2)②组情况表明,c
(3)从③组实验结果分析,说明HA的电离程度
(4)①组实验所得混合溶液中由水电离出的c(OH-)=
您最近一年使用:0次
10 . 水中存在电离平衡:H2O H++OH-。若在水中分别加入下列各物质:
H++OH-。若在水中分别加入下列各物质:
①NaOH(s) ②NH4Cl(s) ③Na2CO3(s) ④CH3COOH(l) ⑤K2SO4(s),试回答下列问题:
(1)能使水的电离平衡向左移动的是___________ ,不发生移动的是___________ 。(用序号填空)
(2)溶液呈酸性的是___________ ,溶液呈碱性的是___________ 。(用序号填空)
(3)能促进水的电离,且溶液pH>7的是___________ 。(用序号填空)
(4)将0.1mol CH3COOH溶于水制成1L溶液,此溶液的物质的量浓度为0.1mol/L,经测定溶液中c(CH3COO-)为1.4×10-3mol∙L-1,此温度下醋酸的电离常数Ka=___________ ,温度升高,Ka将___________ (填“变大”、“不变”或“变小”)。
(5)向 溶液中滴入酚酞试液,观察到的现象是
溶液中滴入酚酞试液,观察到的现象是___________ ,若微热溶液,观察到的现象是___________ ,由此证明碳酸钠的水解是___________ (填“吸热”或“放热”)反应。 溶液中
溶液中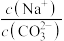
___________ 2(填“大于”或“小于”),能使其比值接近2的措施是___________ (填序号)。
①加入适量盐酸 ②加入适量NaOH固体 ③加入适量KOH固体 ④加热
 H++OH-。若在水中分别加入下列各物质:
H++OH-。若在水中分别加入下列各物质:①NaOH(s) ②NH4Cl(s) ③Na2CO3(s) ④CH3COOH(l) ⑤K2SO4(s),试回答下列问题:
(1)能使水的电离平衡向左移动的是
(2)溶液呈酸性的是
(3)能促进水的电离,且溶液pH>7的是
(4)将0.1mol CH3COOH溶于水制成1L溶液,此溶液的物质的量浓度为0.1mol/L,经测定溶液中c(CH3COO-)为1.4×10-3mol∙L-1,此温度下醋酸的电离常数Ka=
(5)向
 溶液中滴入酚酞试液,观察到的现象是
溶液中滴入酚酞试液,观察到的现象是 溶液中
溶液中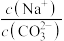
①加入适量盐酸 ②加入适量NaOH固体 ③加入适量KOH固体 ④加热
您最近一年使用:0次



