1 . 室温下,将 溶液滴加到己二酸
溶液滴加到己二酸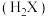 溶液中,混合溶液的
溶液中,混合溶液的 与离子浓度变化的关系如图所示。下列叙述错误的是
与离子浓度变化的关系如图所示。下列叙述错误的是
 溶液滴加到己二酸
溶液滴加到己二酸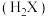 溶液中,混合溶液的
溶液中,混合溶液的 与离子浓度变化的关系如图所示。下列叙述错误的是
与离子浓度变化的关系如图所示。下列叙述错误的是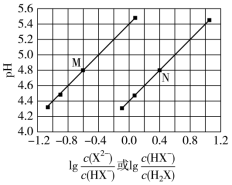
A.当混合溶液呈中性时,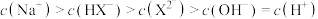 |
B.曲线 表示 表示 与 与 的变化关系 的变化关系 |
C.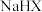 溶液中 溶液中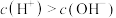 |
D. 的数量级为10-5 的数量级为10-5 |
您最近半年使用:0次
真题
名校
2 . 下表列出25℃时不同羧酸的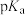 (即
(即 )。根据表中的数据推测,结论正确的是
)。根据表中的数据推测,结论正确的是
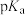 (即
(即 )。根据表中的数据推测,结论正确的是
)。根据表中的数据推测,结论正确的是| 羧酸 |  |  | 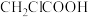 |  |
| pKa | 4.76 | 2.59 | 2.87 | 2.90 |
A.酸性强弱: |
| B.对键合电子的吸引能力强弱:F<Cl<Br |
C.25℃时的pKa大小: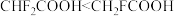 |
D.25℃时0.1mol/L溶液的碱性强弱: |
您最近半年使用:0次
2024-04-07更新
|
846次组卷
|
3卷引用:广东省肇庆市加美学校2023-2024学年高二下学期竞赛化学试题
3 . 砷及其化合物有着广泛的用途。砷有两种常见的弱酸,砷酸(H3AsO4)和亚砷酸(H3AsO3)。已知砷酸(H3AsO4)的pKa1、pKa2、pKa3依次为2.25、6.77、11.40(pKa=-lgKa)。亚砷酸(H3AsO3)水溶液中存在多种微粒形态,各种微粒分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与溶液的pH关系如图所示。下列说法正确的是


A.砷酸(H3AsO4)的电离方程式为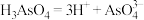 |
B.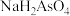 溶液呈碱性 溶液呈碱性 |
C.以酚酞为指示剂(变色范围pH8.2~10.0)将NaOH溶液逐滴加入到H3AsO3溶液中,当溶液由无色变为浅红色时停止滴加。该过程中主要反应的离子方程式为 |
D.在H3AsO4溶液中有: |
您最近半年使用:0次
名校
解题方法
4 . 下列问题与盐的水解有关的是
①草木灰(主要成分 )与铵态氮肥不能混合施用
)与铵态氮肥不能混合施用
② 与
与 两种溶液可作泡沫灭火剂
两种溶液可作泡沫灭火剂
③实验室中盛放 溶液的试剂瓶不能用磨口玻璃塞
溶液的试剂瓶不能用磨口玻璃塞
④ 与
与 溶液可作焊接金属时的除锈剂
溶液可作焊接金属时的除锈剂
⑤加热蒸干 溶液并灼烧,可以得到
溶液并灼烧,可以得到 固体
固体
⑥ 溶液不能保存在玻璃试剂瓶中
溶液不能保存在玻璃试剂瓶中
①草木灰(主要成分
 )与铵态氮肥不能混合施用
)与铵态氮肥不能混合施用②
 与
与 两种溶液可作泡沫灭火剂
两种溶液可作泡沫灭火剂③实验室中盛放
 溶液的试剂瓶不能用磨口玻璃塞
溶液的试剂瓶不能用磨口玻璃塞④
 与
与 溶液可作焊接金属时的除锈剂
溶液可作焊接金属时的除锈剂⑤加热蒸干
 溶液并灼烧,可以得到
溶液并灼烧,可以得到 固体
固体⑥
 溶液不能保存在玻璃试剂瓶中
溶液不能保存在玻璃试剂瓶中| A.①②③ | B.①②③④ | C.①②③④⑤ | D.①②③④⑤⑥ |
您最近半年使用:0次
2023-12-03更新
|
299次组卷
|
3卷引用:山东省临沂市平邑县第一中学西校区2023-2024学年高二上学期元旦竞赛考试化学试题
名校
5 . 下列各离子浓度的比较正确的是
A.含有 、 、 、 、 、 、 的溶液中,离子浓度大小关系可能为: 的溶液中,离子浓度大小关系可能为: |
B. 溶液和 溶液和 盐酸等体积混合,在混合溶液中: 盐酸等体积混合,在混合溶液中: |
C. 和 和 等体积混合后溶液呈碱性: 等体积混合后溶液呈碱性: |
D.向 NaOH溶液中加入等体积的 NaOH溶液中加入等体积的 醋酸溶液: 醋酸溶液: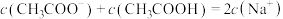 |
您最近半年使用:0次
2023-11-29更新
|
248次组卷
|
2卷引用:山东省临沂市平邑县第一中学西校区2023-2024学年高二上学期元旦竞赛考试化学试题
名校
解题方法
6 . 常温下,下列各离子组在指定的溶液中一定能够大量共存的是
A.pH=11的NaOH溶液中: 、K+、 、K+、 、 、 |
B.明矾溶液中: 、 、 、 、 、 、 |
C.中性溶液中:Fe3+、K+、 、 、 |
D.水电离出的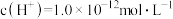 的溶液中: 的溶液中: 、 、 、 、 、 、 |
您最近半年使用:0次
2023-11-17更新
|
76次组卷
|
2卷引用:山东省临沂市平邑县第一中学西校区2023-2024学年高二上学期元旦竞赛考试化学试题
名校
解题方法
7 . 完成下列问题
(1)已知某温度下有如下三个反应:
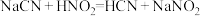


①则该温度下HF、HCN和 三种弱酸的电离常数由大到小的顺序是
三种弱酸的电离常数由大到小的顺序是___________
②已知:乙二酸( ,可简写为
,可简写为 ),俗称草酸;25℃
),俗称草酸;25℃
 ,
,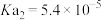 ,25℃
,25℃ ,请写出少量草酸(
,请写出少量草酸( )与NaF溶液反应的化学方程式:
)与NaF溶液反应的化学方程式:___________ 。
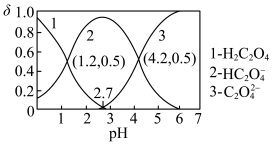
(2)常温下,向某浓度的草酸溶液中逐滴加入一定物质的量浓度的KOH溶液,所得溶液中 、
、 、
、 三种微粒的物质的量分数(δ)与溶液pH的关系如图所示,回答下列问题:
三种微粒的物质的量分数(δ)与溶液pH的关系如图所示,回答下列问题:
①如果所得溶液溶质为 ,则该溶液显
,则该溶液显___________ (填“酸性”、“碱性”或“中性”),其电离方程式为___________ ;
②如果所得溶液溶质为 ,则该溶液中各离子浓度由大到小顺序为
,则该溶液中各离子浓度由大到小顺序为___________ ;
③当所得溶液 时,溶液中
时,溶液中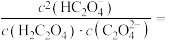
___________ ;
(3)已知25℃草酸钙的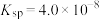 ,碳酸钙的
,碳酸钙的 。回答下列问题:25℃时向10mL碳酸钙的饱和溶液中逐滴加入
。回答下列问题:25℃时向10mL碳酸钙的饱和溶液中逐滴加入 的草酸钾溶液10mL,
的草酸钾溶液10mL,___________ 产生草酸钙沉淀(填“能”或“否”)。
(1)已知某温度下有如下三个反应:
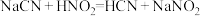


①则该温度下HF、HCN和
 三种弱酸的电离常数由大到小的顺序是
三种弱酸的电离常数由大到小的顺序是②已知:乙二酸(
 ,可简写为
,可简写为 ),俗称草酸;25℃
),俗称草酸;25℃
 ,
,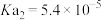 ,25℃
,25℃ ,请写出少量草酸(
,请写出少量草酸( )与NaF溶液反应的化学方程式:
)与NaF溶液反应的化学方程式:(2)常温下,向某浓度的草酸溶液中逐滴加入一定物质的量浓度的KOH溶液,所得溶液中
 、
、 、
、 三种微粒的物质的量分数(δ)与溶液pH的关系如图所示,回答下列问题:
三种微粒的物质的量分数(δ)与溶液pH的关系如图所示,回答下列问题:
①如果所得溶液溶质为
 ,则该溶液显
,则该溶液显②如果所得溶液溶质为
 ,则该溶液中各离子浓度由大到小顺序为
,则该溶液中各离子浓度由大到小顺序为③当所得溶液
 时,溶液中
时,溶液中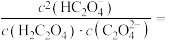
(3)已知25℃草酸钙的
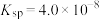 ,碳酸钙的
,碳酸钙的 。回答下列问题:25℃时向10mL碳酸钙的饱和溶液中逐滴加入
。回答下列问题:25℃时向10mL碳酸钙的饱和溶液中逐滴加入 的草酸钾溶液10mL,
的草酸钾溶液10mL,
您最近半年使用:0次
2023-11-09更新
|
404次组卷
|
2卷引用:湖南省邵阳市第二中学2023-2024学年高二上学期基础知识竞赛化学试题
8 . Ni-Cd蓄电池是一类重要的电池,其具有使用寿命长、放电电压稳定、机械性能好等优点,广泛应用于现代军事及航天事业等领域。其中,Ni-Cd蓄电池的正极活性物质为 。资料显示,目前T业上常用化学沉淀法和粉末金属法等方法来制备
。资料显示,目前T业上常用化学沉淀法和粉末金属法等方法来制备 。
。
Ⅰ.化学沉淀法的生产流程图如下所示:
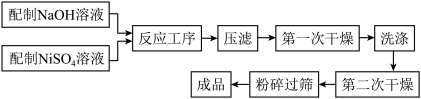
(1)写出该合成方法的化学反应方程式。_______
(2)该反应若在弱碱性条件下进行,则得到碱式硫酸盐 沉淀,请写出该化学反应方程式。
沉淀,请写出该化学反应方程式。_______
(3)在“反应工序”中, 溶液以喷淋形式加入到不断搅拌的过量的NaOH溶液中,搅拌的主要目的是什么?
溶液以喷淋形式加入到不断搅拌的过量的NaOH溶液中,搅拌的主要目的是什么?_______
(4)蒸汽干燥时,干燥温度不能超过200℃,为什么?_______
(5)“洗涤”过程的目的是洗去什么离子?可用什么溶液检验该离子是否洗净?_______
Ⅱ.粉末金属法是以粉末状金属镍为原料,通过镍粉在适当物理化学条件下的氧化水解反应来制备 。
。
(6)写出该方法的化学反应方程式。_______
(7)从动力学角度考虑,通常条件下该反应速度很小,请写出提高反应速率的方法(一条即可)。_______
 。资料显示,目前T业上常用化学沉淀法和粉末金属法等方法来制备
。资料显示,目前T业上常用化学沉淀法和粉末金属法等方法来制备 。
。Ⅰ.化学沉淀法的生产流程图如下所示:

(1)写出该合成方法的化学反应方程式。
(2)该反应若在弱碱性条件下进行,则得到碱式硫酸盐
 沉淀,请写出该化学反应方程式。
沉淀,请写出该化学反应方程式。(3)在“反应工序”中,
 溶液以喷淋形式加入到不断搅拌的过量的NaOH溶液中,搅拌的主要目的是什么?
溶液以喷淋形式加入到不断搅拌的过量的NaOH溶液中,搅拌的主要目的是什么?(4)蒸汽干燥时,干燥温度不能超过200℃,为什么?
(5)“洗涤”过程的目的是洗去什么离子?可用什么溶液检验该离子是否洗净?
Ⅱ.粉末金属法是以粉末状金属镍为原料,通过镍粉在适当物理化学条件下的氧化水解反应来制备
 。
。(6)写出该方法的化学反应方程式。
(7)从动力学角度考虑,通常条件下该反应速度很小,请写出提高反应速率的方法(一条即可)。
您最近半年使用:0次
9 . 实验I和实验Ⅱ中,均有气体产生下列分析错误的是
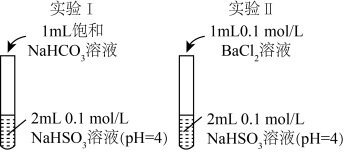

| A.Ⅱ中无沉淀生成 |
| B.I、Ⅱ中生成的气体均可使澄清石灰水变浑浊 |
C.NaHCO3溶液中:c(Na+)> c( ) ) |
D.NaHSO3溶液中:c( )>c(H2SO3) )>c(H2SO3) |
您最近半年使用:0次
2023-05-25更新
|
213次组卷
|
2卷引用:2023年第37届中国化学奥林匹克广西预选赛化学试题
10 . 常温下,向1L 1.0 molLNaClO溶液中缓慢通入SO2气体,使其充分吸收,溶液pH与通入SO2物质的量关系如图所示(忽略溶液体积的变化和NaClO、HClO的分解),下列说法正确的是


| A.常温下,NaClO水解平衡常数的数量级为10-4 |
| B.a点溶液中存在c(HClO)=c(ClO-) |
C.b点时溶液发生反应的离子方程式为SO2+H2O+ClO- =SO +Cl- +2H+ +Cl- +2H+ |
D.c点溶液中存在c(H+)>c(Na+)=c(SO )=c(Cl- )>c(OH-) )=c(Cl- )>c(OH-) |
您最近半年使用:0次
2023-05-25更新
|
256次组卷
|
2卷引用:2023年第37届中国化学奥林匹克广西预选赛化学试题



