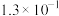解题方法
1 . 室温下,关于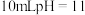 的氨水的说法中,错误的是
的氨水的说法中,错误的是
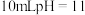 的氨水的说法中,错误的是
的氨水的说法中,错误的是A.加入少量 固体,溶液中 固体,溶液中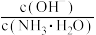 变小 变小 |
B.加入蒸馏水, 的电离程度增大,溶液导电性增强 的电离程度增大,溶液导电性增强 |
C.加入稀硫酸至 ,溶液中: ,溶液中: |
D.与 的盐酸等体积混合后,溶液使甲基橙显黄色 的盐酸等体积混合后,溶液使甲基橙显黄色 |
您最近一年使用:0次
2 .  为阿伏伽德罗常数的值。下列叙述正确的是
为阿伏伽德罗常数的值。下列叙述正确的是
 为阿伏伽德罗常数的值。下列叙述正确的是
为阿伏伽德罗常数的值。下列叙述正确的是A. 的 的 溶液中 溶液中 的数目为 的数目为 |
B.精炼铜阴极增重 时,阳极生成 时,阳极生成 数目为 数目为 |
C. 的 的 溶液中 溶液中 的数目为 的数目为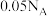 |
D.反应 ,生成 ,生成 ,分子总数减少 ,分子总数减少 |
您最近一年使用:0次
解题方法
3 . 类比推理是化学中常用的思维方法。下列推理正确的是
A.第一电离能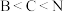 ,推测第一电离能 ,推测第一电离能 |
B.电解熔融 可制得 可制得 ,推测电解熔融 ,推测电解熔融 可制得 可制得 |
C.蒸干 溶液得到 溶液得到 ,推测蒸干 ,推测蒸干 溶液得到 溶液得到 |
D.稀盐酸可降低 的溶解度,推测稀硫酸可降低 的溶解度,推测稀硫酸可降低 的溶解度 的溶解度 |
您最近一年使用:0次
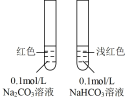
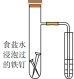
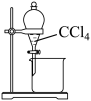
4 . 下列实验装置(部分夹持装置略)或现象错误的是
|
|
|
|
| A.滴入酚酞溶液 | B.吸氧腐蚀 | C.萃取碘水中的碘 | D.由 制取无水 制取无水 固体 固体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-04更新
|
45次组卷
|
2卷引用:湖北省武汉市常青联合体联考2023-2024学年高二上学期1月期末考试化学试题
名校
5 . 某学生欲用已知浓度的氢氧化钠溶液来滴定未知浓度的盐酸溶液,以酚酞试液为滴定指示剂。请填写下列空白:
(1)对于一支洁净的滴定管,使用前两步操作为___________ 、___________ 。

(2)排除碱式滴定管中气泡的方法应采用如图所示操作中的___________ (填序号),然后小心操作使尖嘴部分充满碱液。
(3)用标准的氢氧化钠溶液滴定待测的盐酸溶液时,眼睛应注视___________ 中溶液颜色变化。
(4)下列操作中可能使所测盐酸溶液的浓度偏低的是___________(填字母)。
(5)定量实验应用广泛,如以下两个实验:

①室温时,向100 mL0.1mol·L-1NH4HSO4溶液中滴加0.1mol·L-1NaOH溶液,所得溶液pH与NaOH溶液体积的关系曲线如图所示。试分析图中a、b、c、d四个点,水的电离程度最大的是___________ 点;在b点,溶液中各离子浓度由大到小的排列顺序是___________ 。
②酸性KMnO4溶液滴定Na2C2O4溶液求算Na2C2O4的纯度。反应的离子方程式为___________ 。实验步骤:准确称取1gNa2C2O4固体,配成100mL溶液,取出20.00mL于锥形瓶中。再向瓶中加入足量稀硫酸,用0.016mol·L-1高锰酸钾溶液滴定,滴定至终点时消耗高锰酸钾溶液25.00mL。高锰酸钾溶液应装在___________ (填“酸式”或“碱式”)滴定管中。计算Na2C2O4的纯度为___________ 。
(1)对于一支洁净的滴定管,使用前两步操作为

(2)排除碱式滴定管中气泡的方法应采用如图所示操作中的
(3)用标准的氢氧化钠溶液滴定待测的盐酸溶液时,眼睛应注视
(4)下列操作中可能使所测盐酸溶液的浓度偏低的是___________(填字母)。
| A.量取一定体积的待测液最后读数时滴定管尖嘴处悬挂一滴溶液 |
| B.滴定前盛放盐酸溶液的锥形瓶用蒸馏水洗净后没有干燥 |
| C.碱式滴定管在滴定前有气泡,滴定后气泡消失 |
| D.读取氢氧化钠溶液体积时,开始仰视读数,滴定结束时俯视读数 |
(5)定量实验应用广泛,如以下两个实验:

①室温时,向100 mL0.1mol·L-1NH4HSO4溶液中滴加0.1mol·L-1NaOH溶液,所得溶液pH与NaOH溶液体积的关系曲线如图所示。试分析图中a、b、c、d四个点,水的电离程度最大的是
②酸性KMnO4溶液滴定Na2C2O4溶液求算Na2C2O4的纯度。反应的离子方程式为
您最近一年使用:0次
解题方法
6 . 下列有关化学用语表示正确的是
A. 电离: 电离: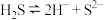 |
B.硫酸氢钠熔融状态下发生电离: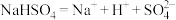 |
C.泡沫灭火器原理: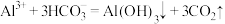 |
D. 水解: 水解: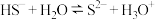 |
您最近一年使用:0次
7 . 医学上常用酸性 溶液和草酸溶液的反应来测定血钙的含量。测定方法如下:
溶液和草酸溶液的反应来测定血钙的含量。测定方法如下:
①将2.00mL血液用蒸馏水稀释至20.00mL后,向其中加入足量 溶液,反应生成
溶液,反应生成 沉淀,过滤后,将沉淀用足量稀硫酸处理得
沉淀,过滤后,将沉淀用足量稀硫酸处理得 溶液;
溶液;
②将①得到的 溶液装入锥形瓶内,再用
溶液装入锥形瓶内,再用 酸性
酸性 溶液滴定,达到终点时用去
溶液滴定,达到终点时用去 溶液的体积为10.00mL。
溶液的体积为10.00mL。
(1)酸性 溶液与
溶液与 反应的离子方程式为
反应的离子方程式为___________ 。
(2)滴定时,酸性 溶液可盛放在___________中。
溶液可盛放在___________中。
(3)判断滴定终点的颜色变化是___________ 。
(4)实验测得该血液中钙的含量为___________  。
。
(5)若滴定过程中,锥形瓶内液体外溅,将导致测定结果___________ 。
(6)已知:25℃时, 的
的 ,
, 的
的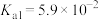 ,
,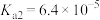 。
。 溶液中,
溶液中,
___________  (填“>”“=”或“<”)。
(填“>”“=”或“<”)。
 溶液和草酸溶液的反应来测定血钙的含量。测定方法如下:
溶液和草酸溶液的反应来测定血钙的含量。测定方法如下:①将2.00mL血液用蒸馏水稀释至20.00mL后,向其中加入足量
 溶液,反应生成
溶液,反应生成 沉淀,过滤后,将沉淀用足量稀硫酸处理得
沉淀,过滤后,将沉淀用足量稀硫酸处理得 溶液;
溶液;②将①得到的
 溶液装入锥形瓶内,再用
溶液装入锥形瓶内,再用 酸性
酸性 溶液滴定,达到终点时用去
溶液滴定,达到终点时用去 溶液的体积为10.00mL。
溶液的体积为10.00mL。(1)酸性
 溶液与
溶液与 反应的离子方程式为
反应的离子方程式为(2)滴定时,酸性
 溶液可盛放在___________中。
溶液可盛放在___________中。| A.酸式滴定管 | B.碱式滴定管 | C.聚四氟乙烯滴定管 | D.锥形瓶 |
(4)实验测得该血液中钙的含量为
 。
。(5)若滴定过程中,锥形瓶内液体外溅,将导致测定结果
(6)已知:25℃时,
 的
的 ,
, 的
的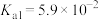 ,
,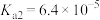 。
。 溶液中,
溶液中,
 (填“>”“=”或“<”)。
(填“>”“=”或“<”)。
您最近一年使用:0次
名校
8 . 常温下,向 溶液中不断通入
溶液中不断通入 。
。 、
、 、
、 在溶液中所占物质的量分数(
在溶液中所占物质的量分数( )与
)与 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是

 溶液中不断通入
溶液中不断通入 。
。 、
、 、
、 在溶液中所占物质的量分数(
在溶液中所占物质的量分数( )与
)与 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是
A.当 时, 时, 的 的 |
B.当溶液呈中性时 |
C.随着 的通入 的通入 一直减小 一直减小 |
D.将等浓度等体积的 与 与 溶液混合后,体系内粒子浓度大小的顺序: 溶液混合后,体系内粒子浓度大小的顺序: |
您最近一年使用:0次
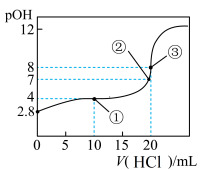
9 . 在25℃时,向50.00mL未知浓度的氨水中逐滴加入0.5 的HCl溶液,滴定过程中,溶液的pOH[
的HCl溶液,滴定过程中,溶液的pOH[ ]与滴入HCl溶液体积的关系如图所示,则下列说法中正确的是
]与滴入HCl溶液体积的关系如图所示,则下列说法中正确的是
 的HCl溶液,滴定过程中,溶液的pOH[
的HCl溶液,滴定过程中,溶液的pOH[ ]与滴入HCl溶液体积的关系如图所示,则下列说法中正确的是
]与滴入HCl溶液体积的关系如图所示,则下列说法中正确的是
| A.图中②点所示溶液的导电能力弱于①点 |
B.③点处水电离出的 |
C.图中点①所示溶液中, |
D.25℃时氨水的 约为 约为 |
您最近一年使用:0次
10 . 已知25℃时,部分弱电解质的电离常数如下表所示:
(1)四种酸 、
、 、
、 、
、 的酸性从强到弱的顺序
的酸性从强到弱的顺序______ 。
(2) 时,将
时,将 溶液和
溶液和
 氨水混合,所得溶液呈
氨水混合,所得溶液呈______ (填“酸”“中”或“碱”)性。
(3) 时,向
时,向 的
的 溶液中逐滴加入
溶液中逐滴加入 溶液,所得混合溶液呈酸性。
溶液,所得混合溶液呈酸性。
①混合溶液中的粒子浓度由大到小的顺序( 除外):
除外):______ 。
②针对该混合溶液,下列说法正确的是______ 。
A.混合溶液存在
B.向混合溶液中继续滴加蒸馏水,溶液酸性减弱, 数值会增大
数值会增大
C.继续向溶液中滴加 溶液至
溶液至 值为6,
值为6,
D.继续滴加 溶液至大于
溶液至大于 时,可能有水电离出
时,可能有水电离出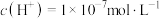
(4)若向 溶液中通入少量
溶液中通入少量 气体,写出发生反应的离子方程式:
气体,写出发生反应的离子方程式:______ 。
弱酸 |
|
|
|
|
|
电离常数 |
|
|
|
|
|
(1)四种酸
 、
、 、
、 、
、 的酸性从强到弱的顺序
的酸性从强到弱的顺序(2)
 时,将
时,将 溶液和
溶液和
 氨水混合,所得溶液呈
氨水混合,所得溶液呈(3)
 时,向
时,向 的
的 溶液中逐滴加入
溶液中逐滴加入 溶液,所得混合溶液呈酸性。
溶液,所得混合溶液呈酸性。①混合溶液中的粒子浓度由大到小的顺序(
 除外):
除外):②针对该混合溶液,下列说法正确的是
A.混合溶液存在

B.向混合溶液中继续滴加蒸馏水,溶液酸性减弱,
 数值会增大
数值会增大C.继续向溶液中滴加
 溶液至
溶液至 值为6,
值为6,
D.继续滴加
 溶液至大于
溶液至大于 时,可能有水电离出
时,可能有水电离出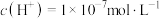
(4)若向
 溶液中通入少量
溶液中通入少量 气体,写出发生反应的离子方程式:
气体,写出发生反应的离子方程式:
您最近一年使用:0次