解题方法
1 . 下列化学用语表述不正确的是
A.醋酸的电离方程式:CH3COOH+H2O CH3COO-+H3O+ CH3COO-+H3O+ |
| B.钢铁发生吸氧腐蚀时,Fe作负极被氧化:Fe-2e-=Fe2+ |
C.Na2CO3溶液显碱性:CO +2H2O +2H2O H2CO3+2OH- H2CO3+2OH- |
D.SO2通入碘水中,反应的离子方程式为SO2+I2+2H2O=SO +2I-+4H+ +2I-+4H+ |
您最近一年使用:0次
名校
2 . 下列方程式书写正确的是( )
A.H2S 的电离方程式:H2S+H2O H3O++HS- H3O++HS- |
| B.NaHCO3在水溶液中的电离方程式:NaHCO3 = Na++H++CO32- |
C.CO32-的水解方程式:CO32-+2H2O  H2CO3+2OH- H2CO3+2OH- |
D.HS-的水解方程式:HS-+H2O  S2-+H3O+ S2-+H3O+ |
您最近一年使用:0次
2017-12-20更新
|
472次组卷
|
9卷引用:河南省漯河市漯河实验高中2020-2021学年高二上学期期中考试化学试题
河南省漯河市漯河实验高中2020-2021学年高二上学期期中考试化学试题福建省闽侯第六中学2017-2018学年高二12月月考化学试题(已下线)2017-2018学年上学期期末复习备考之精准复习模拟题高二化学选修4(B卷)黑龙江省牡丹江市第一高级中学2017-2018学年高二上学期期末考试化学试题【全国百强校】湖南省长沙市雅礼中学2017-2018学年高二下学期期末考试化学试题江西省南昌市八一中学2017-2018学年高二1月月考化学试题湖北省浠水县实验高级中学2018-2019学年高二上学期12月月考化学试题.山东省淄博市淄川中学2019-2020学年高二上学期期中考试化学试题人教版选修四2019-2020学年高二上学期期末复习化学综合训练
3 . 根据叙述判断下列化学用语错误的是
A.电镀时在铁片上镀铜的阴极反应: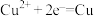 |
B.硫酸氢钠溶液呈酸性的原理 |
C. 溶液的 溶液的 的原因: 的原因: |
D.用 溶液处理水垢中 溶液处理水垢中 的原理: 的原理: |
您最近一年使用:0次
名校
4 . 下列离子方程式书写正确的是( )
A.NaHS的水解:HS-+ H2O S2-+ H3O+ S2-+ H3O+ |
B.NaHCO3在水溶液中的电离:HCO3−+ H2O H2 CO3+ OH− H2 CO3+ OH− |
| C.NH4Cl的水解:NH4+ + H2O = NH3·H2O + OH− |
| D.硫酸铝溶液和碳酸氢钠溶液混合: Al3+ + 3HCO3− = Al(OH)3↓+3CO2↑ |
您最近一年使用:0次
2019-10-20更新
|
177次组卷
|
2卷引用:河南省鲁山县第一高级中学2019-2020学年高二10月月考化学试题
5 . 下列用来表示物质变化的化学用语中,正确的是
A.HS- 的水解方程式:HS-+H2O S2-+H3O+ S2-+H3O+ |
| B.钢铁发生电化学腐蚀的正极反应式:Fe-2e-=Fe2+ |
C.AlCl3溶液与Na2CO3溶液混合:2Al3++3CO =Al2(CO3)3↓ =Al2(CO3)3↓ |
D.CO 的水解方程式:CO 的水解方程式:CO +H2O +H2O HCO HCO +OH- +OH- |
您最近一年使用:0次
12-13高二上·河南许昌·期末
6 . 在25℃时,对于0. 1mol·L-1的氨水,请回答以下问题:
(1)若向氨水中加入少量硫酸铵固体,此时溶液中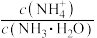 将
将____ (填“增大”、 “减小”或“不变”);
(2)若向氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1∶1,此时溶液的pH____ 7(填“大于”、“小于”或“等于”),用离子方程式表示其原因___________ ,此时溶液中各离子浓度由大到小的顺序为___________________ ;
(3)若向氨水中加入0.05mol·L-1稀硫酸至溶液正好呈中性,所用氨水的体积V1与稀硫酸的体积V2的关系为V1_____ V2(填“大于”、“小于”或“等于”),写出溶液中各离子浓度之间满足的电荷守恒表达式为______________________________________ 。
(1)若向氨水中加入少量硫酸铵固体,此时溶液中
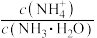 将
将(2)若向氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1∶1,此时溶液的pH
(3)若向氨水中加入0.05mol·L-1稀硫酸至溶液正好呈中性,所用氨水的体积V1与稀硫酸的体积V2的关系为V1
您最近一年使用:0次
解题方法
7 . 反应 可用于工业上制备
可用于工业上制备 。下列化学用语表示错误的是
。下列化学用语表示错误的是
 可用于工业上制备
可用于工业上制备 。下列化学用语表示错误的是
。下列化学用语表示错误的是A.中子数为20的硫原子: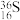 |
B. 的电子式: 的电子式: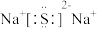 |
C. 溶液显碱性的主要原因: 溶液显碱性的主要原因: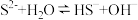 |
D. 溶于稀硫酸生成沉淀和有刺激性气味的气体: 溶于稀硫酸生成沉淀和有刺激性气味的气体: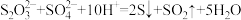 |
您最近一年使用:0次
解题方法
8 . 已知水在 25℃和100℃时,电离平衡曲线如图所示:

(1)25℃时水的电离平衡曲线应为___________ (填“A” 或“B”)。
(2)常温下 ,某溶液中由水电离的 c( H+)=1×10-13mol•L-1,该溶液可能是________
①二氧化硫水溶液② 氯化铵水溶液③ 硝酸钠水溶液④氢氧化钠水溶液
A.①④ B.①② C.②③ D.③④
(3)侯氏制碱法广泛用于工业制纯碱(Na2CO3),是我国科学家为人类做出的重大贡献。现有 25℃时,浓度为0. 10 mol• L-1Na2CO3溶液。请回答:
①该溶液中c( H+)__________ c( OH-)(填“> ”、“< ”或“=”)。
②用离子方程式解释① 的原因_____________ 。
(4)已知在 25℃时,醋酸和亚硫酸的电离平衡常数分别为 :醋酸: K= l. 75× l0- 5;亚硫酸:K1= 1. 54 ×10 - 2K2= 1. 02 × 10-7
①25℃时,相同浓度的醋酸和亚硫酸溶液的酸性强弱:CH3COOH______ H 2SO3(填“> ”、“<”或“=”)。
②25℃时,向0.10mol• L-1CH3COOH溶液中加入少量盐酸,若溶液中c( OH-)为1.0 ×10-12mol•L-1,则该溶液的 pH =______ 。
③向0.10 mol•L-1的CH3COONa溶液中加入少量水, 比值的变化情况是
比值的变化情况是________ (填“增大”、“减少” 或“不变”) 。

(1)25℃时水的电离平衡曲线应为
(2)常温下 ,某溶液中由水电离的 c( H+)=1×10-13mol•L-1,该溶液可能是
①二氧化硫水溶液② 氯化铵水溶液③ 硝酸钠水溶液④氢氧化钠水溶液
A.①④ B.①② C.②③ D.③④
(3)侯氏制碱法广泛用于工业制纯碱(Na2CO3),是我国科学家为人类做出的重大贡献。现有 25℃时,浓度为0. 10 mol• L-1Na2CO3溶液。请回答:
①该溶液中c( H+)
②用离子方程式解释① 的原因
(4)已知在 25℃时,醋酸和亚硫酸的电离平衡常数分别为 :醋酸: K= l. 75× l0- 5;亚硫酸:K1= 1. 54 ×10 - 2K2= 1. 02 × 10-7
①25℃时,相同浓度的醋酸和亚硫酸溶液的酸性强弱:CH3COOH
②25℃时,向0.10mol• L-1CH3COOH溶液中加入少量盐酸,若溶液中c( OH-)为1.0 ×10-12mol•L-1,则该溶液的 pH =
③向0.10 mol•L-1的CH3COONa溶液中加入少量水,
 比值的变化情况是
比值的变化情况是
您最近一年使用:0次
9 . 下列方程式不能准确解释相应实验现象的是
A.向碘的 溶液加入浓KI溶液,振荡,下层颜色变浅: 溶液加入浓KI溶液,振荡,下层颜色变浅: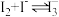 |
B.用碳酸钠溶液处理锅炉水垢: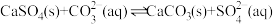 |
C. 水溶液显碱性: 水溶液显碱性: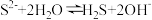 |
D.向 浊液中滴加NaOH溶液,浊液变清: 浊液中滴加NaOH溶液,浊液变清: |
您最近一年使用:0次
名校
10 . 下列实验现象及结论正确的是
| A.向AgNO3溶液中加入几滴NaCl溶液生成白色沉淀,再向试管内加入KI溶液若生成黄色沉淀,则证明KSP (AgCl)> KSP (AgI) |
| B.Na2CO3溶液滴入硼酸溶液中,无气泡生成,说明Ka: H2CO3>H3BO3 |
| C.等物质的量浓度、等体积的CH3COONa和NaClO阴离子的总数前者小于后者 |
| D.若弱酸的酸性H2A>H2B>HA->HB-,则等物质的量浓度等体积的Na2A、Na2B溶液中,离子数目前者等于后者 |
您最近一年使用:0次
2018-01-16更新
|
273次组卷
|
2卷引用:河南省西华县第一高级中学2017-2018学年高二上学期期末选拔考试化学试题



