解题方法
1 . 三硫代碳酸钠(Na2CS3)是强碱弱酸盐,可用于矿石浮选,一般情况下Na2CS3都是以溶液形式存在。某化学兴趣小组利用下图装置测定其溶液的浓度,实验步骤如下:
I.取100.0mL Na2CS3溶液置于仪器M中,打开K,通入一段时间氮气;
II.关闭K,打开分液漏斗活塞,滴入足量2.0mol·L-1稀H2SO4,关闭活塞;
III.反应结束后,再打开K,通入一段时间的热氮气;
IV.将B中混合物进行过滤、洗涤、干燥、称量,得到14.4g固体。
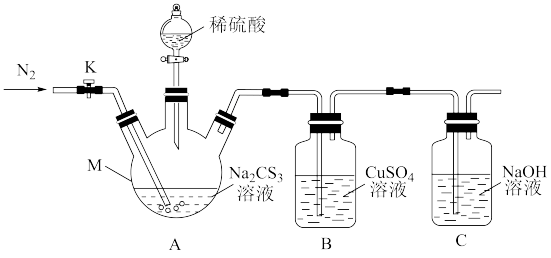
已知:Na2CS3+H2SO4=Na2SO4+CS2+H2S↑。CS2和H2S均有毒,且CS2不溶于水,沸点46℃,与CO2某些性质相似。
回答下列问题:
(1)Na2CS3溶液遇酚酞试液变红,原因是___________ (用离子方程式表示)。
(2)仪器M的名称是___________ ;反应开始前通入氮气的目的是___________ 。
(3)B中发生反应的离子方程式为___________ 。
(4)装置C的作用是___________ 。
(5)根据实验数据计算,Na2CS3溶液的物质的量浓度为___________ 。
(6)反应结束后通入热氮气的目的是___________ 。
I.取100.0mL Na2CS3溶液置于仪器M中,打开K,通入一段时间氮气;
II.关闭K,打开分液漏斗活塞,滴入足量2.0mol·L-1稀H2SO4,关闭活塞;
III.反应结束后,再打开K,通入一段时间的热氮气;
IV.将B中混合物进行过滤、洗涤、干燥、称量,得到14.4g固体。

已知:Na2CS3+H2SO4=Na2SO4+CS2+H2S↑。CS2和H2S均有毒,且CS2不溶于水,沸点46℃,与CO2某些性质相似。
回答下列问题:
(1)Na2CS3溶液遇酚酞试液变红,原因是
(2)仪器M的名称是
(3)B中发生反应的离子方程式为
(4)装置C的作用是
(5)根据实验数据计算,Na2CS3溶液的物质的量浓度为
(6)反应结束后通入热氮气的目的是
您最近一年使用:0次
解题方法
2 . 下列化学用语或图示表达不正确的是
A.砷原子的简化电子排布式为: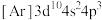 |
B. 的水解方程式: 的水解方程式: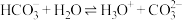 |
C.硫酸钡在水中的沉淀溶解平衡: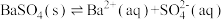 |
| D.一个电子从3p能级跃迁到3s能级,产生的原子光谱为发射光谱 |
您最近一年使用:0次
名校
解题方法
3 . 醋酸是日常生活中最常见的调味剂和重要的化工原料,醋酸钠是其常见的盐。[已知:25℃,Ka(CH3COOH)=1.69×10-5]。请回答下列问题:
(1)写出醋酸钠溶液中存在的平衡(离子方程式):___________ 。
(2)常温时,pH=3的醋酸和pH=11的NaOH溶液等体积混合后,溶液中c(Na+)___________ c(CH3COO-)(填“>”“<”或“=”),该溶液中电荷守恒表达式为___________ 。
(3)常温时,将mmol·L-1的醋酸和nmol·L-1的NaOH溶液等体积混合后,所得溶液的pH=7,则m与n的大小关系是m________ n,醋酸溶液中c(H+)_________ NaOH溶液中c(OH-)(填“>”“<”或“=”)。
(4)某小组研究25℃下CH3COOH电离平衡的影响因素。
提出假设稀释CH3COOH溶液或改变CH3COO-浓度,CH3COOH电离平衡会发生移动。
设计方案并完成实验用浓度均为0.1mol·L-1的CH3COOH和CH3COONa溶液,按下表配制总体积相同的系列溶液;测定pH,记录数据。
①根据表中信息,补充数据:a=___________ ,b=___________ 。
②由实验Ⅰ和Ⅱ可知,稀释CH3COOH溶液,电离平衡___________ (填“正”或“逆”)向移动;结合表中数据,给出判断理由:___________ 。
③由实验Ⅱ~Ⅷ可知,增大CH3COO-浓度,CH3COOH电离平衡逆向移动。
实验结论假设成立。
(1)写出醋酸钠溶液中存在的平衡(离子方程式):
(2)常温时,pH=3的醋酸和pH=11的NaOH溶液等体积混合后,溶液中c(Na+)
(3)常温时,将mmol·L-1的醋酸和nmol·L-1的NaOH溶液等体积混合后,所得溶液的pH=7,则m与n的大小关系是m
(4)某小组研究25℃下CH3COOH电离平衡的影响因素。
提出假设稀释CH3COOH溶液或改变CH3COO-浓度,CH3COOH电离平衡会发生移动。
设计方案并完成实验用浓度均为0.1mol·L-1的CH3COOH和CH3COONa溶液,按下表配制总体积相同的系列溶液;测定pH,记录数据。
| 序号 | V(CH3COOH)/mL | V(CH3COONa)/mL | V(H2O)/mL | n(CH3COONa)∶n(CH3COOH) | pH |
| Ⅰ | 40.00 | / | / | 0 | 2.86 |
| Ⅱ | 4.00 | / | 36.00 | 0 | 3.36 |
| … | |||||
| Ⅶ | 4.00 | a | b | 3∶4 | 4.53 |
| Ⅷ | 4.00 | 4.00 | 32.00 | 1∶1 | 4.65 |
②由实验Ⅰ和Ⅱ可知,稀释CH3COOH溶液,电离平衡
③由实验Ⅱ~Ⅷ可知,增大CH3COO-浓度,CH3COOH电离平衡逆向移动。
实验结论假设成立。
您最近一年使用:0次
4 . 为探究镁与铵盐溶液的反应的速率,现用等质量的镁粉与以下等体积的不同的溶液进行反应,并将实验现象、反应进行至4h时V(H2)记录如下:
①0.5mol/LNH4Cl溶液:有气体产生,并产生白色沉淀、223mL;
②0.25mol/L(NH4)2SO4溶液:有气体产生,并产生白色沉淀、135mL;
③0.1mol/LNH4Cl溶液:有气体产生,并产生白色沉淀、226mL;
④H2O:几乎看不到现象、12mL。
已知:上述溶液中,铵根离子浓度越大,酸性越强。根据上述实验所得结论正确的是
①0.5mol/LNH4Cl溶液:有气体产生,并产生白色沉淀、223mL;
②0.25mol/L(NH4)2SO4溶液:有气体产生,并产生白色沉淀、135mL;
③0.1mol/LNH4Cl溶液:有气体产生,并产生白色沉淀、226mL;
④H2O:几乎看不到现象、12mL。
已知:上述溶液中,铵根离子浓度越大,酸性越强。根据上述实验所得结论正确的是
A.溶液中c(NH )越大,反应速率越快 )越大,反应速率越快 |
B.镁与铵盐溶液反应的离子方程式为Mg + NH + 2H2O= Mg2++2NH3·H2O+H2 + 2H2O= Mg2++2NH3·H2O+H2 |
| C.溶液的pH越小,产生H2的速率越快 |
| D.溶液中阴离子的种类不同会影响产生H2的反应速率 |
您最近一年使用:0次
5 . 下列表示对应化学反应的离子方程式正确的是( )
A.稀硝酸中加入过量铁粉: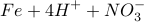  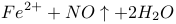 |
B.用铜作电极电解饱和食盐水: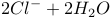  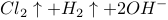 |
C.硫化钠的水解反应: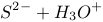  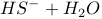 |
D.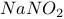 溶液中加入酸性 溶液中加入酸性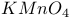 溶液: 溶液: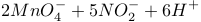  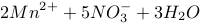 |
您最近一年使用:0次



