1 . 已知 为二元弱酸,且
为二元弱酸,且 ,向
,向 溶液中逐滴加入一元弱酸HB溶液,溶液中的离子浓度变化关系如图所示:
溶液中逐滴加入一元弱酸HB溶液,溶液中的离子浓度变化关系如图所示:
 为二元弱酸,且
为二元弱酸,且 ,向
,向 溶液中逐滴加入一元弱酸HB溶液,溶液中的离子浓度变化关系如图所示:
溶液中逐滴加入一元弱酸HB溶液,溶液中的离子浓度变化关系如图所示:
A. 为 为 随 随 的变化关系 的变化关系 |
B.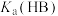 的数量级为 的数量级为 |
C.NaHA溶液中: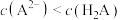 |
D.向 溶液中滴入足量HB溶液的离子方程式为 溶液中滴入足量HB溶液的离子方程式为 |
您最近半年使用:0次
解题方法
2 . 已知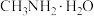 为一元弱碱。常温下,将
为一元弱碱。常温下,将 气体通入
气体通入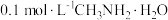 水溶液中,混合溶液的
水溶液中,混合溶液的 与
与 和
和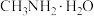 四种微粒浓度对数值(
四种微粒浓度对数值( )的关系如图所示(忽略溶液体积的变化)。下列说法错误的是
)的关系如图所示(忽略溶液体积的变化)。下列说法错误的是
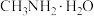 为一元弱碱。常温下,将
为一元弱碱。常温下,将 气体通入
气体通入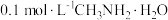 水溶液中,混合溶液的
水溶液中,混合溶液的 与
与 和
和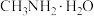 四种微粒浓度对数值(
四种微粒浓度对数值( )的关系如图所示(忽略溶液体积的变化)。下列说法错误的是
)的关系如图所示(忽略溶液体积的变化)。下列说法错误的是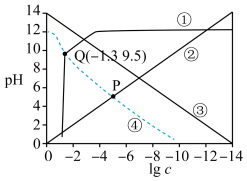
A.①线表示 浓度对数值与溶液 浓度对数值与溶液 的关系 的关系 |
B.常温下, |
C.该体系中, |
D.P点之后,溶液中不可能存在 |
您最近半年使用:0次
7日内更新
|
26次组卷
|
2卷引用:湖北省黄冈市2023-2024学年高二上学期期末调研考试化学试题
名校
解题方法
3 . 一种脱除烟气中 并除去水溶液中
并除去水溶液中 的方法如下图甲所示。室温下用NaOH溶液吸收
的方法如下图甲所示。室温下用NaOH溶液吸收 ,过程中气体挥发和溶液体积的变化可忽略。吸收液中含硫微粒的浓度
,过程中气体挥发和溶液体积的变化可忽略。吸收液中含硫微粒的浓度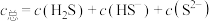 ,含硫微粒分布百分数如下图乙所示。已知室温时
,含硫微粒分布百分数如下图乙所示。已知室温时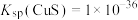

室温时,下列说法正确的是
 并除去水溶液中
并除去水溶液中 的方法如下图甲所示。室温下用NaOH溶液吸收
的方法如下图甲所示。室温下用NaOH溶液吸收 ,过程中气体挥发和溶液体积的变化可忽略。吸收液中含硫微粒的浓度
,过程中气体挥发和溶液体积的变化可忽略。吸收液中含硫微粒的浓度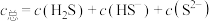 ,含硫微粒分布百分数如下图乙所示。已知室温时
,含硫微粒分布百分数如下图乙所示。已知室温时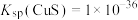

室温时,下列说法正确的是
A.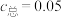 mol⋅L-1的吸收液中: mol⋅L-1的吸收液中: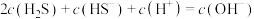 |
B. mol⋅L-1的吸收液中: mol⋅L-1的吸收液中: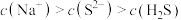 |
C.除铜后所得溶液中一定存在: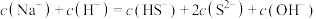 |
D.反应 的平衡常数 的平衡常数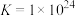 |
您最近半年使用:0次
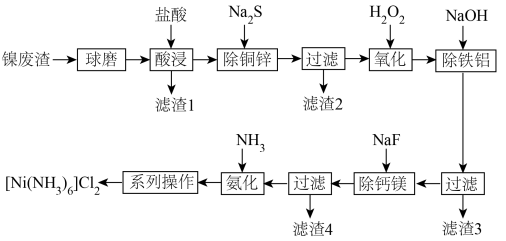
4 . [Ni(NH3)6]Cl2在有机合成中有广泛应用。以镍废渣(主要含Ni、CuO、FeO、ZnO、Al2O3、MgO、CaCO3和SiO2)为原料制备[Ni(NH3)6]Cl2的工艺流程如下。回答下列问题: 都不能氧化
都不能氧化 。
。
②25℃时,几种氢氧化物和氟化物的 如表所示:
如表所示:
③25℃时,几种金属硫化物的 如表所示:
如表所示:
(1)“酸浸”之前“球磨”,目的是___________ ,“酸浸”时适当加热可以提高反应速率,但是温度过高,速率反而减小,其原因是___________ 。
(2)“除铜锌”时,测得溶液中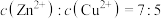 ,最先沉淀的离子是
,最先沉淀的离子是___________ (填离子符号,下同),若溶液中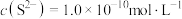 ,此时溶液中被除干净的离子是
,此时溶液中被除干净的离子是___________ (当溶液中某离子的浓度小于或等于 时,认为该离子已被除干净)。
时,认为该离子已被除干净)。
(3)Na2S溶液呈碱性的原因是___________ (用离子方程式表示)。
(4)“除铁铝”中, 时,
时,
___________  。
。
(5)已知常温下, ,则NaF的水解常数
,则NaF的水解常数
___________ ;“除钙镁”时,不能选用玻璃仪器,其原因是___________ 。
 都不能氧化
都不能氧化 。
。②25℃时,几种氢氧化物和氟化物的
 如表所示:
如表所示:| 物质 | Fe(OH)3 | Al(OH)3 | Ni(OH)2 | CaF2 | MgF2 |
 |  | 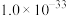 | 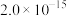 |  |  |
 如表所示:
如表所示:| 金属硫化物 | FeS | NiS | CuS | ZnS |
 | 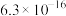 |  |  | 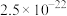 |
(1)“酸浸”之前“球磨”,目的是
(2)“除铜锌”时,测得溶液中
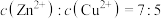 ,最先沉淀的离子是
,最先沉淀的离子是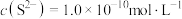 ,此时溶液中被除干净的离子是
,此时溶液中被除干净的离子是 时,认为该离子已被除干净)。
时,认为该离子已被除干净)。(3)Na2S溶液呈碱性的原因是
(4)“除铁铝”中,
 时,
时,
 。
。(5)已知常温下,
 ,则NaF的水解常数
,则NaF的水解常数
您最近半年使用:0次
2024-01-19更新
|
113次组卷
|
2卷引用:江西省部分学校2023-2024学年高三上学期12月月考化学试题
名校
解题方法
5 . 重金属有毒,会对水造成污染,某工厂生产的废水中含有 和少量的
和少量的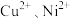 ,可采用图流程进行逐一分离,实现资源再利用。
,可采用图流程进行逐一分离,实现资源再利用。 的
的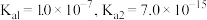 。
。
回答下列问题:
(1) 中
中 元素的化合价为
元素的化合价为_____ , 在还原池中发生反应的离子方程式为
在还原池中发生反应的离子方程式为______ 。
(2)沉淀1是 ,若
,若 时沉淀1恰好沉淀完全,则其
时沉淀1恰好沉淀完全,则其
_______ (已知: ,化为最简),其性质与
,化为最简),其性质与 相似,请写出
相似,请写出 与
与 反应的化学方程式:
反应的化学方程式:_______ 。
(3)① 溶液呈碱性的原因是
溶液呈碱性的原因是_____ (用离子方程式表示),沉淀2是_____ 。
②若有一种溶液由等体积、等物质的量浓度的氢硫酸和硫化钠溶液混合而成,则混合后溶液中的离子浓度关系正确的是_____ (填序号)。
A.
B.
C.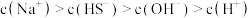
D.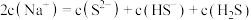
(4)若 时
时 平衡浓度为
平衡浓度为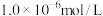 ,则此时沉淀池2中
,则此时沉淀池2中 的浓度为
的浓度为____  。
。
 和少量的
和少量的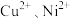 ,可采用图流程进行逐一分离,实现资源再利用。
,可采用图流程进行逐一分离,实现资源再利用。
 的
的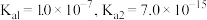 。
。回答下列问题:
(1)
 中
中 元素的化合价为
元素的化合价为 在还原池中发生反应的离子方程式为
在还原池中发生反应的离子方程式为(2)沉淀1是
 ,若
,若 时沉淀1恰好沉淀完全,则其
时沉淀1恰好沉淀完全,则其
 ,化为最简),其性质与
,化为最简),其性质与 相似,请写出
相似,请写出 与
与 反应的化学方程式:
反应的化学方程式:(3)①
 溶液呈碱性的原因是
溶液呈碱性的原因是②若有一种溶液由等体积、等物质的量浓度的氢硫酸和硫化钠溶液混合而成,则混合后溶液中的离子浓度关系正确的是
A.

B.

C.
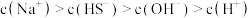
D.
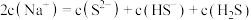
(4)若
 时
时 平衡浓度为
平衡浓度为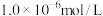 ,则此时沉淀池2中
,则此时沉淀池2中 的浓度为
的浓度为 。
。
您最近半年使用:0次
名校
解题方法
6 . 下列说法正确的是
A.常温下, 的 的 溶液和 溶液和 的 的 溶液等体积混合后所得溶液的 溶液等体积混合后所得溶液的 |
B.两种溶液溶质的物质的量浓度分别为 和 和 ,pH分别为a和 ,pH分别为a和 ,则 ,则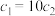 |
C.向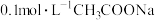 溶液中加入少量水,溶液中 溶液中加入少量水,溶液中 比值增大 比值增大 |
D.常温下, 浓度均为 浓度均为 的 的 、 、 混合溶液中: 混合溶液中: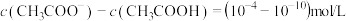 |
您最近半年使用:0次
单选题
|
较难(0.4)
|
7 . 甘氨酸(NH2CH2CO0H)是人体必需氨基酸之一,在25℃时, 、
、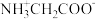 、
、 的分布分数[如
的分布分数[如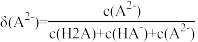 ]与溶液pH关系如图,下列说法错误的是
]与溶液pH关系如图,下列说法错误的是
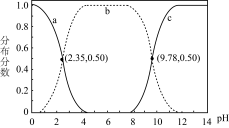
 、
、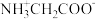 、
、 的分布分数[如
的分布分数[如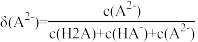 ]与溶液pH关系如图,下列说法错误的是
]与溶液pH关系如图,下列说法错误的是
| A.甘氨酸具有两性 |
B.曲线a代表NH CH2COOH CH2COOH |
C.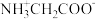 +H2O= +H2O= +OH-的平衡常数K=10-11.65 +OH-的平衡常数K=10-11.65 |
D.c( )·c( )·c( )>c2( )>c2(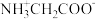 ) ) |
您最近半年使用:0次
2023-12-28更新
|
238次组卷
|
3卷引用:重庆市巴蜀中学校2023-2024学年高三上学期11月期中化学试题
8 . 常温下,将 溶液滴加到乙二酸(
溶液滴加到乙二酸( )溶液中,混合溶液的
)溶液中,混合溶液的 与
与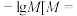
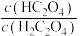 或
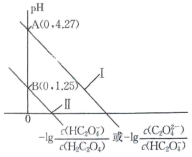
或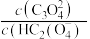 ]的关系如图所示。下列叙述错误的是
]的关系如图所示。下列叙述错误的是
 溶液滴加到乙二酸(
溶液滴加到乙二酸( )溶液中,混合溶液的
)溶液中,混合溶液的 与
与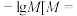
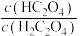 或
或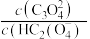 ]的关系如图所示。下列叙述错误的是
]的关系如图所示。下列叙述错误的是
A.曲线II表示 与 与 的变化关系 的变化关系 |
B.乙二酸的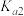 的数量级为 的数量级为 |
C. 溶液呈碱性 溶液呈碱性 |
D. 时, 时,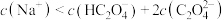 |
您最近半年使用:0次
2023-12-21更新
|
256次组卷
|
3卷引用:山东省级联考2023-2024学年高二上学期12月月考化学试题
解题方法
9 . 25℃时,醋酸的 ,磷酸的
,磷酸的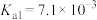 、
、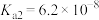 、
、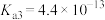 。下列说法不正确的有
。下列说法不正确的有
 ,磷酸的
,磷酸的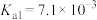 、
、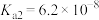 、
、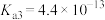 。下列说法不正确的有
。下列说法不正确的有A.0.1mol⋅L  溶液: 溶液: |
B.0.1mol⋅L  溶液: 溶液: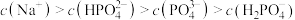 |
C.浓度均为0.1mol⋅L  和 和 混合溶液: 混合溶液: |
D.浓度均为0.1mol⋅L 醋酸和NaOH溶液等体积混合 醋酸和NaOH溶液等体积混合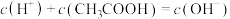 |
您最近半年使用:0次
10 . 草酸亚铁 作为一种化工原料,可广泛用于生产锂离子电池材料、感光材料。以废铁屑为原料生产草酸亚铁的流程如下:
作为一种化工原料,可广泛用于生产锂离子电池材料、感光材料。以废铁屑为原料生产草酸亚铁的流程如下:
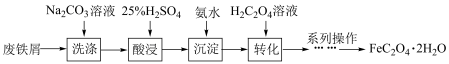
Ⅰ、 为淡黄色固体,难溶于水。
为淡黄色固体,难溶于水。
Ⅱ、25℃时,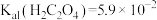 、
、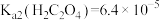 。
。
Ⅲ、25℃时,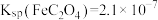 、
、 。
。
(1)用热的饱和碳酸钠溶液洗涤废铁屑的原因是_____ 。
(2)由题中信息判断,25℃时,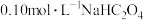 溶液中存在:
溶液中存在: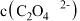
_____  (选填“>”、“<”或“=”)。
(选填“>”、“<”或“=”)。
(3)“转化”步骤在如图所示的装置中进行。

仪器X的名称是_____ ,导管A的作用是_____ 。
(4)“转化”步骤的离子方程式为_____。
(5)说明“转化”步骤中不能用 溶液代替
溶液代替 溶液的原因
溶液的原因_____ 。
(6)流程图中“系列操作”指的是_____ 。
A.过滤、洗涤、干燥
B.蒸发结晶、趁热过滤、洗涤、干燥
C.蒸发浓缩、冷却结晶、过滤、洗涤、干燥
上述制备的草酸亚铁晶体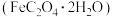 含有
含有 杂质,测定其纯度步骤如下:
杂质,测定其纯度步骤如下:
①准确称取 草酸亚铁晶体样品,溶于稀硫酸中,配成100mL溶液。
草酸亚铁晶体样品,溶于稀硫酸中,配成100mL溶液。
②取20.00mL①中所得的溶液,用 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 。
。
③向滴定后的溶液中加入适量锌粉充分反应后,过滤,洗涤,洗涤液并入滤液中。
④继续用 标准溶液滴定步骤③中所得滤液至终点,消耗
标准溶液滴定步骤③中所得滤液至终点,消耗 。
。
已知:

(7)配制上述100mL溶液,用到的玻璃仪器除了玻璃棒、烧杯外,还有_____ 。
(8)步骤②滴定终点的现象为_____ ;步骤③中加入锌粉的目的是_____ 。
(9)草酸亚铁晶体样品的纯度为_____ 。(用 、
、 、
、 、
、 表示)
表示)
 作为一种化工原料,可广泛用于生产锂离子电池材料、感光材料。以废铁屑为原料生产草酸亚铁的流程如下:
作为一种化工原料,可广泛用于生产锂离子电池材料、感光材料。以废铁屑为原料生产草酸亚铁的流程如下:
Ⅰ、
 为淡黄色固体,难溶于水。
为淡黄色固体,难溶于水。Ⅱ、25℃时,
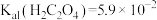 、
、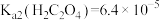 。
。Ⅲ、25℃时,
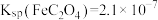 、
、 。
。(1)用热的饱和碳酸钠溶液洗涤废铁屑的原因是
(2)由题中信息判断,25℃时,
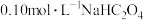 溶液中存在:
溶液中存在: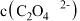
 (选填“>”、“<”或“=”)。
(选填“>”、“<”或“=”)。(3)“转化”步骤在如图所示的装置中进行。

仪器X的名称是
(4)“转化”步骤的离子方程式为_____。
A.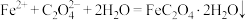 |
B.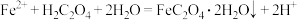 |
C.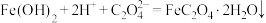 |
D.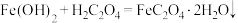 |
(5)说明“转化”步骤中不能用
 溶液代替
溶液代替 溶液的原因
溶液的原因(6)流程图中“系列操作”指的是
A.过滤、洗涤、干燥
B.蒸发结晶、趁热过滤、洗涤、干燥
C.蒸发浓缩、冷却结晶、过滤、洗涤、干燥
上述制备的草酸亚铁晶体
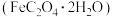 含有
含有 杂质,测定其纯度步骤如下:
杂质,测定其纯度步骤如下:①准确称取
 草酸亚铁晶体样品,溶于稀硫酸中,配成100mL溶液。
草酸亚铁晶体样品,溶于稀硫酸中,配成100mL溶液。②取20.00mL①中所得的溶液,用
 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 。
。③向滴定后的溶液中加入适量锌粉充分反应后,过滤,洗涤,洗涤液并入滤液中。
④继续用
 标准溶液滴定步骤③中所得滤液至终点,消耗
标准溶液滴定步骤③中所得滤液至终点,消耗 。
。已知:


(7)配制上述100mL溶液,用到的玻璃仪器除了玻璃棒、烧杯外,还有
(8)步骤②滴定终点的现象为
(9)草酸亚铁晶体样品的纯度为
 、
、 、
、 、
、 表示)
表示)
您最近半年使用:0次



