名校
解题方法
1 . 硫酸亚铁铵 的制备是化学、化工、材料专业需要完成的无机化学实验,步骤如下:
的制备是化学、化工、材料专业需要完成的无机化学实验,步骤如下:
Ⅰ.称取0.70 g铁屑放在烧杯中,加入足量3mol·L 的
的 溶液,再加入22mL蒸馏水,在70℃水浴锅中反应50~60 min;
溶液,再加入22mL蒸馏水,在70℃水浴锅中反应50~60 min;
Ⅱ.抽滤,在得到的滤液中添加足量 ,
, 溶解后,用3 mol⋅L
溶解后,用3 mol⋅L 的稀硫酸将溶液pH调至1~2;
的稀硫酸将溶液pH调至1~2;
Ⅲ.再将溶液转移至蒸发皿中,用酒精灯加热蒸发,冷却结晶,抽滤,用无水乙醇洗涤晶体1~2次,所得到的产物质量为3.92 g。
回答下列问题:
(1)“步骤Ⅰ”中铁屑发生反应的离子方程式为___________ ,该步骤要在通风橱中进行,其目的是___________ ;若铁屑中混有少量FeS,需将生成的气体通入 溶液,反应过程中该溶液的pH
溶液,反应过程中该溶液的pH___________ (填“升高”“降低”或“不变”)。
(2)“步骤Ⅱ”中用3 mol⋅L 的稀硫酸将溶液pH调至1~2,其目的是
的稀硫酸将溶液pH调至1~2,其目的是___________ , 时该溶液中
时该溶液中
___________ (实验条件下, 的电离常数
的电离常数 、
、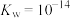 ,保留两位有效数字)。
,保留两位有效数字)。
(3)“步骤Ⅲ”中用酒精灯加热蒸发至___________ 时,停止加热;用无水乙醇洗涤晶体的目的是___________ 。
(4)该实验中硫酸亚铁铵的产率为___________ 。
 的制备是化学、化工、材料专业需要完成的无机化学实验,步骤如下:
的制备是化学、化工、材料专业需要完成的无机化学实验,步骤如下:Ⅰ.称取0.70 g铁屑放在烧杯中,加入足量3mol·L
 的
的 溶液,再加入22mL蒸馏水,在70℃水浴锅中反应50~60 min;
溶液,再加入22mL蒸馏水,在70℃水浴锅中反应50~60 min;Ⅱ.抽滤,在得到的滤液中添加足量
 ,
, 溶解后,用3 mol⋅L
溶解后,用3 mol⋅L 的稀硫酸将溶液pH调至1~2;
的稀硫酸将溶液pH调至1~2;Ⅲ.再将溶液转移至蒸发皿中,用酒精灯加热蒸发,冷却结晶,抽滤,用无水乙醇洗涤晶体1~2次,所得到的产物质量为3.92 g。
回答下列问题:
(1)“步骤Ⅰ”中铁屑发生反应的离子方程式为
 溶液,反应过程中该溶液的pH
溶液,反应过程中该溶液的pH(2)“步骤Ⅱ”中用3 mol⋅L
 的稀硫酸将溶液pH调至1~2,其目的是
的稀硫酸将溶液pH调至1~2,其目的是 时该溶液中
时该溶液中
 的电离常数
的电离常数 、
、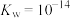 ,保留两位有效数字)。
,保留两位有效数字)。(3)“步骤Ⅲ”中用酒精灯加热蒸发至
(4)该实验中硫酸亚铁铵的产率为
您最近一年使用:0次
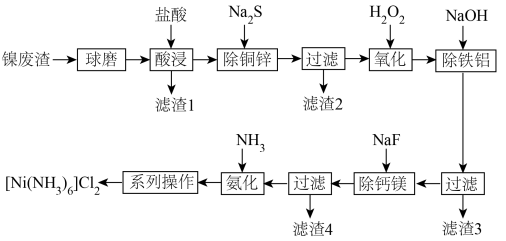
2 . [Ni(NH3)6]Cl2在有机合成中有广泛应用。以镍废渣(主要含Ni、CuO、FeO、ZnO、Al2O3、MgO、CaCO3和SiO2)为原料制备[Ni(NH3)6]Cl2的工艺流程如下。回答下列问题: 都不能氧化
都不能氧化 。
。
②25℃时,几种氢氧化物和氟化物的 如表所示:
如表所示:
③25℃时,几种金属硫化物的 如表所示:
如表所示:
(1)“酸浸”之前“球磨”,目的是___________ ,“酸浸”时适当加热可以提高反应速率,但是温度过高,速率反而减小,其原因是___________ 。
(2)“除铜锌”时,测得溶液中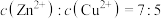 ,最先沉淀的离子是
,最先沉淀的离子是___________ (填离子符号,下同),若溶液中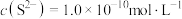 ,此时溶液中被除干净的离子是
,此时溶液中被除干净的离子是___________ (当溶液中某离子的浓度小于或等于 时,认为该离子已被除干净)。
时,认为该离子已被除干净)。
(3)Na2S溶液呈碱性的原因是___________ (用离子方程式表示)。
(4)“除铁铝”中, 时,
时,
___________  。
。
(5)已知常温下, ,则NaF的水解常数
,则NaF的水解常数
___________ ;“除钙镁”时,不能选用玻璃仪器,其原因是___________ 。
 都不能氧化
都不能氧化 。
。②25℃时,几种氢氧化物和氟化物的
 如表所示:
如表所示:| 物质 | Fe(OH)3 | Al(OH)3 | Ni(OH)2 | CaF2 | MgF2 |
 |  | 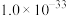 | 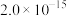 |  |  |
 如表所示:
如表所示:| 金属硫化物 | FeS | NiS | CuS | ZnS |
 | 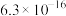 |  |  | 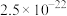 |
(1)“酸浸”之前“球磨”,目的是
(2)“除铜锌”时,测得溶液中
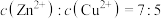 ,最先沉淀的离子是
,最先沉淀的离子是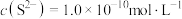 ,此时溶液中被除干净的离子是
,此时溶液中被除干净的离子是 时,认为该离子已被除干净)。
时,认为该离子已被除干净)。(3)Na2S溶液呈碱性的原因是
(4)“除铁铝”中,
 时,
时,
 。
。(5)已知常温下,
 ,则NaF的水解常数
,则NaF的水解常数
您最近一年使用:0次
2024-01-19更新
|
121次组卷
|
2卷引用:江西省部分学校2023-2024学年高三上学期12月月考化学试题
名校
解题方法
3 . 重金属有毒,会对水造成污染,某工厂生产的废水中含有 和少量的
和少量的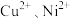 ,可采用图流程进行逐一分离,实现资源再利用。
,可采用图流程进行逐一分离,实现资源再利用。 的
的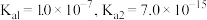 。
。
回答下列问题:
(1) 中
中 元素的化合价为
元素的化合价为_____ , 在还原池中发生反应的离子方程式为
在还原池中发生反应的离子方程式为______ 。
(2)沉淀1是 ,若
,若 时沉淀1恰好沉淀完全,则其
时沉淀1恰好沉淀完全,则其
_______ (已知: ,化为最简),其性质与
,化为最简),其性质与 相似,请写出
相似,请写出 与
与 反应的化学方程式:
反应的化学方程式:_______ 。
(3)① 溶液呈碱性的原因是
溶液呈碱性的原因是_____ (用离子方程式表示),沉淀2是_____ 。
②若有一种溶液由等体积、等物质的量浓度的氢硫酸和硫化钠溶液混合而成,则混合后溶液中的离子浓度关系正确的是_____ (填序号)。
A.
B.
C.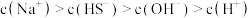
D.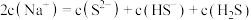
(4)若 时
时 平衡浓度为
平衡浓度为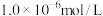 ,则此时沉淀池2中
,则此时沉淀池2中 的浓度为
的浓度为____  。
。
 和少量的
和少量的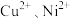 ,可采用图流程进行逐一分离,实现资源再利用。
,可采用图流程进行逐一分离,实现资源再利用。
 的
的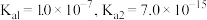 。
。回答下列问题:
(1)
 中
中 元素的化合价为
元素的化合价为 在还原池中发生反应的离子方程式为
在还原池中发生反应的离子方程式为(2)沉淀1是
 ,若
,若 时沉淀1恰好沉淀完全,则其
时沉淀1恰好沉淀完全,则其
 ,化为最简),其性质与
,化为最简),其性质与 相似,请写出
相似,请写出 与
与 反应的化学方程式:
反应的化学方程式:(3)①
 溶液呈碱性的原因是
溶液呈碱性的原因是②若有一种溶液由等体积、等物质的量浓度的氢硫酸和硫化钠溶液混合而成,则混合后溶液中的离子浓度关系正确的是
A.

B.

C.
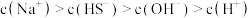
D.
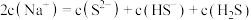
(4)若
 时
时 平衡浓度为
平衡浓度为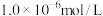 ,则此时沉淀池2中
,则此时沉淀池2中 的浓度为
的浓度为 。
。
您最近一年使用:0次
4 . 草酸亚铁 作为一种化工原料,可广泛用于生产锂离子电池材料、感光材料。以废铁屑为原料生产草酸亚铁的流程如下:
作为一种化工原料,可广泛用于生产锂离子电池材料、感光材料。以废铁屑为原料生产草酸亚铁的流程如下:
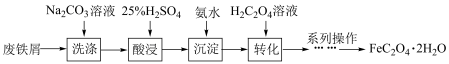
Ⅰ、 为淡黄色固体,难溶于水。
为淡黄色固体,难溶于水。
Ⅱ、25℃时,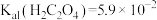 、
、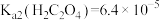 。
。
Ⅲ、25℃时,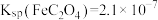 、
、 。
。
(1)用热的饱和碳酸钠溶液洗涤废铁屑的原因是_____ 。
(2)由题中信息判断,25℃时,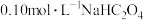 溶液中存在:
溶液中存在: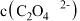
_____  (选填“>”、“<”或“=”)。
(选填“>”、“<”或“=”)。
(3)“转化”步骤在如图所示的装置中进行。

仪器X的名称是_____ ,导管A的作用是_____ 。
(4)“转化”步骤的离子方程式为_____。
(5)说明“转化”步骤中不能用 溶液代替
溶液代替 溶液的原因
溶液的原因_____ 。
(6)流程图中“系列操作”指的是_____ 。
A.过滤、洗涤、干燥
B.蒸发结晶、趁热过滤、洗涤、干燥
C.蒸发浓缩、冷却结晶、过滤、洗涤、干燥
上述制备的草酸亚铁晶体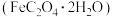 含有
含有 杂质,测定其纯度步骤如下:
杂质,测定其纯度步骤如下:
①准确称取 草酸亚铁晶体样品,溶于稀硫酸中,配成100mL溶液。
草酸亚铁晶体样品,溶于稀硫酸中,配成100mL溶液。
②取20.00mL①中所得的溶液,用 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 。
。
③向滴定后的溶液中加入适量锌粉充分反应后,过滤,洗涤,洗涤液并入滤液中。
④继续用 标准溶液滴定步骤③中所得滤液至终点,消耗
标准溶液滴定步骤③中所得滤液至终点,消耗 。
。
已知:

(7)配制上述100mL溶液,用到的玻璃仪器除了玻璃棒、烧杯外,还有_____ 。
(8)步骤②滴定终点的现象为_____ ;步骤③中加入锌粉的目的是_____ 。
(9)草酸亚铁晶体样品的纯度为_____ 。(用 、
、 、
、 、
、 表示)
表示)
 作为一种化工原料,可广泛用于生产锂离子电池材料、感光材料。以废铁屑为原料生产草酸亚铁的流程如下:
作为一种化工原料,可广泛用于生产锂离子电池材料、感光材料。以废铁屑为原料生产草酸亚铁的流程如下:
Ⅰ、
 为淡黄色固体,难溶于水。
为淡黄色固体,难溶于水。Ⅱ、25℃时,
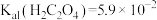 、
、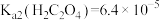 。
。Ⅲ、25℃时,
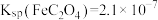 、
、 。
。(1)用热的饱和碳酸钠溶液洗涤废铁屑的原因是
(2)由题中信息判断,25℃时,
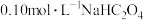 溶液中存在:
溶液中存在: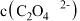
 (选填“>”、“<”或“=”)。
(选填“>”、“<”或“=”)。(3)“转化”步骤在如图所示的装置中进行。

仪器X的名称是
(4)“转化”步骤的离子方程式为_____。
A.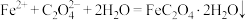 |
B.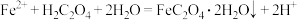 |
C.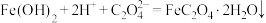 |
D.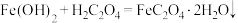 |
(5)说明“转化”步骤中不能用
 溶液代替
溶液代替 溶液的原因
溶液的原因(6)流程图中“系列操作”指的是
A.过滤、洗涤、干燥
B.蒸发结晶、趁热过滤、洗涤、干燥
C.蒸发浓缩、冷却结晶、过滤、洗涤、干燥
上述制备的草酸亚铁晶体
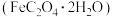 含有
含有 杂质,测定其纯度步骤如下:
杂质,测定其纯度步骤如下:①准确称取
 草酸亚铁晶体样品,溶于稀硫酸中,配成100mL溶液。
草酸亚铁晶体样品,溶于稀硫酸中,配成100mL溶液。②取20.00mL①中所得的溶液,用
 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 。
。③向滴定后的溶液中加入适量锌粉充分反应后,过滤,洗涤,洗涤液并入滤液中。
④继续用
 标准溶液滴定步骤③中所得滤液至终点,消耗
标准溶液滴定步骤③中所得滤液至终点,消耗 。
。已知:


(7)配制上述100mL溶液,用到的玻璃仪器除了玻璃棒、烧杯外,还有
(8)步骤②滴定终点的现象为
(9)草酸亚铁晶体样品的纯度为
 、
、 、
、 、
、 表示)
表示)
您最近一年使用:0次
名校
解题方法
5 . A~E是周期表中1~36号的元素,它们的原子序数递增,对它们的性质及结构的描述如下:A的基态原子只有一种形状的电子云,并容易形成共价键;B的基态原子有3个不同的能级,各能级中电子数相等;C与B同周期,其第一电离能高于周期表中与之邻的所有元素;D在周期表中位于C的下一周期,其电负性在同周期主族元素中最大;E的基态原子在前四周期中未成对电子数最多。
(1)基态B原子的价电子中,两种自旋状态的电子数之比为___________ 。 中C原子的杂化方式为
中C原子的杂化方式为___________ 。
(2)已知元素的电负性:C>D,则C与D形成的化合物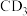 的空间构型为
的空间构型为___________ ,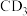 与水发生水解反应的化学方程式为
与水发生水解反应的化学方程式为___________ 。
(3)E位于元素周期表的___________ 区。
(4)已知常温下 的水解常数
的水解常数 。
。
常温下,含等物质的量浓度的HBC与NaBC的混合溶液显___________ (填“酸”“碱”或“中”)性,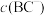
___________ (填“>”“<”或“=”)c(HBC)。常温下,若将 盐酸与
盐酸与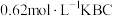 溶液等体积混合后恰好得到中性溶液,则c=
溶液等体积混合后恰好得到中性溶液,则c=___________ (小数点后保留4位数字)。
(1)基态B原子的价电子中,两种自旋状态的电子数之比为
 中C原子的杂化方式为
中C原子的杂化方式为(2)已知元素的电负性:C>D,则C与D形成的化合物
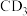 的空间构型为
的空间构型为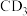 与水发生水解反应的化学方程式为
与水发生水解反应的化学方程式为(3)E位于元素周期表的
(4)已知常温下
 的水解常数
的水解常数 。
。常温下,含等物质的量浓度的HBC与NaBC的混合溶液显
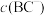
 盐酸与
盐酸与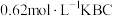 溶液等体积混合后恰好得到中性溶液,则c=
溶液等体积混合后恰好得到中性溶液,则c=
您最近一年使用:0次
2023-12-03更新
|
483次组卷
|
3卷引用:辽宁省沈阳市五校协作体2023-2024学年高二上学期期中考试化学试题
名校
解题方法
6 . 醋酸钠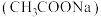 是一种常用的防腐剂和缓冲剂。
是一种常用的防腐剂和缓冲剂。
(1)配制 溶液,需要称量醋酸钠晶体(
溶液,需要称量醋酸钠晶体( ,
,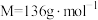 )的质量为
)的质量为_______ 。实验需要的仪器有天平、药匙、玻璃棒、量筒、_______ (从下列图中选择,写出名称)。 水解程度的影响。
水解程度的影响。
甲同学设计实验方案如下(表中溶液浓度均为 ):
):
i.实验_______ 和_______ (填序号),探究加水稀释对 水解程度的影响;
水解程度的影响;
ii.实验1和3,探究加入 对
对 水解程度的影响;
水解程度的影响;
iii.实验1和4,探究温度对 水解程度的影响。
水解程度的影响。
①根据甲同学的实验方案,补充数据:
_______ 。
②实验测得 ,该结果不足以证明加入
,该结果不足以证明加入 促进了
促进了 的水解。根据
的水解。根据_______ (填一种微粒的化学式)的浓度增大可以说明加入 能促进
能促进 的水解。
的水解。
③已知 水解为吸热反应,甲同学预测
水解为吸热反应,甲同学预测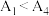 ,但实验结果为
,但实验结果为 。实验结果与预测不一致的原因是
。实验结果与预测不一致的原因是_______ 。
(3)小组通过测定不同温度下 的水解常数
的水解常数 确定温度对
确定温度对 水解程度的影响。
水解程度的影响。
查阅资料: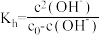 ,
, 为
为 溶液起始浓度。
溶液起始浓度。
试剂: 溶液、
溶液、 盐酸、
盐酸、 计。
计。
实验:测定40℃下 水解常数
水解常数 ,完成下表中序号7的实验。
,完成下表中序号7的实验。
在50℃和60℃下重复上述实验。
数据处理:40℃,
_______ (用含 、
、 、
、 的计算式表示)
的计算式表示)
实验结论: ,温度升高,促进
,温度升高,促进 水解。
水解。
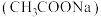 是一种常用的防腐剂和缓冲剂。
是一种常用的防腐剂和缓冲剂。(1)配制
 溶液,需要称量醋酸钠晶体(
溶液,需要称量醋酸钠晶体( ,
,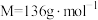 )的质量为
)的质量为
 水解程度的影响。
水解程度的影响。甲同学设计实验方案如下(表中溶液浓度均为
 ):
):i.实验
 水解程度的影响;
水解程度的影响;ii.实验1和3,探究加入
 对
对 水解程度的影响;
水解程度的影响;iii.实验1和4,探究温度对
 水解程度的影响。
水解程度的影响。| 序号 | 温度 | 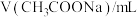 |  | 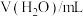 |  |
| 1 | 25℃ | 40.0 | 0 | 0 |  |
| 2 | 25℃ | 4.0 | 0 | 36.0 |  |
| 3 | 25℃ | 20.0 | 10.0 |  |  |
| 4 | 40℃ | 40.0 | 0 | 0 |  |

②实验测得
 ,该结果不足以证明加入
,该结果不足以证明加入 促进了
促进了 的水解。根据
的水解。根据 能促进
能促进 的水解。
的水解。③已知
 水解为吸热反应,甲同学预测
水解为吸热反应,甲同学预测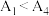 ,但实验结果为
,但实验结果为 。实验结果与预测不一致的原因是
。实验结果与预测不一致的原因是(3)小组通过测定不同温度下
 的水解常数
的水解常数 确定温度对
确定温度对 水解程度的影响。
水解程度的影响。查阅资料:
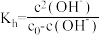 ,
, 为
为 溶液起始浓度。
溶液起始浓度。试剂:
 溶液、
溶液、 盐酸、
盐酸、 计。
计。实验:测定40℃下
 水解常数
水解常数 ,完成下表中序号7的实验。
,完成下表中序号7的实验。| 序号 | 实验 | 记录的数据 |
| 5 | 取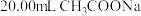 溶液,用 溶液,用 盐酸滴定至终点 盐酸滴定至终点 | 消耗盐酸体积为 |
| 6 | 测40℃纯水的 |  |
| 7 |  |
数据处理:40℃,

 、
、 、
、 的计算式表示)
的计算式表示)实验结论:
 ,温度升高,促进
,温度升高,促进 水解。
水解。
您最近一年使用:0次
2023-03-16更新
|
2368次组卷
|
5卷引用:广东省广州市2023届高三一模考试化学试题
广东省广州市2023届高三一模考试化学试题(已下线)专题19 实验综合题(已下线)广东省广州市天河区2023届高三二模化学试题变式题(实验综合题)广东省广州市2022-2023学年高三普通高中毕业班综合测试(一)化学试题 广东省揭阳华侨高级中学2023-2024学年高三下学期第二次阶段(期中)考试化学试题
解题方法
7 . 研究化学平衡对学习化学具有重要意义。
Ⅰ.在恒容密闭容器中发生如下反应:2NO2(g) N2O4(g) ΔH<0
N2O4(g) ΔH<0
(1)升高温度,该反应的平衡常数_______ (填“增大”“减小”或“不变”)。
(2)判断该反应是否达到平衡,下列可以作为判断依据的是_______。
Ⅱ.一定温度下,向2L的恒容密闭容器中充入一定量的N2和CO2发生反应:N2(g)+CO2(g) C(s)+2NO(g)。其中N2、NO物质的量随时间变化的曲线如下图所示。请回答下列问题。
C(s)+2NO(g)。其中N2、NO物质的量随时间变化的曲线如下图所示。请回答下列问题。

(3)0~10min内NO的反应速率为_______ 。
(4)图中A点υ(正)_______ υ(逆)(填“>”“<”或“=”)。
(5)第10min时,外界改变的条件可能是_______。
Ⅲ.含氯化合物广泛用于水处理剂及漂白剂。已知:工业上将Cl2通入7mol/L的NaOH溶液中制备NaClO;25℃时NaClO溶液中HClO、ClO-的物质的量分数随pH变化的分布如下图所示。

(6)写出上述制备NaClO的离子方程式_______ ;
(7)当NaClO溶液pH=9时,该溶液中主要存在的含氯阴离子有_______ (填离子符号);
(8)25℃时,反应ClO-+H2O HClO+OH-的平衡常数K=
HClO+OH-的平衡常数K=_______ (填数值)。
Ⅰ.在恒容密闭容器中发生如下反应:2NO2(g)
 N2O4(g) ΔH<0
N2O4(g) ΔH<0(1)升高温度,该反应的平衡常数
(2)判断该反应是否达到平衡,下列可以作为判断依据的是_______。
| A.容器内气体密度不再变化 | B.容器内各气体浓度不再变化 |
| C.体系中颜色不再变化 | D.υ正(NO2)=2υ正(N2O4) |
Ⅱ.一定温度下,向2L的恒容密闭容器中充入一定量的N2和CO2发生反应:N2(g)+CO2(g)
 C(s)+2NO(g)。其中N2、NO物质的量随时间变化的曲线如下图所示。请回答下列问题。
C(s)+2NO(g)。其中N2、NO物质的量随时间变化的曲线如下图所示。请回答下列问题。
(3)0~10min内NO的反应速率为
(4)图中A点υ(正)
(5)第10min时,外界改变的条件可能是_______。
| A.加催化剂 | B.增大C(s)的量 |
| C.升温 | D.减小CO2的量 |
Ⅲ.含氯化合物广泛用于水处理剂及漂白剂。已知:工业上将Cl2通入7mol/L的NaOH溶液中制备NaClO;25℃时NaClO溶液中HClO、ClO-的物质的量分数随pH变化的分布如下图所示。

(6)写出上述制备NaClO的离子方程式
(7)当NaClO溶液pH=9时,该溶液中主要存在的含氯阴离子有
(8)25℃时,反应ClO-+H2O
 HClO+OH-的平衡常数K=
HClO+OH-的平衡常数K=
您最近一年使用:0次
解题方法
8 . Ce2(CO3)3可用于催化剂载体及功能材料的制备。天然独居石中,铈(Ce)主要以 CePO4形式存在,还含有 SiO2、Al2O3、Fe2O3、CaF2等物质。以独居石为原料制备Ce2(CO3)3·nH2O的工艺流程如下:
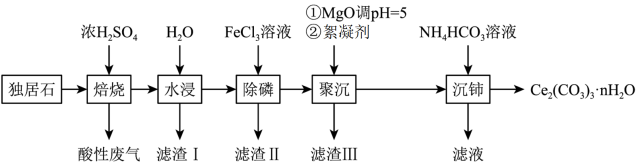
回答下列问题:
(1)CePO4中Ce的化合价为
(2)为提高“水浸”效率,可采取的措施有
(3)滤渣I的主要成分是
(4)“聚沉”过程中,调pH=5的目的是
(5)“沉铈”过程中有CO2气体生成,写出生成Ce2(CO3)3·nH2O时发生的离子方程式:
(6)滤渣Ⅱ的主要成分为FePO4,在高温条件下,Li2CO3、葡萄糖(C6H12O6)和 FePO4可制备电极材料LiFePO4,同时生成CO和H2O,该反应的化学方程式为
您最近一年使用:0次
2023-02-12更新
|
294次组卷
|
2卷引用:广东省汕头市潮阳区教师发展中心教学研究室 2022-2023学年高二上学期期末质量检测化学试题
解题方法
9 . 实验室模拟拉希法用氨和次氯酸钠反应制备肼 ,并探究肼的性质,制备装置如图所示。
,并探究肼的性质,制备装置如图所示。
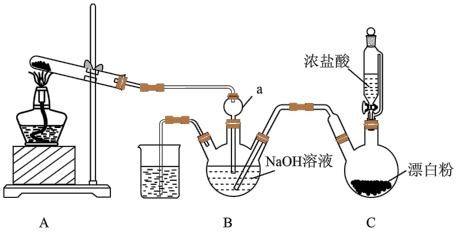
回答下列问题:
(1)肼的电子式为_______ 。
(2)装置A试管中的试剂为_______ ,仪器a的作用是_______ 。
(3)装置B中制备肼的化学方程式为_______ 。
(4)上述装置中存在一处缺陷,会导致肼的产率降低,改进方法是_______ 。
(5)①探究性质。
已知 是一种二元弱碱,在水中的电离与
是一种二元弱碱,在水中的电离与 相似,请写出肼的第二步电离的电离方程式:
相似,请写出肼的第二步电离的电离方程式:_______ ,室温下向 水溶液中滴加某强酸,溶液的
水溶液中滴加某强酸,溶液的 与
与 或
或 的变化关系如图所示,下列说法正确的是
的变化关系如图所示,下列说法正确的是_______ (填标号)。
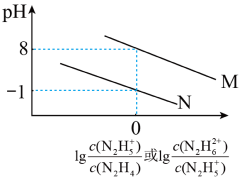
A. 在水溶液中第二步电离的平衡常数为
在水溶液中第二步电离的平衡常数为
B.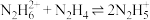 的平衡常数为
的平衡常数为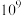
C. 的水解能力大于其电离能力
的水解能力大于其电离能力
D.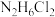 溶液中:
溶液中: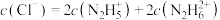
②测定产品中肼的质量分数。
称取装置B中溶液mg,加入适量 固体(滴定过程中,调节溶液的
固体(滴定过程中,调节溶液的 ),加水配成
),加水配成 溶液,移取
溶液,移取 置于锥形瓶中,并滴加
置于锥形瓶中,并滴加 滴指示剂,用
滴指示剂,用 的碘标准溶液滴定,滴定过程中有无色无味无毒气体产生,定终点时平均消耗标准溶液VmL,产品中肼的质量分数为
的碘标准溶液滴定,滴定过程中有无色无味无毒气体产生,定终点时平均消耗标准溶液VmL,产品中肼的质量分数为_______ (用含m、c、V的式子表示)。
 ,并探究肼的性质,制备装置如图所示。
,并探究肼的性质,制备装置如图所示。
回答下列问题:
(1)肼的电子式为
(2)装置A试管中的试剂为
(3)装置B中制备肼的化学方程式为
(4)上述装置中存在一处缺陷,会导致肼的产率降低,改进方法是
(5)①探究性质。
已知
 是一种二元弱碱,在水中的电离与
是一种二元弱碱,在水中的电离与 相似,请写出肼的第二步电离的电离方程式:
相似,请写出肼的第二步电离的电离方程式: 水溶液中滴加某强酸,溶液的
水溶液中滴加某强酸,溶液的 与
与 或
或 的变化关系如图所示,下列说法正确的是
的变化关系如图所示,下列说法正确的是
A.
 在水溶液中第二步电离的平衡常数为
在水溶液中第二步电离的平衡常数为
B.
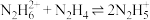 的平衡常数为
的平衡常数为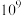
C.
 的水解能力大于其电离能力
的水解能力大于其电离能力D.
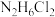 溶液中:
溶液中: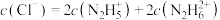
②测定产品中肼的质量分数。
称取装置B中溶液mg,加入适量
 固体(滴定过程中,调节溶液的
固体(滴定过程中,调节溶液的 ),加水配成
),加水配成 溶液,移取
溶液,移取 置于锥形瓶中,并滴加
置于锥形瓶中,并滴加 滴指示剂,用
滴指示剂,用 的碘标准溶液滴定,滴定过程中有无色无味无毒气体产生,定终点时平均消耗标准溶液VmL,产品中肼的质量分数为
的碘标准溶液滴定,滴定过程中有无色无味无毒气体产生,定终点时平均消耗标准溶液VmL,产品中肼的质量分数为
您最近一年使用:0次
解题方法
10 . 200℃时,气态肼(N2H4)在Cu-Ni双金属表面分解的过程如下:
过程Ⅰ:3N2H4(g)=N2(g)+4NH3(g) △H1=akJ•mol-1
过程Ⅱ:2NH3(g)=N2(g)+3H2(g) △H2=+92kJ•mol-1
已知相关化学键的数据如表所示:
(1)过程Ⅰ中a=_____ ,写出气态肼(N2H4)在Cu-Ni双金属表面分解成氮气和氢气的热化学方程式_____ 。
(2)300℃时,向2L刚性容器中充入1molN2H4发生分解成N2和H2的反应,不同时刻测得容器内压强的变化如表所示:
反应前5小时内的平均反应速率v(N2)为_____ mol•L-1•h-1,平衡时H2的分压p(H2)=_____ MPa。
(3)在温度为573K、压强为100kPa的反应条件下,对于n(N2H4):n(Ne)分别为3:1、1:1、1:3、1:6的N2H4-Ne混合气在热分解反应过程中N2H4的转化率随时间的变化如图所示:

①n(N2H4):n(Ne)的比值越小,N2H4的平衡转化率越_____ (填“大”或“小”),理由是_____ 。
②n(N2H4):n(Ne)=1:3所对应的曲线是_____ (填字母代号)。
(4)肼(N2H4)又称联氨,溶于水可以发生与氨水类似的电离,是一种二元弱碱。肼溶于水的电离方程式为:
N2H4+H2O N2H
N2H +OH- Kb1=2×10-8
+OH- Kb1=2×10-8
N2H +H2O
+H2O N2H
N2H +OH- Kb2=6×10-10
+OH- Kb2=6×10-10
现将等浓度等体积的肼的水溶液与硫酸溶液混合,混合后生成的盐的化学式为_____ ,混合后溶液中 =
=_____ 。
过程Ⅰ:3N2H4(g)=N2(g)+4NH3(g) △H1=akJ•mol-1
过程Ⅱ:2NH3(g)=N2(g)+3H2(g) △H2=+92kJ•mol-1
已知相关化学键的数据如表所示:
| 化学键 | H-H | N-N | N≡N | H-N |
| E/(kJ•mol-1) | x | 265 | 946 | y |
(2)300℃时,向2L刚性容器中充入1molN2H4发生分解成N2和H2的反应,不同时刻测得容器内压强的变化如表所示:
| 时间/h | 0 | 1 | 2 | 3 | 5 | 6 | 7 |
| p/MPa | 50 | 60 | 80 | 120 | 140 | 140 | 140 |
(3)在温度为573K、压强为100kPa的反应条件下,对于n(N2H4):n(Ne)分别为3:1、1:1、1:3、1:6的N2H4-Ne混合气在热分解反应过程中N2H4的转化率随时间的变化如图所示:

①n(N2H4):n(Ne)的比值越小,N2H4的平衡转化率越
②n(N2H4):n(Ne)=1:3所对应的曲线是
(4)肼(N2H4)又称联氨,溶于水可以发生与氨水类似的电离,是一种二元弱碱。肼溶于水的电离方程式为:
N2H4+H2O
 N2H
N2H +OH- Kb1=2×10-8
+OH- Kb1=2×10-8N2H
 +H2O
+H2O N2H
N2H +OH- Kb2=6×10-10
+OH- Kb2=6×10-10现将等浓度等体积的肼的水溶液与硫酸溶液混合,混合后生成的盐的化学式为
 =
=
您最近一年使用:0次



