研究化学平衡对学习化学具有重要意义。
Ⅰ.在恒容密闭容器中发生如下反应:2NO2(g) N2O4(g) ΔH<0
N2O4(g) ΔH<0
(1)升高温度,该反应的平衡常数_______ (填“增大”“减小”或“不变”)。
(2)判断该反应是否达到平衡,下列可以作为判断依据的是_______。
Ⅱ.一定温度下,向2L的恒容密闭容器中充入一定量的N2和CO2发生反应:N2(g)+CO2(g) C(s)+2NO(g)。其中N2、NO物质的量随时间变化的曲线如下图所示。请回答下列问题。
C(s)+2NO(g)。其中N2、NO物质的量随时间变化的曲线如下图所示。请回答下列问题。

(3)0~10min内NO的反应速率为_______ 。
(4)图中A点υ(正)_______ υ(逆)(填“>”“<”或“=”)。
(5)第10min时,外界改变的条件可能是_______。
Ⅲ.含氯化合物广泛用于水处理剂及漂白剂。已知:工业上将Cl2通入7mol/L的NaOH溶液中制备NaClO;25℃时NaClO溶液中HClO、ClO-的物质的量分数随pH变化的分布如下图所示。

(6)写出上述制备NaClO的离子方程式_______ ;
(7)当NaClO溶液pH=9时,该溶液中主要存在的含氯阴离子有_______ (填离子符号);
(8)25℃时,反应ClO-+H2O HClO+OH-的平衡常数K=
HClO+OH-的平衡常数K=_______ (填数值)。
Ⅰ.在恒容密闭容器中发生如下反应:2NO2(g)
 N2O4(g) ΔH<0
N2O4(g) ΔH<0(1)升高温度,该反应的平衡常数
(2)判断该反应是否达到平衡,下列可以作为判断依据的是_______。
| A.容器内气体密度不再变化 | B.容器内各气体浓度不再变化 |
| C.体系中颜色不再变化 | D.υ正(NO2)=2υ正(N2O4) |
Ⅱ.一定温度下,向2L的恒容密闭容器中充入一定量的N2和CO2发生反应:N2(g)+CO2(g)
 C(s)+2NO(g)。其中N2、NO物质的量随时间变化的曲线如下图所示。请回答下列问题。
C(s)+2NO(g)。其中N2、NO物质的量随时间变化的曲线如下图所示。请回答下列问题。
(3)0~10min内NO的反应速率为
(4)图中A点υ(正)
(5)第10min时,外界改变的条件可能是_______。
| A.加催化剂 | B.增大C(s)的量 |
| C.升温 | D.减小CO2的量 |
Ⅲ.含氯化合物广泛用于水处理剂及漂白剂。已知:工业上将Cl2通入7mol/L的NaOH溶液中制备NaClO;25℃时NaClO溶液中HClO、ClO-的物质的量分数随pH变化的分布如下图所示。

(6)写出上述制备NaClO的离子方程式
(7)当NaClO溶液pH=9时,该溶液中主要存在的含氯阴离子有
(8)25℃时,反应ClO-+H2O
 HClO+OH-的平衡常数K=
HClO+OH-的平衡常数K=
更新时间:2023-02-13 15:45:37
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】现代工业生产过程注重氮、硫、碳等元素的化合物的综合利用。工业上可利用CO或CO2来生产燃料甲醇。已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如表所示:
(1)若恒容密闭容器中反应①,下列叙述中不能说明反应①达到平衡状态的是____ 。
(2)工业上利用反应①合成甲醇时,既能加快反应速率,又能提高CO平衡转化率的措施有____ 。
(3)在3L容积可变的密闭容器中发生反应②,已知c(CO)—反应时间t变化曲线I如图所示,若在t0时刻分别改变一个条件,曲线I变为曲线II和曲线III。

①当曲线I变为曲线I时,改变的条件是____ 。
②当曲线I变为曲线III时,改变的条件是(指明具体操作)____ 。
(4)反应③是____ 反应(填“吸热”或者“放热”),理由是____ 。
(5)500℃时测得反应③在某时刻,H2(g)、CO2(g)、CH3OH(g)、H2O(g)的浓度(mol•L-1)分别为0.8、0.1、0.3、0.15,则此时v正____ v逆(填“>”、“=”或“<”),理由是____ 。
| 化学反应 | 平衡常数 | 温度/℃ | |
| 500 | 800 | ||
①2H2(g)+CO(g) CH3OH(g) CH3OH(g) | K1 | 2.5 | 0.15 |
②H2(g)+CO2(g) H2O(g)+CO(g) H2O(g)+CO(g) | K2 | 1.0 | 2.50 |
③3H2(g)+CO2(g) CH3OH(g)+H2O(g) CH3OH(g)+H2O(g) | K3 | ||
| A.体系压强不再变化 | B.气体平均摩尔质量不再变化 |
| C.H2的消耗速率和CO的消耗速率之比为2:1 | D.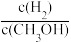 保持不变 保持不变 |
| A.升高温度 | B.加入催化剂 | C.将甲醇及时分离出去 | D.增大反应体系的压强 |

①当曲线I变为曲线I时,改变的条件是
②当曲线I变为曲线III时,改变的条件是(指明具体操作)
(4)反应③是
(5)500℃时测得反应③在某时刻,H2(g)、CO2(g)、CH3OH(g)、H2O(g)的浓度(mol•L-1)分别为0.8、0.1、0.3、0.15,则此时v正
您最近一年使用:0次
【推荐2】新技术的开发应用,不仅有利于改善环境质量,而且能充分开发“废物”的潜在价值。
回答下列问题:
(1)用烟道气与氢气来合成甲醇涉及到如下几个反应:
①CO(g)+2H2(g)=CH3OH(g) △H=-91kJ·mol-1
②2CO2(g)=2CO(g)+O2(g) △H=+566kJ·mol-1
③2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ·mol-1
④CO2(g)+3H2(g)=CH3OH(g)+H2O(g)∆H=__ kJ·mol-1。
(2)在容积均为2L的两个恒容密闭容器中发生反应CO(g)+H2O(g) CO2(g)+H2(g),有关数据如下:
CO2(g)+H2(g),有关数据如下:
①800°C时该反应的平衡常数K=__ 。
②容器2中x=__ ,n=___ 。
③若800℃起始时,在2L恒容密闭容器中加入CO、H2O、CO2、H2各1mol,则此时v正__ v逆(填“>”“<”或“=”)。
(3)反应(NH4)2CO3+H2O+CO2 2NH4HCO3OH可用于捕捉空气中的CO2,为研究温度对(NH4)2CO3捕获CO2效率的影响,在某温度T1下,将一定量的(NH4)2CO3溶液置于密闭容器中,并充入一定量的CO2气体,在t时刻,测得容器中CO2气体的浓度。然后分别在温度为T2、T3、T4、T5下,保持其他初始实验条件不变,重复上述实验,经过相同时间测定CO2气体的浓度,得到的曲线图如图:
2NH4HCO3OH可用于捕捉空气中的CO2,为研究温度对(NH4)2CO3捕获CO2效率的影响,在某温度T1下,将一定量的(NH4)2CO3溶液置于密闭容器中,并充入一定量的CO2气体,在t时刻,测得容器中CO2气体的浓度。然后分别在温度为T2、T3、T4、T5下,保持其他初始实验条件不变,重复上述实验,经过相同时间测定CO2气体的浓度,得到的曲线图如图:
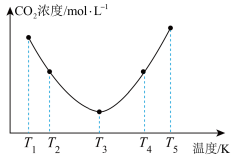
①∆H__ 0(填“>”“<”或“=”)。T1~T2区间,c(CO2)变化的原因是___ 。
②已知常温下NH3·H2O的电离常数K=1.8×10-5,碳酸的电离常数K1=4.4×10-7、K2=4.7×10-11,则恰好完全反应时所得的NH4HCO3溶液中c(H+)__ c(OH-)(填“>”“<”或“=”)。
③在图中所示五种温度下,该反应的平衡常数最大的温度是__ 。
回答下列问题:
(1)用烟道气与氢气来合成甲醇涉及到如下几个反应:
①CO(g)+2H2(g)=CH3OH(g) △H=-91kJ·mol-1
②2CO2(g)=2CO(g)+O2(g) △H=+566kJ·mol-1
③2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ·mol-1
④CO2(g)+3H2(g)=CH3OH(g)+H2O(g)∆H=
(2)在容积均为2L的两个恒容密闭容器中发生反应CO(g)+H2O(g)
 CO2(g)+H2(g),有关数据如下:
CO2(g)+H2(g),有关数据如下:| 容器 | 温度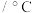 | 起始量 | 达到平衡 | |||
| CO/mol | H2O/mol | H2/mol | CO转化率 | 所需时间/min | ||
| 1 | 800 | 2 | 1 | 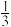 | 3 | |
| 2 | 800 | 1 | 2 | n | x | |
②容器2中x=
③若800℃起始时,在2L恒容密闭容器中加入CO、H2O、CO2、H2各1mol,则此时v正
(3)反应(NH4)2CO3+H2O+CO2
 2NH4HCO3OH可用于捕捉空气中的CO2,为研究温度对(NH4)2CO3捕获CO2效率的影响,在某温度T1下,将一定量的(NH4)2CO3溶液置于密闭容器中,并充入一定量的CO2气体,在t时刻,测得容器中CO2气体的浓度。然后分别在温度为T2、T3、T4、T5下,保持其他初始实验条件不变,重复上述实验,经过相同时间测定CO2气体的浓度,得到的曲线图如图:
2NH4HCO3OH可用于捕捉空气中的CO2,为研究温度对(NH4)2CO3捕获CO2效率的影响,在某温度T1下,将一定量的(NH4)2CO3溶液置于密闭容器中,并充入一定量的CO2气体,在t时刻,测得容器中CO2气体的浓度。然后分别在温度为T2、T3、T4、T5下,保持其他初始实验条件不变,重复上述实验,经过相同时间测定CO2气体的浓度,得到的曲线图如图:
①∆H
②已知常温下NH3·H2O的电离常数K=1.8×10-5,碳酸的电离常数K1=4.4×10-7、K2=4.7×10-11,则恰好完全反应时所得的NH4HCO3溶液中c(H+)
③在图中所示五种温度下,该反应的平衡常数最大的温度是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】锰及其化合物在现代工业及国防建设中具有十分重要的地位,回答下列问题:
(1) 中锰为+6价,溶液显绿色,只能在强碱性环境中存在,在中性和酸性环境中会发生歧化反应生成高锰酸根离子和二氧化锰或低价的锰盐。
中锰为+6价,溶液显绿色,只能在强碱性环境中存在,在中性和酸性环境中会发生歧化反应生成高锰酸根离子和二氧化锰或低价的锰盐。
已知存在如下平衡:3 +2H2O
+2H2O MnO2+2
MnO2+2 +4OH−。
+4OH−。
①若溶液由绿色变为紫色,则向溶液中滴加的试剂为______________ (填标号);
A.碳酸钠 B.氢氧化钠 C.稀硫酸 D.硫酸钠
②其他条件不变,升高温度,溶液的pH减小,则该反应的ΔH____ 0(填“大于”“小于”或“等于”);
③该反应的平衡常数表达式K=____________ 。
(2)用硫酸酸化的高锰酸钾溶液与草酸(H2C2O4)反应,溶液颜色褪去,有气体生成,无沉淀产生。高锰酸钾溶液与草酸反应过程中草酸溶液浓度随时间变化关系如图所示。

①写出发生反应的化学方程式:__________________________ ;
②计算前10 s用高锰酸钾表示的平均反应速率v(高锰酸钾)=________________ ;
③10 s~15 s的反应速率比前10 s快,其原因可能是_________________________________ 。
(3)碳酸锰是制造电信器材软磁铁氧体、合成二氧化锰和制造其他锰盐的原料。工业上常用MnSO4和NaHCO3反应制备MnCO3。
①该反应的离子方程式为_________________________ ;
②加入稍过量的NaHCO3,MnSO4的转化率将_________ (填“增大”“减小”或“不变”);
③向物质的量浓度均为0.01 mol·L−1的MnCl2和BaCl2混合溶液中,滴加Na2CO3溶液,先沉淀的离子是_________ (填离子符号),当两种难溶电解质共存时,溶液中 =
=____________ [此温度下,Ksp(BaCO3)=8.1×10−9、Ksp(MnCO3)=1.8×10−11]。
(1)
 中锰为+6价,溶液显绿色,只能在强碱性环境中存在,在中性和酸性环境中会发生歧化反应生成高锰酸根离子和二氧化锰或低价的锰盐。
中锰为+6价,溶液显绿色,只能在强碱性环境中存在,在中性和酸性环境中会发生歧化反应生成高锰酸根离子和二氧化锰或低价的锰盐。已知存在如下平衡:3
 +2H2O
+2H2O MnO2+2
MnO2+2 +4OH−。
+4OH−。 ①若溶液由绿色变为紫色,则向溶液中滴加的试剂为
A.碳酸钠 B.氢氧化钠 C.稀硫酸 D.硫酸钠
②其他条件不变,升高温度,溶液的pH减小,则该反应的ΔH
③该反应的平衡常数表达式K=
(2)用硫酸酸化的高锰酸钾溶液与草酸(H2C2O4)反应,溶液颜色褪去,有气体生成,无沉淀产生。高锰酸钾溶液与草酸反应过程中草酸溶液浓度随时间变化关系如图所示。

①写出发生反应的化学方程式:
②计算前10 s用高锰酸钾表示的平均反应速率v(高锰酸钾)=
③10 s~15 s的反应速率比前10 s快,其原因可能是
(3)碳酸锰是制造电信器材软磁铁氧体、合成二氧化锰和制造其他锰盐的原料。工业上常用MnSO4和NaHCO3反应制备MnCO3。
①该反应的离子方程式为
②加入稍过量的NaHCO3,MnSO4的转化率将
③向物质的量浓度均为0.01 mol·L−1的MnCl2和BaCl2混合溶液中,滴加Na2CO3溶液,先沉淀的离子是
 =
=
您最近一年使用:0次
【推荐1】I.已知:CO2(g)+H2(g) CO(g)+H2O(g) △H1=+41.2kJ·mol-1 K1
CO(g)+H2O(g) △H1=+41.2kJ·mol-1 K1
CO(g)+2H2(g) CH3OH(g) △H2=-90.6kJ·mol-1 K2
CH3OH(g) △H2=-90.6kJ·mol-1 K2
则CO2(g)和H2(g)的反应生成CH3OH(g)的热化学方程式III为_______ ,该反应的化学平衡常数K3=_______ 。(用K1,K2表示)
II.已知A(g)+B(g)⇌C(g)+D(g)反应的平衡常数和温度的关系如下:
回答下列问题:
(1)该反应的△H=_______ 0(填“<”“>”“=”);
(2)900℃时,向一个固定容器为2L的密闭容器中充入0.20mol的A和0.80mol的B,若反应初始到2s内A浓度变化0.05mol•L-1。则A的平均反应速率v(A)=_______ 。该反应达到平衡时A的转化率为 _______ ,如果这时向该密闭容器中再充入1mol氩气,平衡时A的转化率 _______ (填”变大“、”变小“或”不变“)
(3)1200℃时,若向另一相同容器中充入0.30molA、0.40mol B、0.40mol C和0.50molD,此时v正_______ v逆(填”大于“、”小于“或”等于“)。
 CO(g)+H2O(g) △H1=+41.2kJ·mol-1 K1
CO(g)+H2O(g) △H1=+41.2kJ·mol-1 K1CO(g)+2H2(g)
 CH3OH(g) △H2=-90.6kJ·mol-1 K2
CH3OH(g) △H2=-90.6kJ·mol-1 K2则CO2(g)和H2(g)的反应生成CH3OH(g)的热化学方程式III为
II.已知A(g)+B(g)⇌C(g)+D(g)反应的平衡常数和温度的关系如下:
| 温度/℃ | 700 | 800 | 900 | 1000 | 1200 |
| 平衡常数 | 0.5 | 0.6 | 1.0 | 1.6 | 2.0 |
回答下列问题:
(1)该反应的△H=
(2)900℃时,向一个固定容器为2L的密闭容器中充入0.20mol的A和0.80mol的B,若反应初始到2s内A浓度变化0.05mol•L-1。则A的平均反应速率v(A)=
(3)1200℃时,若向另一相同容器中充入0.30molA、0.40mol B、0.40mol C和0.50molD,此时v正
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】回答下列问题:
(1)一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示。

①从反应开始到10s,用Z的浓度变化表示的反应速率为____ 。Y的转化率____ 。该反应的化学方程式为____ 。
②10s后的某一时刻(t1)改变了外界条件,其反应速率随时间的变化图象如图所示。则下列说法符合该图象的是_____ 。

A.t1时,增大了X的浓度 B.t1时,升高了体系温度
C.t1时,缩小了容器体积 D.t1时,使用了催化剂
(2)已知:CO(g)+H2O(g) CO2(g)+H2(g) ΔH=Q,其平衡常数随温度变化如表所示:
CO2(g)+H2(g) ΔH=Q,其平衡常数随温度变化如表所示:
请回答下列问题:
①上述反应的化学平衡常数表达式为_____ ,该反应的Q____ 0(填“>”或“<”)。
②恒温条件下,该反应达到化学平衡状态的依据是_____ (填字母)。
a.c(CO2)=c(CO) b.K不变 c.容器中的压强不变 d.v正(H2)=v逆(CO2) e.c(H2)保持不变
③在850℃时,在平衡体系中含有1molCO2、1.2molH2、2molCO、1.5molH2O,则此时反应所处的状态为____ (填“向正反应方向进行”“向逆反应方向进行”或“平衡状态”)。
(1)一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示。

①从反应开始到10s,用Z的浓度变化表示的反应速率为
②10s后的某一时刻(t1)改变了外界条件,其反应速率随时间的变化图象如图所示。则下列说法符合该图象的是

A.t1时,增大了X的浓度 B.t1时,升高了体系温度
C.t1时,缩小了容器体积 D.t1时,使用了催化剂
(2)已知:CO(g)+H2O(g)
 CO2(g)+H2(g) ΔH=Q,其平衡常数随温度变化如表所示:
CO2(g)+H2(g) ΔH=Q,其平衡常数随温度变化如表所示:| 温度/℃ | 400 | 500 | 850 |
| 平衡常数 | 9.94 | 9 | 1 |
请回答下列问题:
①上述反应的化学平衡常数表达式为
②恒温条件下,该反应达到化学平衡状态的依据是
a.c(CO2)=c(CO) b.K不变 c.容器中的压强不变 d.v正(H2)=v逆(CO2) e.c(H2)保持不变
③在850℃时,在平衡体系中含有1molCO2、1.2molH2、2molCO、1.5molH2O,则此时反应所处的状态为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】铁及铁的氧化物广泛应用于生产、生活、航天、科研等领域,利用Fe2O3与CH4可制备“纳米级”金属铁,回答下列问题:
①3H2(g)+Fe2O3(s)⇌2Fe(s)+3H2O(g) ΔH1=-26.5kJ·mol-1
②CO2(g)+4H2(g)⇌CH4(g)+2H2O(g) ΔH2=-160kJ·mol-1
(1)3CH4(g)+4Fe2O3(s)⇌8Fe(s)+6H2O(g)+3CO2(g) ΔH=_______ 。
(2)一定温度下,向盛有足量Fe2O3(s)的1L恒容容器中充入1molH2和1molCH4,发生反应①、②,一段时间后,反应达平衡,此时n(CO2)=amol,n(H2O)=bmol,则该温度下反应②的平衡常数为_______ 。
(3)在T℃下,向某密闭容器中加入3molCH4(g)和2molFe2O3(s)发生反应3CH4(g)+4Fe2O3(s)⇌8Fe(s)+6H2O(l)+3CO2(g),反应起始时压强为p0,反应进行至10min时达到平衡状态,测得此时容器中n(CH4)∶n(H2O)=1∶1,10min内用Fe2O3(s)表示的平均反应速率为_______ g·min-1;T℃下该反应的Kp=_______ (以分压表示,分压=总压×物质的量分数);T℃下若起始时向该容器中加入2molCH4(g)、4molFe2O3(s)、1molFe(s)、2molH2O(l)、2molCO2(g),则起始时v(正)_______ v(逆)(填“>”“<”或“=”)。
(4)一定温度下,密闭容器中进行反应3CH4(g)+4Fe2O3(s)⇌8Fe(s)+6H2O(g)+
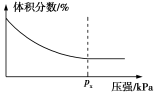
3CO2(g),测得平衡时混合物中某气体物质的体积分数随压强的变化如图所示,则纵坐标表示的物质是_______ ,随着压强增大,纵坐标的体积分数变化的原因是_______ 。
①3H2(g)+Fe2O3(s)⇌2Fe(s)+3H2O(g) ΔH1=-26.5kJ·mol-1
②CO2(g)+4H2(g)⇌CH4(g)+2H2O(g) ΔH2=-160kJ·mol-1
(1)3CH4(g)+4Fe2O3(s)⇌8Fe(s)+6H2O(g)+3CO2(g) ΔH=
(2)一定温度下,向盛有足量Fe2O3(s)的1L恒容容器中充入1molH2和1molCH4,发生反应①、②,一段时间后,反应达平衡,此时n(CO2)=amol,n(H2O)=bmol,则该温度下反应②的平衡常数为
(3)在T℃下,向某密闭容器中加入3molCH4(g)和2molFe2O3(s)发生反应3CH4(g)+4Fe2O3(s)⇌8Fe(s)+6H2O(l)+3CO2(g),反应起始时压强为p0,反应进行至10min时达到平衡状态,测得此时容器中n(CH4)∶n(H2O)=1∶1,10min内用Fe2O3(s)表示的平均反应速率为
(4)一定温度下,密闭容器中进行反应3CH4(g)+4Fe2O3(s)⇌8Fe(s)+6H2O(g)+
3CO2(g),测得平衡时混合物中某气体物质的体积分数随压强的变化如图所示,则纵坐标表示的物质是

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】弱电解质在水溶液中的电离状况可以进行定量计算和推测。
(1)25℃时两种酸的电离平衡常数如表所示。
①25℃时,0.100mol·L-1的NaA溶液中H+、OH-、Na+、A-、HA的物质的量浓度由大到小的顺序是:___ 。pH=8的NaA溶液中由水电离出的c(OH-)=___ mol·L-1。
②25℃时,0.100mol·L-1的NaHB溶液pH___ 7,理由是___ 。
③25℃时,向0.100mol·L-1的Na2B溶液中滴加足量0.100mol·L-1的HA溶液,反应的离子方程式为___ 。
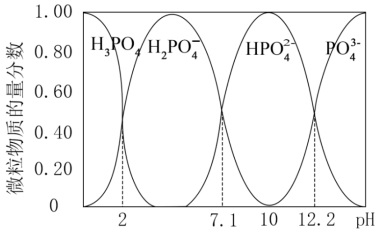
(2)已知25℃时,向0.100mol·L-1的H3PO4溶液中滴加NaOH溶液,各含磷微粒的物质的量分数随pH变化的关系如图所示。
①当溶液pH由11到14时,所发生反应的离子方程式为:___ 。
(1)25℃时两种酸的电离平衡常数如表所示。
| Ka1 | Ka2 | |
| HA | 1×10-4 | |
| H2B | 1×10-2 | 5×10-6 |
①25℃时,0.100mol·L-1的NaA溶液中H+、OH-、Na+、A-、HA的物质的量浓度由大到小的顺序是:
②25℃时,0.100mol·L-1的NaHB溶液pH
③25℃时,向0.100mol·L-1的Na2B溶液中滴加足量0.100mol·L-1的HA溶液,反应的离子方程式为
(2)已知25℃时,向0.100mol·L-1的H3PO4溶液中滴加NaOH溶液,各含磷微粒的物质的量分数随pH变化的关系如图所示。

①当溶液pH由11到14时,所发生反应的离子方程式为:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】雾霾含有大量的 等污染性气体,工业上通过雾霾处理可获得
等污染性气体,工业上通过雾霾处理可获得 和
和 。下图为工业处理
。下图为工业处理 和
和 制
制 和
和 的一种流程(
的一种流程( 为铈元素)。
为铈元素)。

(1) 中S元素的化合价为
中S元素的化合价为______ 。
(2)装置IV获得 粗产品的实验操作依次为蒸发浓缩、冷却结晶、
粗产品的实验操作依次为蒸发浓缩、冷却结晶、______ 、洗涤、低温干燥。
(3)已知 的电离平衡常数
的电离平衡常数 ;则
;则 溶液中
溶液中
______  (填“>”、<”或“=”)。
(填“>”、<”或“=”)。
(4)装置Ⅱ中 被
被 (酸性环境下)氧化为
(酸性环境下)氧化为 的离子方程式为
的离子方程式为______ 。
(5)装置Ⅲ电解时, 在
在______ (填“阴”或“阳”)极反应,使 得到再生;每生成
得到再生;每生成 时,可得到
时,可得到______  ;电解后溶液
;电解后溶液
______ (填“增大”、“减小”或“不变”)。
 等污染性气体,工业上通过雾霾处理可获得
等污染性气体,工业上通过雾霾处理可获得 和
和 。下图为工业处理
。下图为工业处理 和
和 制
制 和
和 的一种流程(
的一种流程( 为铈元素)。
为铈元素)。
(1)
 中S元素的化合价为
中S元素的化合价为(2)装置IV获得
 粗产品的实验操作依次为蒸发浓缩、冷却结晶、
粗产品的实验操作依次为蒸发浓缩、冷却结晶、(3)已知
 的电离平衡常数
的电离平衡常数 ;则
;则 溶液中
溶液中
 (填“>”、<”或“=”)。
(填“>”、<”或“=”)。(4)装置Ⅱ中
 被
被 (酸性环境下)氧化为
(酸性环境下)氧化为 的离子方程式为
的离子方程式为(5)装置Ⅲ电解时,
 在
在 得到再生;每生成
得到再生;每生成 时,可得到
时,可得到 ;电解后溶液
;电解后溶液
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】25℃时,0.1 mol·L-1的HA溶液中 =1010,0.01 mol·L-1的BOH溶液pH=12。请回答下列问题:
=1010,0.01 mol·L-1的BOH溶液pH=12。请回答下列问题:
(1)HA是_______ (填“强电解质”或“弱电解质”),BOH是______ 。(填“强电解质”或“弱电解质”)
(2)在体积相等、pH相等的HA溶液与盐酸溶液中加入足量Zn,HA溶液中产生的气体比盐酸中产生的气体________ (填“多”“少”或“相等”)。
(3)在25℃下,将amol/L的氨水与0.01mol/L的盐酸等体积混合,反应平衡时溶液中c( )=c(Cl-),则溶液显
)=c(Cl-),则溶液显________ 性(填“酸”、“碱”或“中”);用含a的代数式表示NH3·H2O的电离常数Kb=________ 。
(4)水电离生成H3O+ 和OH- 叫做水的自偶电离。同水一样,液氨也有自偶电离,其自偶电离的电离方程式为:________________________________ 。
 =1010,0.01 mol·L-1的BOH溶液pH=12。请回答下列问题:
=1010,0.01 mol·L-1的BOH溶液pH=12。请回答下列问题:(1)HA是
(2)在体积相等、pH相等的HA溶液与盐酸溶液中加入足量Zn,HA溶液中产生的气体比盐酸中产生的气体
(3)在25℃下,将amol/L的氨水与0.01mol/L的盐酸等体积混合,反应平衡时溶液中c(
 )=c(Cl-),则溶液显
)=c(Cl-),则溶液显(4)水电离生成H3O+ 和OH- 叫做水的自偶电离。同水一样,液氨也有自偶电离,其自偶电离的电离方程式为:
您最近一年使用:0次



