名校
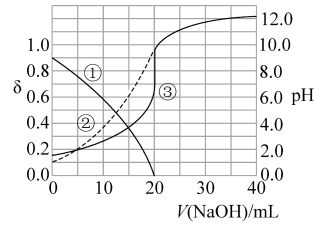
1 . 次磷酸(H3PO2)是一种精细磷化工产品。常温下,某实验小组以酚酞为指示剂,用0.100mol·L-1的NaOH溶液滴定20.00mL0.100mol·L-1的次磷酸(H3PO2)溶液。溶液pH、所有含磷微粒的分布系数δ随滴加NaOH溶液体积V(NaOH)的变化关系如图所示[比如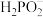 的分布系数:
的分布系数: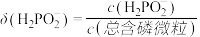 ],下列叙述正确的是
],下列叙述正确的是
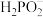 的分布系数:
的分布系数: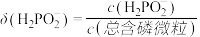 ],下列叙述正确的是
],下列叙述正确的是
A.曲线①代表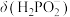 ,曲线②代表 ,曲线②代表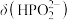 |
| B.NaH2PO2是酸式盐,其水溶液显碱性 |
C.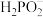 水解常数Kh≈1.0×10-9 水解常数Kh≈1.0×10-9 |
D.当滴定至中性时,溶液中存在: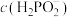 +c(H3PO2)>c(Na+) +c(H3PO2)>c(Na+) |
您最近一年使用:0次
2021-07-20更新
|
543次组卷
|
2卷引用:山西省运城市2022届高三上学期入学摸底测试化学试题
2 . 2020年9月22日,中国国家主席习近平在第七十五届联合国大会上庄严宣布,中国将力争2030年前实现碳达峰、2060年前实现碳中和。研究CO2的转化及高值化利用具有重要意义。
I.已知CO2溶于水的过程及其平衡常数可表示为:
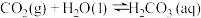
 ,
,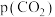 表示CO2的平衡压强,
表示CO2的平衡压强,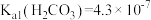 ,
, ,
,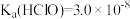
(1)天然雨水的pH<7,用电离方程式解释其原因___________ 。
(2)将CO2通入NaClO水溶液中,发生的主要反应为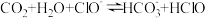 。写出该反应的平衡常数表达式:K=
。写出该反应的平衡常数表达式:K=___________ [用 、
、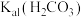 和
和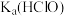 的式子表示]
的式子表示]
(3)根据平衡常数计算说明 CO2通入NaClO水溶液中,主要反应并非:
 :
:___________ 。
II.在双功能催化剂作用下。由CO2加氢可以合成二甲醚。涉及以下主要反应。
反应1(甲醇合成):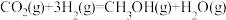
反应2(甲醇脱水):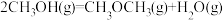
反应3(逆水汽变换):
相关物质变化的焓变示意图如下:
双功能催化剂通常由甲醇合成活性中心和甲醇脱水活性中心组成。在一定条件下,将CO2与H2以1:3体积比通过双功能催化剂,测定含碳产物的物质的量分数随时间变化如图1所示。
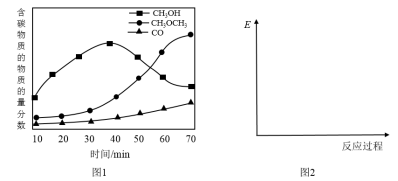
(4)写出反应3的热化学方程式___________ 。
(5)在图2中画出采用双功能催化剂由CO2加氢合成二甲醚的能量变化图_____ 。
(6)下列说法正确的是___________ 。
A.为提高工业生产效率,合成二甲醚的适宜条件是高温高压
B.可通过监测反应体系中CH3OCH3和H2O浓度比判断是否达到平衡
C.反应达平衡时,若缩小容器体积,反应3平衡不发生移动
D.一定温度、压强下,寻找活性更高的催化剂,是提高CO2平衡转化率的研究方向
I.已知CO2溶于水的过程及其平衡常数可表示为:
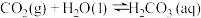
 ,
,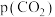 表示CO2的平衡压强,
表示CO2的平衡压强,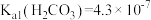 ,
, ,
,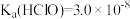
(1)天然雨水的pH<7,用电离方程式解释其原因
(2)将CO2通入NaClO水溶液中,发生的主要反应为
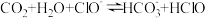 。写出该反应的平衡常数表达式:K=
。写出该反应的平衡常数表达式:K= 、
、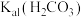 和
和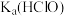 的式子表示]
的式子表示](3)根据平衡常数
 :
:II.在双功能催化剂作用下。由CO2加氢可以合成二甲醚。涉及以下主要反应。
反应1(甲醇合成):
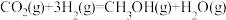
反应2(甲醇脱水):
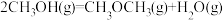
反应3(逆水汽变换):

相关物质变化的焓变示意图如下:
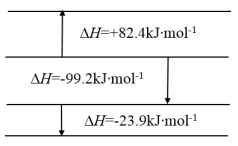 | 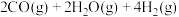 |
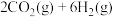 | |
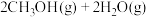 | |
 |
双功能催化剂通常由甲醇合成活性中心和甲醇脱水活性中心组成。在一定条件下,将CO2与H2以1:3体积比通过双功能催化剂,测定含碳产物的物质的量分数随时间变化如图1所示。

(4)写出反应3的热化学方程式
(5)在图2中画出采用双功能催化剂由CO2加氢合成二甲醚的能量变化图
(6)下列说法正确的是
A.为提高工业生产效率,合成二甲醚的适宜条件是高温高压
B.可通过监测反应体系中CH3OCH3和H2O浓度比判断是否达到平衡
C.反应达平衡时,若缩小容器体积,反应3平衡不发生移动
D.一定温度、压强下,寻找活性更高的催化剂,是提高CO2平衡转化率的研究方向
您最近一年使用:0次
2021-06-28更新
|
172次组卷
|
2卷引用:浙江省天台中学2021-2022学年高二上学期返校考试化学试题
3 . 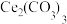 可用于催化剂载体及功能材料的制备。天然独居石中,铈(Ce)主要以
可用于催化剂载体及功能材料的制备。天然独居石中,铈(Ce)主要以 形式存在,还含有
形式存在,还含有 、
、 、
、 、
、 等物质。以独居石为原料制备
等物质。以独居石为原料制备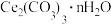 的工艺流程如下:
的工艺流程如下:
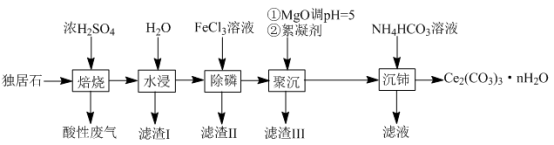
回答下列问题:
(1)铈的某种核素含有58个质子和80个中子,该核素的符号为_______ ;
(2)为提高“水浸”效率,可采取的措施有_______ (至少写两条);
(3)滤渣Ⅲ的主要成分是_______ (填化学式);
(4)加入絮凝剂的目的是_______ ;
(5)“沉铈”过程中,生成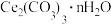 的离子方程式为
的离子方程式为_______ ,常温下加入的 溶液呈
溶液呈_______ (填“酸性”“碱性”或“中性”)(已知: 的
的 ,
, 的
的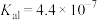 ,
, );
);
(6)滤渣Ⅱ的主要成分为 ,在高温条件下,
,在高温条件下, 、葡萄糖(
、葡萄糖( )和
)和 可制备电极材料
可制备电极材料 ,同时生成
,同时生成 和
和 ,该反应的化学方程式为
,该反应的化学方程式为_______
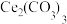 可用于催化剂载体及功能材料的制备。天然独居石中,铈(Ce)主要以
可用于催化剂载体及功能材料的制备。天然独居石中,铈(Ce)主要以 形式存在,还含有
形式存在,还含有 、
、 、
、 、
、 等物质。以独居石为原料制备
等物质。以独居石为原料制备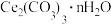 的工艺流程如下:
的工艺流程如下:
回答下列问题:
(1)铈的某种核素含有58个质子和80个中子,该核素的符号为
(2)为提高“水浸”效率,可采取的措施有
(3)滤渣Ⅲ的主要成分是
(4)加入絮凝剂的目的是
(5)“沉铈”过程中,生成
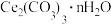 的离子方程式为
的离子方程式为 溶液呈
溶液呈 的
的 ,
, 的
的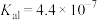 ,
, );
);(6)滤渣Ⅱ的主要成分为
 ,在高温条件下,
,在高温条件下, 、葡萄糖(
、葡萄糖( )和
)和 可制备电极材料
可制备电极材料 ,同时生成
,同时生成 和
和 ,该反应的化学方程式为
,该反应的化学方程式为
您最近一年使用:0次
2021-06-09更新
|
11116次组卷
|
32卷引用:黑龙江省齐齐哈尔市讷河市第一中学2023-2024学年高二下学期开学考试化学试题
黑龙江省齐齐哈尔市讷河市第一中学2023-2024学年高二下学期开学考试化学试题2021年新高考湖南化学高考真题(已下线)微专题32 化学工艺流程题——核心反应与条件控制-备战2022年高考化学考点微专题(已下线)微专题31 化学工艺流程题——原料的预处理-备战2022年高考化学考点微专题(已下线)考点15 铁及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点15 铁及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点31 化学实验与工艺流程-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考向09 工艺流程初探-备战2022年高考化学一轮复习考点微专题(已下线)专题讲座(六)化工流程的解题策略(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)2021年湖南省高考化学试卷变式题11-19(已下线)解密06 金属及其化合物(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)解密06 金属及其化合物(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)专题27 无机化工流程-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)(已下线)专题15 工艺流程综合题-2022年高考化学二轮复习重点专题常考点突破练(已下线)专题11 无机工艺流程题—2022年高考化学二轮复习讲练测(全国版)-练习(已下线)押新高考卷14题 工艺流程综合题-备战2022年高考化学临考题号押题(新高考通版)(已下线)回归教材重难点08 化学工艺流程分析-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)专题16 工艺流程题-三年(2020-2022)高考真题分项汇编(已下线)考点14 铁及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)微专题28 有关工艺流程和实验探究方程式的书写-备战2023年高考化学一轮复习考点微专题(已下线)第09讲 无机非金属材料(讲)-2023年高考化学一轮复习讲练测(新教材新高考)湖南省常德市汉寿县第一中学2022-2023学年高三上学期第一次月考化学试题山东省滨州市沾化区实验高级中学2022-2023学年高三上学期第二次月考化学试题第二部分 热点专项突破——解题能力稳提升 专项1 物质制备类的工艺流程 热点1 以矿物为载体的工艺流程(已下线)第八章 水溶液中的离子反应与平衡 第55讲 无机化工流程题的解题策略(已下线)第二部分 工业生产流程 综合提能训练(已下线)专题18 工艺流程题(已下线)专题18 工艺流程题福建省永春第一中学2022-2023学年高二下学期6月月考化学试题(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(全国通用)(已下线)考点47 无机工艺流程(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)微专题 无机化工流程题的解题策略
解题方法
4 . 硫及其化合物在生产生活中有广泛的应用。请回答:
(1)室温下, 溶液呈碱性的原因是
溶液呈碱性的原因是___________ (用离子方程式表示)。
(2)下列关于硫及其化合物的说法,正确的是___________ (填字母)。
A.硫元素在自然界中只能以化合态形式存在
B. 通入紫色石蕊试液,先变红后褪色
通入紫色石蕊试液,先变红后褪色
C.酸雨是 的降水,主要是由污染物
的降水,主要是由污染物 、
、 造成
造成
D.浓硫酸中加入少量胆矾晶体,搅拌,固体逐渐变成白色
(3)光谱研究表明, 的水溶液中存在下列平衡:
的水溶液中存在下列平衡:
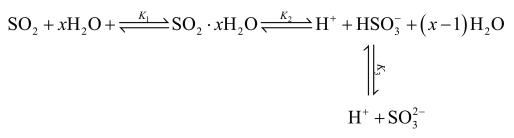
其中 、
、 、
、 为各步的平衡常数,且
为各步的平衡常数,且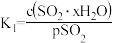 (
( 表示
表示 的平衡压强)。
的平衡压强)。
①当 的平衡压强为p时,测得
的平衡压强为p时,测得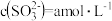 ,则溶液
,则溶液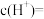
___________ 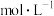 。
。
(用含p、a、 、
、 、
、 的式子表示)
的式子表示)
②滴加NaOH至 时,溶液中
时,溶液中 。如果溶液中
。如果溶液中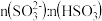
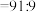 ,需加NaOH将溶液pH调整为约等于
,需加NaOH将溶液pH调整为约等于___________ 。
(4)“钙基固硫”是利用石灰石将燃煤烟气中的 转化为
转化为 。但高温时CO会与
。但高温时CO会与 反应而影响脱硫效率。相关反应如下:
反应而影响脱硫效率。相关反应如下:
Ⅰ.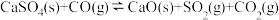
Ⅱ.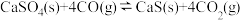
当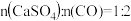 时,反应25min,体系中
时,反应25min,体系中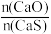 的比值随温度变化如表所示:
的比值随温度变化如表所示:
请结合题给反应过程能量图,说明:
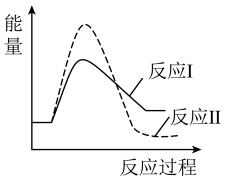
①750K→1250K时,比值随温度升高逐渐减小的原因是___________ 。
②1250K后,比值随温度升高逐渐增大的原因是___________ 。
(5)氨水也可吸收 :
: ,
,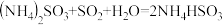 。能提高
。能提高 去除率的措施有
去除率的措施有___________ (填字母)。
A.增大氨水浓度 B.加热煮沸
C.降低烟气的流速 D.补充 ,将
,将 氧化为
氧化为
(1)室温下,
 溶液呈碱性的原因是
溶液呈碱性的原因是(2)下列关于硫及其化合物的说法,正确的是
A.硫元素在自然界中只能以化合态形式存在
B.
 通入紫色石蕊试液,先变红后褪色
通入紫色石蕊试液,先变红后褪色C.酸雨是
 的降水,主要是由污染物
的降水,主要是由污染物 、
、 造成
造成D.浓硫酸中加入少量胆矾晶体,搅拌,固体逐渐变成白色
(3)光谱研究表明,
 的水溶液中存在下列平衡:
的水溶液中存在下列平衡: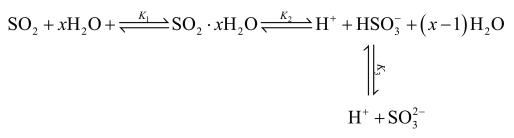
其中
 、
、 、
、 为各步的平衡常数,且
为各步的平衡常数,且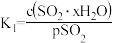 (
( 表示
表示 的平衡压强)。
的平衡压强)。①当
 的平衡压强为p时,测得
的平衡压强为p时,测得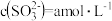 ,则溶液
,则溶液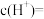
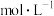 。
。(用含p、a、
 、
、 、
、 的式子表示)
的式子表示)②滴加NaOH至
 时,溶液中
时,溶液中 。如果溶液中
。如果溶液中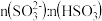
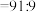 ,需加NaOH将溶液pH调整为约等于
,需加NaOH将溶液pH调整为约等于(4)“钙基固硫”是利用石灰石将燃煤烟气中的
 转化为
转化为 。但高温时CO会与
。但高温时CO会与 反应而影响脱硫效率。相关反应如下:
反应而影响脱硫效率。相关反应如下:Ⅰ.
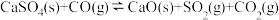
Ⅱ.
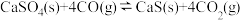
当
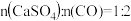 时,反应25min,体系中
时,反应25min,体系中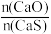 的比值随温度变化如表所示:
的比值随温度变化如表所示:| 温度 | 750K | 1250K | 1750K |
| 比值 | 3.57 | 1.08 | 3.42 |

①750K→1250K时,比值随温度升高逐渐减小的原因是
②1250K后,比值随温度升高逐渐增大的原因是
(5)氨水也可吸收
 :
: ,
,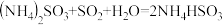 。能提高
。能提高 去除率的措施有
去除率的措施有A.增大氨水浓度 B.加热煮沸
C.降低烟气的流速 D.补充
 ,将
,将 氧化为
氧化为
您最近一年使用:0次
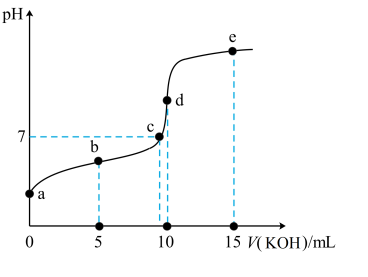
5 . 常温下,用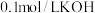 溶液滴定
溶液滴定 溶液的滴定曲线如图所示。下列说法错误的是
溶液的滴定曲线如图所示。下列说法错误的是
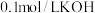 溶液滴定
溶液滴定 溶液的滴定曲线如图所示。下列说法错误的是
溶液的滴定曲线如图所示。下列说法错误的是
| A.根据c点或d点可以确定HA是弱酸 |
B.若 ,则HA的电离平衡常数为 ,则HA的电离平衡常数为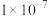 |
C.e点溶液中: |
D.对d点溶液加热 不考虑挥发 不考虑挥发 ,则 ,则 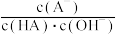 一定增大 一定增大 |
您最近一年使用:0次
2021-04-29更新
|
455次组卷
|
2卷引用:山东省聊城市第三中学2021-2022学年高三下学期开学考试化学试题
名校
6 . 在 时,向
时,向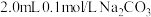 溶液中逐滴加入
溶液中逐滴加入 的
的 溶液,滴加时溶液中含碳微粒物质的量(
溶液,滴加时溶液中含碳微粒物质的量(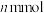 )与溶液
)与溶液 的关系如图所示(
的关系如图所示( 因逸出未画出)。下列选项错误的是
因逸出未画出)。下列选项错误的是

 时,向
时,向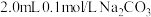 溶液中逐滴加入
溶液中逐滴加入 的
的 溶液,滴加时溶液中含碳微粒物质的量(
溶液,滴加时溶液中含碳微粒物质的量(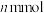 )与溶液
)与溶液 的关系如图所示(
的关系如图所示( 因逸出未画出)。下列选项错误的是
因逸出未画出)。下列选项错误的是 
A. 的水解平衡常数 的水解平衡常数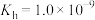 |
B. 点对应溶液中 点对应溶液中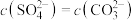 |
C.曲线②表示 的物质的量变化情况 的物质的量变化情况 |
D. 溶液中 溶液中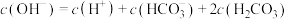 |
您最近一年使用:0次
2021-04-24更新
|
425次组卷
|
5卷引用:湖北省应城市第一高级中学2022-2023学年高三上学期8月热身考试化学试题
名校
7 . 2020年春季,全球出现了罕见的新型冠状病毒肺炎疫情,酒精、84消毒液(有效成分 )、过氧乙酸
)、过氧乙酸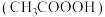 等消毒剂都能有效杀灭环境中的病毒。已知
等消毒剂都能有效杀灭环境中的病毒。已知 的电离常数
的电离常数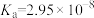 。下列有关说法正确的是
。下列有关说法正确的是
 )、过氧乙酸
)、过氧乙酸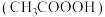 等消毒剂都能有效杀灭环境中的病毒。已知
等消毒剂都能有效杀灭环境中的病毒。已知 的电离常数
的电离常数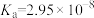 。下列有关说法正确的是
。下列有关说法正确的是| A.医用酒精的体积分数为95%,浓度越大效果越好 |
B.反应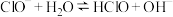 的 的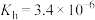 |
| C.使用84消毒液和过氧乙酸消毒剂时无需采取防护措施 |
| D.过氧乙酸具有酸性和强氧化性,能使蛋白质变性 |
您最近一年使用:0次
2021-04-13更新
|
176次组卷
|
3卷引用:湖南省益阳市2020-2021学年高三上学期复学摸底考试化学试题
湖南省益阳市2020-2021学年高三上学期复学摸底考试化学试题(已下线)单科化学-2021年秋季高三开学摸底考试卷01(课标全国专用) 江西省南昌市八一中学2020-2021学年高二下学期期末考试化学试题
8 . 常温下,用 的盐酸滴定20mL
的盐酸滴定20mL NaCN溶液时,溶液中由水电离出的H+浓度的负对数
NaCN溶液时,溶液中由水电离出的H+浓度的负对数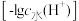 与滴加的盐酸体积[V(HCl)]的关系如图所示。甲基橙的变色范围见下表。
与滴加的盐酸体积[V(HCl)]的关系如图所示。甲基橙的变色范围见下表。
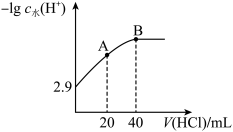
下列叙述正确的是
 的盐酸滴定20mL
的盐酸滴定20mL NaCN溶液时,溶液中由水电离出的H+浓度的负对数
NaCN溶液时,溶液中由水电离出的H+浓度的负对数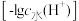 与滴加的盐酸体积[V(HCl)]的关系如图所示。甲基橙的变色范围见下表。
与滴加的盐酸体积[V(HCl)]的关系如图所示。甲基橙的变色范围见下表。
甲基橙变色范围 | |||
| 溶液pH | <3.1 | 3.1~4.4 | >4.4 |
| 颜色 | 红色 | 橙色 | 黄色 |
A.常温下, 的数量级为 的数量级为 |
B.常温下, 的HCN溶液使甲基橙试液显红色 的HCN溶液使甲基橙试液显红色 |
C.浓度均为 的HCN和NaCN混合溶液中: 的HCN和NaCN混合溶液中: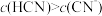 |
D.B点对应溶液中: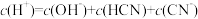 |
您最近一年使用:0次
2021-04-09更新
|
788次组卷
|
5卷引用:湖南省岳阳县第一中学2022-2023学年高二下学期开学考试化学试题
湖南省岳阳县第一中学2022-2023学年高二下学期开学考试化学试题山东省百所名校2021届高三下学期4月份(第三次)联考化学试题广东部分学校2021届高三4月模拟考试化学试题(已下线)难点7 溶液稀释与酸碱中和滴定曲线分析-2021年高考化学【热点·重点·难点】专练(山东专用)(已下线)专题21 电解质溶液图像分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)
13-14高三·浙江嘉兴·阶段练习
名校
解题方法
9 . 已知:常温下浓度为0.1mol•L-1的下列溶液的pH如表:
下列有关说法正确的是
| 溶质 | NaF | NaClO | Na2CO3 |
| pH | 7.5 | 9.7 | 11.6 |
| A.在相同温度下,同浓度的三种酸溶液的导电能力顺序:H2CO3<HClO<HF |
B.若将CO2通入0.1mol•L-1Na2CO3溶液中至溶液中性,则溶液2c(CO )+c(HCO )+c(HCO )=0.1mol•L-1 )=0.1mol•L-1 |
C.根据上表,水解方程式ClO-+H2O HClO+OH-的水解常数K≈10-7.6 HClO+OH-的水解常数K≈10-7.6 |
| D.向上述NaClO溶液中通HF气体至恰好完全反应时:c(Na+)>c(F-)>c(H+)> c(HClO)>c(OH-) |
您最近一年使用:0次
2021-03-20更新
|
476次组卷
|
14卷引用:广东省广州市荔湾区广州市西关外国语学校2020—2021学年高二培优选拔测试化学试题
广东省广州市荔湾区广州市西关外国语学校2020—2021学年高二培优选拔测试化学试题(已下线)2014届浙江省嘉兴市高三教学测试(一)理综化学试卷2015届山东省沂水县一中高三上学期12月月考化学试卷2015届浙江省丽水中学高三第二次模拟理综化学试卷2015届山东省枣庄市八中高三4月模拟考试化学试卷2015届重庆一中高高三下期第三次月考化学试卷2016届黑龙江省大庆实验中学高三考训练四理综化学试卷江西省临川第二中学2018届高三上学期第四次月考(期中)化学试题安徽省合肥二中2019-2020学年度高三上学期第一次段考化学试题江西省南昌市莲塘第一中学2019-2020学年高二上学期期末质量检测化学试题安徽省淮北市树人高级中学2020-2021学年高二下学期第一次阶段考试化学试题辽宁省滨海实验中学2019-2020学年高二上学期期末化学试题河南省延津第一高级中学2021-2022学年高二上学期第五次考试化学试题广东省新南方联盟2024届高三下学期4月联考化学试题
解题方法
10 . 常温下,H2SO3的电离常数Ka1=1×10-2,Ka2=6.3×10-3,H2CO3的电离常数Ka1=4.5×10-7,Ka2=4.7×10-11。
(1)浓度均为0.1mol/L的Na2SO3和Na2CO3的混合溶液中,SO 、CO
、CO 、HSO
、HSO 、HCO
、HCO 浓度从大到小的顺序为
浓度从大到小的顺序为___ 。
(2)25℃时,NaHSO3的水解平衡常数Kh=___ mol•L-1,若向NaHSO3溶液中加入少量的I2,则溶液中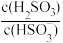 将
将___ (填“增大”“减小”或“不变”)。(已知H2SO3+I2+H2O=4H++SO +2I-);
+2I-);
(3)某同学设计实验验证H2SO3酸性强于H2CO3:将SO2和CO2气体分别通入水中至饱和,立即用酸度计测两溶液的pH,若前者的pH小于后者,则H2SO3酸性强于H2CO3。该实验设计不正确,错误在于___ 。设计合理实验验证H2SO3酸性强于H2CO3(简要说明实验步骤、现象和结论)。___ 。
仪器自选,供选的试剂:CO2、SO2、Na2CO3、NaHCO3、KMnO4、NaHSO3、蒸馏水、饱和石灰水、酸性KMnO4溶液、品红溶液、pH试纸。
(1)浓度均为0.1mol/L的Na2SO3和Na2CO3的混合溶液中,SO
 、CO
、CO 、HSO
、HSO 、HCO
、HCO 浓度从大到小的顺序为
浓度从大到小的顺序为(2)25℃时,NaHSO3的水解平衡常数Kh=
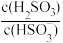 将
将 +2I-);
+2I-);(3)某同学设计实验验证H2SO3酸性强于H2CO3:将SO2和CO2气体分别通入水中至饱和,立即用酸度计测两溶液的pH,若前者的pH小于后者,则H2SO3酸性强于H2CO3。该实验设计不正确,错误在于
仪器自选,供选的试剂:CO2、SO2、Na2CO3、NaHCO3、KMnO4、NaHSO3、蒸馏水、饱和石灰水、酸性KMnO4溶液、品红溶液、pH试纸。
您最近一年使用:0次



