名校
1 . 海水中含有80多种元素,是重要的物质资源宝库,同时海水具有强大的自然调节能力,为解决环境污染问题提供了广阔的空间。
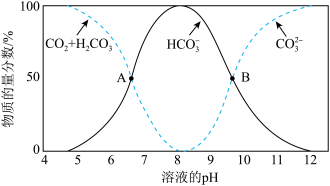
(1)25℃,不同pH条件下,水溶液中碳元素的存在形态如图所示。
①下列说法正确的是_________ (填字母)。
a.A点,溶液中H2CO3和HCO 浓度相同
浓度相同
b.pH=8时,溶液中含碳元素的微粒主要是HCO
c.当c(HCO )=c(CO
)=c(CO )时,c(H+)>c(OH﹣)
)时,c(H+)>c(OH﹣)
②上述中性水溶液中,阴离子浓度由大到小的关系是___________ ;pH=6时,由水电离出的c(H+)=___________ 。
(2)海水pH稳定在7.9~8.4之间,可用于烟道气中CO2和SO2的吸收剂。
①海水呈弱碱性是因为主要含有___________ 、___________ 、OH﹣(填微粒符号)。
②已知:25℃时,H2CO3电离平衡常数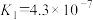 、
、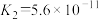 ;H2SO3电离平衡常数
;H2SO3电离平衡常数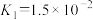 、
、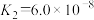 。海水中含有的HCO
。海水中含有的HCO 可用于吸收SO2,该过程的离子方程式是
可用于吸收SO2,该过程的离子方程式是___________ ,吸收后溶液呈弱酸性的原因是___________ 。
(3)洗涤烟气后的海水呈酸性,需处理后再排放。通入O2可将酸性海水中的硫(Ⅳ)(主要以HSO 形式存在)氧化,该反应的离子方程式是
形式存在)氧化,该反应的离子方程式是___________ 。
(1)25℃,不同pH条件下,水溶液中碳元素的存在形态如图所示。

①下列说法正确的是
a.A点,溶液中H2CO3和HCO
 浓度相同
浓度相同b.pH=8时,溶液中含碳元素的微粒主要是HCO

c.当c(HCO
 )=c(CO
)=c(CO )时,c(H+)>c(OH﹣)
)时,c(H+)>c(OH﹣)②上述中性水溶液中,阴离子浓度由大到小的关系是
(2)海水pH稳定在7.9~8.4之间,可用于烟道气中CO2和SO2的吸收剂。
①海水呈弱碱性是因为主要含有
②已知:25℃时,H2CO3电离平衡常数
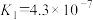 、
、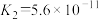 ;H2SO3电离平衡常数
;H2SO3电离平衡常数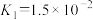 、
、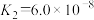 。海水中含有的HCO
。海水中含有的HCO 可用于吸收SO2,该过程的离子方程式是
可用于吸收SO2,该过程的离子方程式是(3)洗涤烟气后的海水呈酸性,需处理后再排放。通入O2可将酸性海水中的硫(Ⅳ)(主要以HSO
 形式存在)氧化,该反应的离子方程式是
形式存在)氧化,该反应的离子方程式是
您最近一年使用:0次
2 . 室温下,向Mg(NO3)2溶液、HF溶液、CH3CH2COOH溶液中分别滴加NaOH溶液,测得溶液中pH与pX[pX=-lgX,X代表 、
、 、
、 ]的关系如图所示。
]的关系如图所示。
 ,HF的酸性比CH3CH2COOH强。下列叙述正确的是
,HF的酸性比CH3CH2COOH强。下列叙述正确的是
已知:
 、
、 、
、 ]的关系如图所示。
]的关系如图所示。
 ,HF的酸性比CH3CH2COOH强。下列叙述正确的是
,HF的酸性比CH3CH2COOH强。下列叙述正确的是已知:

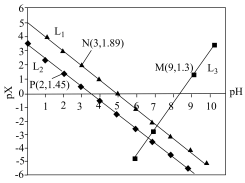
A. 代表的是pH与 代表的是pH与 的关系 的关系 |
B. 的 的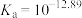 |
C.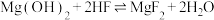 的 的 |
| D.含相同浓度NaF、HF的混合溶液的pH>7 |
您最近一年使用:0次
2024-04-01更新
|
439次组卷
|
4卷引用:内蒙古自治区赤峰第四中学2023-2024学年高三下学期开学考试理综试题-高中化学
内蒙古自治区赤峰第四中学2023-2024学年高三下学期开学考试理综试题-高中化学贵州省黔东南州2024届高三下学期模拟统测(二模)化学试题(已下线)化学(福建卷02)-2024年高考押题预测卷2024届山西省太原市第五中学高三下学期一模理综试题-高中化学
名校
3 . 25℃时,用HCl气体调节0.1mol/L氨水的pH,溶液中微粒浓度的对数值(lgc、反应物的物质的量之比[n(HCl)/n(NH3·H2O)]与pH的关系如下图。若忽略通入气体后溶液体积的变化。下列说法错误的是
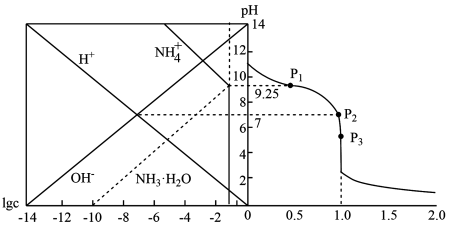

| A.P2所示溶液中:c(Cl-)>c(NH3·H2O) |
| B.P1所示溶液中:c(Cl-)<0.05mol/L |
C.[n(HCl)/n(NH3·H2O)]=1.5时溶液中: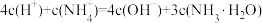 |
| D.25℃时,NH4Cl水解平衡常数数量级为10-10 |
您最近一年使用:0次
名校
4 . 常温下亚砷酸 在溶液中存在多种微粒形态,向溶液中逐滴加入
在溶液中存在多种微粒形态,向溶液中逐滴加入 调节
调节 ,得到微粒形态分布优势
,得到微粒形态分布优势 区域如图所示(虚线处表示两种形态的浓度相等),
区域如图所示(虚线处表示两种形态的浓度相等), 、
、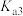 分别表示
分别表示 的第二步、第三步电离平衡常数。下列有关说法错误的是
的第二步、第三步电离平衡常数。下列有关说法错误的是
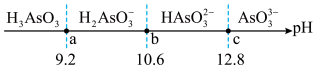
 在溶液中存在多种微粒形态,向溶液中逐滴加入
在溶液中存在多种微粒形态,向溶液中逐滴加入 调节
调节 ,得到微粒形态分布优势
,得到微粒形态分布优势 区域如图所示(虚线处表示两种形态的浓度相等),
区域如图所示(虚线处表示两种形态的浓度相等), 、
、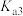 分别表示
分别表示 的第二步、第三步电离平衡常数。下列有关说法错误的是
的第二步、第三步电离平衡常数。下列有关说法错误的是
A. 点对应的溶液中, 点对应的溶液中, |
B.常温下, 的第一步水解平衡常数的数量级为 的第一步水解平衡常数的数量级为 |
C.溶液中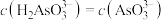 时, 时,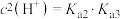 |
D.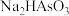 为酸式盐 为酸式盐 |
您最近一年使用:0次
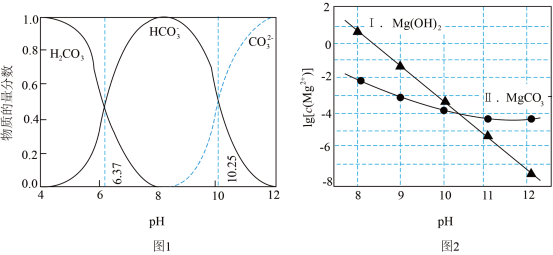
5 . 常温下, 在Na2CO3溶液中发生反应,可能生成
在Na2CO3溶液中发生反应,可能生成 或MgCO3。图1表示Na2CO3溶液中各含碳物种的物质的量分数与溶液pH的关系;图2中曲线Ⅰ的离子浓度关系符合
或MgCO3。图1表示Na2CO3溶液中各含碳物种的物质的量分数与溶液pH的关系;图2中曲线Ⅰ的离子浓度关系符合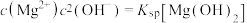 ;曲线Ⅱ的离子浓度关系符合
;曲线Ⅱ的离子浓度关系符合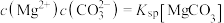 。利用平衡原理分析,下列说法正确的是
。利用平衡原理分析,下列说法正确的是
 在Na2CO3溶液中发生反应,可能生成
在Na2CO3溶液中发生反应,可能生成 或MgCO3。图1表示Na2CO3溶液中各含碳物种的物质的量分数与溶液pH的关系;图2中曲线Ⅰ的离子浓度关系符合
或MgCO3。图1表示Na2CO3溶液中各含碳物种的物质的量分数与溶液pH的关系;图2中曲线Ⅰ的离子浓度关系符合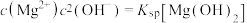 ;曲线Ⅱ的离子浓度关系符合
;曲线Ⅱ的离子浓度关系符合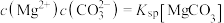 。利用平衡原理分析,下列说法正确的是
。利用平衡原理分析,下列说法正确的是
A.常温时, 的水解常数 的水解常数 |
B.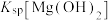 的数量级为 的数量级为 |
C.由图2,当pH=11, 时,有沉淀生成 时,有沉淀生成 |
D.由图1和图2,在pH=8,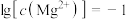 时,溶液中发生反应: 时,溶液中发生反应: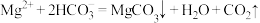 |
您最近一年使用:0次
名校
6 . 在常温下,向0.1mol·L1HR酸溶液中滴加NaOH溶液。混合溶液中存在c(HR)+c(R)=0.1mol·L1,c(HR)、c(R)随溶液pH变化曲线如图所示。下列说法错误的是
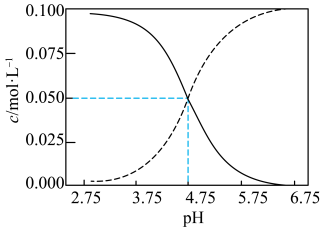

| A.pH=4对应溶液中存在:c(HR)>c(R)>c(H)>c(OH) |
| B.随着c(R)增大,水的电离程度逐渐增大 |
| C.在2L纯水中同时加入0.1molHR、0.1molNaR得到溶液pH=4.75 |
D.常温下,R的水解常数Kh(已知:Kh=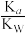 )的数量级为1010 )的数量级为1010 |
您最近一年使用:0次
名校
7 . 常温下,向20mL 0.1mol/L的Na2CO3溶液中通入HCl气体(溶液体积变化忽略不计),溶液中含碳元素的各种微粒(CO2气体因逸出不考虑)物质的量分数δ随溶液pH变化的部分情况如下图所示。下列说法错误的是
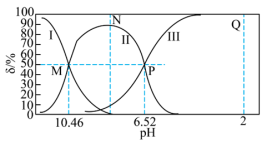

A.曲线Ⅰ表示CO 物质的量分数 物质的量分数 |
B.CO 水解的平衡常数为Kh1 = 10-3.54 水解的平衡常数为Kh1 = 10-3.54 |
C.pH = 7时,满足c(HCO ) > c(H2CO3) > c(CO ) > c(H2CO3) > c(CO ) ) |
D.Q点存在:c(HCO ) + c(H2CO3) + c(CO ) + c(H2CO3) + c(CO ) = 0.1 mol/L ) = 0.1 mol/L |
您最近一年使用:0次
名校
解题方法
8 . 常温下,在20 mL 溶液中逐滴加入
溶液中逐滴加入 盐酸40 mL,溶液中含碳元素的各种微粒(
盐酸40 mL,溶液中含碳元素的各种微粒( 因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如图所示。下列有关说法不正确的是
因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如图所示。下列有关说法不正确的是

 溶液中逐滴加入
溶液中逐滴加入 盐酸40 mL,溶液中含碳元素的各种微粒(
盐酸40 mL,溶液中含碳元素的各种微粒( 因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如图所示。下列有关说法不正确的是
因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如图所示。下列有关说法不正确的是
A.实验室盛放 溶液的试剂瓶不能用磨口玻璃塞 溶液的试剂瓶不能用磨口玻璃塞 |
B.同一溶液中, 、 、 、 、 不能大量共存 不能大量共存 |
C. ,溶液中离子浓度的大小关系为:c(Na+)>c(Cl-)>c( ,溶液中离子浓度的大小关系为:c(Na+)>c(Cl-)>c( )>c(H+)=c(OH-) )>c(H+)=c(OH-) |
D. 时,溶液中 时,溶液中 , , 的水解常数 的水解常数 |
您最近一年使用:0次
9 . 下列说法正确的是
| A.强电解质溶液一定比弱电解质溶液的导电性强 |
B.中和等体积、等物质的量浓度的盐酸和醋酸所消耗的 相等 相等 |
C.常温下,将 的盐酸与醋酸各1 mL分别稀释至100 mL,醋酸溶液pH更大 的盐酸与醋酸各1 mL分别稀释至100 mL,醋酸溶液pH更大 |
D.加水稀释,水解平衡正向移动,水解常数 增大 增大 |
您最近一年使用:0次
名校
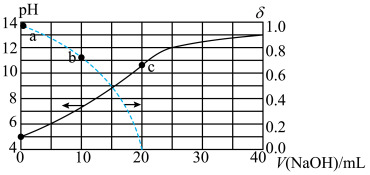
10 . 常温时,用 的
的 溶液滴定20.00mL
溶液滴定20.00mL 的
的 溶液。溶液的
溶液。溶液的 、分布系数
、分布系数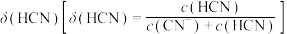 随滴加
随滴加 溶液体积的变化关系如图所示。下列有关说法正确的是
溶液体积的变化关系如图所示。下列有关说法正确的是
 的
的 溶液滴定20.00mL
溶液滴定20.00mL 的
的 溶液。溶液的
溶液。溶液的 、分布系数
、分布系数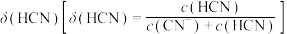 随滴加
随滴加 溶液体积的变化关系如图所示。下列有关说法正确的是
溶液体积的变化关系如图所示。下列有关说法正确的是
A. 酸的 酸的 约为 约为 |
B.b点溶液粒子浓度关系为: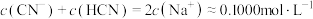 |
C.c点溶液离子浓度关系为: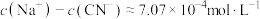 |
D.滴定过程中,水的电离程度 |
您最近一年使用:0次



