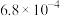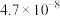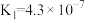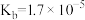名校
1 . 已知常温下水溶液中 、
、 、
、 、HB、
、HB、 的分布分数δ[如
的分布分数δ[如 ]随pH变化曲线如图1;溶液中
]随pH变化曲线如图1;溶液中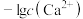 和
和 关系如图2.用
关系如图2.用
 溶液滴定20.00mL
溶液滴定20.00mL
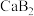 溶液,下列说法错误的是
溶液,下列说法错误的是

 、
、 、
、 、HB、
、HB、 的分布分数δ[如
的分布分数δ[如 ]随pH变化曲线如图1;溶液中
]随pH变化曲线如图1;溶液中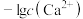 和
和 关系如图2.用
关系如图2.用
 溶液滴定20.00mL
溶液滴定20.00mL
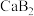 溶液,下列说法错误的是
溶液,下列说法错误的是
| A.曲线d表示δ(HB) |
B. 的水解平衡常数 的水解平衡常数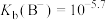 |
| C.滴定过程中溶液会变浑浊 |
D.滴定过程中始终存在: |
您最近一年使用:0次
2023-04-10更新
|
1876次组卷
|
12卷引用:重庆市七校2023-2024学年高三上学期开学考试化学试题
重庆市七校2023-2024学年高三上学期开学考试化学试题河北省石家庄市部分学校2023届高中毕业年级教学质量检测(二)(一模)化学试题河北省邢台市2022-2023学年高三下学期4月第一次模拟考试化学试题(已下线)专题15 水溶液中的离子平衡山东省东营市第一中学2023届高三下学期二模化学试题东北育才学校高中部2023届高三下学期适应性考试化学试题湖南省长郡中学2024届高三上学期月考卷(一)化学试题湖南省长沙市长郡中学2024届高三上学期9月月考化学试题江西省宜丰中学创新部2023-2024学年高二上学期第一次(10月)月考化学试题四川省宜宾市叙州区第一中学校2023-2024学年高二上学期12月月考化学试题(已下线)化学(九省联考考后提升卷,河南卷)-2024年1月“九省联考”真题完全解读与考后提升(已下线)热点18 电解质溶液图像分析
名校
解题方法
2 . 自然界是各类物质相互依存的复杂体系,水溶液的离子平衡是一个重要方面。
(1) 时,在
时,在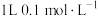 的
的 溶液中,有
溶液中,有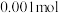 的
的 电离成离子,则该温度下的电离平衡常数为
电离成离子,则该温度下的电离平衡常数为_____ 。
(2)在 时,将
时,将 的
的 溶液
溶液 与
与 的
的 溶液
溶液 混合,若所得溶液为中性,则
混合,若所得溶液为中性,则
_______ 。
(3)常温下将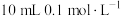 的
的 溶液与
溶液与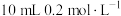 的醋酸溶液混合后溶液显酸性,则混合后溶液中各离子浓度的大小顺序为
的醋酸溶液混合后溶液显酸性,则混合后溶液中各离子浓度的大小顺序为________________ 。
(4)已知常温下部分弱电解质的电离平衡常数如下表:
常温下, 相同的三种溶液①
相同的三种溶液① 溶液;②
溶液;② 溶液;③
溶液;③ 溶液,其物质的量浓度由大到小的顺序是
溶液,其物质的量浓度由大到小的顺序是________ (填序号)。
(5)已知 时,
时, 的溶度积常数
的溶度积常数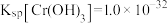 。则使
。则使 恰好完全沉淀,即溶液中
恰好完全沉淀,即溶液中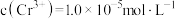 时,应调节
时,应调节 的最小值a为多少
的最小值a为多少________ 。
(6)查阅资料获得 时部分弱酸
时部分弱酸 的数据:
的数据: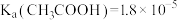 、
、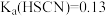 、
、 。
。
①已知 溶液呈弱碱性,试用离子反应方程式解释原因
溶液呈弱碱性,试用离子反应方程式解释原因________________ 。
②常温下,氢氟酸溶液加水稀释过程中,下列表达式数据变大的是________ (填序号)。
A. B.
B. C.
C.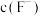 D.
D.
(7)已知在 时,将浓度相等的
时,将浓度相等的 与
与 溶液等体积混合,溶液呈酸性。解释溶液呈酸性的原因
溶液等体积混合,溶液呈酸性。解释溶液呈酸性的原因________________________ 。
(8)同浓度的 溶液和
溶液和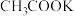 溶液相比:(选填“<”、“=”或“>”)后者溶液中:
溶液相比:(选填“<”、“=”或“>”)后者溶液中: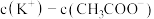
_____ 前者溶液中
(9)已加 溶液为中性,又知
溶液为中性,又知 溶液加到
溶液加到 溶液中有无色无味气体放出,现有
溶液中有无色无味气体放出,现有 时等浓度的5种溶液:请回答下列问题:
时等浓度的5种溶液:请回答下列问题:
a. b.
b. c.
c. d.
d. e.
e.
问题1:试推断 溶液的
溶液的
______ 7(填“>”、“<”或=)
问题2:将5种溶液按 浓度由大到小的顺序排列是:
浓度由大到小的顺序排列是:________ (填序号)。
(10)已知常温下,相同物质的量浓度的 溶液和
溶液和 溶液相比,
溶液相比, 溶液的
溶液的 较小。现将
较小。现将 溶液和
溶液和 溶液等体积混合,各离子浓度关系正确的是________(填序号)。
溶液等体积混合,各离子浓度关系正确的是________(填序号)。
(1)
 时,在
时,在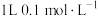 的
的 溶液中,有
溶液中,有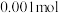 的
的 电离成离子,则该温度下的电离平衡常数为
电离成离子,则该温度下的电离平衡常数为(2)在
 时,将
时,将 的
的 溶液
溶液 与
与 的
的 溶液
溶液 混合,若所得溶液为中性,则
混合,若所得溶液为中性,则
(3)常温下将
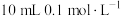 的
的 溶液与
溶液与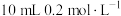 的醋酸溶液混合后溶液显酸性,则混合后溶液中各离子浓度的大小顺序为
的醋酸溶液混合后溶液显酸性,则混合后溶液中各离子浓度的大小顺序为(4)已知常温下部分弱电解质的电离平衡常数如下表:
化学式 |
|
|
|
|
电离常数 |
|
|
|
|
 相同的三种溶液①
相同的三种溶液① 溶液;②
溶液;② 溶液;③
溶液;③ 溶液,其物质的量浓度由大到小的顺序是
溶液,其物质的量浓度由大到小的顺序是(5)已知
 时,
时, 的溶度积常数
的溶度积常数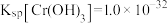 。则使
。则使 恰好完全沉淀,即溶液中
恰好完全沉淀,即溶液中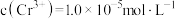 时,应调节
时,应调节 的最小值a为多少
的最小值a为多少(6)查阅资料获得
 时部分弱酸
时部分弱酸 的数据:
的数据: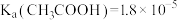 、
、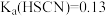 、
、 。
。①已知
 溶液呈弱碱性,试用离子反应方程式解释原因
溶液呈弱碱性,试用离子反应方程式解释原因②常温下,氢氟酸溶液加水稀释过程中,下列表达式数据变大的是
A.
 B.
B. C.
C.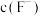 D.
D.
(7)已知在
 时,将浓度相等的
时,将浓度相等的 与
与 溶液等体积混合,溶液呈酸性。解释溶液呈酸性的原因
溶液等体积混合,溶液呈酸性。解释溶液呈酸性的原因(8)同浓度的
 溶液和
溶液和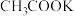 溶液相比:(选填“<”、“=”或“>”)后者溶液中:
溶液相比:(选填“<”、“=”或“>”)后者溶液中: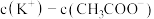

(9)已加
 溶液为中性,又知
溶液为中性,又知 溶液加到
溶液加到 溶液中有无色无味气体放出,现有
溶液中有无色无味气体放出,现有 时等浓度的5种溶液:请回答下列问题:
时等浓度的5种溶液:请回答下列问题:a.
 b.
b. c.
c. d.
d. e.
e.
问题1:试推断
 溶液的
溶液的
问题2:将5种溶液按
 浓度由大到小的顺序排列是:
浓度由大到小的顺序排列是:(10)已知常温下,相同物质的量浓度的
 溶液和
溶液和 溶液相比,
溶液相比, 溶液的
溶液的 较小。现将
较小。现将 溶液和
溶液和 溶液等体积混合,各离子浓度关系正确的是________(填序号)。
溶液等体积混合,各离子浓度关系正确的是________(填序号)。A.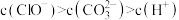 |
B. |
C. |
D.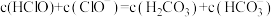 |
您最近一年使用:0次
3 . 实验室模拟拉希法用氨和次氯酸钠反应制备肼(N2H4),并探究肼的性质,制备装置如图所示。
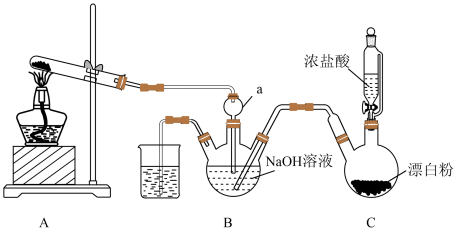
回答下列问题:
(1)肼的电子式为_______ 。
(2)装置A试管中的试剂为_______ 。
(3)装置B中制备肼的化学方程式为_______ 。
(4)上述装置中存在一处缺陷,会导致肼的产率降低,改进方法是_______ 。
(5)①探究性质。
已知N2H4是一种二元弱碱,在水中的电离与NH3相似,请写出肼的第二步电离的电离方程式:_______ ,室温下向N2H4水溶液中滴加某强酸,溶液的pH与 或
或 的变化关系如图所示,下列说法正确的是
的变化关系如图所示,下列说法正确的是_______ (填标号)。

A.N2H4在水溶液中第二步电离的平衡常数为10-1
B. 的平衡常数为109
的平衡常数为109
C. 的水解能力大于其电离能力
的水解能力大于其电离能力
D.N2H6Cl2溶液中: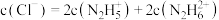
②测定产品中肼的质量分数。
称取装置B中溶液m g,加入适量NaHCO3固体(滴定过程中,调节溶液的pH=6),加水配成100 mL溶液,移取25.00 mL置于锥形瓶中,并滴加2~3滴指示剂,用c mol/L的碘标准溶液滴定,滴定过程中有无色无味无毒气体产生,定终点时平均消耗标准溶液V mL,产品中肼的质量分数为_______ (用含m、c、V的式子表示)。

回答下列问题:
(1)肼的电子式为
(2)装置A试管中的试剂为
(3)装置B中制备肼的化学方程式为
(4)上述装置中存在一处缺陷,会导致肼的产率降低,改进方法是
(5)①探究性质。
已知N2H4是一种二元弱碱,在水中的电离与NH3相似,请写出肼的第二步电离的电离方程式:
 或
或 的变化关系如图所示,下列说法正确的是
的变化关系如图所示,下列说法正确的是
A.N2H4在水溶液中第二步电离的平衡常数为10-1
B.
 的平衡常数为109
的平衡常数为109C.
 的水解能力大于其电离能力
的水解能力大于其电离能力D.N2H6Cl2溶液中:
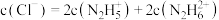
②测定产品中肼的质量分数。
称取装置B中溶液m g,加入适量NaHCO3固体(滴定过程中,调节溶液的pH=6),加水配成100 mL溶液,移取25.00 mL置于锥形瓶中,并滴加2~3滴指示剂,用c mol/L的碘标准溶液滴定,滴定过程中有无色无味无毒气体产生,定终点时平均消耗标准溶液V mL,产品中肼的质量分数为
您最近一年使用:0次
解题方法
4 . 我国科学家开发新型高效催化剂,在太阳能作用下制备双氧水。
I.双氧水不稳定。
(1)实验研究发现,碘离子催化双氧水分解反应分两步进行,其反应历程如图所示。
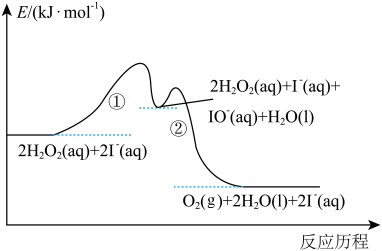
①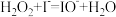 ;
;
②_______ (补充离子方程式)。其中,反应_______ 控制总反应速率(填“①”或“②”)。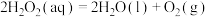

_______ 0(填“>”“<”或“=”)。
(2)双氧水在碘离子催化下发生分解反应: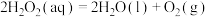 ,其速率方程为
,其速率方程为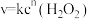 (k为速率常数,只与温度、催化剂有关;n为反应级数,可以为零、分数或整数)。双氧水在常温下的分解速率与浓度的关系如表所示。
(k为速率常数,只与温度、催化剂有关;n为反应级数,可以为零、分数或整数)。双氧水在常温下的分解速率与浓度的关系如表所示。
常温下,该反应的速率常数
_______ (不写单位)。
II.查阅资料知: 是一种弱酸,298K时
是一种弱酸,298K时 的
的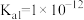 ,
,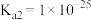 。
。
(3)298K时,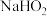 溶液中
溶液中 的水解常数为
的水解常数为_______ 。
III.测定双氧水溶液的浓度。
(4)已知:酸性条件下,双氧水和高锰酸钾反应, 生成,写出反应的离子方程式:
生成,写出反应的离子方程式:_______ 。
(5)取 mL某双氧水溶液于锥形瓶中,稀释至250 mL。取稀释后的溶液25.00 mL于锥形瓶中,加入适量的稀硫酸,用c mol·L
mL某双氧水溶液于锥形瓶中,稀释至250 mL。取稀释后的溶液25.00 mL于锥形瓶中,加入适量的稀硫酸,用c mol·L
 标准溶液滴定至终点时,消耗滴定液V mL。该双氧水溶液中
标准溶液滴定至终点时,消耗滴定液V mL。该双氧水溶液中
_______ mol·L (用含c、V、
(用含c、V、 的代数式表示)。若滴定管用蒸馏水洗涤后没有用
的代数式表示)。若滴定管用蒸馏水洗涤后没有用 标准溶液润洗,则测得的结果
标准溶液润洗,则测得的结果_______ (填“偏高”“偏低”或“无影响”)。
I.双氧水不稳定。
(1)实验研究发现,碘离子催化双氧水分解反应分两步进行,其反应历程如图所示。

①
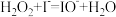 ;
;②
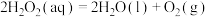

(2)双氧水在碘离子催化下发生分解反应:
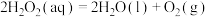 ,其速率方程为
,其速率方程为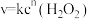 (k为速率常数,只与温度、催化剂有关;n为反应级数,可以为零、分数或整数)。双氧水在常温下的分解速率与浓度的关系如表所示。
(k为速率常数,只与温度、催化剂有关;n为反应级数,可以为零、分数或整数)。双氧水在常温下的分解速率与浓度的关系如表所示。| 序号 | 反应时间/min |  /(mol·L /(mol·L ) ) | v/(mol·L ·min ·min ) ) |
| ① | 0 | 0.80 | 0 |
| ② | 20 | 0.40 | 0.020 |
| ③ | 40 | 0.20 | 0.010 |
| ④ | 60 | 0.10 | 0.005 |
| ⑤ | 80 | 0.05 | 0.0025 |

II.查阅资料知:
 是一种弱酸,298K时
是一种弱酸,298K时 的
的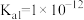 ,
,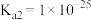 。
。(3)298K时,
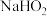 溶液中
溶液中 的水解常数为
的水解常数为III.测定双氧水溶液的浓度。
(4)已知:酸性条件下,双氧水和高锰酸钾反应,
 生成,写出反应的离子方程式:
生成,写出反应的离子方程式:(5)取
 mL某双氧水溶液于锥形瓶中,稀释至250 mL。取稀释后的溶液25.00 mL于锥形瓶中,加入适量的稀硫酸,用c mol·L
mL某双氧水溶液于锥形瓶中,稀释至250 mL。取稀释后的溶液25.00 mL于锥形瓶中,加入适量的稀硫酸,用c mol·L
 标准溶液滴定至终点时,消耗滴定液V mL。该双氧水溶液中
标准溶液滴定至终点时,消耗滴定液V mL。该双氧水溶液中
 (用含c、V、
(用含c、V、 的代数式表示)。若滴定管用蒸馏水洗涤后没有用
的代数式表示)。若滴定管用蒸馏水洗涤后没有用 标准溶液润洗,则测得的结果
标准溶液润洗,则测得的结果
您最近一年使用:0次
2023-02-18更新
|
121次组卷
|
2卷引用:海南省儋州市2022-2023学年高二下学期开学考试化学试题
5 . 次氯酸为一元弱酸,具有漂白和杀菌作用,室温下,其电离平衡体系中各成分的组成分数δ[δ(X)=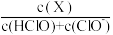 ×100%,X为HClO或ClO-]与pH的关系如图所示。下列说法错误的是
×100%,X为HClO或ClO-]与pH的关系如图所示。下列说法错误的是
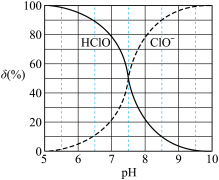
| A.室温下Ka(HClO)≈10-7.5 |
| B.等浓度的HClO和NaClO的混合溶液显碱性 |
| C.NaClO溶液中存在c(H+)+c(HClO)=c(OH-) |
| D.将HClO溶液逐滴滴入NaOH溶液至中性的过程中,水的电离程度逐渐增大 |
您最近一年使用:0次
2023-02-16更新
|
150次组卷
|
2卷引用:陕西省安康市2022-2023学年高二下学期开学摸底考试化学试题
名校
6 . 亚磷酸(H3PO3)是二元弱酸,可用于农药中间体以及有机磷水处理剂的原料。常温下向1L0.5mol·L-1H3PO3溶液中滴加等浓度的NaOH溶液,混合溶液中含磷粒子的物质的量分数(δ)与溶液pH的关系如图所示,下列说法正确的是
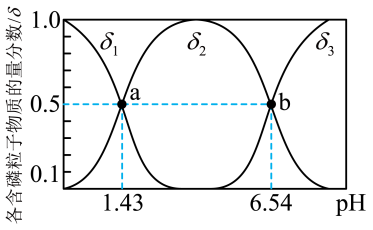

| A.a、b两点,水分别电离出的c (OH-)水之比为10-6.54:10-1.43 |
B.b点对应溶液中存在:c(Na+)>3 c (HPO ) ) |
C.当V(NaOH)=1L时,c (Na+)>c (H2PO )>c (H3PO3) >c (HPO )>c (H3PO3) >c (HPO ) ) |
D.反应H3PO3+HPO  2H2PO 2H2PO 的平衡常数为105.11 的平衡常数为105.11 |
您最近一年使用:0次
名校
解题方法
7 . 已知:常温下,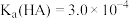 ,
, ,
, 。下列说法正确的是
。下列说法正确的是
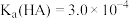 ,
, ,
, 。下列说法正确的是
。下列说法正确的是A. 与等浓度等体积的 与等浓度等体积的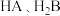 溶液完全反应,消耗 溶液完全反应,消耗 的物质的量前者更大 的物质的量前者更大 |
B. 的 的 溶液中,水电离出的 溶液中,水电离出的 为 为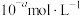 |
C.向 溶液中滴加少量 溶液中滴加少量 溶液的离子方程式为 溶液的离子方程式为 |
D.向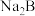 溶液中滴加等浓度等体积的盐酸,充分反应后溶液呈碱性 溶液中滴加等浓度等体积的盐酸,充分反应后溶液呈碱性 |
您最近一年使用:0次
2023-02-14更新
|
144次组卷
|
7卷引用:浙江省名校协作体(绍兴市第一中学等)2022届高三上学期期初联考化学试题
浙江省名校协作体(绍兴市第一中学等)2022届高三上学期期初联考化学试题(已下线)解密10 水溶液中的离子平衡(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)二轮拔高卷1-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(浙江专用)(已下线)第八章 水溶液中的离子反应与平衡 第54练 水溶液中四大平衡常数的综合应用云南省昆明市第一中学2022-2023学年高二下学期期中考试化学试题云南省楚雄第一中学2022-2023学年高二下学期期末考试化学试题云南省马关县第一中学校2022-2023学年高二下学期期末考试化学试题
名校
8 . 乙二酸( 或HOOCCOOH)俗称草酸,是一种二元弱酸,在工业上可作漂白剂、鞣革剂,在实验研究和化学工业中应用广泛。
或HOOCCOOH)俗称草酸,是一种二元弱酸,在工业上可作漂白剂、鞣革剂,在实验研究和化学工业中应用广泛。
(1)草酸第一步电离的电离方程式为___________________________ 。
(2)草酸可用来测定未知浓度的 溶液(用草酸滴定
溶液(用草酸滴定 溶液)。
溶液)。
①实验过程中,草酸应用___________ (填“酸式”或“碱式”)滴定管盛装。
②判断达到滴定终点时的现象为_______________________________________________________ 。
③若滴定完成后仰视读数,则测得的 溶液浓度
溶液浓度___________ (“偏高”、“偏低”或“无影响”)。
(3)常温下,草酸溶液中微粒的物质的量分数随溶液pH的变化如图所示:
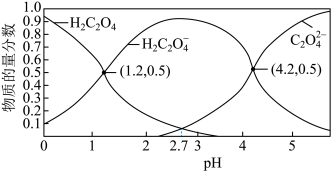
已知:常温下, 的电离平衡常数
的电离平衡常数 ,
, 。
。
①常温下,草酸的电离平衡常数
___________ 。
②相同条件下,物质的量浓度均为0.1 的
的 溶液的pH比
溶液的pH比 溶液的pH
溶液的pH__________ (填“大”或“小”)。
③常温下,向10mL 0.1
 溶液中逐滴加入0.1
溶液中逐滴加入0.1 KOH溶液,随着KOH溶液体积的增加,当溶液中
KOH溶液,随着KOH溶液体积的增加,当溶液中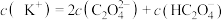 时,加入的V(KOH溶液)
时,加入的V(KOH溶液)___________ (填“>”、“=”或“<”)10mL,若加入KOH溶液体积为10mL溶液中 、
、 、
、 的浓度由大到小的顺序为
的浓度由大到小的顺序为________________________ 。
 或HOOCCOOH)俗称草酸,是一种二元弱酸,在工业上可作漂白剂、鞣革剂,在实验研究和化学工业中应用广泛。
或HOOCCOOH)俗称草酸,是一种二元弱酸,在工业上可作漂白剂、鞣革剂,在实验研究和化学工业中应用广泛。(1)草酸第一步电离的电离方程式为
(2)草酸可用来测定未知浓度的
 溶液(用草酸滴定
溶液(用草酸滴定 溶液)。
溶液)。①实验过程中,草酸应用
②判断达到滴定终点时的现象为
③若滴定完成后仰视读数,则测得的
 溶液浓度
溶液浓度(3)常温下,草酸溶液中微粒的物质的量分数随溶液pH的变化如图所示:

已知:常温下,
 的电离平衡常数
的电离平衡常数 ,
, 。
。①常温下,草酸的电离平衡常数

②相同条件下,物质的量浓度均为0.1
 的
的 溶液的pH比
溶液的pH比 溶液的pH
溶液的pH③常温下,向10mL 0.1

 溶液中逐滴加入0.1
溶液中逐滴加入0.1 KOH溶液,随着KOH溶液体积的增加,当溶液中
KOH溶液,随着KOH溶液体积的增加,当溶液中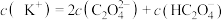 时,加入的V(KOH溶液)
时,加入的V(KOH溶液) 、
、 、
、 的浓度由大到小的顺序为
的浓度由大到小的顺序为
您最近一年使用:0次
2023-02-11更新
|
189次组卷
|
2卷引用:河南省名校2022-2023学年高二下学期开学考试化学试题
9 . 酒石酸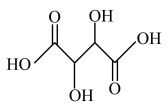 (简写为
(简写为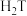 )是一种常用的食品添加剂,已知常温下酒石酸的电离平衡常数
)是一种常用的食品添加剂,已知常温下酒石酸的电离平衡常数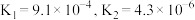 ,草酸
,草酸 的电离平衡常数
的电离平衡常数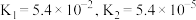 。下列说法正确的是
。下列说法正确的是
 (简写为
(简写为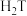 )是一种常用的食品添加剂,已知常温下酒石酸的电离平衡常数
)是一种常用的食品添加剂,已知常温下酒石酸的电离平衡常数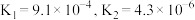 ,草酸
,草酸 的电离平衡常数
的电离平衡常数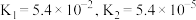 。下列说法正确的是
。下列说法正确的是A.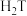 在水溶液中的电离方程式为: 在水溶液中的电离方程式为: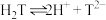 |
B.常温下,往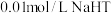 水溶液中继续加水稀释,溶液的 水溶液中继续加水稀释,溶液的 逐渐增大 逐渐增大 |
C.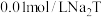 水溶液中: 水溶液中: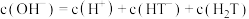 |
D. 与过量的 与过量的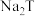 水溶液反应的离子方程式: 水溶液反应的离子方程式: |
您最近一年使用:0次
2023-02-11更新
|
668次组卷
|
5卷引用:湖南省部分学校2022-2023学年高三下学期开学考试化学试题
湖南省部分学校2022-2023学年高三下学期开学考试化学试题湖南省衡阳市第八中学2023-2024学年高三上学期开学(暑假检测)化学试题湖南省四大名校名师团队2022-2023学年高三下学期2月模拟冲刺卷(1)化学试题(已下线)江苏省南京市盐城市2023届高三3月第二次模拟考试化学试题变式题(选择题11-13)福建省泉州市永春第一中学2022-2023学年高二下学期6月期末考试化学试题
名校
10 . 常温下,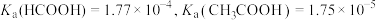 。下列说法正确的是
。下列说法正确的是
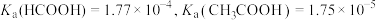 。下列说法正确的是
。下列说法正确的是A.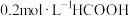 与 与 等体积混合后: 等体积混合后: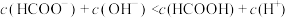 |
B.相同体积 均为2的 均为2的 和 和 溶液,中和 溶液,中和 的能力相同 的能力相同 |
C.等浓度的 溶液与 溶液与 溶液,前者溶液 溶液,前者溶液 大 大 |
D.将 溶液从 溶液从 升温至 升温至 ,溶液中 ,溶液中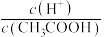 减小 减小 |
您最近一年使用:0次