2024·全国·二模
解题方法
1 . 乙二胺( ,简写为X)为二元弱碱。25℃时,向
,简写为X)为二元弱碱。25℃时,向 其盐酸盐溶液
其盐酸盐溶液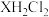 中加入固体NaOH(溶液体积变化忽略不计),溶液pOH与体系中
中加入固体NaOH(溶液体积变化忽略不计),溶液pOH与体系中 、
、 、X三种粒子浓度的对数值(
、X三种粒子浓度的对数值( )与
)与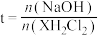 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
 ,简写为X)为二元弱碱。25℃时,向
,简写为X)为二元弱碱。25℃时,向 其盐酸盐溶液
其盐酸盐溶液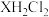 中加入固体NaOH(溶液体积变化忽略不计),溶液pOH与体系中
中加入固体NaOH(溶液体积变化忽略不计),溶液pOH与体系中 、
、 、X三种粒子浓度的对数值(
、X三种粒子浓度的对数值( )与
)与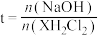 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是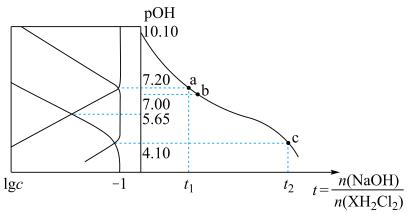
A.乙二胺第一、二步电离常数的数量级分别为 、 、 |
B.当 时, 时, |
C.b点时,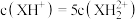 |
D.c点时,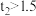 |
您最近一年使用:0次
2 . 某固体混合物X,含有Al2(SO4)3、FeCl3、Na2CO3和CuSO4中的几种,进行如下实验:
①X与水作用有气泡冒出,得到有色沉淀Y和弱碱性溶液Z;
②沉淀Y与NaOH溶液作用,无变化。
下列说法不正确 的是
①X与水作用有气泡冒出,得到有色沉淀Y和弱碱性溶液Z;
②沉淀Y与NaOH溶液作用,无变化。
下列说法
| A.混合物X中必定含有Na2CO3,不含Al2(SO4)3 |
| B.溶液Z中溶质主要是钠盐,且必含NaHCO3 |
| C.灼烧沉淀Y,可能得到黑色物质 |
| D.往溶液Z中加入Cu粉,若不溶解,说明X中不含FeCl3 |
您最近一年使用:0次
2021-12-26更新
|
3608次组卷
|
35卷引用:黑龙江省齐齐哈尔中学2022-2023学年高三上学期11月期中考试化学试题
黑龙江省齐齐哈尔中学2022-2023学年高三上学期11月期中考试化学试题(已下线)浙江省2020年1月选考(学考)化学试题2020年浙江省高考化学试卷(1月选考)浙江省丽水市松阳县第二中学2019-2020学年高二4月线上教学检测化学试题四川省成都市树德中学2019-2020学年高二下学期期中考试化学试题(已下线)小题必刷05 离子检验与推断——2021年高考化学一轮复习小题必刷(通用版)湖北省宜昌市长阳土家族自治县第一高级中学2020-2021学年高二上学期期中考试化学试题(已下线)小题必刷32 盐类的水解影响因素及应用——2021年高考化学一轮复习小题必刷(通用版本)(已下线)解密04 离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密04 离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练浙江省杭州市长征中学2020-2021学年高二下学期第二学期阶段性练习化学试题浙江省宁波市北仑中学2020-2021学年高二下学期期中考试化学(1班)试题(已下线)课时08 离子检验与推断-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点04 离子反应-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点04 离子反应-备战2022年高考化学一轮复习考点帮(浙江专用)江苏省淮安市车桥中学2022届高三上学期入学调研(A)化学试题(已下线)第3章 水溶液中的离子反应与平衡(能力提升卷)-【高效检测】2021-2022学年高二化学章末测试卷(人教版2019选择性必修1)(已下线)专题3.3.2 影响盐类水解的主要因素(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)(已下线)专题04.离子反应-十年(2012-2021)高考化学真题分项汇编(浙江专用)辽宁省实验中学2022届高三第一次阶段性考试化学试题(已下线)考点03 离子反应-备战2022年高考化学学霸纠错(全国通用)(已下线)解密04 离子反应(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)3.3.1 盐溶液的酸碱性及其原因(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)(已下线)解密04 离子反应(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)2020年全国卷Ⅱ化学真题变式题西藏拉萨中学2022届高三第七次月考理综化学试题(已下线)考点04 离子反应-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第25讲 盐类水解(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)第28讲 物质的分离、提纯和检验(练)-2023年高考化学一轮复习讲练测(全国通用)浙江省余姚中学2022-2023学年高二上学期期中考试化学试题北京市清华大学附属中学2022-2023学年高二上学期12月月考化学试题(已下线)专题06 离子共存、检验和推断-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)题型6 离子定性、定量推断-高考必备50个题型(已下线)考点03 离子共存、离子的检验与推断(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)四川省合江县马街中学校2023-2024学年高二上学期1月期末化学试题
名校
解题方法
3 . 为了除去氯化镁酸性溶液中的铁离子,可在加热搅拌的条件下加入一种试剂,过滤后,再向滤液中加入适量的盐酸,这种试剂是( )
| A.一水合氨 | B.烧碱 | C.碳酸镁 | D.碳酸钠 |
您最近一年使用:0次
2020-07-03更新
|
254次组卷
|
13卷引用:黑龙江省大庆第一中学2017-2018学年高二上学期期末(第四次月考)考试化学试题
黑龙江省大庆第一中学2017-2018学年高二上学期期末(第四次月考)考试化学试题黑龙江省哈尔滨师范大学青冈实验中学校2018-2019学年高二上学期10月考试化学试题(已下线)2011-2012学年浙江省温州市十校联合体高二下学期期末考试化学试卷(已下线)2012-2013学年江苏省宿迁市泗洪县洪翔中学高二下学期期中考化学卷(已下线)2012-2013学年四川省雅安市高二下学期期末检测化学试卷(已下线)2014届福建省福州市高三上学期期末质量检测化学试卷2015届福建省三明市一中高三上学期第二次月考化学试卷陕西省吴起高级中学2019-2020学年高二上学期期中考试化学(能力卷)试题2020届高三化学二轮冲刺新题专练——过滤(抽滤)、蒸发、结晶等除杂分离法北京市中国人民大学附属中学 2019-2020 学年度高二下学期期末练习化学试题(已下线)3.3.2 影响盐类水解的因素(重点练)-2020-2021学年高二化学十分钟同步课堂专练(苏教版选修4)山西省稷山中学2021-2022学年高二上学期第二次月考化学试题云南省昆明师范专科学校附属中学2021-2022学年高二上学期期末考试化学试题
解题方法
4 . 常温下,0.1mol/L 的下列溶液中,c(NH4+)最大的是( )
| A.NH4Cl | B.(NH4)2Fe(SO4)2 | C.(NH4)2CO3 | D.CH3COONH4 |
您最近一年使用:0次
2019-12-31更新
|
123次组卷
|
2卷引用:黑龙江省宾县一中2019-2020学年高二上学期第二次月考化学试题
名校
解题方法
5 . 回答下列问题:
(1)泡沫灭火器原理(用离子方程式表示)___________
(2)碳酸钠溶液蒸干灼烧得到的固体是_____ , 原因是____________
(3)已知NaHR溶液中c(H2R)<c(R2-),则该溶液中c(H+)________ c(OH-)(填写“<”或“=”或“>”)
(4)相同条件下,同浓度的NH3•H2O , NH4Cl,NH4Al(SO4)2,NH4HSO4水溶液,NH4+浓度分别为a,b,c,d,则几种物质NH4+浓度由大到小的顺序为_______ (用a,b,c,d,表示)
(5)二氯亚砜(SOCl2)是一种无色易挥发液体,与水剧烈水解生成两种气体,常做脱水剂。用硫磺(用S表示)、液氯和三氧化硫为原料在一定条件下合成二氯亚砜,原子利用率达到百分之百,则三者的物质的量之比为____________ 写出SOCl2吸收水蒸气的化学方程式___________
(1)泡沫灭火器原理(用离子方程式表示)
(2)碳酸钠溶液蒸干灼烧得到的固体是
(3)已知NaHR溶液中c(H2R)<c(R2-),则该溶液中c(H+)
(4)相同条件下,同浓度的NH3•H2O , NH4Cl,NH4Al(SO4)2,NH4HSO4水溶液,NH4+浓度分别为a,b,c,d,则几种物质NH4+浓度由大到小的顺序为
(5)二氯亚砜(SOCl2)是一种无色易挥发液体,与水剧烈水解生成两种气体,常做脱水剂。用硫磺(用S表示)、液氯和三氧化硫为原料在一定条件下合成二氯亚砜,原子利用率达到百分之百,则三者的物质的量之比为
您最近一年使用:0次
名校
解题方法
6 . 按要求填空:
(1)AlCl3的水溶液 pH______ 7(填>、=、<),其原因为______________ (用离子方程式表示),将其溶液加热蒸干并灼烧最终得到物质是______ (填化学式)。
(2)常温下,Cr(OH)3的溶度积Ksp=c(Cr3+)·c3(OH−)=10−32,要使c(Cr3+)降至10−5mol/L,溶液的pH应调至_____ 。
(3)物质的量浓度相同的三种溶液:①NH4Cl ②氨水 ③NH4HSO4,c(NH4+)大小顺序正确的是______________ 。 (用序号表示)
(4)常温下两种溶液:a.pH=4 NH4Cl b.pH=4盐酸溶液,其中水电离出C(H+)之比为____________________ 。
(5)室温,将pH=9的NaOH溶液与pH=4的盐酸溶液混合,若所得混合溶液的pH=6,则NaOH溶液与盐酸的体积比为____________ 。
(1)AlCl3的水溶液 pH
(2)常温下,Cr(OH)3的溶度积Ksp=c(Cr3+)·c3(OH−)=10−32,要使c(Cr3+)降至10−5mol/L,溶液的pH应调至
(3)物质的量浓度相同的三种溶液:①NH4Cl ②氨水 ③NH4HSO4,c(NH4+)大小顺序正确的是
(4)常温下两种溶液:a.pH=4 NH4Cl b.pH=4盐酸溶液,其中水电离出C(H+)之比为
(5)室温,将pH=9的NaOH溶液与pH=4的盐酸溶液混合,若所得混合溶液的pH=6,则NaOH溶液与盐酸的体积比为
您最近一年使用:0次
7 . 工业制胆矾时,将粗制CuO粉末(含杂质FeO、Fe2O3)慢慢加入适量的稀H2SO4中完全溶解后,除去杂质离子后,再蒸发结晶可得纯净的胆矾晶体。已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;pH在3~4时,Fe3+以Fe(OH)3的形式完全沉淀.回答下列问题:
(1)为除去溶液中的Fe2+,可先加入______ (填化学式)将Fe2+氧化为Fe3+,反应的离子方程式为__________ ,然后再加入适量的__________ 调整溶液的pH到______ ,使Fe3+转化为Fe(OH)3。
(2)甲同学怀疑调整至溶液pH=4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计算确定,他查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp=1×10-38,Cu(OH)2的溶度积Ksp=3×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol•L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3mol•L-1,则Cu(OH)2开始沉淀时溶液的pH为______ ,Fe3+完全沉淀时溶液的pH为______ ,通过计算确定上述方案______ (填“可行”或“不可行”)。
(1)为除去溶液中的Fe2+,可先加入
(2)甲同学怀疑调整至溶液pH=4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计算确定,他查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp=1×10-38,Cu(OH)2的溶度积Ksp=3×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol•L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3mol•L-1,则Cu(OH)2开始沉淀时溶液的pH为
您最近一年使用:0次
2018-01-18更新
|
496次组卷
|
3卷引用:黑龙江省鸡西中学2017-2018学年高二上学期期末考试化学试题
名校
解题方法
8 . 如图是工业制取菱镁矿MgCO3(含杂质Al2O3、FeCO3)制取镁的工艺流程
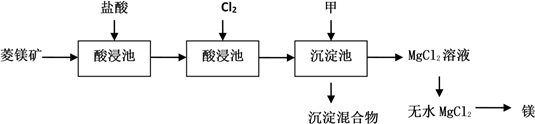
请回答有关问题:
(1)菱镁矿进入酸浸池前需要粉碎,目的是___________ 。
(2)氧化池通入Cl2的目的是氧化___________ (填化学式),工业上不选用硝酸做氧化剂的原因是___________ 和___________ 。
(3)物质甲可以是___________
A、MgO B、Mg(OH)2 C、NaOH溶液 D、稀氨水
(4)由MgCl2溶液制取无水MgCl2的操作方法___________ 。
(5)当Fe3+完全沉淀时,求最小pH___________ 。已知:氢氧化铁ksp=1.0×10-38,离子浓度小于1×10-5 mol/L认为沉淀完全

请回答有关问题:
(1)菱镁矿进入酸浸池前需要粉碎,目的是
(2)氧化池通入Cl2的目的是氧化
(3)物质甲可以是
A、MgO B、Mg(OH)2 C、NaOH溶液 D、稀氨水
(4)由MgCl2溶液制取无水MgCl2的操作方法
(5)当Fe3+完全沉淀时,求最小pH
您最近一年使用:0次
2017-09-01更新
|
373次组卷
|
3卷引用:黑龙江省大庆实验中学2018届高三上学期期初考试化学试题



