名校
1 . 下列装置(部分夹持仪器省略)能达到实验目的的是
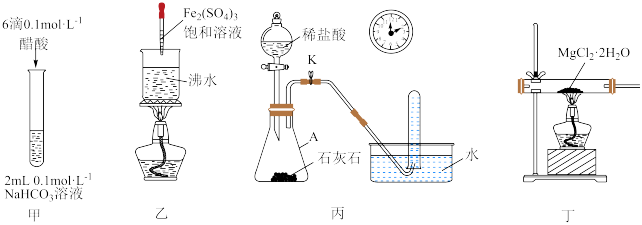

A.用装置甲比较相同温度下醋酸与碳酸的 大小 大小 | B.用装置乙制备 胶体 胶体 |
| C.用装置丙测定石灰石与盐酸反应的速率 | D.用装置丁制取无水 |
您最近一年使用:0次
2023-12-03更新
|
209次组卷
|
2卷引用:山东省德州市2023-2024学年高二上学期期中考试化学试题
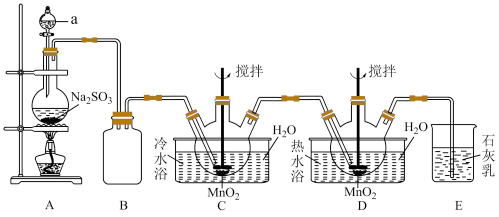
2 . 连二硫酸锰(MnS2O6)常用于灭菌以及水果、蔬菜的保鲜。硫酸锰(MnSO4)是重要的微量元素肥料之一,也用作饲料添加剂,在涂料、造纸、陶瓷、电子、纺织等领域也有广泛应用。利用MnO2悬浊液吸收SO2气体制取MnS2 O6和MnSO4的装置如图所示(部分夹持仪器、加热仪器未画出)。
②连二硫酸锰晶体的化学式为MnS2O6·4H2O。
③连二硫酸钡(BaS2O6)易溶于水,氢氧化锰[Mn(OH)2]难溶于水。
回答下列问题:
(1)仪器a的名称为___________ ,该仪器中装入的试剂最好为___________ (填标号)。
A.稀盐酸 B.70%的浓硫酸 C.98%的浓硫酸 D.稀硝酸
(2)连二硫酸锰在装置___________ (填标号)中生成,装置B的作用为___________ 。
(3)从实验后过滤所得的反应混合液(含有少量杂质MnSO4)中得到纯净的MnS2O6溶液的操作方法和除杂的反应原理为___________ 。
(4)由MnS2O6溶液得到MnS2O6·4H2O晶体的操作方法是___________ 。
(5)测定MnS2O6中锰的含量:称取wg产品充分加热,加适量水溶解,用amol·L-1KMnO4标准溶液进行滴定(Mn元素均转化为MnO2),滴定终点时消耗bmL标准溶液。___________ 。(填标号)
A.滴定管活塞涂凡士林:取下活塞,用滤纸擦干,用手指蘸取少量凡士林涂抹一薄层在活塞a、c(如图)处的四周,平行插入活塞槽中,然后朝同一个方向转动
B.滴定开始时可以将液体成线状快速流下,接近终点时减慢滴加速度,必要时采用半滴操作
C.读数时可将滴定管从滴定管架上取下,捏住管上端无刻度处,使滴定管保持垂直
D.第一次滴定终点时,若测得消耗标准溶液体积小于5.00mL,则第二次滴定时可稀释待测液后重新滴定来减小误差
②实验过程中若晶体加热不充分,测得产品中锰的质量分数将___________ (填“偏大”“偏小”或“无影响”)。
③产品中锰的质量分数是___________ (列出计算式)。
②连二硫酸锰晶体的化学式为MnS2O6·4H2O。
③连二硫酸钡(BaS2O6)易溶于水,氢氧化锰[Mn(OH)2]难溶于水。
回答下列问题:
(1)仪器a的名称为
A.稀盐酸 B.70%的浓硫酸 C.98%的浓硫酸 D.稀硝酸
(2)连二硫酸锰在装置
(3)从实验后过滤所得的反应混合液(含有少量杂质MnSO4)中得到纯净的MnS2O6溶液的操作方法和除杂的反应原理为
(4)由MnS2O6溶液得到MnS2O6·4H2O晶体的操作方法是
(5)测定MnS2O6中锰的含量:称取wg产品充分加热,加适量水溶解,用amol·L-1KMnO4标准溶液进行滴定(Mn元素均转化为MnO2),滴定终点时消耗bmL标准溶液。

A.滴定管活塞涂凡士林:取下活塞,用滤纸擦干,用手指蘸取少量凡士林涂抹一薄层在活塞a、c(如图)处的四周,平行插入活塞槽中,然后朝同一个方向转动
B.滴定开始时可以将液体成线状快速流下,接近终点时减慢滴加速度,必要时采用半滴操作
C.读数时可将滴定管从滴定管架上取下,捏住管上端无刻度处,使滴定管保持垂直
D.第一次滴定终点时,若测得消耗标准溶液体积小于5.00mL,则第二次滴定时可稀释待测液后重新滴定来减小误差
②实验过程中若晶体加热不充分,测得产品中锰的质量分数将
③产品中锰的质量分数是
您最近一年使用:0次
2023-09-14更新
|
232次组卷
|
2卷引用:山东省金科大联考2023-2024学年高三9月联考化学试题
3 . GaCl3溶液中存在平衡: 。常温下,向
。常温下,向 溶液中加入
溶液中加入 溶液,
溶液,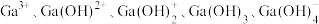 的浓度分数
的浓度分数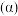 随溶液
随溶液 变化如图所示。下列说法错误的是
变化如图所示。下列说法错误的是

 。常温下,向
。常温下,向 溶液中加入
溶液中加入 溶液,
溶液,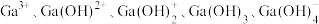 的浓度分数
的浓度分数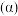 随溶液
随溶液 变化如图所示。下列说法错误的是
变化如图所示。下列说法错误的是
A.曲线b表示 的浓度分数随溶液pH的变化 的浓度分数随溶液pH的变化 |
B.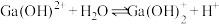 ,该平衡常数K的数量级为 ,该平衡常数K的数量级为 |
C.x点,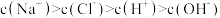 |
D.y点,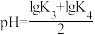 |
您最近一年使用:0次
2022-02-22更新
|
886次组卷
|
2卷引用:山东省临沂市2022届高三下学期一模考试化学试题
名校
解题方法
4 . 常温下,下列各组离子在指定的条件下可能大量共存的是
A.c(OH-)/c(H+)=1012的溶液中: 、Al3+、 、Al3+、 、 、 |
B.有Fe3+存在的溶液中: 、 、 、 、 、Cl- 、Cl- |
C.pH=0的溶液中:Fe2+、Mg2+、 、 、 |
D.由水电离出的c(H+)=1×10-13mol/L的溶液:Al3+、K+、 、Cl﹣ 、Cl﹣ |
您最近一年使用:0次
2021-01-04更新
|
933次组卷
|
10卷引用:山东省泰安市新泰第一中学(东校)2020-2021学年高二上学期第二次质量检测化学试题
山东省泰安市新泰第一中学(东校)2020-2021学年高二上学期第二次质量检测化学试题(已下线)解密04 离子反应(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密04 离子反应(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)课时07 离子共存-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点04 离子反应-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点04 离子反应-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点04 离子反应-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点04 离子反应(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)河南省济源市高级中学2023-2024学年高三上学期9月高考模拟检测理科综合试题-高中化学浙江省杭州市精诚联盟2023-2024学年高二上学期12月月考化学试题
名校
解题方法
5 . 向含Na2CO3、Na[Al(OH)4](NaAlO2)的混合溶液中逐滴加入150mL1mol·L-1HCl溶液,测得溶液中的某几种离子物质的量的变化如图所示,则下列说法不正确的是( )
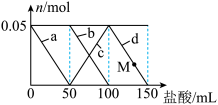

| A.a曲线表示的离子方程式为:[Al(OH)4]-+H+=Al(OH)3↓+H2O |
| B.b和c曲线表示的离子反应是不相同的 |
| C.M点时,溶液中沉淀的质量为3.9g |
D.原混合溶液中的CO 与[Al(OH)4]-的物质的量之比为1∶2 与[Al(OH)4]-的物质的量之比为1∶2 |
您最近一年使用:0次
名校
6 . 等物质的量浓度、等体积的下列溶液中(1)H2CO3 (2)Na2CO3 (3)NaHCO3 (4)NH4HCO3 (5)(NH4)2CO3。下列关系或者说法正确的是( )
| A.c(HCO3-)的大小关系为:(4)>(3)>(5)>(2)>(1) |
| B.c(CO32-)的大小关系为:(1)<(4)<(3)<(5)<(2) |
| C.将溶液蒸干后灼烧后只有(1)不能得到对应的固体物质 |
| D.(2)(3)(4)(5)既能与盐酸反应,又能与NaOH溶液反应 |
您最近一年使用:0次
2019-11-24更新
|
338次组卷
|
12卷引用:2016-2017学年山东省桓台二中高二上学期期中化学试卷
2016-2017学年山东省桓台二中高二上学期期中化学试卷山东省枣庄市第八中学南校区2017-2018学年高二上学期第二次月考(12月)化学试题2016届河北省行唐启明中学高三上学期12月月考化学试卷2017届河北省定州中学高三上学期第二次月考化学卷2016-2017学年吉林省长春市第十一高中高二上学期期初考试化学试卷2016-2017学年河北省邢台一中高二上月考二化学卷苏教版高三单元精练检测八化学试题福建省闽侯第六中学2017-2018学年高二12月月考化学试题河南省鲁山县第一高级中学2019-2020学年高二11月月考化学试题江西省吉安市省重点中学2020-2021学年高二上学期期中联合考试化学试题江西省吉安市2020-2021学年高二上学期期中统考化学试题第3课时 溶液中粒子浓度的大小比较



